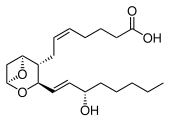
Eicosanoide

Eicosanoides son moléculas de señalización producidas por la oxidación enzimática o no enzimática del ácido araquidónico u otros ácidos grasos poliinsaturados (PUFA) que, de manera similar al ácido araquidónico, tienen alrededor de 20 unidades de carbono de longitud. Los eicosanoides son una subcategoría de oxilipinas, es decir, ácidos grasos oxidados de diversas unidades de carbono de longitud, y se distinguen de otras oxilipinas por su abrumadora importancia como moléculas de señalización celular. Los eicosanoides funcionan en diversos sistemas fisiológicos y procesos patológicos tales como: aumentar o inhibir la inflamación, alergia, fiebre y otras respuestas inmunes; regular el aborto del embarazo y el parto normal; contribuir a la percepción del dolor; regular el crecimiento celular; controlar la presión arterial; y modular el flujo regional de sangre a los tejidos. Al realizar estas funciones, los eicosanoides actúan con mayor frecuencia como agentes de señalización autocrinos para impactar sus células de origen o como agentes de señalización paracrinos para impactar las células cercanas a sus células de origen. Los eicosanoides también pueden actuar como agentes endocrinos para controlar la función de células distantes.
Existen múltiples subfamilias de eicosanoides, entre las que destacan las prostaglandinas, tromboxanos, leucotrienos, lipoxinas, resolvinas y eoxinas. Para cada subfamilia, existe la posibilidad de tener al menos 4 series separadas de metabolitos, dos series derivadas de los AGPI ω-6 (ácidos araquidónico y dihomo-gamma-linolénico), una serie derivada de los AGPI ω-3 (ácido eicosapentaenoico), y una serie derivada del PUFA ω-9 (ácido hidromiel). Esta distinción de subfamilia es importante. Los mamíferos, incluidos los humanos, no pueden convertir ω-6 en ω-3 PUFA. En consecuencia, los niveles tisulares de los AGPI ω-6 y ω-3 y sus correspondientes metabolitos eicosanoides se vinculan directamente con la cantidad de AGPI ω-6 versus ω-3 consumidos en la dieta. Dado que algunas de las series de metabolitos de los AGPI ω-6 y ω-3 tienen actividades fisiológicas y patológicas casi diametralmente opuestas, a menudo se ha sugerido que las consecuencias nocivas asociadas con el consumo de dietas ricas en AGPI ω-6 reflejan una producción y actividades excesivas. de eicosanoides derivados de ω-6 PUFA, mientras que los efectos beneficiosos asociados con el consumo de dietas ricas en ω-3 PUFA reflejan la producción excesiva y las actividades de los eicosanoides derivados de ω-3 PUFA. Desde este punto de vista, los efectos opuestos de los eicosanoides derivados de los AGPI ω-6 y los derivados de los AGPI ω-3 sobre las células diana clave subyacen a los efectos perjudiciales y beneficiosos de las dietas ricas en AGPI ω-6 y ω-3 sobre la inflamación y las reacciones alérgicas. aterosclerosis, hipertensión, crecimiento del cáncer y muchos otros procesos.
Nomenclatura
Fuentes de ácidos grasos
"Eicosanoide" (eicosa-, en griego significa "veinte"; ver icosaedro) es el término colectivo para los ácidos grasos poliinsaturados (PUFA) de cadena lineal de 20 unidades de carbono. de longitud que han sido metabolizados o convertidos de otro modo en productos que contienen oxígeno. Los precursores de PUFA de los eicosanoides incluyen:
- Ácido Araquidonico (Acido Araquidonico)AA), es decir, 5Z, 8Z,11Z,14Z- El ácido eicosatetraenoico es un ácido graso ω-6 con cuatro dobles lazos en la configuración de cis (ver Cis–trans isomerismo), cada uno situado entre los carbonos 5-6, 8-9, 11-12 y 14-15.
- Ácido Adrenico (Acido Adrenico)AdA), 7,10,13,16-docosatetraenoico ácido, es un ácido graso ω-6 con cuatro cis dobles límites, cada uno situado entre carbonos 7-8, 10-11, 13-14, y 17-18.
- Ácido eicosapentaenoicoEPA), i.e.i.e. 5Z, 8Z,11Z,14Z,17Z- ácido eicosapentaenoico es un ácido graso ω-3 con cinco bonos dobles de cis, cada uno situado entre carbonos 5-6, 8-9, 11-12, 14-15 y 17-18.
- Ácido dihomo-gamma-linolénicoDGLA), 8Z, 11Z,14Z- ácido eicosatrienoico es un ácido graso ω-6 con tres bonos dobles cis, cada uno situado entre carbonos 8-9, 11-12 y 14-15.
- Ácido de carga, es decir, 5Z8Z,11Z- ácido eicosatrienoico, es un ácido graso ω-9 que contiene tres bonos dobles cis, cada uno situado entre carbonos 5-6, 8-9 y 11-12.
Abreviatura
Un eicosanoide particular se indica mediante una abreviatura de cuatro caracteres, compuesta por:
- su abreviatura de dos letrasLT, EX o PG, como se describe a continuación),
- un A-B-C secuencia-letter,
- Un número de subscripto o de script simple siguiendo el nombre trivial de eicosanoid designado indica el número de sus dobles lazos. Ejemplos son:
- Los prostanoides impulsados por la EPA tienen tres bonos dobles (por ejemplo, PGG3 o PGG3), mientras que las leucotrinas derivadas de la EPA tienen cinco bonos dobles (por ejemplo, LTB5 o LTB5).
- Los prostanoides de AA tienen dos bonos dobles (por ejemplo, PGG2 o PGG2) mientras que sus leucotrinas AA-derived tienen cuatro dobles bonos (por ejemplo, LTB4 o LTB4).
- Hydroperoxy-, hydroxyl-, and oxo-eicosanoids possess a hydroperoxy (-OOH), hydroxy (-OH), or oxígeno atom (=O) substituents link to a PUFA carbon by a single (-) or double (=) bond. Sus nombres triviales indican que el sustituto es: Hp o HP para un residuo hidroperoxi (por ejemplo, 5-hidroperooxi-eicosatraenoico ácido o 5-HpETE o 5-HPETE); H para un residuo hidroxi (por ejemplo, ácido hidroxi-eicosatetraenoico 5-HETE); y oxo- para un residuo de oxo (por ejemplo, ácido 5-oxo-eicosatetraenioico o 5-oxo-ETE o 5-oxoETE). El número de sus dobles límites se indica por sus nombres completos y triviales: los metabolitos hidroxid AA tienen cuatro (es decir, 'tetra' o 'T') dobles vínculos (por ejemplo, 5-hidroxi-eicosatetraácido enoico o 5-HETE; Los metabolitos hidroxigenados de EPA tienen cinco ('penta' o 'P') dobles lazos (por ejemplo, 5-hidroxi-eicosapentaácido enoico o 5-HEPE); y los metabolitos hidroxi-derados por DGLA tienen tres ('tri' o 'Tr') dobles vínculos (por ejemplo, 5-hidroxy-eicosatácido enoico o 5-HETrE).
La estereoquímica de los productos eicosanoides formados puede diferir entre las vías. En el caso de las prostaglandinas, esto suele indicarse con letras griegas (por ejemplo, PGF2α frente a PGF2β). Para hidroperoxi e hidroxieicosanoides, una S o una R designa la quiralidad de sus sustituyentes (por ejemplo, ácido 5S-hidroxi-eicosateteraenoico [también denominado 5(S)-, 5S-hidroxi- y 5(S)-hidroxi-eicosatetraenoico] recibe los nombres triviales de 5S-HETE, 5( S)-HETE, 5S-HETE o 5(S)-HETE). Dado que las enzimas formadoras de eicosanoides suelen producir productos isómeros S con marcada preferencia o esencialmente exclusivamente, el uso de designaciones S/R a menudo se ha abandonado. (por ejemplo, 5S-HETE es 5-HETE). No obstante, ciertas vías de formación de eicosanoides forman isómeros R y sus productos isoméricos S versus R pueden exhibir actividades biológicas dramáticamente diferentes. No especificar los isómeros S/R puede ser engañoso. Aquí, todos los sustituyentes hidroperoxi e hidroxi tienen la configuración S a menos que se indique lo contrario.
Eicosanoides clásicos
El uso actual limita el término eicosanoide a:
- Eicosanoides de serie ω-6 derivados del ácido araquidónico:
- Ácidos hidroxieicosatetraenoicos (Acidos hidroxieicosatetraenoicos)HETE) incluyen los siguientes metabolitos de ácido araquidónico:
- 5-HETE, 12-HETE, ácido 15-hidroxieicosatetraenoico (es decir, 15-HETE), ácido 20-hidroxieicosatetraenoico (es decir, 20-HETE) y 19-HETE.
- LeukotrienesLT) incluyen los siguientes metabolitos de ácido araquidónico:
- LTA4, LTB4, LTC4, LTD4, y LTE4.
- Eoxinas (EX) incluyen los siguientes metabolitos del ácido araquidnoico:
- EXA4, EXC4, EXD4, y EXE4.
- Prostanoides consistentes en varios tipos diferentes:
- Prostaglandins (prostaglandins)PG) incluyen los siguientes metabolitos de ácido araquidónico:
- PGG2, PGH2, PGE2, PGD2, PGF2alpha, PGA2, PGB2, (ver Mediadores Especializados Pro-Resolving § Prostaglandins and isoprostanes).
- Las prostaciclinas incluyen:
- PGI2.
- ThromboxanesTX) incluyen los siguientes metabolitos de ácido aracidonico:
- TXA2 y TXB2.
- Las prostaglandinas de Cyclopentenone incluyen los siguientes metabolitos del ácido araquidónico:
- PGA1, PGA2 (ver Prostanoid, PGJ2, Δ12-PGJ2, y 15-deoxy-Δ12,14-PGJ2).
- Prostaglandins (prostaglandins)PG) incluyen los siguientes metabolitos de ácido araquidónico:
- Ácidos hidroxieicosatetraenoicos (Acidos hidroxieicosatetraenoicos)HETE) incluyen los siguientes metabolitos de ácido araquidónico:
- Eicosanoides de la serie ω-6 derivados del ácido dihomo-gamma-linolénico. Estos metabolitos son análogos de eicosanoides derivados del ácido araquidónico pero carecen de un doble vínculo entre los carbonos 5 y 6 y, por lo tanto, tienen 1 límite menos doble que sus análogos derivados del ácido araquidónico. Los siguientes son:
- PGA1, PGE1, y TXA1.
- ω-3 Serie eicosanoides:
- Resoluciones de la serie E (E)RvE) (Resolvinas de la serie D (Los RvD son metabolitos del ácido docosahexaenoico 22-carbono ω-3; véase Mediadores prorresolventes especializados § DHA-derived resolvins). RvE incluye los siguientes metabolitos de ácido eicosapentaenoico:
- RvE1, 18S-RvE1, RvE2, y RvE3.
- Otros eicosanoides derivados de ácidos eicosapentaenoicos de la serie ω-3 son análogos de metabolitos derivados de ácidos grasos ω-6 pero contienen un doble vínculo entre carbono 17 y 18 y por lo tanto tienen un doble límite que sus análogos araquidonicos derivados de ácido. Incluyen (HEPE es ácido hidroxieicosapentaenoico):
- 5-HEPE, 12-HEPE, 15-HEPE, y 20-HETE; LTA5, LTB5, LTC5, LTD5, y LTE5 (ver Arachidonate 5-lipoxygenase § Eicosapentaenoic acid); PGE3, PGD3, PGF3α, y Δ(17)-6-keto PGF1α; PGI3 ácido esencial
- Resoluciones de la serie E (E)RvE) (Resolvinas de la serie D (Los RvD son metabolitos del ácido docosahexaenoico 22-carbono ω-3; véase Mediadores prorresolventes especializados § DHA-derived resolvins). RvE incluye los siguientes metabolitos de ácido eicosapentaenoico:
- Eicosanoides de la serie ω-9
- Hidroxi son ácido de la forma derivada, se metaboliza a la 3 doble unión que contiene análogo de 5-HETE viz., 5-HETrE (ver Arachidonate 5-lipoxygenase § Ácido de la carga).
Los ácidos hidroxieicosatetraenoicos, los leucotrienos, las eoxinas y los prostanoides a veces se denominan "eicosanoides clásicos"
Eicosanoides no clásicos
A diferencia de los eicosanoides clásicos, varias otras clases de metabolitos de AGPI se han denominado compuestos 'novedosos', 'similares a los eicosanoides' o 'eicosanoides no clásicos'. Estos incluyeron las siguientes clases:
- Oxoeicosanoidesoxo-ETE) incluyen los siguientes metabolitos:
- 5-Oxo-eicosatetraenoico Ácido (5-oxo-ETE), 12-oxo-ETE (ver 12-HETE § Más metabolismo), y 15-oxo-ETE, que son metabolitos de ácido araquidónico (ver ácido 15-Hydroxieicosatetraenoico) y 5-oxo-ETrE que es un metabolito de ácido mead (véase Arachixydongena).
- HepoxilinasHx) incluyen los siguientes metabolitos de ácido araquidónico:
- HxA3 y HxB3.
- LipoxinasLx) incluyen los siguientes metabolitos de ácido araquidónico:
- LxA4 y LxB4 (ver mediadores de resolución especializados).
- Epi-lipoxinasepi-Lx) incluyen los siguientes metabolitos de ácido araquidónico:
- 15-epi-LxA4 (también llamado AT-LxA4) y 15-epi-LxB4 (también llamado AT-LxB4).
- Ácidos epoxieicosatrienoicos (Acidos epoxieicosatrienoicos)EET) incluyen los siguientes metabolitos de ácido araquidónico:
- 5,6-EET, 8,9-EET, 11,12-EET y 14,15-EET.
- Ácidos epoxieicosatetraenoicos (Acidos epoxieicosatetraenoicos)EEQ) incluyen los siguientes metabolitos del ácido eicosapentaenoico:
- 5,6-EEQ, 8,9-EEQ, 11,12-EEQ, 14,15-EEQ y 15,16-EEQ.
- Isoprostanes (Isoprostanes)isoP) son derivados no-enzimáticamente formados de ácidos grasos poliinsaturados estudiados como marcadores de estrés oxidativo; incluyen los siguientes isoP de ácido araquidónico que se denominan basados en sus similitudes estructurales a los PG:
- D2-isoPs, E2-isoPs, A2-isoPs y J2-isoPs; y dos isopos que contienen epoxido Ps, 5,6-epoxyisoprostane E2 y 5,6-epoxyisoprostane A2. Algunos de estos iso Se ha demostrado que los ps poseen actividad antiinflamatoria (ver mediadores prorresolventes especializados § Prostaglandinas e isoprostáneos).
- Los isofuranos son derivados no-enzimáticamente formados de ácidos grasos poliinsaturados que poseen una estructura de anillo furano; son estudiados como marcadores de estrés oxidativo. Hay 256 isómeros que contienen anillos furanos potencialmente diferentes que pueden derivarse de ácido araquidónico.
- Los endocannabinoides son ciertos gliceroloides o dopamina que son esterificados a ácidos grasos poliinsaturados que activan los receptores cannabinoides. Incluyen los siguientes agentes araquidonicos de ácido esterificado:
- Arachidonoylethanolamina, 2-arachidonoylglycerol, 2-arachidonyl glyceryl ether, O-arachidonoyl-ethanolamine, y N-arachidonoyl dopamine.
Metabolismo del ácido eicosapentaenoico a HEPE, leucotrienos, prostanoides y ácidos epoxieicosatetraenoicos, así como el metabolismo del ácido dihomo-gamma-linolénico a prostanoides y del ácido hidromiel a ácido 5(S)-hidroxi-6E,8Z,11Z-eicosatrienoico. (5-HETrE), ácido 5-oxo-6,8,11-eicosatrienoico (5-oxo-ETrE), LTA3 y LTC3 implican las mismas vías enzimáticas que producen sus análogos derivados del ácido araquidónico.
Biosíntesis
Por lo general, los eicosanoides no se almacenan dentro de las células, sino que se sintetizan según sea necesario. Derivan de los ácidos grasos que forman la membrana celular y la membrana nuclear. Estos ácidos grasos deben liberarse de sus sitios de membrana y luego metabolizarse inicialmente en productos que con mayor frecuencia se metabolizan aún más a través de diversas vías para producir la gran variedad de productos que reconocemos como eicosanoides bioactivos.
Movilización de ácidos grasos
La biosíntesis eicosanoide comienza cuando una célula es activada por trauma mecánico, isquemia, otras perturbaciones físicas, ataque por patógenos, o estímulos hechos por células cercanas, tejidos o patógenos como factores quimiotácticos, citocinas, factores de crecimiento e incluso ciertos eicosanoides. Las células activadas luego movilizan enzimas, denominadas fosfolipasa A2 (PLA)2s), capaz de liberar ácidos grasos ω-6 y ω-3 del almacenamiento de membrana. Estos ácidos grasos están ligados en ester enlace a la posición SN2 de la membrana fosfolípidos; PLA2s actuar como esterases para liberar el ácido graso. Hay varias clases de PLA2s con PLA citosolica tipo IV2s (cPLA2s) parece ser responsable de liberar los ácidos grasos bajo muchas condiciones de activación celular. El CPLA2s act specifically on phospholipids that contain AA, EPA or GPLA at their SN2. cPLA2 también puede liberar el lisofosfolípido que se convierte en factor de activación de plaquetas.
Peroxidación y especies reactivas de oxígeno
A continuación, el ácido graso libre se oxigena a lo largo de cualquiera de varias vías; consulte la tabla Rutas. Las vías de los eicosanoides (vía lipoxigenasa o COX) añaden oxígeno molecular (O2). Aunque el ácido graso es simétrico, los eicosanoides resultantes son quirales; las oxidaciones se desarrollan con alta estereoselectividad (las oxidaciones enzimáticas se consideran prácticamente estereoespecíficas).
Cuatro familias de enzimas inician o contribuyen al inicio de la catálisis de ácidos grasos a eicosanoides:
- Cyclooxygenases (COXs): COX-1 y COX-2 inician el metabolismo del ácido araquidónico a prostanoides que contienen dos dobles lazos, es decir, las prostaglandinas (p. ej. PGE2), prostaciclinas (p.e. PGI2), y tromboxanes (p. ej. TXA2). Las dos enzimas COX también inician el metabolismo de: a) Ácido eicosapentaenoico, que tiene 5 lazos dobles en comparación con los 4 lazos dobles de ácido araquidónico, a prostanoide, prostaciclina y productos thromboxano que tienen tres lazos dobles, por ejemplo PGE3, PGI3, y TXA3 y b) Dihomo-γ-linolénico ácido, que tiene tres dobles lazos, a prostanoide, prostaciclina y los productos thromboxane que tienen sólo un doble lazo, por ejemplo PGE1, PGI1, y TXA1.
- Lipoxygenases (LOXs): 5-Lipoxygenasa (5-LOX o ALOX5) inicia el metabolismo del ácido araquidonico a ácido 5-hidroperoxieicosatetraenoico (5-HpETE) que luego puede ser reducido rápidamente a ácido 5-hidroxieicosatetraenoico (5-HETE) o metabolizado más a las leucotrinas (exio). De manera similar, 15-lipoxigenasa (15-lipoxygenasa 1, 15-LOX, 15-LOX1, o ALOX15) inicia el metabolismo del ácido araquidónico a 15-HpETE, 15-HETE, eoxinas, 8,15-dihidroxieicosatetraenoico ácido (i.e. 8,15-DiHETE) y 15-oxio Estas enzimas también inician el metabolismo de; a) Ácido eicosapentaenoico a análogos de los metabolitos ácido araquidónico que contienen 5 en lugar de cuatro lazos dobles, por ejemplo 5-hidroxieicosapentaenoico ácido (5-HEPE), LTB5, LTC5, 5-oxo-EPE, 15-HEPE y 12-HEPE; b) Los tres dobles ácido dihomo-γ-linolénico que contienen 3 dobles lazos, por ejemplo, ácido 8-hidroxi-eicosatrienoico (8-HETrE), 12-HETrE y 15-HETrE (este ácido graso no se puede convertir en leucotrines); y los tres dobles ácidos que contienen la unión (por ALOXperoricos) a 5- En las vías más estudiadas, ALOX5 metaboliza ácido eicosapentaenoico a ácido 5-hidroperoxieicosapentaenoico (5-HpEPE), 5-HEPE y LTB5, y 5-oxo-EPE, todos ellos menos activos que los análogos de ácido araquidónico. Dado que el ácido eicosapentaenoico compite con el ácido araquidonico para ALOX5, la producción de los metabolitos eicosapentaenonato conduce a una reducción en los metabolitos eicosatetraenonatos y por lo tanto la reducción en la señalización de estos últimos metabolitos. Los primeros productos monohidroperoxi y monohidroxi elaborados por las lipoxigenasas antes mencionadas tienen sus residuos hidroperosicos e hidroxilos colocados en los S configuración chiral y se denominan más correctamente 5S-HpETE, 5S-HETE, 12S-HpETE, 12S-HETE, 15S-HpETE y, 15S-HETE. ALOX12B (es decir, arachidonate 12-lipoxygenase, tipo 12R) formas R productos quirality, es decir, 12R-HpETE y 12R- Hola. Del mismo modo, ALOXE3 (es decir, epidermis-tipo lipoxygenase 3 o eLOX3) metaboliza el ácido araquidonico a 12R-HpETE y 12R-HETE; sin embargo, estos son productos menores que esta enzima forma sólo bajo un conjunto limitado de condiciones. ALOXE3 metaboliza preferentemente el ácido araquidónico a las hepoxilinas.
- Epoxigenasas: son enzimas citocromas P450 que generan epoxidas eicosanoides no clásicas derivadas de: a) Ácido araquidonico viz., 5,6-epoxi-eicosatrienoico ácido (5,6-EET), 8,9-EET, 11,12-EET y 14,15-EET (ver ácido epoxieicosatrienoico); b) Ácido eicosapentaenoico viz., 5,6,-epoxi-eicosatetraenoico ácido (5,6-EEQ), 8,9-EEQ, 11,12-EEQ, 14,15-EEQ y 17,18-EEQ (ver ácido epoxieicosatetraenoico); c) Dihomo-γ-linolenic acid viz., 8,9-epoxy-eicosadienoic acid (8,9-EpEDE), 11,12-EpEDE, and 14,15-EpEDE; and d) Ácido adrenico viz., 7,8-epox-eicosatrienoico ácido (7,8-EpETrR), 10,11-EpTrE, 13,14-EpTrE y 16,17-EpETrE. Todas estas epoxidas se convierten, a veces rápidamente, a sus metabolitos dihidroxi, por varias células y tejidos. Por ejemplo, 5,6-EET se convierte en ácido 5,6-dihidroxi-eicosatrienoico (5,6-DiHETrE), 8,9-EEQ a 8,9-dihidroxi-eicosatetraenoico (8,9-DiHETE, 11,12-EpEDE a 11,12-dihidroxiicosadienoico (11,12DiHED
- Cytochrome P450 microsome ω-hydroxylases: CYP4A11, CYP4A22, CYP4F2, y CYP4F3 metabolizan el ácido araquidonico principalmente a 20-hidroxieicosatetraenoico ácido (20-HETE) pero también a 16-HETE, 17-HETE, 18-HETE principalmente
Dos enzimas diferentes pueden actuar en serie sobre un AGPI para formar metabolitos más complejos. Por ejemplo, ALOX5 actúa con ALOX12 o COX-2 tratada con aspirina para metabolizar el ácido araquidónico en lipoxinas y con monooxigenasa(s) del citocromo P450, citocromo P450 bacteriano (en tejidos infectados) o COX2 tratada con aspirina para metabolizar el ácido eicosapentaenoico en E. resolvinas en serie (RvE) (ver Mediadores pro-resolutivos especializados). Cuando esto ocurre con enzimas ubicadas en diferentes tipos de células e implica la transferencia del producto de una enzima a una célula que utiliza la segunda enzima para producir el producto final, se denomina metabolismo transcelular o biosíntesis transcelular.
La oxidación de los lípidos es peligrosa para las células, especialmente cuando están cerca del núcleo. Existen mecanismos elaborados para prevenir la oxidación no deseada. La COX, las lipoxigenasas y las fosfolipasas están estrictamente controladas: hay al menos ocho proteínas activadas para coordinar la generación de leucotrienos. Varios de estos existen en múltiples isoformas.
La oxidación por COX o lipoxigenasa libera especies reactivas de oxígeno (ROS) y los productos iniciales en la generación de eicosanoides son en sí mismos peróxidos altamente reactivos. LTA4 puede formar aductos con el ADN tisular. Otras reacciones de las lipoxigenasas generan daño celular; Los modelos murinos implican a la 15-lipoxigenasa en la patogénesis de la aterosclerosis. La oxidación en la generación de eicosanoides está compartimentada; esto limita los peróxidos' daño. Las enzimas que son biosintéticas para los eicosanoides (p. ej., glutatión-S-transferasas, epóxido hidrolasas y proteínas transportadoras) pertenecen a familias cuyas funciones están involucradas en gran medida con la desintoxicación celular. Esto sugiere que la señalización de eicosanoides podría haber evolucionado a partir de la desintoxicación de ROS.
La célula debe obtener algún beneficio al generar hidroperóxidos lipídicos cerca de su núcleo. Las PG y LT pueden señalar o regular la transcripción del ADN allí; LTB4 es ligando de PPARα. (Ver diagrama en PPAR).
Vías de prostanoides
Tanto la COX1 como la COX2 (también denominadas prostaglandina-endoperóxido sintasa-1 (PTGS1) y PTGS2, respectivamente) metabolizan el ácido araquidónico añadiendo O2 molecular entre los carbonos 9 y 11 para formar un puente de endoperóxido entre estos dos carbonos, agregando O2 molecular al carbono 15 para producir un producto 15-hidroperoxi, creando un enlace carbono-carbono entre los carbonos 8 y 12 para crear un anillo de ciclopentano en el medio del ácido graso, y en el proceso de fabricación de PGG2, un producto que tiene dos dobles enlaces menos que el ácido araquidónico. Luego, el residuo 15-hidroperoxi de PGG2 se reduce a un residuo 15-hidroxilo, formando así PGH2. PGH2 es el prostanoide original de todos los demás prostanoides. Se metaboliza mediante (ver diagrama en Prostanoide): a) La vía de la prostaglandina E sintasa en la que cualquiera de las tres isoenzimas, PTGES, PTGES2 o PTGES3, convierte PGH2 en PGE2 (productos posteriores de esta vía incluyen PGA2 y PGB2 (ver Prostanoide § Biosíntesis de prostaglandinas); b) PGF sintasa que convierte PGH2 en PGF2α; c) Prostaglandina D2 sintasa que convierte PGH2 en PGD2 (los productos posteriores en esta vía incluyen 15-dPGJ2 (ver Prostaglandina ciclopentenona); d) Tromboxano sintasa que convierte PGH2 en TXA2 (los productos posteriores en esta vía incluyen TXB2); y e) Prostaciclina sintasa que convierte PGH2 en PGI2 (los productos posteriores en esta vía incluyen 6-ceto-PGFα. Se ha demostrado o, en algunos casos, se presume que estas vías metabolizan el ácido eicosapentaenoico en análogos de eicosanoides del sitio productos que tienen tres dobles enlaces en lugar de dos y por lo tanto contienen el número 3 en lugar de 2 adjunto a sus nombres (por ejemplo, PGE3 en lugar de PGE2).
Los productos PGE2, PGE1 y PGD2 formados en las vías recién citadas pueden sufrir una reacción de deshidratación espontánea para formar PGA2, PGA1 y PGJ2, respectivamente; Luego, PGJ2 puede sufrir una isomerización espontánea seguida de una reacción de deshidratación para formar en serie Δ12-PGJ2 y 15-desoxi-Δ12,14-PGJ2.
PGH2 tiene un anillo de 5 carbonos unido por oxígeno molecular. Sus PGS derivados han perdido este puente de oxígeno y contienen un único anillo insaturado de 5 carbonos con la excepción del tromboxano A2 que posee un anillo de 6 miembros que consta de un átomo de oxígeno y 5 átomos de carbono. El anillo de 5 carbonos de la prostaciclina está unido a un segundo anillo que consta de 4 átomos de carbono y un átomo de oxígeno. Y el anillo de cinco miembros de las prostaglandinas ciclopentenona posee un enlace insaturado en un sistema conjugado con un grupo carbonilo que hace que estas PG formen enlaces con una amplia gama de proteínas bioactivas (para obtener más información, consulte los diagramas en Prostanoid).
Vías del hidroxieicosatetraenoico (HERE) y de los leucotrienos (LT)
La enzima 5-lipoxigenasa (5-LO o ALOX5) convierte el ácido araquidónico en ácido 5-hidroperoxieicosatetraenoico (5-HPETE), que puede liberarse y reducirse rápidamente a ácido 5-hidroxieicosatetraenoico (5-HETE) mediante el omnipresente glutatión celular. -peroxidasas dependientes. Alternativamente, ALOX5 utiliza su actividad LTA sintasa para convertir 5-HPETE en leucotrieno A4 (LTA4). Luego, LTA4 se metaboliza a LTB4 por la leucotrieno A4 hidrolasa o leucotrieno C4 (LTC4) por la LTC4 sintasa o la glutatión S-transferasa 2 microsomal (MGST2). Cualquiera de las dos últimas enzimas actúa para unir el azufre del grupo tio (es decir, SH) de la cisteína en el tripéptido glutamato-cisteína-glicina al carbono 6 de LTA4, formando así LTC4. Después de la liberación de su célula madre, los residuos de glutamato y glicina de LTC4 se eliminan paso a paso mediante la gamma-glutamiltransferasa y una dipeptidasa para formar LTD4 y LTE4 secuencialmente. La decisión de formar LTB4 versus LTC4 depende del contenido relativo de LTA4 hidrolasa versus LTC4 sintasa (o glutatión S-transferasa en las células; los eosinófilos, mastocitos y macrófagos alveolares poseen niveles relativamente altos de LTC4 sintasa y, en consecuencia, forman LTC4 en lugar de o para en mucha mayor medida que LTB4. 5-LOX también puede funcionar en serie con oxigenasas del citocromo P450 o COX2 tratada con aspirina para formar resolvinas RvE1, RvE2 y 18S-RvE1 (consulte Mediadores proresolutivos especializados § resolvinas derivadas de EPA).
La enzima araquidonato 12-lipoxigenasa (12-LO o ALOX12) metaboliza el ácido araquidónico al estereoisómero S del ácido 12-hidroperoxieicosatetraenoico (12-HPETE), que se reduce rápidamente mediante peroxidasas celulares a < Es estereoisómero del ácido 12-hidroxieicosatetraenoico (12-HETE) o se metaboliza posteriormente a hepoxilinas (Hx), como HxA3 y HxB.
Las enzimas 15-lipoxigenasa-1 (15-LO-1 o ALOX15) y 15-lipoxigenasa-2 (15-LO-2, ALOX15B) metabolizan el ácido araquidónico al estereoisómero S de 15 -Ácido hidroperoxieicosatetraenoico (15(S)-HPETE), que se reduce rápidamente mediante peroxidasas celulares al estereoisómero S del ácido 15-hidroxieicosatetraenoico (15(S)-HETE). Las 15-lipoxigenasas (particularmente ALOX15) también pueden actuar en serie con 5-lipoxigenasa, 12-lipoxigenasa o COX2 tratada con aspirina para formar lipoxinas y epilipoxinas o con oxigenasas P450 o COX2 tratadas con aspirina. para formar Resolvin E3 (ver Mediadores pro-resolutivos especializados § resolvinas derivadas de la EPA).
Un subconjunto de ω-hidroxilasas unidas a microsomas del citocromo P450 (CYP450) metaboliza el ácido araquidónico a ácido 20-hidroxieicosatetraenoico (20-HETE) y ácido 19-hidroxieicosatetraenoico mediante una reacción de oxidación omega.
Vía del epoxi eicosanoide
Las epoxigenasas del citocromo P450 (CYP) humano, CYP1A1, CYP1A2, CYP2C8, CYP2C9, CYP2C18, CYP2C19, CYP2E1, CYP2J2 y CYP2S1 metabolizan el ácido araquidónico en ácidos epoxieicosatrienoicos (EET) no clásicos mediante la conversión de uno de los ácidos grasos. #39;s dobles enlaces a su epóxido para formar uno o más de los siguientes EET, 14,15-ETE, 11,12-EET, 8,9-ETE y 4,5-ETE. 14,15-EET y 11,12-EET son los principales EET producidos por tejidos de mamíferos, incluidos los humanos. Los mismos CYP, pero también CYP4A1, CYP4F8 y CYP4F12, metabolizan el ácido eicosapentaenoico en cinco ácidos epoxieicosatetraenoicos (EEQ), a saber, 17,18-EEQ, 14,15-EEQ, 11,12-EEQ. 8,9-EEQ y 5,6-EEQ.
Función, farmacología e importancia clínica
La tabla siguiente enumera un muestreo de los principales eicosanoides que poseen actividad biológica clínicamente relevante, los receptores celulares (ver Receptor de superficie celular) que estimulan o, cuando se señala, antagonizan para alcanzar esta actividad, algunas de las principales funciones que regulan (ya sea promover o inhibir) en los seres humanos y los modelos de ratón, y algunas de sus relevancias a las enfermedades humanas.
| Eicosanoide | Receptores dirigidos | Funciones reguladas | Relevancia clínica |
|---|---|---|---|
| PGE2 | PTGER1, PTGER2, PTGER3, PTGER4 | inflamación; fiebre; percepción del dolor; alodynia; parturición | Los NSAID inhiben su producción para reducir la inflamación, la fiebre y el dolor; utilizados para promover el trabajo en el parto; un abortivo |
| PGD2 | Prostaglandin DP1 receptor 1, Prostaglandin DP2 receptor | reacciones de alergia; alodynia; crecimiento del cabello | Los NSAID pueden apuntarlo a inhibir la alodynia y la pérdida de cabello masculina |
| TXA2 | Receptor de Thromboxane α y β | agregación de plaquetas de sangre; coagulación de sangre; reacciones alérgicas | Los NSAID inhiben su producción para reducir la incidencia de accidentes cerebrovasculares y ataques cardíacos |
| PGI2 | Receptor de prostaciclina | agregación de plaquetas, contracción muscular lisa vascular | análogos PGI2 usados para tratar trastornos vasculares como hipertensión pulmonar, síndrome de Raynaud y enfermedad de Buerger |
| 15-d-Δ12,14-PGJ2 | PPARγ, receptor Prostaglandin DP2 | inhibe la inflamación y el crecimiento celular | inhibe diversas respuestas inflamatorias en modelos animales; modelo estructural para el desarrollo de agentes antiinflamatorios |
| 20-HETE | ? | vasoconstricción, inhibe plaquetas | mutaciones inactivadoras en la enzima formadora 20-HETE, CYP2U1, asociada con paraplegia espástica hereditaria |
| 5-Oxo-ETE | OXER1 | factor quimiotáctico para y activador de eosinófilos | estudios necesarios para determinar si inhibir su producción o acción inhibe las reacciones alérgicas |
| LTB4 | LTB4R, LTB4R2 | factor químico para y activador de leucocitos; inflamación | estudios hasta la fecha no muestran beneficios claros de los antagonistas del receptor LTB4 para enfermedades inflamatorias humanas |
| LTC4 | CYSLTR1, CYSLTR2, GPR17 | permeabilidad vascular; contracción muscular lisa vascular; alergia | antagonistas de CYSLTR1 utilizados en asma, así como otras reacciones alérgicas y alérgicas |
| LTD4 | CYSLTR1, CYSLTR2, GPR17 | permeabilidad vascular; contracción muscular lisa vascular; alergia | antagonistas de CYSLTR1 utilizados en asma, así como otras reacciones alérgicas y alérgicas |
| LTE4 | GPR99 | aumenta la permeabilidad vascular y secreción de la mucina de la vía aérea | pensado para contribuir al asma así como otras reacciones alérgicas y alérgicas |
| LxA4 | FPR2 | inhibir las funciones de las células pro-inflamatorias | Clase de mediadores especializadas en solución de reacciones inflamatorias |
| LxB4 | FPR2, GPR32, AHR | inhibir las funciones de las células pro-inflamatorias | Clase de mediadores especializadas en solución de reacciones inflamatorias |
| RvE1 | CMKLR1, inhibe BLT, TRPV1, TRPV3, NMDAR, TNFR | inhibir las funciones de las células pro-inflamatorias | Clase de analgésicos de reacción inflamatoria especializada en la solución de problemas; también suprime la percepción del dolor |
| RvE2 | CMKLR1, antagonista receptor de BLT | inhibir las funciones de las células pro-inflamatorias | Clase de mediadores especializadas en solución de reacciones inflamatorias |
| 14,15-EET | ? | vasodilatación, inhibe plaquetas y células pro-inflamatorias | papel(s) en la enfermedad humana aún no probada |
Prostanoides
Se sabe que muchos de los prostanoides median los síntomas locales de inflamación: vasoconstricción o vasodilatación, coagulación, dolor y fiebre. La inhibición de la COX-1 y/o de las isoformas inducibles de la COX-2 es la característica distintiva de los AINE (medicamentos antiinflamatorios no esteroideos), como la aspirina. Los prostanoides también activan los miembros PPARγ de la familia de receptores hormonales nucleares esteroides/tiroideos e influyen directamente en la transcripción genética. Los prostanoides tienen muchas otras relevancias para la medicina clínica como evidencia de su uso, el uso de sus análogos farmacológicos más estables, del uso de sus antagonistas de receptores como se indica en el siguiente cuadro.
| Medicina | Tipo | Condiciones médicas o uso | Medicina | Tipo | Condiciones médicas o uso | |
|---|---|---|---|---|---|---|
| Alprostadil | PGE1 | Disfunción eréctil, manteniendo una patente ductus arteriosus en el feto | Beraprost | PGI1 analog | Hipertensión pulmonar, evitando lesiones por reperfusión | |
| Bimatoprost | PGF2α análogo | Glaucoma, hipertensión ocular | Carboprost | PGF2α análogo | Inducción laboral, abortivo en embarazos precoces | |
| Dinoprostone | PGE2 | Inducción laboral | Iloprost | PGI2 analog | Hipertensión arterial pulmonar | |
| Latanoprost | PGF2α análogo | Glaucoma, hipertensión ocular | Misoprostol | PGE1 analog | úlceras estomacales inducción laboral, abortifacient | |
| Travoprost | PGF2α análogo | Glaucoma, hipertensión ocular | U46619 | Más largo vivió TX analog Longer vivió TX analog | Investigación solamente |
Prostaglandinas ciclopentenona
PGA1, PGA2, PGJ2, Δ12-PGJ2 y 15-deox-Δ12,14-PGJ2 exhiben una amplia gama de acciones antiinflamatorias y de resolución de la inflamación en diversos modelos animales. Por lo tanto, parecen funcionar de manera similar a los mediadores pro-resolución especializados, aunque uno de sus mecanismos de acción, la formación de enlaces covalentes con proteínas de señalización clave, difiere de los de los mediadores pro-resolución especializados.
HETE y oxo-ETE
Como se indica en sus páginas individuales de Wikipedia, el ácido 5-hidroxieicosatetraenoico (que, al igual que el ácido 5-oxo-eicosatetraenoico, actúa a través del receptor OXER1), el ácido 5-oxo-eicosatetraenoico, el ácido 12-hidroxieicosatetraenoico, el ácido 15-hidroxieicosatetraenoico, y el ácido 20-hidroxieicosatetraenoico muestran numerosas actividades en células animales y humanas, así como en modelos animales, que están relacionadas, por ejemplo, con inflamación, reacciones alérgicas, crecimiento de células cancerosas, flujo sanguíneo a los tejidos y/o presión arterial. Sin embargo, aún no se ha demostrado su función y relevancia para la fisiología y patología humana.
Leucotrienos
Los tres leucotrienos cistenicos, LTC4, LTD4, y LTE4, son potentes broncoconstrictores, incrementadores de permeabilidad vascular en venulos postcapilares, y estimuladores de secreción mucosa que se liberan del tejido pulmonar de sujetos asmáticos expuestos a alérgenos específicos. Ellos juegan un papel fisiofisiológico en diversos tipos de reacciones inmediatas de hipersensibilidad. Medicamentos que bloquean su activación del receptor CYSLTR1 viz., montelukast, zafirlukast y pranlukast, se utilizan clínicamente como tratamiento de mantenimiento para el asma y rinitis inducidas por alérgenos; asma y rinitis inducidas por antiinflamatorios no esteroideos (véase la enfermedad respiratoria excerbada por aspirina) Cuando se combinan con la terapia antihistamínica, también parecen útiles para tratar enfermedades urticales como urticarias.
Lipoxinas y epilipoxinas
LxA4, LxB4, 15-epi-LxA4 y 15-epi-LXB4, al igual que otros miembros de la clase de eicosanoides mediadores especializados pro-resolución, poseen actividad antiinflamatoria y de resolución de inflamación. En un ensayo controlado aleatorio, AT-LXA4 y un análogo comparativamente estable de LXB4, 15R/S-metil-LXB4, redujeron la gravedad del eccema en un estudio de 60 bebés y, en otro estudio, La LXA4 inhalada disminuyó la broncoprovocación iniciada por LTC4 en pacientes con asma.
Eoxinas
Las eoxinas (EXC4, EXD4, EXE5) se describen recientemente. Estimulan la permeabilidad vascular en un sistema modelo endotelial vascular humano ex vivo, y en un pequeño estudio de 32 voluntarios, la producción de EXC4 por eosinófilos aislados de asmáticos graves e intolerantes a la aspirina fue mayor que la de voluntarios sanos y pacientes asmáticos leves; Se ha sugerido que estos hallazgos indican que las eoxinas tienen acciones proinflamatorias y, por lo tanto, están potencialmente involucradas en diversas reacciones alérgicas. La producción de eoxinas por las células de Reed-Sternburg también ha llevado a sugerir que están implicadas en la enfermedad de Hodgkins. Sin embargo, aún no se ha demostrado la importancia clínica de las eoxinas.
Metabolitos de resolvina del ácido eicosapentaenoico
RvE1, 18S-RvE1, RvE2 y RvE3, al igual que otros miembros de la clase de eicosanoides especializados en mediadores proresolutivos, poseen actividad antiinflamatoria y resolutiva de la inflamación. Un análogo sintético de RvE1 se encuentra en pruebas clínicas de fase III (consulte Fases de investigación clínica) para el tratamiento del síndrome del ojo seco basado en inflamación; Junto con este estudio, se están llevando a cabo otros ensayos clínicos (NCT01639846, NCT01675570, NCT00799552 y NCT02329743) que utilizan un análogo de RvE1 para tratar diversas afecciones oculares. RvE1 también se encuentra en estudios de desarrollo clínico para el tratamiento de enfermedades neurodegenerativas y pérdida auditiva.
Otros metabolitos del ácido eicosapentaenoico
Los metabolitos del ácido eicosapentaenoico que son análogos de sus homólogos prostanoides derivados del ácido araquidónico, HETE y LT incluyen: los prostanoides de la serie 3 (p. ej., PGE3, PGD3, PGF3α, PGI3 y TXA3), los ácidos hidroxieicosapentaenoicos (p. ej. 5-HEPE, 12-HEPE, 15-HEPE y 20-HEPE) y los LT de la serie 5 (por ejemplo, LTB5, LTC5, LTD5 y LTE5). Se ha demostrado o se cree que muchos de los prostanoides de la serie 3, los ácidos hidroxieicosapentaenoicos y la LT de la serie 5 son estimuladores más débiles de sus células y tejidos diana que sus análogos derivados del ácido araquidónico. Se proponen reducir las acciones de sus análogos derivados del aracidonato reemplazando su producción con análogos más débiles. No se han descrito homólogos de las eoxinas derivados del ácido eicosapentaenoico.
Epoxieicosanoides
Los ácidos epoxi eicosatrienoicos (o EET), y, presumiblemente, los ácidos epoxi eicosatetraenoicos, tienen acciones vasodilatadoras en el corazón, los riñones y otros vasos sanguíneos, así como en la reabsorción de sodio y agua por parte de los riñones, y actuar para reducir la presión arterial y las lesiones isquémicas y de otro tipo en el corazón, el cerebro y otros tejidos; también pueden actuar para reducir la inflamación, promover el crecimiento y la metástasis de ciertos tumores, promover el crecimiento de nuevos vasos sanguíneos, en el sistema nervioso central, regular la liberación de hormonas neuropeptídicas y en el sistema nervioso periférico inhibir o reducir la percepción del dolor.
Las series ω-3 y ω-6
La reducción de los eicosanoides derivados de AA y la actividad disminuida de los productos alternativos generados por los ácidos grasos ω-3 sirven como base para explicar algunos de los efectos beneficiosos de la mayor NIC-3 ingesta.
—Kevin Fritsche, Fatty Acids como Moduladores de la Respuesta Inmunitaria
El ácido araquidónico (AA; 20:4 ω-6) se encuentra a la cabeza de la "cascada del ácido araquidónico" – más de veinte vías de señalización mediadas por eicosanoides que controlan una amplia gama de funciones celulares, especialmente aquellas que regulan la inflamación, la inmunidad y el sistema nervioso central.
En la respuesta inflamatoria, otros dos grupos de ácidos grasos de la dieta forman cascadas que son paralelas y compiten con la cascada del ácido araquidónico. EPA (20:5 ω-3) proporciona la cascada competitiva más importante. DGLA (20:3 ω-6) proporciona una tercera cascada menos prominente. Estas dos cascadas paralelas suavizan los efectos inflamatorios de AA y sus productos. La ingesta dietética baja de estos ácidos grasos menos inflamatorios, especialmente los ω-3, se ha relacionado con varias enfermedades relacionadas con la inflamación y quizás con algunas enfermedades mentales.
Los Institutos Nacionales de Salud de EE. UU. y la Biblioteca Nacional de Medicina afirman que existe 'A' evidencia de nivel de que el aumento de ω-3 en la dieta mejora los resultados en la hipertrigliceridemia, la prevención de enfermedades cardiovasculares secundarias y la hipertensión. Hay 'B' nivel de evidencia ('buena evidencia científica') para un aumento de ω-3 en la dieta en la prevención primaria de enfermedades cardiovasculares, artritis reumatoide y protección contra la toxicidad de la ciclosporina en pacientes con trasplante de órganos. También señalan más evidencia preliminar que muestra que el ω-3 en la dieta puede aliviar los síntomas de varios trastornos psiquiátricos.
Además de la influencia sobre los eicosanoides, las grasas poliinsaturadas de la dieta modulan la respuesta inmune a través de otros tres mecanismos moleculares. Ellos (a) alterar la composición y función de la membrana, incluida la composición de las balsas lipídicas; (b) cambiar la biosíntesis de citoquinas; y (c) activar directamente la transcripción genética. De ellos, la acción sobre los eicosanoides es la mejor explorada.
Mecanismos de acción del ω-3
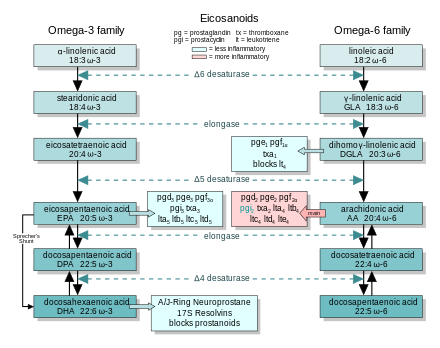
En general, los eicosanoides derivados de AA promueven la inflamación, y los de EPA y de GLA (vía DGLA) son menos inflamatorios, o inactivos, o incluso antiinflamatorios y pro-resolutivos.
La figura muestra las cadenas de síntesis ω-3 y -6, junto con los principales eicosanoides de AA, EPA y DGLA.
El ω-3 y el GLA en la dieta contrarrestan los efectos inflamatorios de los eicosanoides AA de tres maneras, a lo largo de las vías de los eicosanoides:
- Desplazamiento—Dietary ω-3 disminuye las concentraciones de tejido de AA, por lo que hay menos que formar ω-6 eicosanoides.
- Inhibición competitiva—DGLA y EPA compiten con AA para acceder a las enzimas de ciclooxigenasa y lipoxigenasa. Así que la presencia de DGLA y EPA en tejidos reduce la salida de los eicosanoides de AA.
- Lucha contra la—Algunos eicosanoides derivados de DGLA y EPA contrarrestan sus contrapartes derivadas de AA.
Papel en la inflamación
Desde la antigüedad, los signos cardinales de la inflamación se conocían como: calor (calor), dolor (dolor), tumor (hinchazón) y rubor (enrojecimiento). Los eicosanoides están implicados en cada uno de estos signos.
Enrojecimiento: la picadura de un insecto desencadenará la clásica respuesta inflamatoria. Los vasoconstrictores de acción corta (TXA2) se liberan rápidamente después de la lesión. El sitio puede palidecer momentáneamente. Entonces TXA2 media la liberación de los vasodilatadores PGE2 y LTB4. Los vasos sanguíneos se hinchan y la lesión enrojece.
Hinchazón: LTB4 hace que los vasos sanguíneos sean más permeables. El plasma se filtra hacia los tejidos conectivos y estos se hinchan. El proceso también pierde citocinas proinflamatorias.
Dolor: las citoquinas aumentan la actividad de la COX-2. Esto eleva los niveles de PGE2, sensibilizando las neuronas del dolor.
Calor: la PGE2 también es un potente agente pirético. La aspirina y los AINE (medicamentos que bloquean las vías de la COX y detienen la síntesis de prostanoides) limitan la fiebre o el calor de la inflamación localizada.
Historia
En 1930, el ginecólogo Raphael Kurzrok y el farmacólogo Charles Leib caracterizaron las prostaglandinas como un componente del semen. Entre 1929 y 1932, Burr y Burr demostraron que la restricción de grasas en las dietas animales conducía a una enfermedad carencial y describieron por primera vez los ácidos grasos esenciales. En 1935, von Euler identificó las prostaglandinas. En 1964, Bergström y Samuelsson vincularon estas observaciones cuando demostraron que el estilo "clásico" Los eicosanoides se derivaban del ácido araquidónico, que anteriormente se consideraba uno de los ácidos grasos esenciales. En 1971, Vane demostró que la aspirina y fármacos similares inhiben la síntesis de prostaglandinas. Von Euler recibió el Premio Nobel de Medicina en 1970, que Samuelsson, Vane y Bergström también lo recibieron en 1982. E. J. Corey lo recibió en química en 1990 en gran parte por su síntesis de prostaglandinas.