Efecto Leidenfrost
El efecto Leidenfrost es un fenómeno físico en el que un líquido, cerca de una superficie significativamente más caliente que el punto de ebullición del líquido, produce una capa de vapor aislante que evita que el líquido hirviendo rápidamente. Debido a esta fuerza de repulsión, una gota flota sobre la superficie, en lugar de hacer contacto físico con ella. El efecto lleva el nombre del médico alemán Johann Gottlob Leidenfrost, quien lo describió en Un tratado sobre algunas cualidades del agua común.
Esto se ve más comúnmente al cocinar, cuando se rocían gotas de agua sobre una sartén caliente. Si la temperatura de la sartén es igual o superior al punto de Leidenfrost, que es de aproximadamente 193 °C (379 °F) para el agua, el agua resbala por la sartén y tarda más en evaporarse que si las gotas de agua se hubieran evaporado. ha sido rociado sobre una bandeja más fría.
Detalles
El efecto se puede ver cuando se rocían gotas de agua sobre una sartén en varios momentos a medida que se calienta. Inicialmente, como la temperatura de la sartén está justo por debajo de los 100 °C (212 °F), el agua se aplana y se evapora lentamente, o si la temperatura de la sartén está muy por debajo de los 100 °C (212 °F), el agua permanece líquido. A medida que la temperatura de la sartén sube por encima de los 100 °C (212 °F), las gotas de agua silban al tocar la sartén y estas gotas se evaporan rápidamente. Cuando la temperatura supera el punto Leidenfrost, aparece el efecto Leidenfrost. Al entrar en contacto con la sartén, las gotas de agua se agrupan en pequeñas bolas de agua y se deslizan, durando mucho más que cuando la temperatura de la sartén era más baja. Este efecto funciona hasta que una temperatura mucho más alta hace que las gotas de agua se evaporen demasiado rápido para causar este efecto.
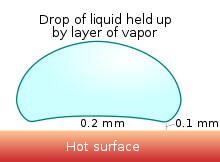
El efecto se produce porque, a temperaturas iguales o superiores al punto de Leidenfrost, la parte inferior de la gota de agua se vaporiza inmediatamente al entrar en contacto con la sartén caliente. El gas resultante suspende el resto de la gota de agua justo encima, evitando cualquier contacto directo entre el agua líquida y la sartén caliente. Como el vapor tiene una conductividad térmica mucho más pobre que la bandeja de metal, la transferencia de calor adicional entre la bandeja y la gota se ralentiza drásticamente. Esto también da como resultado que la gota pueda deslizarse alrededor de la bandeja sobre la capa de gas justo debajo.
La temperatura a la que aparece el efecto Leidenfrost es difícil de predecir. Incluso si el volumen de la gota de líquido sigue siendo el mismo, el punto de Leidenfrost puede ser bastante diferente, con una complicada dependencia de las propiedades de la superficie, así como de las impurezas del líquido. Se han realizado algunas investigaciones sobre un modelo teórico del sistema, pero es bastante complicado.
El efecto también fue descrito por el diseñador victoriano de calderas de vapor, William Fairbairn, en referencia a su efecto en la reducción masiva de la transferencia de calor de una superficie de hierro caliente al agua, como dentro de una caldera. En un par de conferencias sobre el diseño de calderas, citó el trabajo de Pierre Hippolyte Boutigny (1798-1884) y el profesor Bowman del King's College de Londres al estudiar esto. Una gota de agua que se vaporizó casi inmediatamente a 168 °C (334 °F) persistió durante 152 segundos a 202 °C (396 °F). Como resultado, las temperaturas más bajas en la cámara de combustión de una caldera podrían evaporar el agua más rápidamente; comparar el efecto Mpemba. Un enfoque alternativo fue aumentar la temperatura más allá del punto de Leidenfrost. Fairbairn también consideró esto, y puede haber estado contemplando la caldera de vapor flash, pero consideró que los aspectos técnicos eran insuperables en ese momento.
El punto de Leidenfrost también se puede tomar como la temperatura a la que la gota flotante dura más tiempo.
Se ha demostrado que es posible estabilizar la capa de vapor de agua de Leidenfrost explotando superficies superhidrofóbicas. En este caso, una vez que se establece la capa de vapor, el enfriamiento nunca colapsa la capa y no ocurre la ebullición nucleada; en cambio, la capa se relaja lentamente hasta que la superficie se enfría.
Las gotas de diferentes líquidos con diferentes temperaturas de ebullición también exhibirán un efecto Leidenfrost entre sí y se repelerán entre sí.
El efecto Leidenfrost se ha utilizado para el desarrollo de espectrometría de masas ambiental de alta sensibilidad. Bajo la influencia de la condición de Leidenfrost, la gota que levita no libera moléculas y las moléculas se enriquecen dentro de la gota. En el último momento de la evaporación de las gotas, todas las moléculas enriquecidas se liberan en un corto período de tiempo y, por lo tanto, aumentan la sensibilidad.
Se ha creado un prototipo de motor térmico basado en el efecto Leidenfrost; tiene la ventaja de una fricción extremadamente baja.
Punto de Leidenfrost
El punto de Leidenfrost significa el inicio de una película de ebullición estable. Representa el punto de la curva de ebullición donde el flujo de calor es mínimo y la superficie está completamente cubierta por una capa de vapor. La transferencia de calor de la superficie al líquido se produce por conducción y radiación a través del vapor. En 1756, Leidenfrost observó que las gotas de agua sostenidas por la película de vapor se evaporan lentamente a medida que se mueven sobre la superficie caliente. A medida que aumenta la temperatura de la superficie, la radiación a través de la película de vapor se vuelve más significativa y el flujo de calor aumenta al aumentar el exceso de temperatura.
El flujo de calor mínimo para una gran placa horizontal se puede derivar de la ecuación de Zuber,
donde se evalúan las propiedades a temperatura de saturación. Zuber es constante, , es aproximadamente 0.09 para la mayoría de los fluidos a presión moderada.
Correlaciones de transferencia de calor
El coeficiente de transferencia de calor se puede aproximar usando la ecuación de Bromley,
Donde es el diámetro exterior del tubo. La constante de correlación C es 0.62 para cilindros horizontales y placas verticales, y 0.67 para esferas. Las propiedades de vapor se evalúan a temperatura de película.
Para una película de ebullición estable sobre una superficie horizontal, Berenson ha modificado la ecuación de Bromley para producir,
Para tubos verticales, Hsu y Westwater han correlacionado la siguiente ecuación,
donde m es el flujo de masa en en el extremo superior del tubo.
A un exceso de temperatura por encima del flujo de calor mínimo, la contribución de la radiación se vuelve apreciable y se vuelve dominante a un alto exceso de temperatura. El coeficiente de transferencia de calor total es, por lo tanto, una combinación de los dos. Bromley ha sugerido las siguientes ecuaciones para la película de ebullición desde la superficie exterior de los tubos horizontales:
Si ,
El coeficiente de radiación eficaz, puede expresarse como:
Donde es la emisividad del sólido y es la constante Stefan-Boltzmann.
Campo de presión en una gota de Leidenfrost
La ecuación para el campo de presión en la región de vapor entre la gota y la superficie sólida se puede resolver usando las ecuaciones estándar de cantidad de movimiento y continuidad. En aras de la simplicidad en la resolución, se asume un perfil de temperatura lineal y un perfil de velocidad parabólico dentro de la fase de vapor. Se supone que la transferencia de calor dentro de la fase de vapor es por conducción. Con estas aproximaciones, las ecuaciones de Navier-Stokes se pueden resolver para obtener el campo de presión.
Efectos de la temperatura y la tensión superficial de Leidenfrost
La temperatura de Leidenfrost es la propiedad de un conjunto dado de pares sólido-líquido. La temperatura de la superficie sólida más allá de la cual el líquido sufre el fenómeno de Leidenfrost se denomina temperatura de Leidenfrost. El cálculo de la temperatura de Leidenfrost implica el cálculo de la temperatura mínima de ebullición de la película de un fluido. Berenson obtuvo una relación para la temperatura mínima de ebullición de la película a partir de argumentos de flujo de calor mínimo. Si bien la ecuación para la temperatura mínima de ebullición de la película, que se puede encontrar en la referencia anterior, es bastante compleja, sus características se pueden entender desde una perspectiva física. Un parámetro crítico a considerar es la tensión superficial. La relación proporcional entre la temperatura mínima de ebullición de la película y la tensión superficial es de esperar, ya que los fluidos con mayor tensión superficial necesitan mayores cantidades de flujo de calor para el inicio de la ebullición nucleada. Dado que la ebullición pelicular ocurre después de la ebullición nucleada, la temperatura mínima para la ebullición pelicular debe tener una dependencia proporcional de la tensión superficial.
Henry desarrolló un modelo para el fenómeno Leidenfrost que incluye humectación transitoria y evaporación de microcapas. Dado que el fenómeno de Leidenfrost es un caso especial de ebullición de película, la temperatura de Leidenfrost se relaciona con la temperatura mínima de ebullición de película a través de una relación que tiene en cuenta las propiedades del sólido que se utiliza. Si bien la temperatura de Leidenfrost no está directamente relacionada con la tensión superficial del fluido, depende indirectamente de ella a través de la temperatura de ebullición de la película. Para fluidos con propiedades termofísicas similares, el que tiene mayor tensión superficial generalmente tiene una temperatura Leidenfrost más alta.
Por ejemplo, para una interfaz saturada de agua y cobre, la temperatura de Leidenfrost es de 257 °C (495 °F). Las temperaturas de Leidenfrost para el glicerol y los alcoholes comunes son significativamente menores debido a sus valores más bajos de tensión superficial (las diferencias de densidad y viscosidad también son factores que contribuyen).
Efecto Leidenfrost reactivo
En 2015 se descubrió que los materiales no volátiles también exhibían un 'efecto Leidenfrost reactivo', en el que se observaba que las partículas sólidas flotaban sobre superficies calientes y se deslizaban de forma errática. Se completó la caracterización detallada del efecto Leidenfrost reactivo para pequeñas partículas de celulosa (~0,5 mm) en superficies pulidas a alta temperatura mediante fotografía de alta velocidad. Se demostró que la celulosa se descompone en oligómeros de cadena corta que se derriten y humedecen superficies lisas con una transferencia de calor creciente asociada con una temperatura superficial creciente. Por encima de 675 °C (1247 °F), se observó que la celulosa presentaba un punto de ebullición de transición con un burbujeo violento y una reducción asociada en la transferencia de calor. Se observó que el despegue de la gota de celulosa (representada a la derecha) se producía por encima de los 750 °C (1380 °F), asociado con una reducción drástica de la transferencia de calor.
También se demostró que la fotografía de alta velocidad del efecto Leidenfrost reactivo de la celulosa en superficies porosas (alúmina macroporosa) suprime el efecto Leidenfrost reactivo y mejora las tasas generales de transferencia de calor a la partícula desde la superficie. El nuevo fenómeno de un 'efecto Leidenfrost (RL) reactivo' se caracterizó por una cantidad adimensional, (φRL= τconv/τrxn), que relaciona la constante de tiempo de la transferencia de calor de partículas sólidas con la constante de tiempo de la reacción de las partículas, con el efecto Leidenfrost reactivo durante 10−1< φRL< 10+1. El efecto Leidenfrost reactivo con celulosa ocurrirá en numerosas aplicaciones de alta temperatura con polímeros de carbohidratos, incluida la conversión de biomasa en biocombustibles, la preparación y cocción de alimentos y el consumo de tabaco.
El efecto Leidenfrost también se ha utilizado como un medio para promover el cambio químico de varios líquidos orgánicos a través de su conversión por descomposición térmica en varios productos. Los ejemplos incluyen la descomposición de etanol, carbonato de dietilo y glicerol.
En la cultura popular
En el libro Michael Strogoff de Julio Verne de 1876, el protagonista se salva de ser cegado con una cuchilla caliente al evaporarse las lágrimas.
En el final de la temporada 7 de 2009 de MythBusters, "Mini Myth Mayhem", el equipo demostró que una persona puede mojarse la mano y sumergirla brevemente en plomo fundido sin lesionarse. utilizando el efecto Leidenfrost como base científica.
Contenido relacionado
Dispersión de rayos X de gran angular
Teoría cinética de los gases.
Electrodinámica cuántica




![{displaystyle {{frac {q}{A}}_{min}}=C{{h}_{fg}}{{rho }_{v}}{{left[{frac {sigma gleft({{rho }_{L}}-{{rho }_{v}}right)}{{left({{rho }_{L}}+{{rho }_{v}}right)}^{2}}}right]}^{{}^{1}!!diagup !!{}_{4};}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a94fba1cc42308142bf2448820f0cd14a1fdb86d)

![{displaystyle h=C{{left[{frac {k_{v}^{3}{{rho }_{v}}gleft({{rho }_{L}}-{{rho }_{v}}right)left({{h}_{fg}}+0.4{{c}_{pv}}left({{T}_{s}}-{{T}_{sat}}right)right)}{{{D}_{o}}{{mu }_{v}}left({{T}_{s}}-{{T}_{sat}}right)}}right]}^{{}^{1}!!diagup !!{}_{4};}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3f3d23ccc06ec9190f361d504cd6b982deeea09c)

![{displaystyle h=0.425{{left[{frac {k_{vf}^{3}{{rho }_{vf}}gleft({{rho }_{L}}-{{rho }_{v}}right)left({{h}_{fg}}+0.4{{c}_{pv}}left({{T}_{s}}-{{T}_{sat}}right)right)}{{{mu }_{vf}}left({{T}_{s}}-{{T}_{sat}}right){sqrt {sigma /gleft({{rho }_{L}}-{{rho }_{v}}right)}}}}right]}^{{}^{1}!!diagup !!{}_{4};}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f0c9bf294fc90d5b0b54986a8bd1b4684966917b)
![{displaystyle h{{left[{frac {mu _{v}^{2}}{g{{rho }_{v}}left({{rho }_{L}}-{{rho }_{v}}right)k_{v}^{3}}}right]}^{{}^{1}!!diagup !!{}_{3};}}=0.0020{{left[{frac {4m}{pi {{D}_{v}}{{mu }_{v}}}}right]}^{0.6}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/315bcfe771ba9265972a7431972f7de1ab2fd75b)








