Efecto anomérico
En química orgánica, el efecto anomérico o efecto Edward-Lemieux es un efecto estereoelectrónico que describe la tendencia de los sustituyentes heteroatómicos adyacentes a un heteroátomo dentro de un anillo de ciclohexano a preferir la orientación axial en lugar de la orientación ecuatorial menos obstaculizada que se esperaría de consideraciones estéricas.. Este efecto fue observado originalmente en los anillos de piranosa por JT Edward en 1955 cuando estudiaba la química de los carbohidratos.
El término efecto anomérico se introdujo en 1958. El nombre proviene del término utilizado para designar el carbono del anillo con el número más bajo de una piranosa, el carbono anomérico. Los isómeros que difieren únicamente en la configuración del carbono anomérico se denominan anómeros. Los anómeros de D -glucopiranosa son diastereómeros, con el anómero beta que tiene un grupo OH apuntando hacia arriba ecuatorialmente, y el anómero alfa que tiene ese grupo OH apuntando hacia abajo axialmente.
El efecto anomérico también se puede generalizar a cualquier ciclohexilo o sistema lineal con la fórmula general CYCX, donde Y es un heteroátomo con uno o más pares solitarios y X es un átomo o grupo electronegativo. La magnitud del efecto anomérico se estima en alrededor de 1 a 2 kcal/mol en el caso de los azúcares, pero es diferente para cada molécula.

En el caso anterior, el grupo metoxi en el anillo de ciclohexano (arriba) prefiere la posición ecuatorial. Sin embargo, en el anillo de tetrahidropirano (abajo), el grupo metoxi prefiere la posición axial. Esto se debe a que en el anillo de ciclohexano, Y = carbono, que no es un heteroátomo, por lo que no se observa el efecto anomérico y los estéricos dominan la posición del sustituyente observado. En el anillo de tetrahidropirano, Y= oxígeno, que es un heteroátomo, por lo que el efecto anomérico contribuye y estabiliza la posición del sustituyente observado. En ambos casos, X= OMe.
El efecto anomérico se observa con mayor frecuencia cuando Y = oxígeno, pero también se puede ver con otros heteroátomos que contienen pares solitarios en el anillo, como nitrógeno, azufre y fósforo. El método exacto por el cual el efecto anomérico provoca la estabilización es un punto de controversia y se han propuesto varias hipótesis para explicarlo.
Explicación física y controversia
La razón física del efecto anomérico no se entiende completamente. Se han ofrecido varias explicaciones, en parte contradictorias, y el tema aún no está resuelto.
Hiperconjugación
Moléculas cíclicas
Una explicación ampliamente aceptada es que existe una interacción estabilizadora (hiperconjugación) entre el par de electrones no compartidos en el heteroátomo endocíclico (dentro del anillo de azúcar) y el orbital σ* del enlace C-X axial (exocíclico). Esto hace que la molécula alinee el par solitario donante de electrones antiperiplanar (180°) con el enlace exocíclico CX σ, reduciendo la energía general del sistema y provocando una mayor estabilidad.

Algunos autores también cuestionan la validez de este modelo de hiperconjugación basándose en los resultados de la teoría cuántica de átomos en moléculas. Si bien la mayoría de los estudios sobre los efectos anoméricos han sido de naturaleza teórica, la hipótesis n–σ* (hiperconjugación) también ha sido ampliamente criticada sobre la base de que la redistribución de la densidad de electrones en los acetales propuesta por esta hipótesis no es congruente con la química experimental conocida de acetales y, en particular, la química de los monosacáridos.
Moléculas acíclicas
La hiperconjugación también se encuentra en moléculas acíclicas que contienen heteroátomos, otra forma del efecto anomérico. Si una molécula tiene un átomo con un solo par de electrones y el átomo adyacente puede aceptar electrones en el orbital σ*, se produce una hiperconjugación que estabiliza la molécula. Esto forma una forma de resonancia "sin unión". Para que se produzca esta superposición de orbitales, se prefiere la conformación trans, trans para la mayoría de los heteroátomos; sin embargo, para que se produzca la estabilización en el dimetoximetano, la conformación gauche, gauche tiene aproximadamente 3–5 kcal/mol menos de energía (más estable) que la trans, transconformación: esto es aproximadamente dos veces mayor que el efecto en los azúcares porque hay dos enlaces giratorios (por lo tanto, es trans alrededor de ambos enlaces o torpe alrededor de ambos) que se ven afectados.

Minimización de dipolos
Otra explicación aceptada para el efecto anomérico es que la configuración ecuatorial tiene los dipolos que involucran a ambos heteroátomos parcialmente alineados y, por lo tanto, se repelen entre sí. Por el contrario, la configuración axial tiene estos dipolos aproximadamente opuestos, lo que representa un estado de energía más estable y más bajo.

Tanto la hiperconjugación como la minimización del dipolo contribuyen a la conformación (Z) preferida de los ésteres sobre la conformación (E). En la conformación (Z), el par solitario de electrones en el oxígeno alfa puede donarse al orbital σ* CO vecino. Además, el dipolo se minimiza en la conformación (Z) y se maximiza en la conformación (E).

Nn repulsiones y enlaces de hidrógeno CH
Si se muestran los pares de electrones solitarios en los oxígenos en el centro anomérico del 2-metoxipirano, un breve examen de las conformaciones de los anómeros revela que el anómero β siempre tiene al menos un par de electrones eclipsantes (coplanar 1,3- interactuando) pares solitarios, esta nn repulsión es una situación de alta energía. Por otro lado, el anómero α tiene conformaciones en las que no hay repulsiones nn, y eso es cierto en la conformación exoanomérica. Se ha sugerido la repulsión nn energéticamente desfavorable presente en el anómero β, junto con el enlace de hidrógeno energéticamente favorable entre el H-5 axial y un par solitario de electrones en el sustituyente anomérico α axial (enlace de hidrógeno CH/n). referencias 7 y 8] para dar cuenta de la mayor parte de la diferencia energética entre los anómeros, el efecto anomérico.
Influencias
Si bien el efecto anomérico es una explicación general para este tipo de estabilización de una molécula, el tipo y la cantidad de estabilización pueden verse afectados por los sustituyentes que se examinan, así como por el solvente que se estudia.
Efecto sustituyente
En un sistema cerrado, se observa una diferencia en el efecto anomérico para diferentes sustituyentes en un anillo de ciclohexano o tetrahidropirano (Y = Oxígeno). Cuando X=OH, se puede ver el efecto anomérico genérico, como se explicó anteriormente. Cuando X=CN, se observan los mismos resultados, donde se prefiere la posición ecuatorial en el anillo de ciclohexano, pero se prefiere la posición axial en el anillo de tetrahidropirano. Esto es consistente con la estabilización del efecto anomérico. Cuando X=F, el efecto anomérico se observa de hecho para ambos anillos. Sin embargo, cuando X=NH 2, no se observa estabilización por efecto anomérico y ambos sistemas prefieren la posición ecuatorial. Esto se atribuye tanto a estéricos como a un efecto llamado efecto anomérico inverso (ver más abajo).
Efecto solvente
Una crítica común a la teoría de la hiperconjugación es que no explica por qué no se observa el efecto anomérico cuando las moléculas de tetrahidropirano sustituidas se colocan en disolventes polares, y se prefiere una vez más la posición ecuatorial. Sin embargo, se ha demostrado que la hiperconjugación depende del disolvente del sistema. Cada uno de los sistemas sustituidos descritos anteriormente se ensayó en fase gaseosa (es decir, sin disolvente) y en solución acuosa (es decir, disolvente polar). Cuando X=F, el efecto anomérico se observó en ambos medios, y siempre se prefirió la posición axial. Esto se atribuye a la hiperconjugación. Cuando X=OH o CN, el efecto anomérico se observó en la fase gaseosa, cuando se prefirió la posición axial. Sin embargo, en soluciones acuosas, ambos sustituyentes prefirieron la posición ecuatorial. Esto se atribuye al hecho de que hay más repulsiones electrostáticas con el sustituyente en posición axial y el disolvente polar, lo que hace que se prefiera la posición ecuatorial. Cuando X=NH2, de nuevo, no se observó ningún efecto anomérico y siempre se prefirió la posición ecuatorial.
Superando el efecto anomérico
Si bien el efecto anomérico puede causar la estabilización de las moléculas, tiene una magnitud para su estabilización, y este valor puede ser superado por otros efectos más desestabilizadores en algunos casos.
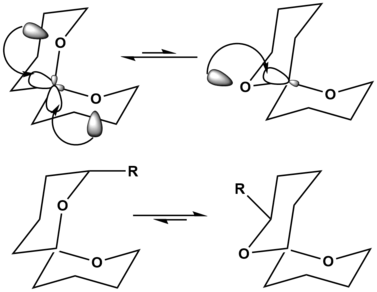
En el ejemplo de las espirocetales, la orientación de la parte superior izquierda muestra la estabilización por el efecto anomérico hiperconjugativo dos veces, lo que estabiliza en gran medida la orientación de la molécula. La orientación en la parte superior derecha solo muestra esta estabilización anomérica hiperconjugativa una vez, lo que hace que sea la estructura menos preferida. Sin embargo, cuando se añaden sustituyentes al esqueleto de espirocetas, se puede cambiar la estructura más preferida. Cuando se agrega un sustituyente grande al esqueleto de la espirocetal, como se ve en la parte inferior izquierda, la tensión de tener este sustituyente grande, R, en la posición axial desestabiliza en gran medida a la molécula. En la molécula de la parte inferior derecha, R ahora está en la posición ecuatorial, lo que ya no causa desestabilización en la molécula. Por lo tanto, sin sustituyentes,
Efecto exoanomérico
Una extensión del efecto anomérico, el efecto exoanomérico es la preferencia de los sustituyentes que salen de un anillo para adoptar la conformación gauche, mientras que los estéricos sugerirían que se preferiría una conformación antiperiplanar.

Un ejemplo de esto es el 2-metoxitetrahidropirano. Como predice el efecto anomérico, el sustituyente metoxi muestra una mayor preferencia por la conformación axial. Sin embargo, en realidad hay más de una posible conformación axial debido a la rotación alrededor del enlace CO entre el sustituyente metoxi y el anillo. Cuando se aplican los principios del efecto anomérico inverso, se puede predecir que se prefiere el confórmero gauche, lo que sugiere que la conformación superior izquierda es la mejor en la figura anterior. Esta predicción está respaldada por evidencia experimental. Además, esta preferencia por la posición gauche todavía se ve en la conformación ecuatorial.
Efecto anomérico inverso
Este término se refiere a la preferencia aparente de los sustituyentes de nitrógeno con carga positiva para la conformación ecuatorial más allá de lo que predecirían las interacciones estéricas normales en anillos que contienen un átomo electronegativo, como el oxígeno. Los sustituyentes que contienen carbonos con cargas parciales positivas no muestran el mismo efecto. Las explicaciones teóricas para el efecto anomérico inverso incluyen una explicación electrostática y la deslocalización de los electrones sp del par solitario de carbono y oxígeno anomérico. Existe cierto debate sobre si esto es o no un fenómeno real. Los sustituyentes que contienen nitrógeno con los que se ha informado son bastante voluminosos, lo que dificulta separar los efectos normales del volumen estérico y el efecto anomérico inverso, si es que existe. Por ejemplo, en la molécula que se muestra a continuación, el sustituyente de piridinio prefiere fuertemente la posición ecuatorial, como lo predecirían los factores estéricos, pero en realidad muestra una preferencia más fuerte por esta conformación de lo previsto, lo que sugiere que está contribuyendo el efecto anomérico inverso.

Efecto metalo-anomérico
Los metales de transición tardíos de los grupos 10, 11 y 12 cuando se colocan en el carbono anomérico muestran fuertes preferencias axiales. Este fenómeno denominado efecto metaloanomérico se origina a partir de la estabilización de las interacciones hiperconjugativas entre el oxígeno u otros heteroátomos con pares solitarios y orbitales de antienlace CM que actúan como buenos aceptores. El efecto metaloanomérico generalizado se refiere a la estabilización termodinámica de los confórmeros sinclinales de compuestos con la fórmula general M-CH 2 -OR. Las preferencias axiales/ecuatoriales pueden verse influenciadas por ligandos unidos al metal y la configuración electrónica. En términos generales, al pasar de un elemento más ligero a uno más pesado en el grupo, la magnitud del efecto metaloanomérico aumenta. Además, los estados de oxidación más altos favorecen los conformadores axiales/sinclinales.
Aplicaciones sintéticas
El efecto anomérico se tiene en cuenta sintéticamente. Debido a su descubrimiento en azúcares, la química de azúcares y carbohidratos es uno de los usos sintéticos más comunes del efecto anomérico. Por ejemplo, la glucosidación de Koenigs-Knorr instala un grupo α-OR o β-OR en alta diastereoselectividad que se efectúa por el efecto anomérico. La lactona soforolípida, (+)-lepicidina A y (-)-litospermósido son algunos de los productos sintetizados a través de la glucosidación de Koenigs-Knorr que superan el efecto anomérico.

Contenido relacionado
Postulado de Hammond
Lantano
Radical metilo