Difluoruro de xenón
El difluoruro de xenón es un potente agente fluorante con la fórmula química XeF
2, y uno de los compuestos de xenón más estables. Como la mayoría de los fluoruros inorgánicos covalentes, es sensible a la humedad. Se descompone al contacto con vapor de agua, pero por lo demás es estable durante el almacenamiento. El difluoruro de xenón es un sólido cristalino, denso e incoloro.
Tiene un olor nauseabundo y baja presión de vapor.
Estructura
El difluoruro de xenón es una molécula lineal con una longitud de enlace Xe–F de 197,73±0,15 pm en la fase de vapor y 200 pm en la fase sólida. La disposición de empaquetamiento en el sólido XeF
2 muestra que los átomos de flúor de las moléculas vecinas evitan la región ecuatorial de cada XeF
2 molécula. Esto concuerda con la predicción de la teoría VSEPR, que predice que hay 3 pares de electrones no enlazantes alrededor de la región ecuatorial del átomo de xenón.
A altas presiones, se pueden obtener nuevas formas no moleculares de difluoruro de xenón. Bajo una presión de ~50 GPa, XeF
2 se transforma en un semiconductor que consiste en XeF
4 unidades unidas en una estructura bidimensional, como el grafito. A presiones aún más altas, por encima de 70 GPa, se vuelve metálico y forma una estructura tridimensional que contiene XeF
8 unidades. Sin embargo, un estudio teórico reciente ha puesto en duda estos resultados experimentales.
Los enlaces Xe–F son débiles. XeF2 tiene una energía de enlace total de 267,8 kJ/mol (64,0 kcal/mol), con energías de enlace primera y segunda de 184,1 kJ/mol (44,0 kcal/mol) y 83,68 kJ/mol (20,00 kcal/mol), respectivamente. Sin embargo, XeF2 es mucho más robusto que KrF2, que tiene una energía de enlace total de solo 92,05 kJ/mol (22,00 kcal/mol).
Química
Síntesis
La síntesis se lleva a cabo mediante la reacción simple:
- Xe + F2 → XeF2
La reacción requiere calor, irradiación o una descarga eléctrica. El producto es un sólido. Se purifica mediante destilación fraccionada o condensación selectiva utilizando una línea de vacío.
El primer informe publicado sobre el XeF2 fue en octubre de 1962 por Chernick et al. Sin embargo, aunque se publicó más tarde, probablemente el XeF2 fue creado por primera vez por Rudolf Hoppe en la Universidad de Münster, Alemania, a principios de 1962, mediante la reacción de mezclas de gases de flúor y xenón en una descarga eléctrica. Poco después de estos informes, Weeks, Chernick y Matheson del Laboratorio Nacional de Argonne informaron sobre la síntesis del XeF2 utilizando un sistema totalmente de níquel con ventanas de alúmina transparente, en el que partes iguales de gases de xenón y flúor reaccionan a baja presión tras la irradiación con una fuente ultravioleta para dar XeF2. Williamson informó que la reacción funciona igualmente bien a presión atmosférica en un bulbo de vidrio Pyrex seco utilizando la luz solar como fuente. Se observó que la síntesis funcionaba incluso en días nublados.
En las síntesis anteriores, el reactivo gaseoso de flúor se había purificado para eliminar el fluoruro de hidrógeno. Šmalc y Lutar descubrieron que si se omite este paso, la velocidad de reacción avanza a un ritmo cuatro veces superior al original.
En 1965, también se sintetizó mediante la reacción del gas xenón con difluoruro de dioxígeno.
Solubility
XeF
2 es soluble en solventes como BrF5, BrF3, IF5, fluoruro de hidrógeno anhidro y acetonitrilo, sin reducción ni oxidación. La solubilidad en fluoruro de hidrógeno es alta, 167 g por 100 g de HF a 29,95 °C.
Compuestos xenones degradados
Otros compuestos de xenón pueden derivarse del difluoruro de xenón. El compuesto organoxenón inestable Xe(CF3
3)
2 se puede fabricar irradiando hexafluoroetano para generar CF•
3 radicales y pasar el gas sobre XeF
2. El sólido blanco ceroso resultante se descompone completamente en 4 horas a temperatura ambiente.
El catión XeF+ se forma combinando difluoruro de xenón con un fuerte aceptor de fluoruro, como un exceso de pentafluoruro de antimonio líquido (SbF
5):
- XeF
2 + SbF
5 → XeF+
+ SbF−
6
Añadir gas xenón a esta solución de color amarillo pálido a una presión de 2 a 3 atmósferas produce una solución verde que contiene el ion paramagnético Xe+
2, que contiene un enlace Xe−Xe: ("apf" denota solución en SbF
5)
- 3 Xeg) + XeF+
(apf) + SbF
5l) ⇌ 2 Xe+
2(apf) + SbF−
6(apf)
Esta reacción es reversible; al eliminar el gas xenón de la solución, el ion Xe+
2 se convierte en gas xenón y XeF+
, y el color de la solución vuelve a ser amarillo pálido.
En presencia de HF líquido, se pueden precipitar cristales de color verde oscuro a partir de la solución verde a -30 °C:
- Xe+
2(apf) + 4 SbF−
6(apf) → Xe+
2Sb
4F−
21s) + 3 F−
(apf)
La cristalografía de rayos X indica que la longitud del enlace Xe–Xe en este compuesto es de 309 pm, lo que indica un enlace muy débil. El ion Xe+
2 es isoelectrónico con el ion I−
2 ion, que también es verde oscuro.
Química de coordinación
El enlace en la molécula de XeF2 se describe adecuadamente mediante el modelo de enlace de tres centros y cuatro electrones.
El XeF2 puede actuar como ligando en complejos de coordinación de metales. Por ejemplo, en solución de HF:- Mg(AsF6)2 + 4 XeF2 → [Mg(XeF2)4[AsF]6)2
El análisis cristalográfico muestra que el átomo de magnesio está coordinado con 6 átomos de flúor. Cuatro de los átomos de flúor se atribuyen a los cuatro ligandos de difluoruro de xenón, mientras que los otros dos son un par de ligandos cis-AsF−
6.
Una reacción similar es:
- Mg(AsF6)2 + 2 XeF2 → [Mg(XeF2)2[AsF]6)2
En la estructura cristalina de este producto, el átomo de magnesio está coordinado octaédricamente y los ligandos XeF2 son axiales, mientras que los ligandos AsF−
6 son ecuatoriales.
Se han observado muchas reacciones similares con productos de la forma [Mx(XeF2)n](AF6)x, donde M puede ser calcio, estroncio, bario, plomo, plata, lantano o neodimio y A puede ser arsénico, antimonio o fósforo.
En 2004 se publicaron los resultados de la síntesis de un solvato en el que parte de los centros catiónicos estaban coordinados únicamente por átomos de flúor XeF2. La reacción puede escribirse como:
- 2 Ca(AsF)6)2 + 9 XeF2 → Ca2(XeF2)9(AsF6)4.
Esta reacción requiere un gran exceso de difluoruro de xenón. La estructura de la sal es tal que la mitad de los iones Ca2+ están coordinados por átomos de flúor del difluoruro de xenón, mientras que los otros iones Ca2+ están coordinados tanto por XeF2 como por AsF−
6.
Aplicaciones
Como agente de fluoración
El difluoruro de xenón es un potente agente oxidante y fluorante. Con aceptores de iones de fluoruro, forma XeF+
y Xe
2F+
3 especies que son fluoradores aún más potentes.
Entre las reacciones de fluoración que sufre el difluoruro de xenón se encuentran:
- fluoración oxidativa:
- Ph3TeF + XeF2 → Ph3TeF3 + Xe
- Fluoración reductiva:
- 2 CrO2F2 + XeF2 → 2 CrOF3 + Xe +O2
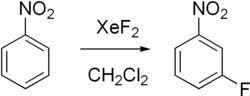
- Fluoración aromática:
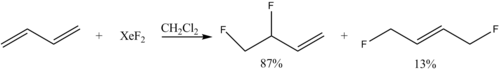
- Fluoración de Alkene:
- Fluoración radical en reacciones radicales de fluoración desencarboxilativa, en reacciones tipo Hunsdiecker donde se utiliza el difluoruro xenón para generar el intermedio radical así como la fuente de transferencia fluorina, y en la generación de radicales aryl de silanes aryl:
XeF
2 es selectivo en cuanto al átomo que fluora, lo que lo convierte en un reactivo útil para fluorar heteroátomos sin tocar otros sustituyentes en compuestos orgánicos. Por ejemplo, fluora el átomo de arsénico en la trimetilarsina, pero deja intactos los grupos metilo:
- (CH)
3)
3As + XeF
2 → (CH)
3)
3AsF
2 + Xe
XeF2 también se puede utilizar para preparar sales de N-fluoroamonio, útiles como reactivos de transferencia de flúor en síntesis orgánica (por ejemplo, Selectfluor), a partir de la amina terciaria correspondiente:
- [R](CH)2CH2)3N:[ ]BF−
4+ XeF2 + NaBF4 [R](CH)2CH2)3-F.BF−
4]2 + NaF + Xe
XeF
2 también descarboxilará oxidativamente los ácidos carboxílicos a los fluoroalcanos correspondientes:
- RCOOH + XeF2 → RF + CO2 + Xe + HF
Se ha descubierto que el tetrafluoruro de silicio actúa como catalizador en la fluoración por XeF
2.
Como un etchant
El difluoruro de xenón también se utiliza como agente de grabado gaseoso isotrópico para silicio, en particular en la producción de sistemas microelectromecánicos (MEMS), como se demostró por primera vez en 1995. Los sistemas comerciales utilizan el grabado por pulsos con una cámara de expansión. Brazzle, Dokmeci, et al. describen este proceso:
El mecanismo del grabado es el siguiente. En primer lugar, el XeF2 se adsorbe y se disocia en átomos de xenón y flúor en la superficie del silicio. El flúor es el principal agente de grabado en el proceso de grabado del silicio. La reacción que describe el silicio con XeF2 es
- 2 XeF2 + Si → 2 Xe + SiF4
Referencias
- ^ a b c d e Melita Tramšek; Boris Žemva (2006). "Sintesis, propiedades y química del fluoruro Xenon(II)" (PDF). Acta Chim. Slov. 53 (2): 105–116. doi:10.1002/chin.200721209.
- ^ Hindermann, D. K., Falconer, W. E. (1969). "Escudo magnético de 19F en XeF2". J. Chem. Phys. 50 (3): 1203. Bibcode:1969JChPh..50.1203H. doi:10.1063/1.1671178.
{{cite journal}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ a b Zumdahl, Steven S. (2009). Principios químicos 6o Ed. Houghton Mifflin Company. p. A23. ISBN 978-0-618-94690-7.
- ^ "Sigma Aldrich Xenon Difluoride SDS". Sigma Aldrich. Millpore Sigma. Retrieved 2 de noviembre 2022.
- ^ "MSDS: xenon difluoride" (PDF). BOC Gases. Retrieved 2010-06-01.
- ^ James L. Weeks; Max S. Matheson (1966). "Xenon Difluoride". Síntesis inorgánica. Vol. 8. pp. 260–264. doi:10.1002/9780470132395.ch69. ISBN 9780470132395.
{{cite book}}:|journal=ignorado (ayuda) - ^ Kim, M.; Debessai, M.; Yoo, C. S. (2010). "Two- and three-dimensional extended solids and metallization of comprimido XeF2". Química Naturaleza. 2 (9): 784–788. Código:2010NatCh...2..784K. doi:10.1038/nchem.724. PMID 20729901.
- ^ Kurzydłowski, D.; Zaleski-Ejgierd, P.; Grochala, W.; Hoffmann, R. (2011). "Freezing in Resonance Structures for Better Packing: XeF2Becomes (XeF+)(F−) at Large Compression". Química Inorgánica. 50 (8): 3832–3840. doi:10.1021/ic200371a. PMID 21438503.
- ^ Cockett, A. H.; Smith, K. C.; Bartlett, Neil (2013). La química de los gases monotómicos. Textos pergamones en química inorgánica. St. Louis, MO: Elsevier Science. ISBN 9781483157368. OCLC 953379200.
- ^ Tius, M. A. (1995). "Difluoruro xenón en síntesis". Tetraedro. 51 (24): 6605–6634. doi:10.1016/0040-4020(95)00362-C.
- ^ Chernick, CL y Claassen, HH y Fields, PR y Hyman, HH y Malm, JG y Manning, WM y Matheson, MS y Quarterman, LA y Schreiner, F. y Selig, HH; et al. (1962). "Fluorine Compounds of Xenon and Radon". Ciencia. 138 136-138. Bibcode:1962Sci...138..136C. doi:10.1126/science.138.3537.136. PMID 17818399. S2CID 10330125.
{{cite journal}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ Hoppe, R.; Daehne, W.; Mattauch, H.; Roedder, K. (1962). "Fluoración de Xenon". Angew. Chem. Ed Engl. 1 11): 599. doi:10.1002/anie.196205992.
- ^ Hoppe, R. (1964). "Die Valenzverbindungen der Edelgase". Angewandte Chemie. 76 (11): 455. Bibcode:1964AngCh.76..455H. doi:10.1002/ange.19640761103. Primera revisión sobre el tema por el pionero de compuestos de gas noble covalente.
- ^ Weeks, J.; Matheson, M.; Chernick, C. (1962). "Preparación fotoquímica de Difluoruro Xenon" Preparación fotoquímica de Difluoruro Xenon". J. Am. Chem. Soc. 84 (23): 4612–4613. doi:10.1021/ja00882a063.
- ^ Williamson, Stanley M.; Sladky, Friedrich O.; Bartlett, Neil (1968). "Xenon Difluoride". Síntesis inorgánica. Vol. 11. pp. 147–151. doi:10.1002/9780470132425.ch31. ISBN 9780470132425.
{{cite book}}:|journal=ignorado (ayuda) - ^ Šmalc, Andrej; Lutar, Karel; Kinkead, Scott A. (2007). "Xenon Difluoride (Modification)". Síntesis inorgánica. Vol. 29. pp. 1–4. doi:10.1002/9780470132609.ch1. ISBN 9780470132609.
{{cite book}}:|journal=ignorado (ayuda) - ^ Morrow, S. I.; Young, A. R. (1965). "La reacción de Xenon con Dioxygen Difluoride. Un nuevo método para la síntesis de Difluoruro Xenon". Química Inorgánica. 4 (5): 759-760. doi:10.1021/ic50027a038.
- ^ a b Harding, Charlie; Johnson, David Arthur; Janes, Rob (2002). Elementos de los p bloque. Sociedad Real de Química, Universidad Abierta. ISBN 978-0-85404-690-4.
- ^ Brown, D. R.; Clegg, M. J.; Downs, A. J.; Fowler, R. C.; Minihan, A. R.; Norris, J. R.; Stein, L. (1992). "La cation dixenon(1+): formación en las fases condensadas y caracterización por ESR, UV-visible y espectroscopia Raman". Química Inorgánica. 31 (24): 5041–5052. doi:10.1021/ic00050a023.
- ^ Stein, L.; Henderson, W. W. (1980). "Producción de la cación de dixenon por oxidación reversible de xenón". Journal of the American Chemical Society. 102 (8): 2856–2857. doi:10.1021/ja00528a065.
- ^ Mackay, Kenneth Malcolm; Mackay, Rosemary Ann; Henderson, W. (2002). Introducción a la química inorgánica moderna (6th ed.). CRC Prensa. ISBN 978-0-7487-6420-4.
- ^ Egon Wiberg; Nils Wiberg; Arnold Frederick Holleman (2001). Química inorgánica. Academic Press. p. 422. ISBN 978-0-12-352651-9.
- ^ Tramšek, M.; Benkič, P.; Žemva, B. (2004). "Primeros compuestos de Magnesio con XeF2". Inorg. Chem. 43 (2): 699–703. doi:10.1021/ic034826o. PMID 14731032.
- ^ Tramšek, M.; Benkič, P.; Žemva, B. (2004). "El primer compuesto que contiene un centro de metal en un ambiente homoléptico de XeF2 Molecules". Angewandte Chemie International Edition. 43 (26): 3456-8. doi:10.1002/anie.200453802. PMID 15221838.
- ^ Halpem, D. F. (2004). "Xenon(II) Fluoride". En Paquette, L. (ed.). Enciclopedia de Reagentes para la Síntesis Orgánica. Nueva York, NY: J. Wiley & Sons.
- ^ Taylor, S.; Kotoris, C.; Hum, G. (1999). "Recent Advances in Electrophilic Fluorination". Tetraedro. 55 (43): 12431–12477. doi:10.1016/S0040-4020(99)00748-6.
- ^ Tius, M. A. (1995). "Difluoruro xenón en síntesis". Tetraedro. 51 (24): 6605–6634. doi:10.1016/0040-4020(95)00362-C.
- ^ Patrick, T. B.; Darling, D. L. (1986). "Fluoración de sistemas aromáticos activados con fluoroxisulfato de cesio". J. Org. Chem. 51 (16): 3242–3244. doi:10.1021/jo00366a044.
- ^ Lothian, A. P.; Ramsden, C. A. (1993). "Rapid fluorodesilylation of aryltrimethylsilanes using xenon difuoride: Una nueva ruta eficiente a los fluoruros aromáticos". Synlett. 1993 (10): 753–755. doi:10.1055/s-1993-22596. S2CID 196734038.
- ^ W. Henderson (2000). Química del grupo principal. Gran Bretaña: Royal Society of Chemistry. p. 150. ISBN 978-0-85404-617-1.
- ^ Shunatona, Hunter P.; Früh, Natalja; Wang, Yi-Ming; Rauniyar, Vivek; Toste, F. Dean (2013-07-22). "Enantioselective Fluoroamination: 1,4-Addition to Conjugated Dienes Using Anionic Phase-Transfer Catalysis". Angewandte Chemie International Edition. 52 (30): 7724–7727. doi:10.1002/anie.201302002. ISSN 1521-3773. PMID 23766145.
- ^ Patrick, Timothy B.; Johri, Kamalesh K.; White, David H.; Bertrand, William S.; Mokhtar, Rodziah; Kilbourn, Michael R.; Welch, Michael J. (1986). "Sustitución de la función de ácido carboxílico con fluorina". Puede. 64: 138–141. doi:10.1139/v86-024.
- ^ Grakauskas, Vytautas (1969). "La fluoración acuosa de sales de ácido carboxílico". J. Org. Chem. 34 (8): 2446–2450. doi:10.1021/jo01260a040.
- ^ Tamura Masanori; Takagi Toshiyuki; Shibakami Motonari; Quan Heng-Dao; Sekiya Akira (1998). "Fluorination of olefins with xenon difluoride-silicon tetrafluoride". Fusso Kagaku Toronkai Koen Yoshishu (en japonés). 22: 62–63. Código de la revista: F0135B; código de adhesión: 99A0711841.
- ^ Chang, F.; Yeh, R.; G., Lin; Chu, P.; Hoffman, E.; Kruglick, E.; Pister, K.; Hecht, M. (1995). "Gas-phase silicon micromachining with xenon difluoride". En Bailey, Wayne; Motamedi, M. Edward; Luo, Fang-Chen (eds.). Microelectrónica Estructuras y dispositivos microelectromecánicos para aplicaciones de procesamiento óptico y multimedia. Vol. 2641. pp. 117–128. Bibcode:1995SPIE.2641..117C. doi:10.1117/12.220933. S2CID 39522253.
{{cite book}}:|journal=ignorado (ayuda) - ^ Chu, P.; Chen, J.; Chu, P.; Lin, G.; Huang, J.; Warneke, B; Pister, K. (1997). Pulso controlado con Difluoride Xenon. Int. Conf. Sensores y actuadores de estado sólido (Transductores 97). pp. 665-668.
- ^ Brazzle, J. D.; Dokmeci, M. R.; Mastrangelo, C. H. (2004). "Modelación y caracterización del grabado de polisilicio sacrificial mediante vapor-fase xenon difluoride". 17a Conferencia Internacional IEEE sobre Sistemas Mecánicos Micro Electro. Maastricht MEMS 2004 Technical Digest17a Conferencia Internacional sobre Sistemas Mecánicos Micro Electromecánicos (MEMS). págs. 737 a 740. doi:10.1109/MEMS.2004.1290690. ISBN 0-7803-8265-X.
Más lectura
- Greenwood, Norman Neill; Earnshaw, Alan (1997). Química de los elementos (2a edición). Butterworth-Heinemann. p. 894. ISBN 978-0-7506-3365-9.
Enlaces externos
- Página del WebBook para XeF2