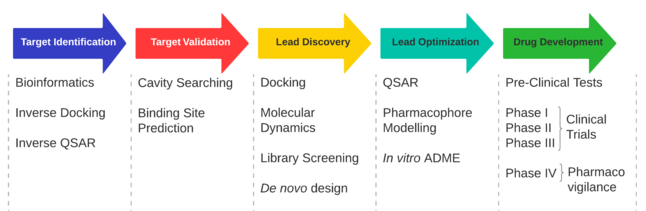
Descubrimiento de medicamento
En los campos de la medicina, la biotecnología y la farmacología, el descubrimiento de fármacos es el proceso mediante el cual se descubren nuevos medicamentos candidatos.
Históricamente, los medicamentos se descubrían identificando el ingrediente activo de los remedios tradicionales o mediante un descubrimiento fortuito, como ocurre con la penicilina. Más recientemente, se examinaron bibliotecas químicas de pequeñas moléculas sintéticas, productos naturales o extractos en células intactas u organismos completos para identificar sustancias que tenían un efecto terapéutico deseable en un proceso conocido como farmacología clásica. Después de que la secuenciación del genoma humano permitió una rápida clonación y síntesis de grandes cantidades de proteínas purificadas, se ha convertido en una práctica común el uso de cribado de alto rendimiento de grandes bibliotecas de compuestos contra dianas biológicas aisladas que, según la hipótesis, modifican la enfermedad en un proceso conocido como proceso inverso. farmacología. Los resultados de estas pantallas luego se prueban en células y luego en animales para determinar su eficacia.
El descubrimiento de fármacos modernos implica la identificación de resultados de detección, química medicinal y optimización de esos resultados para aumentar la afinidad, la selectividad (para reducir el potencial de efectos secundarios), la eficacia/potencia y la estabilidad metabólica (para aumentar la vida media). y biodisponibilidad oral. Una vez que se ha identificado un compuesto que cumple todos estos requisitos, el proceso de desarrollo del fármaco puede continuar. Si tiene éxito, se desarrollan ensayos clínicos.
Por lo tanto, el descubrimiento de fármacos modernos suele ser un proceso que requiere mucho capital y que implica grandes inversiones por parte de las corporaciones de la industria farmacéutica, así como de los gobiernos nacionales (que proporcionan subvenciones y garantías de préstamos). A pesar de los avances en la tecnología y la comprensión de los sistemas biológicos, el descubrimiento de fármacos sigue siendo un proceso largo, "costoso, difícil e ineficiente" con baja tasa de nuevos descubrimientos terapéuticos. En 2010, el coste de investigación y desarrollo de cada nueva entidad molecular fue de aproximadamente 1.800 millones de dólares. En el siglo XXI, la investigación de descubrimiento básico está financiada principalmente por gobiernos y organizaciones filantrópicas, mientras que el desarrollo en las últimas etapas está financiado principalmente por compañías farmacéuticas o capitalistas de riesgo. Para poder salir al mercado, los medicamentos deben pasar por varias fases exitosas de ensayos clínicos y pasar por un proceso de aprobación de nuevos medicamentos, llamado Solicitud de Nuevo Fármaco en los Estados Unidos.
Descubrir medicamentos que puedan ser un éxito comercial o de salud pública implica una interacción compleja entre los inversores, la industria, el mundo académico, las leyes de patentes, la exclusividad regulatoria, el marketing y la necesidad de equilibrar el secreto con la comunicación. Mientras tanto, para los trastornos cuya rareza significa que no se puede esperar un gran éxito comercial o efecto en la salud pública, el proceso de financiación de medicamentos huérfanos garantiza que las personas que experimentan esos trastornos puedan tener alguna esperanza de avances farmacoterapéuticos.
Historia
La idea de que el efecto de un fármaco en el cuerpo humano está mediado por interacciones específicas de la molécula del fármaco con macromoléculas biológicas (proteínas o ácidos nucleicos en la mayoría de los casos) llevó a los científicos a la conclusión de que se necesitan sustancias químicas individuales para el funcionamiento biológico. actividad de la droga. Esto marcó el comienzo de la era moderna en farmacología, cuando los productos químicos puros, en lugar de extractos crudos de plantas medicinales, se convirtieron en los medicamentos estándar. Ejemplos de compuestos farmacológicos aislados de preparados crudos son la morfina, el agente activo del opio, y la digoxina, un estimulante cardíaco procedente de Digitalis lanata. La química orgánica también condujo a la síntesis de muchos de los productos naturales aislados de fuentes biológicas.
Históricamente, las sustancias, ya fueran extractos crudos o productos químicos purificados, eran analizadas para determinar su actividad biológica sin conocer el objetivo biológico. Sólo después de identificar una sustancia activa se hizo un esfuerzo para identificar el objetivo. Este enfoque se conoce como farmacología clásica, farmacología avanzada o descubrimiento de fármacos fenotípicos.
Más tarde, se sintetizaron pequeñas moléculas para atacar específicamente una vía fisiológica/patológica conocida, evitando la detección masiva de bancos de compuestos almacenados. Esto condujo a grandes éxitos, como el trabajo de Gertrude Elion y George H. Hitchings sobre el metabolismo de las purinas, el trabajo de James Black sobre los betabloqueantes y la cimetidina y el descubrimiento de las estatinas por parte de Akira Endo. Otro defensor del enfoque de desarrollo de análogos químicos de sustancias activas conocidas fue Sir David Jack en Allen and Hanbury's, más tarde Glaxo, quien fue pionero en el primer agonista beta2-adrenérgico selectivo inhalado para el asma, el primer esteroide inhalado para el asma, la ranitidina. como sucesor de la cimetidina y apoyó el desarrollo de los triptanos.
Gertrude Elion, trabajando principalmente con un grupo de menos de 50 personas en análogos de purinas, contribuyó al descubrimiento del primer antiviral; el primer inmunosupresor (azatioprina) que permitió el trasplante de órganos humanos; el primer fármaco que induce la remisión de la leucemia infantil; tratamientos fundamentales contra el cáncer; un antipalúdico; un antibacteriano; y un tratamiento para la gota.
La clonación de proteínas humanas hizo posible la detección de grandes bibliotecas de compuestos contra objetivos específicos que se cree que están relacionados con enfermedades específicas. Este enfoque se conoce como farmacología inversa y es el método más utilizado en la actualidad.
En la década de 2020, los qubits y la computación cuántica comenzaron a utilizarse para reducir el tiempo necesario para el descubrimiento de fármacos.
Objetivos
Un "objetivo" se produce dentro de la industria farmacéutica. Generalmente, el "objetivo" es la estructura celular o molecular existente naturalmente involucrada en la patología de interés donde debe actuar el fármaco en desarrollo. Sin embargo, la distinción entre un "nuevo" y "establecido" Se puede establecer un objetivo sin una comprensión completa de qué es un "objetivo" es. Esta distinción la suelen hacer las empresas farmacéuticas dedicadas al descubrimiento y desarrollo de terapias. En una estimación de 2011, se identificaron 435 productos del genoma humano como objetivos terapéuticos de medicamentos aprobados por la FDA.
"Objetivos establecidos" son aquellos para los cuales existe una buena comprensión científica, respaldada por un largo historial de publicaciones, tanto de cómo funciona el objetivo en la fisiología normal como de cómo participa en la patología humana. Esto no implica que se comprenda completamente el mecanismo de acción de los fármacos que se cree que actúan a través de un objetivo determinado establecido. Más bien, "establecido"; se relaciona directamente con la cantidad de información básica disponible sobre un objetivo, en particular información funcional. En general, los "nuevos objetivos" ¿Son todos aquellos objetivos que no son "objetivos establecidos" pero que han sido o son objeto de esfuerzos de descubrimiento de fármacos. La mayoría de los objetivos seleccionados para los esfuerzos de descubrimiento de fármacos son proteínas, como los receptores acoplados a proteína G (GPCR) y las proteínas quinasas.
Proyección y diseño
El proceso de encontrar un nuevo medicamento contra un objetivo elegido para una enfermedad en particular generalmente implica una detección de alto rendimiento (HTS), en la que se prueban grandes bibliotecas de sustancias químicas para determinar su capacidad para modificar el objetivo. Por ejemplo, si el objetivo es un nuevo GPCR, se analizarán los compuestos para determinar su capacidad para inhibir o estimular ese receptor (ver antagonista y agonista): si el objetivo es una proteína quinasa, se probará la capacidad de los químicos para inhibir ese receptor. quinasa.
Otra función de HTS es mostrar cuán selectivos son los compuestos para el objetivo elegido, ya que uno quiere encontrar una molécula que interfiera solo con el objetivo elegido, pero no con otros objetivos relacionados. Para ello se realizarán otras pruebas para comprobar si los "aciertos" contra el objetivo elegido interferirá con otros objetivos relacionados: este es el proceso de selección cruzada. El análisis cruzado es útil porque cuantos más objetivos no relacionados alcance un compuesto, es más probable que se produzca toxicidad fuera del objetivo con ese compuesto una vez que llegue a la clínica.
Es poco probable que surja un fármaco candidato perfecto de estas primeras pruebas de detección. Uno de los primeros pasos es detectar compuestos que probablemente no se conviertan en medicamentos; por ejemplo, los compuestos que son positivos en casi todos los ensayos, clasificados por los químicos médicos como "compuestos de interferencia de todos los ensayos", se eliminan en esta etapa, si aún no se eliminaron de la biblioteca química. A menudo se observa que varios compuestos tienen cierto grado de actividad y, si estos compuestos comparten características químicas comunes, se pueden desarrollar uno o más farmacóforos. En este punto, los químicos medicinales intentarán utilizar las relaciones estructura-actividad (SAR) para mejorar ciertas características del compuesto principal:
- aumentar la actividad contra el objetivo elegido
- reducir la actividad frente a objetivos no relacionados
- mejorar la semejanza de la droga o las propiedades ADME de la molécula.
Este proceso requerirá varias pruebas de detección iterativas, durante las cuales, se espera, las propiedades de las nuevas entidades moleculares mejoren y permitan que los compuestos preferidos pasen a pruebas in vitro e in vivo para determinar su actividad en el modelo de la enfermedad. de elección.
Entre las propiedades fisicoquímicas asociadas con la absorción de fármacos se incluyen la ionización (pKa) y la solubilidad; la permeabilidad puede determinarse mediante PAMPA y Caco-2. PAMPA es atractivo como cribado temprano debido al bajo consumo de fármaco y al bajo costo en comparación con pruebas como Caco-2, tracto gastrointestinal (GIT) y barrera hematoencefálica (BHE) con las que existe una alta correlación.
Se puede utilizar una variedad de parámetros para evaluar la calidad de un compuesto, o de una serie de compuestos, como se propone en la Regla de Cinco de Lipinski. Dichos parámetros incluyen propiedades calculadas como cLogP para estimar la lipofilicidad, el peso molecular, el área de superficie polar y propiedades medidas, como la potencia, la medición in vitro del aclaramiento enzimático, etc. Algunos descriptores como la eficiencia del ligando (LE) y la eficiencia lipófila (LiPE). combinar dichos parámetros para evaluar la semejanza con las drogas.
Si bien HTS es un método comúnmente utilizado para el descubrimiento de nuevos fármacos, no es el único método. A menudo es posible partir de una molécula que ya tiene algunas de las propiedades deseadas. Una molécula de este tipo podría extraerse de un producto natural o incluso ser un medicamento en el mercado que podría mejorarse (los llamados medicamentos "yo también"). Otros métodos, como el cribado virtual de alto rendimiento, en el que el cribado se realiza utilizando modelos generados por ordenador e intentando "acoplar" los datos. También se utilizan a menudo bibliotecas virtuales para un objetivo.
Otro método para el descubrimiento de fármacos es el diseño de fármacos de novo, en el que se hace una predicción de los tipos de sustancias químicas que podrían (por ejemplo) encajar en un sitio activo de la enzima objetivo. Por ejemplo, la detección virtual y el diseño de fármacos asistido por computadora se utilizan a menudo para identificar nuevos restos químicos que pueden interactuar con una proteína objetivo. Los modelos moleculares y las simulaciones de dinámica molecular se pueden utilizar como guía para mejorar la potencia y las propiedades de nuevos fármacos.
También hay un cambio de paradigma en la comunidad de descubrimiento de fármacos al pasar del HTS, que es costoso y puede que solo cubra un espacio químico limitado, al análisis de bibliotecas más pequeñas (como máximo, unos pocos miles de compuestos). Estos incluyen el descubrimiento de pistas basado en fragmentos (FBDD) y la química combinatoria dinámica dirigida a proteínas. Los ligandos en estos enfoques suelen ser mucho más pequeños y se unen a la proteína objetivo con una afinidad de unión más débil que los aciertos identificados a partir de HTS. A menudo se requieren modificaciones adicionales mediante síntesis orgánica en compuestos de plomo. Estas modificaciones suelen estar guiadas por la cristalografía de rayos X de proteínas del complejo proteína-fragmento. Las ventajas de estos enfoques son que permiten una detección más eficiente y la biblioteca de compuestos, aunque pequeña, normalmente cubre un espacio químico grande en comparación con HTS.
Las pruebas fenotípicas también han proporcionado nuevos puntos de partida químicos en el descubrimiento de fármacos. Se han utilizado diversos modelos, incluidos levaduras, peces cebra, gusanos, líneas celulares inmortalizadas, líneas celulares primarias, líneas celulares derivadas de pacientes y modelos animales completos. Estas pruebas de detección están diseñadas para encontrar compuestos que reviertan el fenotipo de una enfermedad, como la muerte, la agregación de proteínas, la expresión de proteínas mutantes o la proliferación celular, como ejemplos en un modelo celular u organismo más holístico. A menudo se utilizan conjuntos de cribado más pequeños para estas cribas, especialmente cuando los modelos son caros o su funcionamiento requiere mucho tiempo. En muchos casos, se desconoce el mecanismo exacto de acción de los impactos de estas pantallas y es posible que sea necesario realizar extensos experimentos de deconvolución de objetivos para determinarlo. El crecimiento del campo de la quimioproteómica ha proporcionado numerosas estrategias para identificar objetivos farmacológicos en estos casos.
Una vez que se haya establecido una serie de compuestos líderes con suficiente potencia y selectividad objetivo y propiedades similares a las de un fármaco favorables, se propondrán uno o dos compuestos para el desarrollo de fármacos. El mejor de ellos generalmente se denomina compuesto principal, mientras que el otro se designará como "de respaldo". Estas decisiones generalmente están respaldadas por innovaciones en modelos computacionales.
La naturaleza como fuente
Tradicionalmente, muchas drogas y otras sustancias químicas con actividad biológica se han descubierto mediante el estudio de sustancias químicas que los organismos crean para afectar la actividad de otros organismos para sobrevivir.
A pesar del auge de la química combinatoria como parte integral del proceso de descubrimiento de pistas, los productos naturales siguen desempeñando un papel importante como material de partida para el descubrimiento de fármacos. Un informe de 2007 encontró que de las 974 nuevas entidades químicas de moléculas pequeñas desarrolladas entre 1981 y 2006, el 63% eran derivados naturales o derivados semisintéticos de productos naturales. Para determinadas áreas terapéuticas, como los antimicrobianos, los antineoplásicos, los antihipertensivos y los antiinflamatorios, las cifras fueron mayores.
Los productos naturales pueden ser útiles como fuente de nuevas estructuras químicas para técnicas modernas de desarrollo de terapias antibacterianas.
Los productos naturales pueden ser útiles como fuente de nuevas estructuras químicas para técnicas modernas de desarrollo de terapias antibacterianas.
Muchos metabolitos secundarios producidos por las plantas tienen posibles propiedades medicinales terapéuticas. Estos metabolitos secundarios contienen, se unen y modifican la función de las proteínas (receptores, enzimas, etc.). En consecuencia, los productos naturales derivados de plantas se han utilizado a menudo como punto de partida para el descubrimiento de fármacos.
Historia
Hasta el Renacimiento, la gran mayoría de los fármacos de la medicina occidental eran extractos derivados de plantas. Esto ha dado como resultado un conjunto de información sobre el potencial de las especies de plantas como fuentes importantes de materiales de partida para el descubrimiento de fármacos. El conocimiento botánico sobre los diferentes metabolitos y hormonas que se producen en diferentes partes anatómicas de la planta (por ejemplo, raíces, hojas y flores) es crucial para identificar correctamente las propiedades bioactivas y farmacológicas de la planta. Identificar nuevos medicamentos y lograr su aprobación para el mercado ha demostrado ser un proceso estricto debido a las regulaciones establecidas por las agencias reguladoras nacionales de medicamentos.
Jasmonates
Los jasmonatos son importantes en las respuestas a lesiones y señales intracelulares. Inducen apoptosis y cascada de proteínas mediante inhibidores de proteinasa, tienen funciones de defensa y regulan las respuestas de las plantas a diferentes estreses bióticos y abióticos. Los jasmonatos también tienen la capacidad de actuar directamente sobre las membranas mitocondriales al inducir la despolarización de la membrana mediante la liberación de metabolitos.
Los derivados de jasmonato (JAD) también son importantes en la respuesta a las heridas y en la regeneración de tejidos en las células vegetales. También se ha identificado que tienen efectos antienvejecimiento en la capa epidérmica humana. Se sospecha que interactúan con polisacáridos de proteoglicanos (PG) y glucosaminoglicanos (GAG), que son componentes esenciales de la matriz extracelular (ECM) para ayudar a remodelar la ECM. El descubrimiento de los JAD en la reparación de la piel ha generado un nuevo interés en los efectos de estas hormonas vegetales en aplicaciones medicinales terapéuticas.
Salicilatos

El ácido salicílico (SA), una fitohormona, se derivó inicialmente de la corteza del sauce y desde entonces se ha identificado en muchas especies. Es un actor importante en la inmunidad de las plantas, aunque los científicos aún no comprenden completamente su papel. Están involucrados en respuestas de inmunidad y enfermedades en tejidos vegetales y animales. Tienen proteínas de unión al ácido salicílico (SABP) que han demostrado afectar a múltiples tejidos animales. Las primeras propiedades medicinales descubiertas del compuesto aislado estaban relacionadas con el control del dolor y la fiebre. También desempeñan un papel activo en la supresión de la proliferación celular. Tienen la capacidad de inducir la muerte en leucemia linfoblástica y otras células cancerosas humanas. Uno de los fármacos más comunes derivados de los salicilatos es la aspirina, también conocida como ácido acetilsalicílico, con propiedades antiinflamatorias y antipiréticas.
De origen animal
Algunos medicamentos utilizados en la medicina moderna se han descubierto en animales o se basan en compuestos que se encuentran en animales. Por ejemplo, los fármacos anticoagulantes hirudina y su congénere sintético, bivalirudina, se basan en la química de la saliva de la sanguijuela, Hirudo medicinalis. Utilizada para tratar la diabetes tipo 2, la exenatida se desarrolló a partir de compuestos de saliva del monstruo de Gila, un lagarto venenoso.
Metabolitos microbianos
Los microbios compiten por el espacio vital y los nutrientes. Para sobrevivir en estas condiciones, muchos microbios han desarrollado habilidades para evitar que proliferen especies competidoras. Los microbios son la principal fuente de medicamentos antimicrobianos. Los aislados de Streptomyces han sido una fuente tan valiosa de antibióticos que se les ha llamado mohos medicinales. El ejemplo clásico de un antibiótico descubierto como mecanismo de defensa contra otro microbio es la penicilina en cultivos bacterianos contaminados por el hongo Penicillium en 1928.
Invertebrados marinos
Los ambientes marinos son fuentes potenciales de nuevos agentes bioactivos. Los nucleósidos de arabinosa descubiertos en invertebrados marinos en la década de 1950 demostraron por primera vez que restos de azúcar distintos de la ribosa y la desoxirribosa pueden producir estructuras de nucleósidos bioactivos. Hubo que esperar hasta 2004 para que se aprobara el primer fármaco de origen marino. Por ejemplo, la toxina del caracol cónico ziconotida, también conocida como Prialt, trata el dolor neuropático severo. Varios otros agentes de origen marino se encuentran ahora en ensayos clínicos para indicaciones como el cáncer, el uso de antiinflamatorios y el dolor. Una clase de estos agentes son los compuestos similares a la briostatina, que se están investigando como terapia contra el cáncer.
Diversidad química
Como se mencionó anteriormente, la química combinatoria fue una tecnología clave que permitió la generación eficiente de grandes bibliotecas de detección para las necesidades de detección de alto rendimiento. Sin embargo, ahora, después de dos décadas de química combinatoria, se ha señalado que, a pesar de la mayor eficiencia en la síntesis química, no se ha logrado ningún aumento en el número de candidatos a fármacos o plomo. Esto ha llevado al análisis de las características químicas de los productos de química combinatoria, en comparación con fármacos o productos naturales existentes. El concepto quimioinformático de diversidad química, representado como la distribución de compuestos en el espacio químico en función de sus características fisicoquímicas, se utiliza a menudo para describir la diferencia entre las bibliotecas de química combinatoria y los productos naturales. Los compuestos sintéticos y combinatorios de la biblioteca parecen cubrir sólo un espacio químico limitado y bastante uniforme, mientras que los medicamentos existentes y, en particular, los productos naturales, exhiben una diversidad química mucho mayor y se distribuyen de manera más uniforme en el espacio químico. Las diferencias más destacadas entre productos naturales y compuestos en las bibliotecas de química combinatoria es el número de centros quirales (mucho mayor en los compuestos naturales), la rigidez de la estructura (mayor en los compuestos naturales) y el número de restos aromáticos (mayor en las bibliotecas de química combinatoria). Otras diferencias químicas entre estos dos grupos incluyen la naturaleza de los heteroátomos (O y N enriquecidos en productos naturales, y S y átomos de halógeno presentes con mayor frecuencia en compuestos sintéticos), así como el nivel de insaturación no aromática (mayor en productos naturales). Como tanto la rigidez estructural como la quiralidad son factores bien establecidos en la química medicinal que se sabe que mejoran la especificidad y la eficacia de los compuestos como fármaco, se ha sugerido que los productos naturales se comparan favorablemente con las bibliotecas de química combinatoria actuales como posibles moléculas principales.
Proyección
Existen dos enfoques principales para encontrar nuevas entidades químicas bioactivas a partir de fuentes naturales.
A veces se hace referencia a la primera como recopilación y selección aleatoria de material, pero la recopilación dista mucho de ser aleatoria. El conocimiento biológico (a menudo botánico) se utiliza a menudo para identificar familias prometedoras. Este enfoque es eficaz porque sólo una pequeña parte de la biodiversidad de la Tierra ha sido sometida a pruebas para detectar actividad farmacéutica. Además, los organismos que viven en un entorno rico en especies necesitan desarrollar mecanismos defensivos y competitivos para sobrevivir. Esos mecanismos podrían explotarse en el desarrollo de fármacos beneficiosos.
Una colección de muestras de plantas, animales y microbios de ecosistemas ricos puede potencialmente dar lugar a nuevas actividades biológicas que valga la pena explotar en el proceso de desarrollo de fármacos. Un ejemplo del uso exitoso de esta estrategia es la detección de agentes antitumorales por parte del Instituto Nacional del Cáncer, que comenzó en la década de 1960. El paclitaxel se identificó en el tejo del Pacífico Taxus brevifolia. Paclitaxel mostró actividad antitumoral mediante un mecanismo no descrito anteriormente (estabilización de microtúbulos) y ahora está aprobado para uso clínico para el tratamiento del cáncer de pulmón, mama y ovario, así como para el sarcoma de Kaposi. A principios del siglo XXI, el cabazitaxel (fabricado por Sanofi, una empresa francesa), otro pariente del taxol, ha demostrado ser eficaz contra el cáncer de próstata, también porque actúa impidiendo la formación de microtúbulos, que separan los cromosomas en las células en división (como como células cancerosas). Otros ejemplos son: 1. Camptoteca (Camptotecina · Topotecán · Irinotecán · Rubitecán · Belotecán); 2. Podophyllum (Etopósido · Tenipósido); 3a. Antraciclinas (Aclarubicina · Daunorrubicina · Doxorrubicina · Epirrubicina · Idarrubicina · Amrubicina · Pirarubicina · Valrubicina · Zorrubicina); 3b. Antracenodionas (Mitoxantrona · Pixantrona).
El segundo enfoque principal involucra la etnobotánica, el estudio del uso general de las plantas en la sociedad, y la etnofarmacología, un área dentro de la etnobotánica, que se centra específicamente en los usos medicinales.
La artemisinina, un agente antipalúdico procedente del gusano dulce Artemisia annua, utilizado en la medicina china desde el año 200 a.C., es un fármaco utilizado como parte de la terapia combinada para el Plasmodium falciparum multirresistente.
Además, dado que el aprendizaje automático se ha vuelto más avanzado, la detección virtual es ahora una opción para los desarrolladores de fármacos. Se están utilizando algoritmos de IA para realizar análisis virtuales de compuestos químicos, lo que implica predecir la actividad de un compuesto frente a un objetivo específico. Al utilizar algoritmos de aprendizaje automático para analizar grandes cantidades de datos químicos, los investigadores pueden identificar posibles nuevos fármacos candidatos que tienen más probabilidades de ser eficaces contra una enfermedad específica. Los algoritmos, como los clasificadores de vecino más cercano, RF, máquinas de aprendizaje extremo, SVM y redes neuronales profundas (DNN), se utilizan para VS en función de la viabilidad de la síntesis y también pueden predecir la actividad y la toxicidad in vivo.
Aclaración estructural
La dilucidación de la estructura química es fundamental para evitar el redescubrimiento de un agente químico que ya es conocido por su estructura y actividad química. La espectrometría de masas es un método en el que se identifican compuestos individuales en función de su relación masa/carga, después de la ionización. Los compuestos químicos existen en la naturaleza como mezclas, por lo que la combinación de cromatografía líquida y espectrometría de masas (LC-MS) se utiliza a menudo para separar las sustancias químicas individuales. Se encuentran disponibles bases de datos de espectros de masas para compuestos conocidos y se pueden utilizar para asignar una estructura a un espectro de masas desconocido. La espectroscopia de resonancia magnética nuclear es la técnica principal para determinar las estructuras químicas de productos naturales. La RMN proporciona información sobre los átomos individuales de hidrógeno y carbono en la estructura, lo que permite una reconstrucción detallada de la arquitectura de la molécula.
Solicitud de nuevo medicamento
Cuando un medicamento se desarrolla con evidencia a lo largo de su historia de investigación que demuestra que es seguro y efectivo para el uso previsto en los Estados Unidos, la compañía puede presentar una solicitud, la Solicitud de Nuevo Fármaco (NDA, por sus siglas en inglés), para que el medicamento comercializado y disponible para aplicación clínica. El estado de NDA permite a la FDA examinar todos los datos presentados sobre el medicamento para tomar una decisión sobre si aprobar o no el medicamento candidato en función de su seguridad, especificidad del efecto y eficacia de las dosis.
