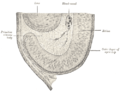
Desarrollo del ojo


La formación del ojo en el embrión humano comienza aproximadamente a las tres semanas de desarrollo embrionario y continúa hasta la décima semana. Las células de los tejidos mesodérmicos y ectodérmicos contribuyen a la formación del ojo. En concreto, el ojo se deriva del neuroepitelio, el ectodermo superficial y el mesénquima extracelular, que consta tanto de la cresta neural como del mesodermo.
El neuroepitelio forma la retina, el cuerpo ciliar, el iris y los nervios ópticos. El ectodermo superficial forma el cristalino, el epitelio corneal y el párpado. El mesénquima extracelular forma la esclerótica, el endotelio y el estroma corneales, los vasos sanguíneos, los músculos y el vítreo.
El ojo comienza a desarrollarse como un par de vesículas ópticas a cada lado del prosencéfalo al final de la cuarta semana de embarazo. Las vesículas ópticas son excrecencias del cerebro que entran en contacto con el ectodermo superficial y este contacto induce cambios necesarios para el desarrollo posterior del ojo. A través de un surco en la parte inferior de la vesícula óptica, conocido como fisura coroidea, los vasos sanguíneos ingresan al ojo. Varias capas, como el tubo neural, la cresta neural, el ectodermo superficial y el mesodermo, contribuyen al desarrollo del ojo.
El desarrollo del ojo se inicia con el gen de control maestro PAX6, un gen homeobox con homólogos conocidos en humanos (aniridia), ratones (ojo pequeño) y Drosophila (sin ojos). El locus del gen PAX6 es un factor de transcripción para los diversos genes y factores de crecimiento involucrados en la formación del ojo. La morfogénesis del ojo comienza con la evaginación o crecimiento de los surcos ópticos. Estos dos surcos en los pliegues neurales se transforman en vesículas ópticas con el cierre del tubo neural. Las vesículas ópticas luego se desarrollan en la copa óptica, con la capa interna formando la retina y la porción externa formando el epitelio pigmentario de la retina. La porción media de la copa óptica se desarrolla en el cuerpo ciliar y el iris. Durante la invaginación de la copa óptica, el ectodermo comienza a engrosarse y forma la placa del cristalino, que finalmente se separa del ectodermo para formar la vesícula del cristalino en el extremo abierto de la copa óptica.
Una mayor diferenciación y reorganización mecánica de las células dentro y alrededor de la copa óptica da lugar al ojo completamente desarrollado.
Inducciones secuenciales
Este desarrollo es un ejemplo de inducción secuencial donde el órgano se forma a partir de tres tejidos diferentes:
Neural tube ectoderm (neuroectoderm)
En primer lugar, se produce una evaginación del tubo neural llamada vesículas ópticas. El desarrollo de las vesículas ópticas comienza en el embrión de 3 semanas, a partir de un surco cada vez más profundo en la placa neural llamado surco óptico. Algunos estudios sugieren que este mecanismo está regulado por el factor de transcripción RX/RAX. Las proteínas Wnt y FGF (factor de crecimiento de fibroblastos) desempeñan un papel en esta etapa temprana y están reguladas por otra proteína llamada Shisa. A medida que esta se expande, el neuroporo rostral (la salida de la cavidad cerebral hacia el exterior del embrión) se cierra y el surco óptico y la placa neural se convierten en la vesícula óptica. Los nervios ópticos surgen de las conexiones de las vesículas con el prosencéfalo.
El neuroectodermo da origen a los siguientes compartimentos del ojo:
- retina
- forro epitelial de cuerpo ciliario e iris
- nervios ópticos
Superficie ectoderm
El desarrollo del cristalino está estrechamente relacionado con el desarrollo de la vesícula óptica. La interacción entre la vesícula en crecimiento y el ectodermo hace que el ectodermo se espese en ese punto. Esta porción engrosada del ectodermo se denomina placoda del cristalino. A continuación, la placoda se invagina y forma una bolsa denominada fosa del cristalino. Los científicos están estudiando las fuerzas de tensión necesarias para la invaginación de la placoda del cristalino y la investigación actual sugiere que los microfilamentos podrían estar presentes en las células retinianas tempranas para permitir el comportamiento de invaginación. La investigación también ha demostrado que los filopodios dependientes de Rho GTPasa del ectodermo precursor del cristalino desempeñan un papel importante en la formación de la fosa del cristalino. Finalmente, la fosa se cierra por completo. Esta estructura cerrada es la vesícula del cristalino. Los estudios han demostrado que el desarrollo del cristalino requiere la presencia del gen Pax6, que es el gen regulador maestro de la morfogénesis ocular. Este gen regulador maestro no es necesario para el desarrollo de la vesícula óptica, estrechamente asociado. Además, se ha demostrado que la activación de Ras es suficiente para iniciar la diferenciación del cristalino, pero no para completarla.
Las vesículas ópticas luego comienzan a formar la copa óptica. La morfogénesis de la copa óptica es el proceso de invaginación que ocurre después de que el movimiento del neuroectodermo forma la vesícula óptica esférica (Fase 1). La invaginación es cuando un tejido se pliega sobre sí mismo. En el transcurso de aproximadamente 12 horas, el extremo distal de la capa interna de la vesícula óptica comienza a aplanarse (Fase 2). Durante las siguientes 18 horas, tanto la capa interna como la externa comienzan a flexionarse hacia adentro en ángulos agudos, comenzando la formación de un borde en forma de C (Fase 3). Las últimas 18 horas implican continuar con esta invaginación apicalmente convexa para formar la copa óptica . En este punto, se pueden observar morfologías como células epiteliales columnares, células pseudoestratificadas y células en forma de cuña estrechas apicalmente.
La capa interna de la copa óptica está formada por neuroepitelio (retina neural), mientras que la capa externa está compuesta por epitelio pigmentario de la retina (EPR). Los experimentos han determinado que la diferenciación y el mantenimiento de las células del EPR requieren interacción con los tejidos vecinos, probablemente la señalización Wnt canónica, mientras que la diferenciación de la retina neural está impulsada por factores autónomos del tejido.
Las proteínas morfogénicas óseas (BMP) son importantes reguladores del desarrollo de la copa óptica. De hecho, estudios de investigación han demostrado que los agonistas y antagonistas de las BMP son necesarios para la precisión del desarrollo de la copa óptica. Las interacciones entre los tejidos y las vías de señalización también desempeñan un papel importante en la morfogénesis de la copa óptica.
Es interesante señalar que las investigaciones han demostrado que el aislamiento de la copa óptica del tejido vecino después de completar la invaginación en un medio de cultivo de tejidos puede conducir al desarrollo de la mayoría de las partes principales del ojo, incluidos los fotorreceptores, las células ganglionares, las células bipolares, las células horizontales, las células amacrinas y la glía de Müller. Esto indica que la morfogénesis de la copa óptica se produce independientemente de las señales externas de su entorno, incluida la presencia del cristalino. Sin embargo, el cristalino es necesario para actuar como inductor del ectodermo para transformarlo en la córnea.
El ectodermo superficial produce las siguientes partes:
- lente
- epitelio corneal
- piel de párpado
Cresta neural
Las células de la cresta neural se derivan del ectodermo y se encuentran cerca del tubo neural:
- sclera
- Cornea: membrana y endotelio de Descemet
- tejido conectivo y estructura ósea de la órbita
Mesoderm
El mesodermo contribuye a las siguientes estructuras:
- músculos extraoculares
- revestimiento endotelial de vasos sanguíneos del ojo
- vasos sanguíneos en esclera
- Esclera & Choroid
- Vitreous
- Fibras suspendidas
- Cornea: membrana y estroma de Bowman
Cascada para el desarrollo
Según Liem et al., la organogénesis del ojo se señala como un ejemplo de una cascada de inducciones del desarrollo. El ojo es esencialmente un derivado del ectodermo a partir del ectodermo somático y del tubo neural, con una sucesión de inducciones por parte del cordamesodermo.
El cordamesodermo induce la porción anterior del tubo neural para formar los precursores del cerebro tripartito sinapomórfico de los vertebrados, y formará un abultamiento llamado diencéfalo. Una inducción posterior por parte del cordamesodermo formará una protrusión: la vesícula óptica. Esta vesícula será posteriormente invaginada mediante inducciones posteriores del cordamesodermo. La vesícula óptica inducirá entonces al ectodermo que se engrosa (placoda del cristalino) y se invagina aún más hasta un punto en el que se desprende del ectodermo y forma una placoda neurogénica por sí misma. La placoda del cristalino es afectada por el cordamesodermo haciendo que se invagine y forme la copa óptica compuesta por una capa interna de la retina neural y una capa externa de la retina pigmentada que se unirán y formarán el tallo óptico. La retina pigmentada está formada por bastones y conos y compuesta por pequeños cilios típicos del epitelio ependimario del tubo neural. Algunas células de la vesícula del cristalino estarán destinadas a formar la córnea y la vesícula del cristalino se desarrollará completamente para formar el cristalino definitivo. El iris se forma a partir de las células de la copa óptica.
Responsabilidad de la epidermis cabeza
Sólo la epidermis de la cabeza es competente para responder a la señal de las vesículas ópticas. Tanto la vesícula óptica como la epidermis de la cabeza son necesarias para el desarrollo del ojo. La competencia de la epidermis de la cabeza para responder a las señales de la vesícula óptica proviene de la expresión de Pax6 en la epidermis. Pax6 es necesario y suficiente para la inducción ocular. Esta competencia se adquiere gradualmente durante la gastrulación y la neurulación a partir de interacciones con el endodermo, el mesodermo y la placa neural.
Regulación e inhibición
Sonic hedgehog reduce la expresión de Pax6. Cuando Shh se inhibe durante el desarrollo, el dominio de expresión de Pax6 se expande y los ojos no se separan, lo que provoca ciclopía. La sobreexpresión de Shh provoca una pérdida de las estructuras oculares.
El ácido retinoico generado a partir de la vitamina A en la retina desempeña un papel esencial en el desarrollo del ojo como señal paracrina secretada que restringe la invasión del mesénquima perióptico alrededor de la copa óptica. La deficiencia de vitamina A durante la embriogénesis produce defectos en el segmento anterior (en particular, la córnea y los párpados) que conducen a la pérdida de la visión o a la ceguera.
Existen algunas evidencias de que LMX1B desempeña un papel en la supervivencia mesenquimal periocular.
Imágenes adicionales
- Copa óptica y fisura choroidal vista desde abajo, desde un embrión humano de aproximadamente cuatro semanas.
- Sección horizontal a través del ojo de un conejo embrión de dieciocho días. X 30.
- Sección de ojo del embrión humano de seis semanas.
- Sección de desarrollo de ojo de trucha.
Referencias
- ^ a b c d e f Ort, D., David, H., "Development of the Eye". Consultado el 22 de abril de 2015.
- ^ a b Sadler, T.W (1990). La embriología médica de Langman (6th ed.). Williams y Wilkins. ISBN 978-0683074932.
- ^ a b c d e f g Hosseini, Hadi S.; Beebe, David C.; Taber, Larry A. (2014). "Efectos mecánicos del ectodermo superficial en la vesícula óptica morfogénesis en el embrión de pollitos". Journal of Biomechanics. 47 (16): 3837–3846. doi:10.1016/j.jbiomech.2014.10.018. PMC 4261019. PMID 25458577.
- ^ a b c d e f g Hosseini, Hadi S.; Taber, Larry A. (2018). "Cómo las fuerzas mecánicas dan forma al ojo en desarrollo". Avances en Biofísica y Biología Molecular. 137 (16): 25–36. doi:10.1016/j.pbiomolbio.2018.01.004. PMC 6085168. PMID 29432780.
- ^ Keller, A. M. V., "Embryonic Development of the Eye" Archivado 2015-04-08 en el Wayback Machine. Consultado el 22 de abril de 2015.
- ^ a b Fuhrmann, S., Levine, E. M. and Reh, T. A. (2000). "Mesenquima extraocular patrones la vesícula óptica durante el desarrollo temprano de los ojos en el pollito embrionario". Desarrollo 127, 4599–4609.
- ^ LifeMap Science, Inc. "Embryonic and Postnatal Development of the Eye". Consultado el 22 de abril de 2015.
- ^ a b Fuhrmann, S., “Eye Morphogenesis and Patterning of the Optic Vesicle” Temas actuales en biología del desarrollo 93, 61-84 (07 de octubre de 2010)
- ^ "eye(vertebrado) McGraw-Hil; Encyclopedia of Science and Technology (2007), vol.6, pp.801-802
- ^ Fuhrmann, Sabine, “Eye Morphogenesis y Patterning of the Optic Vesicle” Temas actuales en biología del desarrollo 93, 61-84 (07 de octubre de 2010)
- ^ a b Hill, M.A. (2015) Embryology Vision - Lens Development. Consultado el 22 de abril de 2015.
- ^ a b Adler, R., Canto-Soler, M.V., “Molecular mechanisms of optic vesicle development: Complexities, ambiguities and controversies”, Developmental Biology 305,1,1-13 (1 May 2007)
- ^ a b c Eiraku et al., "Autoorganización de morfogénesis en la cultura celular tridimensional", Nature 472, 51–56 (07 de abril de 2011)
- ^ "Development of the Vertebrate Eye -- Developmental Biology -- NCBI Bookshelf". Retrieved 2010-04-10.
- ^ Duester, G (septiembre 2008). "Sintesis y señalización de ácido retinoico durante la organogénesis temprana". Celular. 134 (6): 921–31. doi:10.1016/j.cell.2008.09.002. PMC 2632951. PMID 18805086.
- ^ McMahon C, Gestri G, Wilson SW, Link BA (agosto de 2009). "Lmx1b es esencial para la supervivencia de células mesenquimales perioculares e influencias Patinaje retinal mediado por Fgf en peces cebra". Dev. Biol. 332 (2): 287–98. doi:10.1016/j.ydbio.2009.05.577. PMC 2716413. PMID 19500562.
Más lectura
- Keith L. Moore y T.V.N. Persaud (2008). La embriología humana-clínica orientada8a edición. USA: Saunders, una huella de Elsevier Inc. p. 429
Enlaces externos
- Desarrollo del Ojo: Una serie de interacciones inductivas