Defecto cristalográfico
Un defecto cristalográfico es una interrupción de los patrones regulares de disposición de átomos o moléculas en sólidos cristalinos. Las posiciones y orientaciones de las partículas, que se repiten a distancias fijas determinadas por los parámetros de la celda unitaria en los cristales, exhiben una estructura cristalina periódica, pero generalmente es imperfecta. A menudo se caracterizan varios tipos de defectos: defectos puntuales, defectos de línea, defectos planos, defectos de volumen. La homotopía topológica establece un método matemático de caracterización.
Defectos puntuales
Los defectos puntuales son defectos que ocurren solo en o alrededor de un único punto reticular. No se extienden en el espacio en ninguna dimensión. Los límites estrictos de cuán pequeño es un defecto puntual generalmente no se definen explícitamente. Sin embargo, estos defectos generalmente involucran como máximo unos pocos átomos adicionales o faltantes. Los defectos más grandes en una estructura ordenada generalmente se consideran bucles de dislocación. Por razones históricas, muchos defectos puntuales, especialmente en cristales iónicos, se denominan centros: por ejemplo, una vacante en muchos sólidos iónicos se denomina centro de luminiscencia, centro de color o centro F. Estas dislocaciones permiten el transporte iónico a través de cristales que conducen a reacciones electroquímicas. Estos se especifican con frecuencia utilizando la notación Kröger-Vink.
- Los defectos de vacaciones son sitios de celosía que estarían ocupados en un cristal perfecto, pero están vacantes. Si un átomo vecino se mueve a ocupar el sitio vacante, la vacante se mueve en la dirección opuesta al sitio que solía ser ocupado por el átomo en movimiento. La estabilidad de la estructura cristalina circundante garantiza que los átomos vecinos no se derrumben simplemente alrededor de la vacante. En algunos materiales, los átomos vecinos realmente se alejan de una vacante, porque experimentan atracción de los átomos en el entorno. Una vacante (o par de vacantes en un sólido iónico) se llama a veces un defecto de Schottky.
- Los defectos intersticiales son átomos que ocupan un sitio en la estructura cristalina en la que generalmente no hay un átomo. Generalmente son configuraciones de alta energía. Los átomos pequeños (principalmente impurezas) en algunos cristales pueden ocupar intersticios sin alta energía, como el hidrógeno en el palladio.
- Un par cercano de una vacante y un intersticial se llama a menudo un defecto de Frenkel o par de Frenkel. Esto es causado cuando un ión se mueve en un sitio intersticial y crea una vacante.
- Debido a las limitaciones fundamentales de los métodos de purificación de materiales, los materiales nunca son 100% puros, que por definición induce defectos en la estructura de cristal. En el caso de una impureza, el átomo se incorpora a menudo en un sitio atómico regular en la estructura de cristal. Este no es un sitio vacío ni es el átomo en un sitio intersticial y se llama defecto substitucional. El átomo no se supone que esté en ninguna parte del cristal, y por lo tanto es una impureza. En algunos casos en que el radio del átomo sustitucional (ion) es sustancialmente más pequeño que el del átomo (ion) que está reemplazando, su posición de equilibrio puede ser desplazada lejos del sitio de la celosía. Estos tipos de defectos sustitucionales a menudo se denominan iones fuera del centro. Existen dos tipos diferentes de defectos sustitucionales: sustitución isovalenta y sustitución aliovalente. Sustitución isovalent es donde el ion que está sustituyendo el ion original es del mismo estado de oxidación que el ión que está reemplazando. Sustitución Aliovalent es donde el ion que está sustituyendo el ion original es de un estado de oxidación diferente que el ion que está reemplazando. Las sustituciones Aliovalent cambian la carga general dentro del complejo iónico, pero el compuesto iónico debe ser neutral. Por lo tanto, se requiere un mecanismo de compensación de cargos. De ahí que uno de los metales sea parcial o totalmente oxidado o reducido, o se crean vacantes de iones.
- Defectos antisitios ocurre en una aleación ordenada o compuesto cuando átomos de diferentes posiciones de cambio de tipo. Por ejemplo, algunas aleaciones tienen una estructura regular en la que cada otro átomo es una especie diferente; para la ilustración asumen que los átomos tipo A se sientan en las esquinas de una celosía cúbica, y los átomos tipo B se sientan en el centro de los cubos. Si un cubo tiene un átomo A en su centro, el átomo está en un sitio generalmente ocupado por un átomo B, y es por lo tanto un defecto antisitio. Esto no es una vacante ni una intersticial, ni una impureza.
- Los defectos Topológicos son regiones en un cristal donde el entorno de unión química normal es topológicamente diferente del entorno. Por ejemplo, en una hoja perfecta de grafito (graphene) todos los átomos están en anillos que contienen seis átomos. Si la hoja contiene regiones donde el número de átomos en un anillo es diferente de seis, mientras que el número total de átomos sigue siendo el mismo, se ha formado un defecto topológico. Un ejemplo es el defecto de Stone Wales en nanotubes, que consiste en dos anillos de átomo adyacentes de 5 miembros y dos de 7 miembros.
- También los sólidos amorfos pueden contener defectos. Estos son naturalmente un poco difíciles de definir, pero a veces su naturaleza puede ser muy fácil de entender. Por ejemplo, en la silica amorfo idealmente unida todos los átomos Si tienen 4 lazos a los átomos O y todos los átomos O tienen 2 lazos a los átomos de Si. Así, por ejemplo, un átomo de O con sólo un vínculo Si (un vínculo colgante) puede considerarse un defecto en sílice. Además, los defectos también se pueden definir en sólidos amorfos basados en barrios atómicos locales vacíos o empaquetados densamente, y las propiedades de tales 'defectos' se pueden mostrar como similares a las vacantes normales e intersticiales en cristales.
- Los complejos pueden formar entre diferentes tipos de defectos de puntos. Por ejemplo, si una vacante encuentra una impureza, los dos pueden unirse si la impureza es demasiado grande para la celosía. Los intersticiales pueden formar estructuras intersticiales individuales o "dumbbell" donde dos átomos efectivamente comparten un sitio atómico, resultando en que ninguno de los átomos ocupa realmente el sitio.
Defectos de línea
Los defectos de línea se pueden describir mediante teorías de calibre.
Las dislocaciones son defectos lineales, alrededor de los cuales los átomos de la red cristalina están desalineados. Hay dos tipos básicos de dislocaciones, la dislocación borde y la dislocación tornillo. "Mixto" las dislocaciones, que combinan aspectos de ambos tipos, también son comunes.
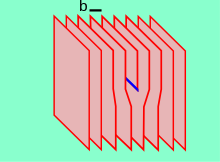
Las dislocaciones de borde son causadas por la terminación de un plano de átomos en el medio de un cristal. En tal caso, los planos adyacentes no son rectos, sino que se doblan alrededor del borde del plano de terminación para que la estructura cristalina esté perfectamente ordenada en ambos lados. La analogía con una pila de papel es adecuada: si se inserta la mitad de una hoja de papel en una pila de papel, el defecto en la pila solo se nota en el borde de la mitad de la hoja.
La dislocación del tornillo es más difícil de visualizar, pero básicamente comprende una estructura en la que los planos atómicos de los átomos en la red cristalina trazan una trayectoria helicoidal alrededor del defecto lineal (línea de dislocación).
La presencia de dislocación da como resultado tensión (distorsión) de la red. La dirección y magnitud de dicha distorsión se expresa en términos de un vector de Burgers (b). Para un tipo de borde, b es perpendicular a la línea de dislocación, mientras que en los casos de tipo tornillo es paralelo. En materiales metálicos, b está alineado con direcciones cristalográficas compactas y su magnitud es equivalente a un espacio interatómico.
Las dislocaciones pueden moverse si los átomos de uno de los planos circundantes rompen sus enlaces y se vuelven a unir con los átomos en el borde de terminación.
Es la presencia de dislocaciones y su capacidad para moverse fácilmente (e interactuar) bajo la influencia de tensiones inducidas por cargas externas lo que conduce a la maleabilidad característica de los materiales metálicos.
Las dislocaciones se pueden observar mediante microscopía electrónica de transmisión, microscopía de iones de campo y técnicas de sonda atómica. La espectroscopia transitoria de nivel profundo se ha utilizado para estudiar la actividad eléctrica de dislocaciones en semiconductores, principalmente silicio.
Las disclinaciones son defectos de línea correspondientes a "agregar" o "restar" un ángulo alrededor de una línea. Básicamente, esto significa que si rastrea la orientación del cristal alrededor del defecto de la línea, obtiene una rotación. Por lo general, se pensaba que solo desempeñaban un papel en los cristales líquidos, pero desarrollos recientes sugieren que también podrían tener un papel en materiales sólidos, p. lo que conduce a la autocuración de las grietas.
Defectos planos
- Los límites de la cola ocurren donde la dirección cristalográfica de la celosía cambia abruptamente. Esto ocurre generalmente cuando dos cristales comienzan a crecer por separado y luego se encuentran.
- Los límites antifase ocurren en aleaciones ordenadas: en este caso, la dirección cristalográfica sigue siendo la misma, pero cada lado del límite tiene una fase opuesta: Por ejemplo, si el pedido es generalmente ABABABAB (cristal hexagonal colgado), un límite antifase toma la forma de ABABBABA.
- Las fallas de apilamiento ocurren en una serie de estructuras de cristal, pero el ejemplo común está en estructuras de cerca. Están formados por una desviación local de la secuencia de apilamiento de capas en un cristal. Un ejemplo sería la secuencia de apilamiento ABABCABAB.
- Un límite gemelo es un defecto que introduce un plano de simetría espejo en el orden de un cristal. Por ejemplo, en cristales cúbicos de cerca empaquetados, la secuencia de apilamiento de un límite gemelo sería ABCABCBACBA.
- En los planos de cristales individuales, los pasos entre las terrazas planas atómicas también se pueden considerar como defectos planos. Se ha demostrado que tales defectos y su geometría tienen una influencia significativa en la adsorción de moléculas orgánicas
Defectos a granel
- Defectos macroscópicos tridimensionales o masivos, como poros, grietas o inclusiones
- Vacíos - regiones pequeñas donde no hay átomos, y que se pueden considerar como grupos de vacantes
- Las impurezas pueden agruparse para formar pequeñas regiones de una fase diferente. Estos son a menudo llamados precipitados.
Métodos de clasificación matemática
Un método de clasificación matemática exitoso para los defectos físicos de la red, que funciona no solo con la teoría de las dislocaciones y otros defectos en los cristales, sino también, por ejemplo, para las disclinaciones en los cristales líquidos y para las excitaciones en los superfluidos 3 He, es la teoría de la homotopía topológica.
Métodos de simulación por computadora
Teoría del funcional de la densidad, dinámica molecular clásica y Monte Carlo cinético Las simulaciones se utilizan ampliamente para estudiar las propiedades de los defectos en los sólidos con simulaciones por computadora. Simulación de atascos de esferas duras de diferentes tamaños y/o en contenedores con tamaños no medibles utilizando el algoritmo de Lubachevsky-Stillinger puede ser una técnica eficaz para demostrar algunos tipos de defectos cristalográficos.
Contenido relacionado
Ciclo CNO
Lev Landau
Profundidad óptica