Datación radiométrica
La datación radiométrica, datación radiactiva o datación radioisotópica es una técnica que se utiliza para datar materiales como rocas o carbono, en los que se han obtenido trazas de impurezas radiactivas. incorporados selectivamente cuando se formaron. El método compara la abundancia de un isótopo radiactivo natural dentro del material con la abundancia de sus productos de desintegración, que se forman a una tasa de desintegración constante conocida. El uso de la datación radiométrica fue publicado por primera vez en 1907 por Bertram Boltwood y ahora es la principal fuente de información sobre la edad absoluta de las rocas y otras características geológicas, incluida la edad de las formas de vida fosilizadas o la edad de la Tierra misma, y también puede ser utilizado hasta la fecha una amplia gama de materiales naturales y artificiales.
Junto con los principios estratigráficos, los métodos de datación radiométrica se utilizan en geocronología para establecer la escala de tiempo geológico. Entre las técnicas más conocidas se encuentran la datación por radiocarbono, la datación por potasio-argón y la datación por uranio-plomo. Al permitir el establecimiento de escalas de tiempo geológicas, proporciona una importante fuente de información sobre las edades de los fósiles y las tasas deducidas de cambio evolutivo. La datación radiométrica también se utiliza para datar materiales arqueológicos, incluidos artefactos antiguos.
Los diferentes métodos de datación radiométrica varían en la escala de tiempo en la que son precisos y los materiales a los que se pueden aplicar.
Fundamentos
Desintegración radiactiva
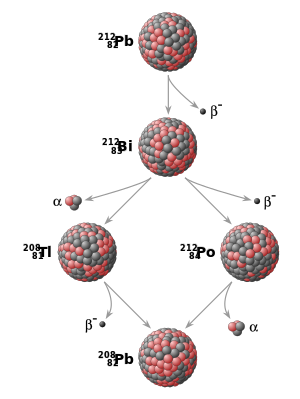
Toda la materia ordinaria está formada por combinaciones de elementos químicos, cada uno con su propio número atómico, que indica el número de protones en el núcleo atómico. Además, los elementos pueden existir en diferentes isótopos, y cada isótopo de un elemento difiere en el número de neutrones en el núcleo. Un isótopo particular de un elemento particular se llama nucleido. Algunos nucleidos son intrínsecamente inestables. Es decir, en algún momento, un átomo de tal nucleido sufrirá una desintegración radiactiva y se transformará espontáneamente en un nucleido diferente. Esta transformación se puede lograr de varias maneras diferentes, incluida la desintegración alfa (emisión de partículas alfa) y la desintegración beta (emisión de electrones, emisión de positrones o captura de electrones). Otra posibilidad es la fisión espontánea en dos o más nucleidos.
Si bien el momento en el tiempo en el que un núcleo en particular se desintegra es impredecible, una colección de átomos de un nucleido radiactivo se desintegra exponencialmente a una velocidad descrita por un parámetro conocido como vida media, que generalmente se expresa en unidades de años cuando se analiza la datación. tecnicas Después de que haya transcurrido una vida media, la mitad de los átomos del nucleido en cuestión se habrán desintegrado en un 'hijo'. nucleido o producto de desintegración. En muchos casos, el propio nucleido hijo es radiactivo, lo que da como resultado una cadena de desintegración que finalmente termina con la formación de un nucleido hijo estable (no radiactivo); cada paso en tal cadena se caracteriza por una vida media distinta. En estos casos, por lo general, la vida media de interés en la datación radiométrica es la más larga de la cadena, que es el factor limitante de la velocidad en la transformación final del nucleido radiactivo en su hijo estable. Los sistemas isotópicos que se han explotado para la datación radiométrica tienen vidas medias que van desde solo unos 10 años (p. ej., tritio) hasta más de 100 000 millones de años (p. ej., samario-147).
Para la mayoría de los nucleidos radiactivos, la vida media depende únicamente de las propiedades nucleares y es esencialmente constante. Esto se sabe porque las constantes de descomposición medidas por diferentes técnicas dan valores consistentes dentro de los errores analíticos y las edades de los mismos materiales son consistentes de un método a otro. No se ve afectado por factores externos como la temperatura, la presión, el entorno químico o la presencia de un campo magnético o eléctrico. Las únicas excepciones son los nucleidos que se desintegran mediante el proceso de captura de electrones, como el berilio-7, el estroncio-85 y el zirconio-89, cuya tasa de desintegración puede verse afectada por la densidad electrónica local. Para todos los demás nucleidos, la proporción del nucleido original con respecto a sus productos de descomposición cambia de manera predecible a medida que el nucleido original se desintegra con el tiempo.
Esta previsibilidad permite que las abundancias relativas de nucleidos relacionados se utilicen como un reloj para medir el tiempo desde la incorporación de los nucleidos originales en un material hasta el presente. La naturaleza nos ha proporcionado convenientemente nucleidos radiactivos que tienen vidas medias que van desde considerablemente más largas que la edad del universo hasta menos de un zeptosegundo. Esto permite medir una gama muy amplia de edades. Los isótopos con vidas medias muy largas se denominan "isótopos estables" y los isótopos con vidas medias muy cortas se conocen como "isótopos extintos".
Determinación de la constante de decaimiento
La constante de desintegración radiactiva, la probabilidad de que un átomo se desintegre por año, es la base sólida de la medición común de la radiactividad. La exactitud y precisión de la determinación de una edad (y la vida media de un nucleido) depende de la exactitud y precisión de la medición de la constante de desintegración. El método de crecimiento interno es una forma de medir la constante de descomposición de un sistema, lo que implica la acumulación de nucleidos hijos. Desafortunadamente, para los nucleidos con constantes de desintegración altas (que son útiles para fechar muestras muy antiguas), se requieren largos períodos de tiempo (décadas) para acumular suficientes productos de desintegración en una sola muestra para medirlos con precisión. Un método más rápido consiste en utilizar contadores de partículas para determinar la actividad alfa, beta o gamma, y luego dividirla por el número de nucleidos radiactivos. Sin embargo, es difícil y costoso determinar con precisión la cantidad de nucleidos radiactivos. Alternativamente, las constantes de descomposición se pueden determinar comparando datos de isótopos para rocas de edad conocida. Este método requiere que al menos uno de los sistemas de isótopos esté calibrado con mucha precisión, como el sistema Pb-Pb.
Precisión de la datación radiométrica
La ecuación básica de la datación radiométrica requiere que ni el núclido padre ni el producto hijo puedan entrar o salir del material después de su formación. Deben considerarse los posibles efectos de confusión de la contaminación de los isótopos padre e hijo, al igual que los efectos de cualquier pérdida o ganancia de tales isótopos desde que se creó la muestra. Por lo tanto, es esencial tener la mayor información posible sobre el material que se está fechando y verificar posibles signos de alteración. La precisión se mejora si se toman medidas en múltiples muestras de diferentes ubicaciones del cuerpo rocoso. Alternativamente, si se pueden fechar varios minerales diferentes de la misma muestra y se supone que se formaron por el mismo evento y estaban en equilibrio con el yacimiento cuando se formaron, deberían formar una isócrona. Esto puede reducir el problema de la contaminación. En la datación con uranio-plomo, se utiliza el diagrama de concordia, que también disminuye el problema de la pérdida de nucleidos. Finalmente, puede ser necesaria la correlación entre diferentes métodos de datación isotópica para confirmar la edad de una muestra. Por ejemplo, la edad de los gneises Amitsoq del oeste de Groenlandia se determinó en 3,60 ± 0,05 Ga (hace mil millones de años) utilizando la datación con uranio-plomo y 3,56 ± 0,10 Ga (hace mil millones de años) utilizando la datación con plomo-plomo, resultados que son consistentes juntos.
La datación radiométrica precisa generalmente requiere que el padre tenga una vida media lo suficientemente larga como para que esté presente en cantidades significativas en el momento de la medición (excepto como se describe a continuación en "Datación con radionúclidos extintos de vida corta").;), la vida media del padre se conoce con precisión y se produce suficiente producto hijo para medirlo con precisión y distinguirlo de la cantidad inicial del hijo presente en el material. Los procedimientos utilizados para aislar y analizar los nucleidos padre e hijo deben ser precisos y exactos. Esto normalmente implica espectrometría de masas de relación isotópica.
La precisión de un método de datación depende en parte de la vida media del isótopo radiactivo involucrado. Por ejemplo, el carbono-14 tiene una vida media de 5.730 años. Después de que un organismo ha estado muerto durante 60.000 años, queda tan poco carbono-14 que no se puede establecer una fecha exacta. Por otro lado, la concentración de carbono-14 cae tan abruptamente que la edad de los restos relativamente jóvenes se puede determinar con precisión en unas pocas décadas.
Temperatura de cierre
La temperatura de cierre o temperatura de bloqueo representa la temperatura por debajo de la cual el mineral es un sistema cerrado para los isótopos estudiados. Si un material que rechaza selectivamente el nucleido hijo se calienta por encima de esta temperatura, cualquier nucleido hijo que se haya acumulado con el tiempo se perderá por difusión, reiniciando el 'reloj' isotópico. a cero. A medida que el mineral se enfría, la estructura cristalina comienza a formarse y la difusión de los isótopos es menos fácil. A cierta temperatura, la estructura cristalina se ha formado lo suficiente como para evitar la difusión de isótopos. Por lo tanto, una roca ígnea o metamórfica o un fundido, que se está enfriando lentamente, no comienza a exhibir un decaimiento radiactivo medible hasta que se enfría por debajo de la temperatura de cierre. La edad que se puede calcular mediante datación radiométrica es, por lo tanto, el momento en que la roca o el mineral se enfrió hasta la temperatura de cierre. Esta temperatura varía para cada mineral y sistema isotópico, por lo que un sistema puede estar cerrado para un mineral pero abierto para otro. La datación de diferentes minerales y/o sistemas de isótopos (con diferentes temperaturas de cierre) dentro de la misma roca, por lo tanto, puede permitir el seguimiento de la historia térmica de la roca en cuestión a lo largo del tiempo y, por lo tanto, la historia de los eventos metamórficos puede conocerse en detalle. Estas temperaturas se determinan experimentalmente en el laboratorio mediante el restablecimiento artificial de minerales de muestra utilizando un horno de alta temperatura. Este campo se conoce como termocronología o termocronometría.
La ecuación de la edad
La expresión matemática que relaciona la desintegración radiactiva con el tiempo geológico es
dónde
- t es la edad de la muestra,
- D* es el número de átomos de la hija radiógena isótopo en la muestra,
- D0 es el número de átomos de la hija isótopo en la composición original o inicial,
- N()t) es el número de átomos del isótopo padre en la muestra a tiempo t (el presente), dado por N()t) N0e−λt, y
- λ es la constante decadente del isótopo padre, igual a la inversa de la media vida radioactiva del padre isótopo tiempos el logaritmo natural de 2.
La ecuación se expresa más convenientemente en términos de la cantidad medida N(t) en lugar del valor inicial constante No.
Para calcular la edad, se supone que el sistema está cerrado (ni los isótopos padre ni los hijos se han perdido del sistema), D0 debe ser insignificante o se puede estimar con precisión, λ se conoce con gran precisión y se tienen medidas exactas y precisas de D* y N(t).
La ecuación anterior utiliza información sobre la composición de los isótopos padre e hijo en el momento en que el material que se está probando se enfrió por debajo de su temperatura de cierre. Esto está bien establecido para la mayoría de los sistemas isotópicos. Sin embargo, la construcción de una isócrona no requiere información sobre las composiciones originales, utilizando simplemente las proporciones actuales de los isótopos padre e hijo a un isótopo estándar. Se utiliza una gráfica isócrona para resolver gráficamente la ecuación de la edad y calcular la edad de la muestra y la composición original.
Métodos modernos de citas
La datación radiométrica se lleva a cabo desde 1905, cuando Ernest Rutherford la inventó como un método para determinar la edad de la Tierra. En el siglo transcurrido desde entonces, las técnicas se han mejorado y ampliado considerablemente. La datación ahora se puede realizar en muestras tan pequeñas como un nanogramo utilizando un espectrómetro de masas. El espectrómetro de masas se inventó en la década de 1940 y comenzó a utilizarse en la datación radiométrica en la década de 1950. Opera generando un haz de átomos ionizados a partir de la muestra bajo prueba. Luego, los iones viajan a través de un campo magnético, que los desvía hacia diferentes sensores de muestreo, conocidos como 'copas de Faraday', según su masa y nivel de ionización. Al impactar en las copas, los iones generan una corriente muy débil que se puede medir para determinar la tasa de impactos y las concentraciones relativas de diferentes átomos en los haces.
Método de datación uranio-plomo

La datación radiométrica de uranio-plomo implica el uso de uranio-235 o uranio-238 para fechar la edad absoluta de una sustancia. Este esquema se ha refinado hasta el punto de que el margen de error en las fechas de las rocas puede ser tan bajo como menos de dos millones de años en dos mil quinientos millones de años. Se ha logrado un margen de error del 2 al 5% en rocas mesozoicas más jóvenes.
La datación con uranio-plomo a menudo se realiza en el mineral circón (ZrSiO4), aunque se puede usar en otros materiales, como la baddeleyita y la monacita (ver: geocronología de la monacita). El circón y la baddeleyita incorporan átomos de uranio en su estructura cristalina como sustitutos del circonio, pero rechazan fuertemente el plomo. El circón tiene una temperatura de cierre muy alta, es resistente a la intemperie mecánica y es químicamente muy inerte. Zircon también forma múltiples capas de cristal durante los eventos metamórficos, cada uno de los cuales puede registrar una edad isotópica del evento. El análisis de microhaz in situ se puede lograr mediante técnicas láser ICP-MS o SIMS.
Una de sus grandes ventajas es que cualquier muestra proporciona dos relojes, uno basado en la descomposición del uranio-235 a plomo-207 con una vida media de unos 700 millones de años, y otro basado en el uranio-238. 39;s decae a plomo-206 con una vida media de aproximadamente 4.500 millones de años, lo que proporciona una verificación cruzada incorporada que permite una determinación precisa de la edad de la muestra, incluso si se ha perdido parte del plomo. Esto se puede ver en el diagrama de concordia, donde las muestras se trazan a lo largo de un cron de error (línea recta) que se cruza con la curva de concordia en la edad de la muestra.
Método de datación samario-neodimio
Esto implica la descomposición alfa de 147Sm a 143Nd con una vida media de 1,06 x 1011 años. Se pueden alcanzar niveles de precisión dentro de los veinte millones de años en edades de dos mil quinientos millones de años.
Método de datación potasio-argón
Esto implica la captura de electrones o la descomposición de positrones de potasio-40 a argón-40. El potasio-40 tiene una vida media de 1300 millones de años, por lo que este método es aplicable a las rocas más antiguas. El potasio-40 radiactivo es común en micas, feldespatos y hornblenda, aunque la temperatura de cierre es bastante baja en estos materiales, alrededor de 350 °C (mica) a 500 °C (hornblenda).
Método de datación rubidio-estroncio
Esto se basa en la desintegración beta del rubidio-87 al estroncio-87, con una vida media de 50 000 millones de años. Este esquema se utiliza para fechar rocas ígneas y metamórficas antiguas, y también se ha utilizado para fechar muestras lunares. Las temperaturas de cierre son tan altas que no son una preocupación. La datación con rubidio-estroncio no es tan precisa como el método de uranio-plomo, con errores de 30 a 50 millones de años para una muestra de 3 mil millones de años. La aplicación de análisis in situ (ICP-MS de ablación por láser) dentro de granos minerales individuales en fallas ha demostrado que el método Rb-Sr puede usarse para descifrar episodios de movimiento de fallas.
Método de datación por uranio-torio
Una técnica de datación de rango relativamente corto se basa en la descomposición del uranio-234 en torio-230, una sustancia con una vida media de unos 80.000 años. Está acompañado por un proceso hermano, en el que el uranio-235 se descompone en protactinio-231, que tiene una vida media de 32.760 años.
Si bien el uranio es soluble en agua, el torio y el protactinio no lo son, por lo que se precipitan selectivamente en los sedimentos del fondo oceánico, a partir de los cuales se miden sus proporciones. El esquema tiene un rango de varios cientos de miles de años. Un método relacionado es la datación por ionio-torio, que mide la proporción de ionio (torio-230) a torio-232 en los sedimentos oceánicos.
Método de datación por radiocarbono
La datación por radiocarbono también se denomina simplemente datación por carbono-14. El carbono-14 es un isótopo radiactivo del carbono, con una vida media de 5.730 años (que es muy corta en comparación con los isótopos anteriores), y se descompone en nitrógeno. En otros métodos de datación radiométrica, los isótopos progenitores pesados se produjeron mediante nucleosíntesis en supernovas, lo que significa que cualquier isótopo progenitor con una vida media corta ya debería estar extinto. Sin embargo, el carbono 14 se crea continuamente a través de colisiones de neutrones generados por rayos cósmicos con nitrógeno en la atmósfera superior y, por lo tanto, permanece en un nivel casi constante en la Tierra. El carbono-14 termina como un componente traza en el dióxido de carbono atmosférico (CO2).
Una forma de vida basada en el carbono adquiere carbono durante su vida. Las plantas lo adquieren a través de la fotosíntesis y los animales lo adquieren del consumo de plantas y otros animales. Cuando un organismo muere, deja de absorber nuevo carbono-14 y el isótopo existente se desintegra con una vida media característica (5730 años). La proporción de carbono-14 que queda cuando se examinan los restos del organismo proporciona una indicación del tiempo transcurrido desde su muerte. Esto hace que el carbono-14 sea un método de datación ideal para fechar la edad de los huesos o los restos de un organismo. El límite de datación por carbono-14 se encuentra entre 58.000 y 62.000 años.
La tasa de creación de carbono-14 parece ser más o menos constante, ya que las comprobaciones cruzadas de la datación por carbono-14 con otros métodos de datación muestran que da resultados consistentes. Sin embargo, las erupciones locales de volcanes u otros eventos que emiten grandes cantidades de dióxido de carbono pueden reducir las concentraciones locales de carbono-14 y dar fechas inexactas. Las liberaciones de dióxido de carbono a la biosfera como consecuencia de la industrialización también han reducido la proporción de carbono-14 en un pequeño porcentaje; por el contrario, la cantidad de carbono-14 aumentó con las pruebas de bombas nucleares sobre el suelo que se llevaron a cabo a principios de la década de 1960. Además, un aumento en el viento solar o el campo magnético de la Tierra por encima del valor actual reduciría la cantidad de carbono-14 creado en la atmósfera.
Método de datación por huella de fisión
Esto implica la inspección de una rebanada pulida de un material para determinar la densidad de la "pista" marcas dejadas en él por la fisión espontánea de impurezas de uranio-238. Se debe conocer el contenido de uranio de la muestra, pero se puede determinar colocando una película de plástico sobre la rebanada pulida del material y bombardeándola con neutrones lentos. Esto provoca la fisión inducida de 235U, a diferencia de la fisión espontánea de 238U. Las huellas de fisión producidas por este proceso se graban en la película de plástico. El contenido de uranio del material se puede calcular a partir del número de pistas y el flujo de neutrones.
Este esquema tiene aplicación en un amplio rango de fechas geológicas. Para fechas de hasta unos pocos millones de años, se utilizan mejor micas, tectitas (fragmentos de vidrio de erupciones volcánicas) y meteoritos. Los materiales más antiguos se pueden fechar utilizando circón, apatito, titanita, epidota y granate, que tienen una cantidad variable de contenido de uranio. Debido a que las huellas de fisión se curan con temperaturas superiores a los 200 °C, la técnica tiene limitaciones además de beneficios. La técnica tiene aplicaciones potenciales para detallar la historia térmica de un depósito.
Método de datación Cloro-36
La irradiación del agua de mar durante las detonaciones atmosféricas de armas nucleares entre 1952 y 1958 produjo grandes cantidades de 36Cl, que de otro modo sería raro (vida media ~300ky). El tiempo de residencia de 36Cl en la atmósfera es alrededor de 1 semana. Por lo tanto, como marcador de eventos del agua en el suelo y las aguas subterráneas de la década de 1950, 36Cl también es útil para datar aguas de menos de 50 años antes del presente. 36Cl se ha utilizado en otras áreas de las ciencias geológicas, incluida la datación de hielo y sedimentos.
Métodos de datación por luminiscencia
Los métodos de datación por luminiscencia no son métodos de datación radiométrica en el sentido de que no dependen de la abundancia de isótopos para calcular la edad. En cambio, son una consecuencia de la radiación de fondo sobre ciertos minerales. Con el tiempo, la radiación ionizante es absorbida por los granos minerales en sedimentos y materiales arqueológicos como el cuarzo y el feldespato potásico. La radiación hace que la carga permanezca dentro de los granos en "trampas de electrones" estructuralmente inestables. La exposición a la luz solar o al calor libera estas cargas, "blanqueando" la muestra y poner el reloj a cero. La carga atrapada se acumula con el tiempo a un ritmo determinado por la cantidad de radiación de fondo en el lugar donde se enterró la muestra. Estimular estos granos minerales utilizando luz (luminiscencia estimulada ópticamente o datación por luminiscencia estimulada por infrarrojos) o calor (datación por termoluminiscencia) hace que se emita una señal de luminiscencia a medida que se libera la energía de electrones inestables almacenada, cuya intensidad varía según la cantidad de radiación. absorbido durante el entierro y propiedades específicas del mineral.
Estos métodos se pueden usar para fechar la edad de una capa de sedimento, ya que las capas depositadas en la parte superior evitarían que los granos se "blanqueen" y reiniciado por la luz del sol. Los fragmentos de cerámica se pueden fechar en la última vez que experimentaron un calor significativo, generalmente cuando se cocieron en un horno.
Otros métodos
Otros métodos incluyen:
- Argon-argon (Ar-Ar)
- Iodine–xenon (I–Xe)
- Lanthanum–barium (La–Ba)
- Lead–lead (Pb–Pb)
- Lutetium-hafnium (Lu-Hf)
- Hafnium-tungsten dating (Hf-W)
- Potasio–calcio (K–Ca)
- Rhenium-osmium (Re-Os)
- Uranio–uranio (U–U)
- Krypton–krypton (Kr–Kr)
- Berilio (Berilio)10Sé...9Be)
Datación con productos de descomposición de radionúclidos extintos de vida corta
La datación radiométrica absoluta requiere que una fracción medible del núcleo principal permanezca en la muestra de roca. Para las rocas que se remontan al comienzo del sistema solar, esto requiere isótopos progenitores extremadamente longevos, por lo que la medición de tales rocas " edades exactas imprecisas. Para poder distinguir las edades relativas de las rocas a partir de material tan antiguo y obtener una mejor resolución de tiempo que la disponible a partir de isótopos de vida larga, se pueden usar isótopos de vida corta que ya no están presentes en la roca.
Al principio del sistema solar, había varios radionucleidos de vida relativamente corta como 26Al, 60Fe, 53Mn, y 129presento dentro de la nebulosa solar. Estos radionúclidos, posiblemente producidos por la explosión de una supernova, están extintos en la actualidad, pero sus productos de descomposición pueden detectarse en material muy antiguo, como el que constituye los meteoritos. Mediante la medición de los productos de desintegración de los radionucleidos extintos con un espectrómetro de masas y el uso de diagramas de isócrono, es posible determinar las edades relativas de diferentes eventos en la historia temprana del sistema solar. Los métodos de datación basados en radionucleidos extinguidos también se pueden calibrar con el método U-Pb para obtener edades absolutas. Así se puede obtener tanto la edad aproximada como una alta resolución temporal. En general, una vida media más corta conduce a una resolución de tiempo más alta a expensas de la escala de tiempo.
El cronómetro 129I – 129Xe
129
I
beta-decae a 129
Xe
con una vida media de 16 millones de años. El cronómetro de yodo-xenón es una técnica isócrona. Las muestras se exponen a neutrones en un reactor nuclear. Esto convierte el único isótopo estable de yodo ( 127
I
) en 128
Xe
mediante captura de neutrones seguida de desintegración beta (de 128
I
). Después de la irradiación, las muestras se calientan en una serie de pasos y se analiza la firma isotópica de xenón del gas que se desprende en cada paso. Cuando un 129
Xe
/128
Xe
se observa una relación de temperatura en varias temperaturas consecutivaspasos, se puede interpretar como correspondiente a un momento en el que la muestra dejó de perder xenón.
Las muestras de un meteorito llamado Shallowater generalmente se incluyen en la irradiación para monitorear la eficiencia de conversión de 127
I
a 128
Xe
. La diferencia entre el 129
Xe
/128
Xe
proporciones de la muestra y Shallowater luego corresponde a las diferentes proporciones de 129
I
/127
I
cuando dejaron de perder xenón. Esto a su vez corresponde a una diferencia en la edad de cierre en el sistema solar primitivo.
El cronómetro 26Al – 26Mg
Otro ejemplo de datación por radionúclidos extintos de corta duración es el 26Al – 26
Mg
cronómetro, que puede usarse para estimar las edades relativas de los cóndrulos. 26
Al
decae a 26
Mg
con una vida media de 720 000 años. La datación es simplemente una cuestión de encontrar la desviación de la abundancia natural de 26
Mg
(el producto de 26
Al
decaimiento) en comparación con la proporción de isótopos estables 27
Al
/24
Mg
.
El exceso de 26
Mg
(a menudo designado 26
Mg
*) se encuentra comparando el 26
Mg
/27
Mg
relación con la de otros materiales del Sistema Solar.
El 26
Al
– 26
Mg
da una estimación del período de tiempo para la formación de meteoritos primitivos de solo unos pocos millones de años (1,4 millones de años para la formación de Chondrule).
Un problema de terminología
En un artículo de julio de 2022 en la revista Applied Geochemistry, los autores propusieron que los términos "isótopo principal" e "isótopo hijo» en favor del "isótopo precursor" más descriptivo e "isótopo de producto", análogo a "ion precursor" e "ion de producto" en espectrometría de masas.
Contenido relacionado
Texline, Texas
Odden, Utah
Sonda atómica



