Curva de disociación oxígeno-hemoglobina
La curva de disociación oxígeno-hemoglobina, también llamada curva de disociación de oxihemoglobina o curva de disociación de oxígeno (ODC ), es una curva que traza la proporción de hemoglobina en su forma saturada (cargada de oxígeno) en el eje vertical frente a la tensión de oxígeno predominante en el eje horizontal. Esta curva es una herramienta importante para comprender cómo nuestra sangre transporta y libera oxígeno. En concreto, la curva de disociación de la oxihemoglobina relaciona la saturación de oxígeno (SO2) y la presión parcial de oxígeno en sangre (PO2 ), y está determinada por lo que se llama "afinidad de la hemoglobina por el oxígeno"; es decir, con qué facilidad la hemoglobina adquiere y libera moléculas de oxígeno en el líquido que la rodea.

Fondo
La hemoglobina (Hb) es el vehículo principal para transportar oxígeno en la sangre. Cada molécula de hemoglobina tiene la capacidad de llevar cuatro moléculas de oxígeno. Estas moléculas de oxígeno se unen al hierro del grupo de prótesis heme.
Cuando la hemoglobina no tiene oxígeno unido ni dióxido de carbono unido, tiene la conformación (forma) libre. La unión de la primera molécula de oxígeno induce un cambio en la forma de la hemoglobina que aumenta su capacidad para unirse a las otras tres moléculas de oxígeno.
En presencia de dióxido de carbono disuelto, el pH de la sangre cambia; esto provoca otro cambio en la forma de la hemoglobina, que aumenta su capacidad para unir dióxido de carbono y disminuye su capacidad para unir oxígeno. Con la pérdida de la primera molécula de oxígeno y la unión de la primera molécula de dióxido de carbono, se produce otro cambio de forma, que disminuye aún más la capacidad de unir oxígeno y aumenta la capacidad de unir dióxido de carbono. El oxígeno unido a la hemoglobina se libera al plasma sanguíneo y se absorbe en los tejidos, y el dióxido de carbono de los tejidos se une a la hemoglobina.
En los pulmones se produce el reverso de este proceso. Con la pérdida de la primera molécula de dióxido de carbono la forma cambia de nuevo y hace más fácil liberar los otros tres dióxidos de carbono.
El oxígeno también se lleva disuelto en el plasma de la sangre, pero en un grado mucho menor. La hemoglobina está contenida en los glóbulos rojos. La hemoglobina libera el oxígeno ligado cuando el ácido carbónico está presente, como está en los tejidos. En los capilares, donde se produce dióxido de carbono, el oxígeno ligado a la hemoglobina se libera en el plasma de la sangre y se absorbe en los tejidos.
La cantidad de esa capacidad que se llena con oxígeno en cualquier momento se llama saturación de oxígeno. Expresada como porcentaje, la saturación de oxígeno es la relación entre la cantidad de oxígeno unido a la hemoglobina y la capacidad de transporte de oxígeno de la hemoglobina. La capacidad de la hemoglobina para transportar oxígeno está determinada por el tipo de hemoglobina presente en la sangre. La cantidad de oxígeno unido a la hemoglobina en cualquier momento está relacionada, en gran parte, con la presión parcial de oxígeno a la que está expuesta la hemoglobina. En los pulmones, en la interfaz alveolar-capilar, la presión parcial de oxígeno suele ser alta y, por lo tanto, el oxígeno se une fácilmente a la hemoglobina presente. A medida que la sangre circula hacia otros tejidos del cuerpo en los que la presión parcial de oxígeno es menor, la hemoglobina libera oxígeno en el tejido porque la hemoglobina no puede mantener su capacidad total de oxígeno ligada en presencia de presiones parciales de oxígeno más bajas.
Forma sigmoidea

La curva generalmente se describe mejor mediante un gráfico sigmoideo, utilizando una fórmula del tipo:
Una molécula de hemoglobina puede unir hasta cuatro moléculas de oxígeno mediante un método reversible.
La forma de la curva resulta de la interacción de las moléculas de oxígeno unidas con las moléculas entrantes. La unión de la primera molécula es difícil. Sin embargo, esto facilita la unión del segundo, tercero y cuarto, esto se debe al cambio conformacional inducido en la estructura de la molécula de hemoglobina inducido por la unión de una molécula de oxígeno.
En su forma más simple, la curva de disociación de la oxihemoglobina describe la relación entre la presión parcial de oxígeno (eje x) y la saturación de oxígeno (eje y). La afinidad de la hemoglobina por el oxígeno aumenta a medida que se unen sucesivas moléculas de oxígeno. Se unen más moléculas a medida que aumenta la presión parcial de oxígeno hasta alcanzar la cantidad máxima que se puede unir. A medida que se acerca a este límite, se produce muy poca unión adicional y la curva se nivela a medida que la hemoglobina se satura con oxígeno. Por tanto, la curva tiene forma sigmoidea o de S. A presiones superiores a aproximadamente 60 mmHg, la curva de disociación estándar es relativamente plana, lo que significa que el contenido de oxígeno de la sangre no cambia significativamente incluso con grandes aumentos en la presión parcial de oxígeno. Para llevar más oxígeno al tejido se necesitarían transfusiones de sangre para aumentar el recuento de hemoglobina (y por tanto la capacidad de transporte de oxígeno), u oxígeno suplementario que aumentaría el oxígeno disuelto en el plasma. Aunque la unión del oxígeno a la hemoglobina continúa hasta cierto punto para presiones de alrededor de 50 mmHg, a medida que las presiones parciales de oxígeno disminuyen en esta zona pronunciada de la curva, el oxígeno se descarga fácilmente al tejido periférico a medida que disminuye la afinidad de la hemoglobina. La presión parcial de oxígeno en la sangre a la que la hemoglobina está saturada al 50%, normalmente alrededor de 26,6 mmHg (3,5 kPa) para una persona sana, se conoce como P50. El P50 es una medida convencional de la afinidad de la hemoglobina por el oxígeno. En presencia de enfermedades u otras condiciones que cambian la afinidad del oxígeno de la hemoglobina y, en consecuencia, desplazan la curva hacia la derecha o hacia la izquierda, el P50 cambia en consecuencia. Un aumento de P50 indica un desplazamiento hacia la derecha de la curva estándar, lo que significa que es necesaria una presión parcial mayor para mantener una saturación de oxígeno del 50 %. Esto indica una afinidad disminuida. Por el contrario, un P50 más bajo indica un desplazamiento hacia la izquierda y una mayor afinidad.
La 'meseta' Una porción de la curva de disociación de la oxihemoglobina es el rango que existe en los capilares pulmonares (reducción mínima del oxígeno transportado hasta que la p(O2) cae 50 mmHg).
El 'empinado' Una porción de la curva de disociación de la oxihemoglobina es el rango que existe en los capilares sistémicos (una pequeña caída en la p(O2) capilar sistémica puede resultar en la liberación de grandes cantidades de oxígeno para las células metabólicamente activas) .
Para ver las afinidades relativas de cada oxígeno sucesivo a medida que elimina/añade oxígeno de/a la hemoglobina de la curva, compare el aumento/disminución relativo en p(O2) necesario para el aumento correspondiente. /disminución en s(O2).
Factores que afectan a la curva de disociación estándar
La fuerza con la que el oxígeno se une a la hemoglobina se ve afectada por varios factores. Estos factores cambian o remodelan la curva de disociación de la oxihemoglobina. Un desplazamiento hacia la derecha indica que la hemoglobina en estudio tiene una afinidad disminuida por el oxígeno. Esto hace que sea más difícil que la hemoglobina se una al oxígeno (lo que requiere una presión parcial de oxígeno más alta para lograr la misma saturación de oxígeno), pero facilita que la hemoglobina libere el oxígeno unido a ella. El efecto de este desplazamiento de la curva aumenta la presión parcial de oxígeno en los tejidos cuando más se necesita, como durante el ejercicio o el shock hemorrágico.
Por el contrario, la curva se desplaza hacia la izquierda por las condiciones opuestas a estas.
Este cambio indica que la hemoglobina en estudio tiene una mayor afinidad por el oxígeno, de modo que la hemoglobina se une al oxígeno más fácilmente, pero lo descarga con más renuencia. El desplazamiento hacia la izquierda de la curva es un signo de una mayor afinidad de la hemoglobina por el oxígeno (por ejemplo, en los pulmones).
De manera similar, el desplazamiento a la derecha muestra una disminución de la afinidad, como aparecería con un aumento en la temperatura corporal, los iones de hidrógeno, la concentración de 2,3-bisfosfoglicerato (2,3-BPG) o la concentración de dióxido de carbono.
| Factores de control | Cambio | Cambio de curva |
|---|---|---|
| Temperatura | ↑ | → |
| ↓ | ← | |
| 2.3-BPG | ↑ | → |
| ↓ | ← | |
| pCO2 | ↑ | → |
| ↓ | ← | |
| Acididad [H+] | ↑ | → |
| ↓ | ← |
Nota:
- Cambio de izquierda: más alto O2 afinidad
- Cambio derecho: menor O2 afinidad
- hemoglobina fetal tiene O superior2 afinidad que hemoglobina adulta; principalmente debido a la afinidad muy reducida a 2,3-bisphosphoglycerate.
Las causas del desplazamiento hacia la derecha se pueden recordar usando la mnemónica "CADETE, ¡cara a la derecha!" para CO2, ácido, 2,3-DPG, Eejercicio y Temperatura. Los factores que mueven la curva de disociación del oxígeno hacia la derecha son aquellos estados fisiológicos en los que los tejidos necesitan más oxígeno. Por ejemplo, durante el ejercicio, los músculos tienen una tasa metabólica más alta y, en consecuencia, necesitan más oxígeno, producen más dióxido de carbono y ácido láctico y su temperatura aumenta.
PH
Una disminución en el pH (aumento en la concentración de iones H+) desplaza la curva estándar hacia la derecha, mientras que un aumento la desplaza hacia la izquierda. Esto ocurre porque a una mayor concentración de iones H+, varios residuos de aminoácidos, como la histidina 146, existen predominantemente en su forma protonada, lo que les permite formar pares de iones que estabilizan la desoxihemoglobina en el estado T. El estado T tiene una menor afinidad por el oxígeno que el estado R, por lo que con mayor acidez, la hemoglobina se une menos O2 para un PO2 determinado (y más H+). Esto se conoce como efecto Bohr. Una reducción en la capacidad total de unión de la hemoglobina al oxígeno (es decir, un desplazamiento de la curva hacia abajo, no solo hacia la derecha) debido a la reducción del pH se denomina efecto raíz. Esto se ve en los peces óseos. La afinidad de unión de la hemoglobina al O2 es mayor en un pH relativamente alto.
Dióxido de carbono
El dióxido de carbono afecta la curva de dos maneras. En primer lugar, la acumulación de CO2 hace que se generen compuestos carbamino a través de interacciones químicas, que se unen a la hemoglobina formando carbaminohemoglobina. El CO2 se considera una regulación alostérica ya que la inhibición no ocurre en el sitio de unión de la hemoglobina. En segundo lugar, influye en el pH intracelular debido a la formación de iones bicarbonato. La formación de carbaminohemoglobina estabiliza la hemoglobina en estado T mediante la formación de pares iónicos. Sólo alrededor del 5 al 10 % del contenido total de CO2 en la sangre se transporta como compuestos carbamino, mientras que (80–90 %) se transporta como iones bicarbonato y una pequeña cantidad se disuelve en el plasma. La formación de un ion bicarbonato liberará un protón en el plasma, lo que disminuirá el pH (aumento de acidez), lo que también desplaza la curva hacia la derecha como se analizó anteriormente; Los niveles bajos de CO2 en el torrente sanguíneo dan como resultado un pH alto y, por lo tanto, proporcionan condiciones de unión más óptimas para la hemoglobina y el O2. Este es un mecanismo fisiológicamente favorecido, ya que la hemoglobina dejará caer más oxígeno a medida que la concentración de dióxido de carbono aumenta dramáticamente cuando la respiración del tejido ocurre rápidamente y se necesita oxígeno.
2,3-BPG
El 2,3-bisfosfoglicerato o 2,3-BPG (anteriormente llamado 2,3-difosfoglicerato o 2,3-DPG) es un organofosfato formado en los glóbulos rojos durante la glucólisis y es la base conjugada del 2,3-bisfosfoglicerato. ácido. La producción de 2,3-BPG es probablemente un mecanismo adaptativo importante, porque la producción aumenta en varias condiciones en presencia de una disponibilidad disminuida de O2 en el tejido periférico, como hipoxemia, enfermedad pulmonar crónica, anemia, e insuficiencia cardíaca congestiva, entre otros, que requieren una descarga más fácil de oxígeno en el tejido periférico. Los niveles altos de 2,3-BPG desplazan la curva hacia la derecha (como en la infancia), mientras que los niveles bajos de 2,3-BPG provocan un desplazamiento hacia la izquierda, que se observa en estados como el shock séptico y la hipofosfatemia. En ausencia de 2,3-BPG, aumenta la afinidad de la hemoglobina por el oxígeno. El 2,3-BPG actúa como un efector heteroalostérico de la hemoglobina, reduciendo la afinidad de la hemoglobina por el oxígeno al unirse preferentemente a la desoxihemoglobina. Una mayor concentración de BPG en los glóbulos rojos favorece la formación del estado T (tenso o tenso), de baja afinidad, de la hemoglobina, por lo que la curva de unión al oxígeno se desplazará hacia la derecha.
Temperatura
El aumento de la temperatura cambia la curva de disociación de oxígeno a la derecha. Cuando se aumenta la temperatura manteniendo constante la concentración de oxígeno, la saturación de oxígeno disminuye a medida que el vínculo entre oxígeno y hierro se desnaturaliza. Además, con mayor temperatura, la presión parcial del oxígeno aumenta también. Por lo tanto, uno tendrá una menor cantidad de hemoglobina saturada para la misma concentración de oxígeno pero a una mayor presión parcial de oxígeno. Por lo tanto, cualquier punto de la curva cambiará hacia la derecha (debido a una mayor presión parcial de oxígeno) y hacia abajo (debido a debilitarse) bond), por lo tanto, el cambio de la curva a la derecha.
Monóxido de carbono
La hemoglobina se une al monóxido de carbono 210 veces más fácilmente que al oxígeno. Debido a esta mayor afinidad de la hemoglobina por el monóxido de carbono que por el oxígeno, el monóxido de carbono es un competidor muy exitoso que desplazará al oxígeno incluso a presiones parciales minúsculas. La reacción HbO2 + CO → HbCO + O2 desplaza casi irreversiblemente las moléculas de oxígeno formando carboxihemoglobina; la unión del monóxido de carbono al centro de hierro de la hemoglobina es mucho más fuerte que la del oxígeno, y el sitio de unión permanece bloqueado durante el resto del ciclo de vida del glóbulo rojo afectado. Con un nivel elevado de monóxido de carbono, una persona puede sufrir una hipoxia tisular grave mientras mantiene una pO2 normal porque la carboxihemoglobina no transporta oxígeno a los tejidos.
Efectos de la metahemoglobinemia
La metahemoglobinemia es una forma de hemoglobina anormal en la que el centro de hierro se ha oxidado del estado de oxidación ferroso +2 (la forma normal, que al unirse con oxígeno cambia al estado férrico) al estado férrico +3. Esto provoca un desplazamiento hacia la izquierda en la curva de disociación de la hemoglobina oxígeno, ya que cualquier grupo hemo residual con hierro ferroso oxigenado (estado +2) es incapaz de descargar su oxígeno ligado a los tejidos (porque el hierro 3+ perjudica la cooperatividad de la hemoglobina), aumentando así su afinidad con el oxígeno. Sin embargo, la metahemoglobina tiene una mayor afinidad por el cianuro y, por tanto, es útil en el tratamiento del envenenamiento por cianuro. En casos de ingestión accidental, se puede utilizar la administración de un nitrito (como el nitrito de amilo) para oxidar deliberadamente la hemoglobina y elevar los niveles de metahemoglobina, restaurando el funcionamiento de la citocromo oxidasa. El nitrito también actúa como vasodilatador, promoviendo el suministro celular de oxígeno, y la adición de una sal de hierro proporciona la unión competitiva del cianuro libre como el ion hexacianoferrato(III), bioquímicamente inerte, [Fe(CN)6< /sub>]3−. Un enfoque alternativo implica la administración de tiosulfato, convirtiendo así el cianuro en tiocianato, SCN-, que se excreta a través de los riñones. La metahemoglobina también se forma en pequeñas cantidades cuando la disociación de la oxihemoglobina da como resultado la formación de metahemoglobina y superóxido, O2-, en lugar de los productos habituales. El superóxido es un radical libre y causa daño bioquímico, pero es neutralizado por la acción de la enzima superóxido dismutasa.
Efectos del ITPP
Trispirofosfato de mioinositol (ITPP), también conocido como OXY111A, es un fosfato de inositol que provoca un desplazamiento hacia la derecha en la curva de disociación de la hemoglobina del oxígeno a través de la modulación alostérica de la hemoglobina dentro de los glóbulos rojos. Es un fármaco experimental destinado a reducir la hipoxia tisular. Los efectos parecen durar aproximadamente mientras los glóbulos rojos afectados permanezcan en circulación.
Hemoglobina fetal
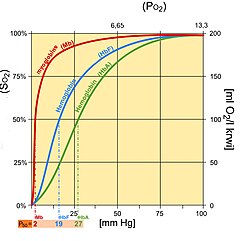
La hemoglobina fetal (HbF) es estructuralmente diferente de la hemoglobina adulta normal (HbA), lo que le da a la HbF una mayor afinidad por el oxígeno que la HbA. La HbF está compuesta por dos cadenas alfa y dos gamma, mientras que la HbA está compuesta por dos cadenas alfa y dos beta. La curva de disociación fetal está desplazada hacia la izquierda con respecto a la curva del adulto normal debido a estas diferencias estructurales:
En la hemoglobina adulta, la unión del 2,3-bisfosfoglicerato (2,3-BPG) se produce principalmente con las cadenas beta, impidiendo la unión del oxígeno con la hemoglobina. Esta unión es crucial para estabilizar el estado desoxigenado de la hemoglobina, promoviendo la liberación eficiente de oxígeno a los tejidos del cuerpo.
En la hemoglobina fetal, que posee una cadena gamma en lugar de una cadena beta, la interacción con 2,3-BPG difiere porque 2,3 - -BPG no se une a la cadena gamma ya que tiene poca o ninguna afinidad con la cadena gamma. Esta distinción contribuye a que la hemoglobina fetal tenga una mayor afinidad por el oxígeno.
Por lo general, las presiones de oxígeno arterial fetal son más bajas que las presiones de oxígeno arterial de un adulto. Por lo tanto, se requiere una mayor afinidad para unir oxígeno a niveles más bajos de presión parcial en el feto para permitir la difusión de oxígeno a través de la placenta. En la placenta, se forma una mayor concentración de 2,3-BPG, y el 2,3-BPG se une fácilmente a las cadenas beta en lugar de a las cadenas alfa. Como resultado, el 2,3-BPG se une más fuertemente a la hemoglobina adulta, lo que hace que la HbA libere más oxígeno para que lo absorba el feto, cuya HbF no se ve afectada por el 2,3-BPG. Luego, la HbF entrega el oxígeno ligado a los tejidos que tienen presiones parciales aún más bajas, donde puede liberarse.

