Curación ósea
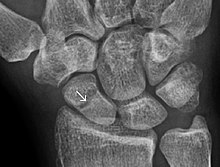
Por lo general, el tratamiento de fracturas óseas consiste en que un médico reduzca (empuje) los huesos desplazados de regreso a su lugar a través de la reubicación con o sin anestesia, estabilice su posición para ayudar a la unión y luego espere a que ocurra el proceso de curación natural del hueso..
Se ha descubierto que la ingesta adecuada de nutrientes afecta significativamente la integridad de la reparación de la fractura. La edad, el tipo de hueso, el tratamiento farmacológico y la patología ósea preexistente son factores que afectan a la cicatrización. El papel de la curación ósea es producir hueso nuevo sin cicatriz como se ve en otros tejidos, lo que sería una debilidad o deformidad estructural.
El proceso de toda la regeneración del hueso puede depender del ángulo de luxación o fractura. Si bien la formación ósea generalmente abarca toda la duración del proceso de curación, en algunos casos, la médula ósea dentro de la fractura se ha curado dos o menos semanas antes de la fase final de remodelación.
Si bien la inmovilización y la cirugía pueden facilitar la curación, una fractura finalmente se cura a través de procesos fisiológicos. El proceso de curación está determinado principalmente por el periostio (la membrana de tejido conectivo que recubre el hueso). El periostio es una fuente de células precursoras que se convierten en condroblastos y osteoblastos que son esenciales para la curación del hueso. Otras fuentes de células precursoras son la médula ósea (cuando está presente), el endostio, los vasos sanguíneos pequeños y los fibroblastos.
Curación primaria
La cicatrización primaria (también conocida como cicatrización directa) requiere una reducción anatómica correcta que sea estable, sin formación de huecos. Tal curación requiere solo la remodelación del hueso lamelar, los canales haversianos y los vasos sanguíneos sin formación de callos. Este proceso puede llevar de unos meses a unos años.
Curación por contacto
Cuando el espacio entre los extremos del hueso es inferior a 0,01 mm y la tensión interfragmentaria es inferior al 2 %, se puede producir la curación por contacto. En este caso, los conos de corte, que consisten en osteoclastos, se forman a lo largo de las líneas de fractura, generando cavidades a una velocidad de 50 a 100 μm/día. Los osteoblastos llenan las cavidades con el sistema haversiano. Esto provoca la formación de hueso lamelar que se orienta longitudinalmente a lo largo del eje longitudinal del hueso. Se forman vasos sanguíneos que penetran en el sistema haversiano. La remodelación del hueso lamelar da como resultado la curación sin formación de callos.
Curación de brechas
Si el espacio de la fractura es de 800 μm a 1 mm, la fractura se rellena con osteoblastos y luego con hueso lamelar orientado perpendicularmente al eje del hueso. Este proceso inicial toma de tres a ocho semanas. La orientación perpendicular del hueso laminar es débil, por lo que se requiere una reconstrucción osteonal secundaria para reorientar el hueso laminar longitudinalmente.
Curación secundaria
La curación secundaria (también conocida como curación indirecta de fracturas) es la forma más común de curación ósea. Por lo general, consiste solo en osificación endocondral. A veces, la osificación intramembranosa ocurre junto con la osificación endocondral. La osificación intramembranosa, mediada por la capa perióstica del hueso, ocurre con la formación de callos. Para la osificación endocondral, el depósito de hueso solo ocurre después del cartílago mineralizado. Este proceso de curación se produce cuando la fractura se trata de forma conservadora con yeso ortopédico o inmovilización, fijación externa o fijación interna.
Reacción
Después de una fractura ósea, las células sanguíneas se acumulan junto al sitio de la lesión. Poco después de la fractura, los vasos sanguíneos se contraen, lo que detiene el sangrado adicional. En unas pocas horas, las células sanguíneas extravasculares forman un coágulo llamado hematoma que actúa como plantilla para la formación de callos. Estas células, incluidos los macrófagos, liberan mediadores inflamatorios como citocinas (factor de necrosis tumoral alfa (TNFα), familia de interleucina-1 (IL-1), interleucina 6 (IL-6), 11 (IL-11) y 18 (IL-11). -18)) y aumentar la permeabilidad de los capilares sanguíneos. La inflamación alcanza su punto máximo a las 24 horas y se completa a los siete días. A través del receptor del factor de necrosis tumoral 1 (TNFR1) y el receptor del factor de necrosis tumoral 2, el TNFα media la diferenciación de las células madre mesenquimales (originadas en la médula ósea) en osteoblastos y condrocitos. El factor 1 derivado de células estromales (SDF-1) y CXCR4 median el reclutamiento de células madre mesenquimales. IL-1 e IL-6 son las citocinas más importantes para la cicatrización ósea. IL-1 promueve la formación de callos y de vasos sanguíneos. IL-6 promueve la diferenciación de osteoblastos y osteoclastos. Todas las células dentro del coágulo de sangre se degeneran y mueren. Dentro de esta área, los fibroblastos se replican. Dentro de 7 a 14 días, forman un agregado suelto de células, entremezclado con pequeños vasos sanguíneos, conocido como tejido de granulación. Los osteoclastos se mueven para reabsorber los extremos del hueso muerto y se elimina otro tejido necrótico.
Reparar
De siete a nueve días después de la fractura, las células del periostio se replican y transforman. Las células periósticas proximales (en el lado cercano) del espacio de la fractura se convierten en condroblastos, que forman cartílago hialino. Las células periósticas distales (en el otro extremo) del espacio de la fractura se convierten en osteoblastos, que forman tejido óseo a través de la reabsorción ósea del cartílago calcificado y el reclutamiento de células óseas y osteoclastos. Los fibroblastos dentro del tejido de granulación se convierten en condroblastos que también forman cartílago hialino. Estos dos nuevos tejidos crecen en tamaño hasta que se unen entre sí. Estos procesos culminan en una nueva masa de tejido heterogéneo conocida como callo de fractura. La formación de callo alcanza su punto máximo el día 14 de la fractura. Eventualmente, la brecha de la fractura se cierra
La siguiente fase es la sustitución del cartílago hialino y el hueso entretejido por hueso lamelar. El proceso de sustitución se conoce como osificación endocondral respecto al cartílago hialino y sustitución ósea respecto al hueso entretejido. La sustitución del tejido óseo ocurre antes que la sustitución del cartílago hialino. El hueso lamelar comienza a formarse poco después de que la matriz de colágeno de cualquiera de los tejidos se mineralice. En esta etapa, el proceso es inducido por IL-1 y TNFα. La matriz mineralizada es penetrada por microvasos y numerosos osteoblastos. Los osteoblastos forman hueso lamelar nuevo sobre la superficie recientemente expuesta de la matriz mineralizada. Este nuevo hueso lamelar tiene la forma de hueso trabecular. Eventualmente, todo el tejido óseo y cartílago del callo de fractura original es reemplazado por hueso trabecular, restaurando la mayor parte de la fuerza original del hueso.
Remodelación
La remodelación comienza tres o cuatro semanas después de la fractura y puede tardar entre tres y cinco años en completarse. El proceso sustituye el hueso trabecular por hueso compacto. El hueso trabecular primero es reabsorbido por los osteoclastos, creando un hoyo de reabsorción poco profundo conocido como "laguna de Howship". Luego, los osteoblastos depositan hueso compacto dentro del hoyo de reabsorción. Eventualmente, el callo de la fractura se remodela en una nueva forma que duplica fielmente la forma y la fuerza originales del hueso. Este proceso se puede lograr mediante la formación de polaridad eléctrica durante la carga parcial de un hueso largo; donde la superficie convexa electropositiva y la superficie cóncava electronegativa activan los osteoclastos y los osteoblastos respectivamente. Este proceso se puede mejorar con ciertos biomateriales sintéticos inyectables, como Cerament, que son osteoconductores y favorecen la cicatrización ósea.
Obstrucciones
- Pobre suministro de sangre que conduce a la muerte de los osteocitos. La muerte de células óseas también depende del grado de fractura e interrupción del sistema haversiano.
- Condición de los tejidos blandos. El tejido blando entre los extremos del hueso restringe la curación.
- Nutrición y terapia de drogas. La mala salud general reduce la tasa de curación. Los medicamentos que perjudican la respuesta inflamatoria impiden también la curación.
- Infección. Divierte la respuesta inflamatoria lejos de la curación para combatir la infección.
- Edad. El hueso joven se une más rápido que el hueso adulto.
- Malignidad ósea preexistente.
- Factores mecánicos como el hueso que no está alineado, y demasiado o muy poco movimiento. La movilidad excesiva puede perturbar el callo, interfiriendo con la unión; pero se ve un ligero movimiento biomecánico para mejorar la formación de callos.
Complicaciones
Las complicaciones de la curación de fracturas incluyen:
- Infección: es la complicación más común de las fracturas y ocurre predominantemente en las fracturas abiertas. La infección por la herida postraumática es la causa más común de la osteomielitis crónica en los pacientes. La osteomielitis también puede ocurrir después de la fijación quirúrgica de una fractura.
- No unión: no progresión de la curación dentro de seis meses de una fractura que ocurre. Las piezas de fractura permanecen separadas y pueden ser causadas por infección y/o falta de suministro de sangre (Ischaemia) al hueso. Hay dos tipos de no unión, atrofia e hipertrófica. La hipertrófica implica la formación de exceso de callo que conduce a extremos óseos que aparecen esclerosis causando una aparición radiológica "Elefantes Pie" debido a la excesiva fractura termina movilidad pero el suministro sanguíneo adecuado. La no unión atrófica resulta en la reabsorción y redondeo de los extremos óseos debido a la insuficiencia del suministro de sangre y la excesiva movilidad de los extremos óseos.
- Mal-unión: la curación ocurre pero el hueso curado tiene 'deformidad, traducción o alineación rotacional que requiere corrección quirúrgica'. Esto es más común en huesos largos como el fémur.
- Unión retrasada: los tiempos de curación varían dependiendo de la ubicación de una fractura y de la edad de un paciente. La unión retrasada se caracteriza por 'persistencia de la línea de fractura y una escasez o ausencia de formación de callos' en la radiografía. La curación sigue ocurriendo pero a un ritmo mucho más lento de lo normal.
Galería
Cronología radiológica en niños pequeños
En las imágenes médicas, la cicatrización ósea secundaria muestra las siguientes características a lo largo del tiempo en niños pequeños:
| Resolución de tejidos blandos | 7 a 10 días (o 2 a 21 días) |
| Gap widening | 4 a 6 semanas (56%) |
| Reacción periosteal | 7 días – 7 semanas |
| Esclerosis marginal | 4 a 6 semanas (85%) |
| Primera llamada | 4 a 7 semanas (100%) |
| Radiodensidad de callus > cortex | 13 semanas (90%) |
| Bridging callus | 2.6 – 13 semanas |
| Incorporación periosteal | 14 semanas |
| Remodelación | 9 semanas (50%) |
Contenido relacionado
PCR
Proteína G
Placebo