Cúmulo de hierro y azufre
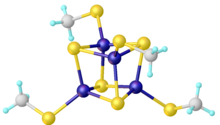
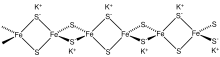
Los clústeres de hierro y azufre son conjuntos moleculares de hierro y sulfuro. Se discuten con mayor frecuencia en el contexto del papel biológico de las proteínas de hierro y azufre, que son omnipresentes. Se conocen muchos grupos de Fe-S en el área de la química organometálica y como precursores de análogos sintéticos de los grupos biológicos (ver Figura). Se cree que el último ancestro común universal tenía muchos grupos de hierro y azufre.
Conglomerados organometálicos
Los grupos organometálicos de Fe–S incluyen los sulfido carbonilos con la fórmula Fe2S2(CO)6, H2 Fe3S(CO)9, y Fe3S2(CO)9. También se conocen compuestos que incorporan ligandos de ciclopentadienilo, como (C5H5)4Fe4S4.
Materiales inorgánicos
Conglomerados biológicos de Fe–S
Los grupos de hierro y azufre se encuentran en muchos sistemas biológicos, a menudo como componentes de proteínas de transferencia de electrones. Las proteínas ferredoxina son los grupos de Fe-S más comunes en la naturaleza. Cuentan con centros 2Fe–2S o 4Fe–4S. Ocurren en todas las ramas de la vida.
Los grupos de Fe–S se pueden clasificar según su estequiometría de Fe:S [2Fe–2S], [4Fe–3S], [3Fe–4S] y [4Fe–4S]. Los grupos [4Fe-4S] se presentan en dos formas: ferredoxinas normales y proteínas de hierro de alto potencial (HiPIP). Ambos adoptan estructuras cuboidales, pero utilizan diferentes estados de oxidación. Se encuentran en todas las formas de vida.
La pareja redox relevante en todas las proteínas Fe-S es Fe(II)/Fe(III).
Muchos clústeres se han sintetizado en el laboratorio con la fórmula [Fe4S4(SR)4]2− , que son conocidos por muchos sustituyentes R y con muchos cationes. Se han preparado variaciones incluyendo los cubanos incompletos [Fe3S4(SR)3]3−.
Las proteínas de Rieske contienen grupos de Fe-S que se coordinan como una estructura 2Fe-2S y se pueden encontrar en el complejo III del citocromo bc1 unido a la membrana en las mitocondrias de eucariotas y bacterias. También forman parte de las proteínas del cloroplasto como el complejo citocromo b6f en los organismos fotosintéticos. Estos organismos fotosintéticos incluyen plantas, algas verdes y cianobacterias, el precursor bacteriano de los cloroplastos. Ambos son parte de la cadena de transporte de electrones de sus respectivos organismos, lo cual es un paso crucial en la recolección de energía para muchos organismos.
En algunos casos, los clústeres de Fe-S son redox inactivos, pero se propone que tengan funciones estructurales. Los ejemplos incluyen endonucleasa III y MutY.
Contenido relacionado
Masculino
Grafito
Canchim