Cultivo de lotes alimentados

El cultivo por lotes alimentados se define, en el sentido más amplio, como una técnica operativa en procesos biotecnológicos en la que uno o más nutrientes (sustratos) se introducen (suministran) al biorreactor durante el cultivo y en la que el producto o los productos permanecen en el biorreactor hasta el final del proceso. Una descripción alternativa del método es la de un cultivo en el que "un medio base sustenta el cultivo celular inicial y se añade un medio de alimentación para evitar el agotamiento de nutrientes". También es un tipo de cultivo por lotes alimentados. En algunos casos, todos los nutrientes se introducen en el biorreactor. La ventaja del cultivo por lotes alimentados es que se puede controlar la concentración de sustrato alimentado en el líquido de cultivo a niveles arbitrarios deseados (en muchos casos, a niveles bajos).
En términos generales, el cultivo en lotes alimentados es superior al cultivo en lotes convencional cuando el control de las concentraciones de un nutriente (o nutrientes) afecta el rendimiento o la productividad del metabolito deseado.
Tipos de bioprocesos
Los tipos de bioprocesos para los que el cultivo en lotes alimentados es eficaz se pueden resumir de la siguiente manera:
1. Inhibición del sustrato[1]
Los nutrientes como el metanol, el etanol, el ácido acético y los compuestos aromáticos inhiben el crecimiento de microorganismos incluso en concentraciones relativamente bajas. Si se añaden estos sustratos de forma adecuada, se puede acortar el tiempo de retardo y reducir considerablemente la inhibición del crecimiento celular.
2. Alta densidad celular (alta concentración celular)[1]
En un cultivo discontinuo, para alcanzar concentraciones celulares muy altas, p. ej., 50-100 g de células secas/L, se necesitan concentraciones iniciales altas de nutrientes en el medio. En concentraciones tan altas, los nutrientes se vuelven inhibidores, aunque no tienen ese efecto en las concentraciones normales utilizadas en cultivos discontinuos.
3. Efecto de la glucosa (efecto Crabtree)[1]
En la producción de levadura de panadería a partir de mosto de malta o melaza, se ha reconocido desde principios del siglo XX que el etanol se produce incluso en presencia de suficiente oxígeno disuelto (OD) si hay un exceso de azúcar presente en el líquido de cultivo. El etanol es una de las principales causas de bajo rendimiento celular. La formación aeróbica de etanol en presencia de concentración de glucosa se conoce como efecto de la glucosa o efecto Crabtree. Para reducir este efecto, generalmente se emplea un proceso de lote alimentado para la producción de levadura de panadería. En cultivos aeróbicos de Escherichia coli y Bacillus subtilis, los ácidos orgánicos como el ácido acético (y en cantidades menores, el ácido láctico y el ácido fórmico) se producen como subproductos cuando la concentración de azúcar es alta, y estos ácidos inhiben el crecimiento celular y muestran un efecto de deterioro en las actividades metabólicas. La formación de estos ácidos se denomina efecto Crabtree bacteriano.
4. Represión de catabolitos[1]
Cuando se proporciona a un microorganismo una fuente de energía de carbono rápidamente metabolizable, como la glucosa, el aumento resultante en la concentración intracelular de ATP conduce a la represión de la biosíntesis de enzimas, lo que provoca una metabolización más lenta de la fuente de energía. Este fenómeno se conoce como represión catabólica. Muchas enzimas, especialmente las que participan en las vías catabólicas, están sujetas a esta regulación represiva. Un método poderoso para superar la represión catabólica en la biosíntesis enzimática es un cultivo de lote alimentado en el que la concentración de glucosa en el líquido de cultivo se mantiene baja, donde se restringe el crecimiento y se desreprime la biosíntesis enzimática. La alimentación lenta de glucosa en la fermentación de penicilina por Penicillium chrysogenum es un ejemplo clásico en la categoría.
5. Mutantes auxótrofos[1]
En un proceso microbiano que emplea un mutante auxotrófico (mutante que requiere nutrientes), el exceso de suministro del nutriente requerido da como resultado un crecimiento celular abundante con poca acumulación del metabolito deseado debido a la inhibición por retroalimentación y/o la represión del producto final. Sin embargo, la falta del nutriente requerido reduce el crecimiento celular, así como la producción general del metabolito deseado, ya que la tasa de producción suele ser proporcional a la concentración celular. En un bioproceso de este tipo, la acumulación del metabolito deseado se puede maximizar cultivando el mutante con una cantidad limitada del nutriente requerido. Para cultivar el mutante con una concentración baja del nutriente requerido, se lo introduce en el cultivo por lotes a una tasa controlada. Esta técnica se utiliza a menudo en producciones industriales de aminoácidos con mutantes auxotróficos. Un ejemplo es la producción de lisina con un mutante que requiere homoserina o treonina/metionina de Corynebacterium glutamicum que carece del gen de la homoserina deshidrogenasa.
6. Control de la expresión de un gen con un promotor reprimible
La transcripción de un gen que tiene un promotor reprimible aguas arriba del marco de lectura abierto se reprime mediante la combinación del llamado holo-represor con la región operadora del ADN. Cuando existe un compuesto químico específico en el líquido de cultivo, el compuesto (o su metabolito) en las células se combina como correpresor con un apo-represor (un tipo de factor de transcripción) para formar el holo-represor. Mantener la concentración de este compuesto lo más baja posible (mientras se permite un crecimiento celular suficiente) permite la expresión continua del gen regulado. El cultivo en lotes alimentados es una técnica poderosa para lograrlo. Ejemplos de promotores reprimibles son el promotor trp y el promotor phoA.
7. Prolongación del tiempo de operación, complementación del agua perdida por evaporación y disminución de la viscosidad del caldo de cultivo[1]
Tipos de estrategias de culto
Cultura de alta densidad celular
La estrategia de lotes alimentados se utiliza normalmente en procesos bioindustriales para alcanzar una alta densidad celular en el biorreactor. Generalmente, la solución de alimentación está muy concentrada para evitar la dilución del biorreactor. La producción de proteínas heterólogas mediante cultivos de lotes alimentados de microorganismos recombinantes ha sido ampliamente estudiada.
La adición controlada del nutriente afecta directamente la tasa de crecimiento del cultivo y ayuda a evitar el metabolismo excesivo (formación de metabolitos secundarios, como el acetato en Escherichia coli, ácido láctico en cultivos de células de mamíferos, etanol en Saccharomyces cerevisiae), la limitación de oxígeno (anaerobiosis).
Cultura de bache constante
El cultivo por lotes alimentados más simple es aquel en el que la tasa de alimentación de un sustrato limitante del crecimiento es constante, es decir, la tasa de alimentación es invariable durante el cultivo. Este caso se muestra en el gráfico (aquí el volumen de cultivo es variable). Este tipo de cultivo por lotes alimentados se denomina cultivo por lotes alimentados constantemente (CFBC, por sus siglas en inglés) y está bien establecido matemática y experimentalmente. En el CFBC, se estudiaron ambos casos de CFBC de volumen fijo y CFBC de volumen variable.
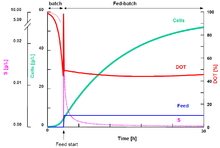
La cultura de los cultivos alimentarios
En condiciones ideales, las células crecen exponencialmente. Si la tasa de alimentación del sustrato limitante del crecimiento se incrementa en proporción a la tasa de crecimiento exponencial de las células, es posible mantener la tasa de crecimiento específica de las células durante un largo tiempo mientras se mantiene la concentración de sustrato en el líquido de cultivo a un nivel constante. La tasa de alimentación requerida (volumétrica o másica) debe aumentarse exponencialmente con el tiempo, de modo que este modo de cultivo por lotes alimentados se denomina cultivo por lotes alimentados exponencialmente (EFBC).
La limitación del sustrato ofrece la posibilidad de controlar las velocidades de reacción para evitar limitaciones tecnológicas relacionadas con el enfriamiento del reactor y la transferencia de oxígeno. La limitación del sustrato también permite el control metabólico, para evitar efectos osmóticos, la represión de catabolitos y el metabolismo excesivo de productos secundarios.
Estrategia de control
Se pueden utilizar diferentes estrategias para controlar el crecimiento en un proceso de lotes alimentados:
| Parámetro de control | Principio de control |
|---|---|
| DOT (pO2) | DOstat (DOT= constant), F~DOT |
| Tasa de absorción de oxígeno (NUESTRO) | OUR=constant, F~OUR |
| Glucose | medición on-line de glucosa (FIA), glucosa=constant |
| Acetato | medición on-line de acetato (FIA), acetato=constant |
| pH (pHstat) | F~pH (la acidificación está conectada a alta glucosa) |
| Amoníaco | medición on-line de amoníaco (FIA), amoníaco=constant |
| Temperatura | T adaptado según NUESTRO pO2 |
Referencias
- ^ Tsuneo Yamanè, Shoichi Shimizu: Fed-batch Techniques in Microbial Processes. Avances en Biochem Eng./Biotechnol 1984, 30:147-194.
- ^ Ngibuini, Mwai (25 de noviembre de 2014). "Cómo un solo uso, los mini bioreactores podrían revolucionar la escala de bioproceso". Tratamiento farmaceutico. Estados Unidos: Advantage Business Media. Archivado desde el original el 20 de octubre de 2015. Retrieved 28 de noviembre 2014.
- ^ Dieter Riesenberg: Cultivo de alta densidad celular Escherichia coli. Curr Opin Biotechnol 1991, 2:380-384.
- ^ L. Yee, Harvey W. Blanch: Recombinant protein expression in high cell densidad fed-batch cultures of Escherichia coli. Bio/Technology (N Y) 1992, 10:1550-1556.
- ^ Sang Yup Lee: Cultura de alta densidad celular Escherichia coli. Tendencias Biotechnol 1996, 14:98-105.
- ^ JosephShiloach, Rephael Fass: Creciendo E. coli a alta densidad celular--una perspectiva histórica sobre el desarrollo de métodos. Biotechnol Adv 2005, 23:345-357.
- ^ O Mendoza-Vega, J. Sabatie, S. W. Brown: Industrial-Production of Heterologous Proteins by Fed-Batch Cultures of the Yeast Saccharomyces-cerevisiae. FEMS Microbiology Reviews 1994, 15:369-410.
- ^ Paulina Balbás: Comprender el arte de producir proteínas y moléculas no proteínas en Escherichia coli. Biotecnología molecular 2001, 19:251-267.
- ^ Neubauer P, Winter J: Estrategias de expresión y fermentación para la producción de proteínas recombinantes en Escherichia coli. In: Merten OW et al. (Eds). Proteína recombinante Producción con células procariotas y eucariotas. A comparative view on host fisilogy. 2001, Kluwer Academic Publisher, Dordrecht, The Netherlands. pp. 195-258.
- ^ Amulya K. Panda: Bioprocesamiento de proteínas terapéuticas de los cuerpos de inclusión de Escherichia coli. Adv Biochem Eng Biotechnol 2003, 85:43-93.
- ^ Jeongseok Lee, Sang Yup Lee, Suwon Park, Anton P. J. Middelberg: Control de fermentaciones alimentadas. Biotechnol Adv 1999, 17:29-48.
- ^ Katie F. Wlaschin, Wei-Shou Hu: Cultura de frito y alimentación dinámica de nutrientes. Adv Biochem Engin/Biotechnol 2006, 101:43-74.
- ^ Tsuneo Yamané, Shigeki Hirano: Semi-batch Cultura de Microorganismos con Constant Feed of Substrate - A Mathematical Simulation -. J Ferment Technol 1977, 55:156-165.
- ^ Tsuneo Yamané, Shigeki Hirano: Semi-batch Cultura de Microorganismos con Constant Feed of Substrate - Un Estudio Experimental -. J Ferment Technol 1977, 55:380-387.
- ^ Tsuneo Yamane, Michimasa Kishimoto, Fumitake Yoshida: Semi-batch Cultura de Bacterias Asistidas al Metanol con Feed de Metanol Aumentada Exponencialmente. J Ferment Technol 1974, 54:229-240.
- ^ J. Zhang, Randolph Greasham: Medios definidos químicamente para fermentaciones comerciales. Microbiología aplicada y biotecnología 1999, 51:407-421.
- ^ Gunnar Liden: Comprender el bioreactor. Bioprocess and Biosystems Engineering 2002, 24:273-279.
- ^ Christopher J. Hewitt, Alvin W. Nienow: La ampliación de los procesos de fermentación de lote microbiano y de lote alimentado. Adv Appl Microbiol 2007, 62:105-135.