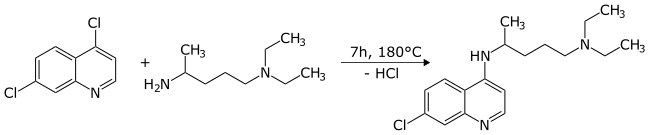
Cloroquina
cloroquina es un medicamento que se utiliza principalmente para prevenir y tratar la malaria en zonas donde la malaria sigue siendo sensible a sus efectos. Ciertos tipos de malaria, cepas resistentes y casos complicados suelen requerir medicación diferente o adicional. La cloroquina también se usa ocasionalmente para la amebiasis que ocurre fuera de los intestinos, la artritis reumatoide y el lupus eritematoso. Si bien no se ha estudiado formalmente durante el embarazo, parece seguro. Se estudió para tratar la COVID-19 al principio de la pandemia, pero estos estudios se detuvieron en gran medida en el verano de 2020 y los NIH no recomiendan su uso para este propósito. Se toma por vía oral.
Los efectos secundarios comunes incluyen problemas musculares, pérdida de apetito, diarrea y erupción cutánea. Los efectos secundarios graves incluyen problemas de visión, daño muscular, convulsiones y niveles bajos de células sanguíneas. La cloroquina es un miembro de la clase de fármacos 4-aminoquinolina. Como antipalúdico, actúa contra la forma asexual del parásito de la malaria en la etapa de su ciclo de vida dentro de los glóbulos rojos. No está claro cómo funciona en la artritis reumatoide y el lupus eritematoso.
La cloroquina fue descubierta en 1934 por Hans Andersag. Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud. Está disponible como medicamento genérico.
Usos médicos
Malaria

♦ Elevated occurrence of chloroquine- or multi-resistant malaria
♦ Occurrence of chloroquine-resistant malaria
♦ No Plasmodium falciparum o resistencia a la cloroquina
♦ No malaria
La cloroquina se ha utilizado en el tratamiento y prevención de la malaria por Plasmodium vivax, P. ovale y P. malariae. Generalmente no se utiliza para Plasmodium falciparum ya que existe una resistencia generalizada al mismo.
La cloroquina se ha utilizado ampliamente en administraciones masivas de medicamentos, lo que puede haber contribuido a la aparición y propagación de resistencia. Se recomienda comprobar si la cloroquina sigue siendo eficaz en la región antes de usarla. En áreas donde hay resistencia, se pueden usar en su lugar otros antipalúdicos, como mefloquina o atovacuona. Los Centros para el Control y la Prevención de Enfermedades recomiendan no tratar la malaria con cloroquina sola debido a que las combinaciones son más efectivas.
Amebiasis
En el tratamiento del absceso hepático amebiano, se puede usar cloroquina en lugar de o además de otros medicamentos en caso de que no mejore con metronidazol u otro nitroimidazol dentro de cinco días o intolerancia al metronidazol o un nitroimidazol.
Enfermedad reumática
Como suprime levemente el sistema inmunológico, la cloroquina se usa en algunos trastornos autoinmunes, como la artritis reumatoide, y tiene una indicación no autorizada para el lupus eritematoso.
Efectos secundarios
Los efectos secundarios incluyen visión borrosa, náuseas, vómitos, calambres abdominales, dolor de cabeza, diarrea, hinchazón de piernas/tobillos, dificultad para respirar, labios/uñas/piel pálida, debilidad muscular, fácil aparición de moretones/sangrado, problemas auditivos y mentales.
- Movimientos no deseados o no controlados (incluyendo la lengua y el toque facial)
- Sordera o tinnitus.
- Nausea, vómitos, diarrea, calambres abdominales.
- Dolor de cabeza.
- Cambios mentales/mood (como confusión, cambios de personalidad, pensamientos inusuales / comportamiento, depresión, sensación de ser observada, alucinante)
- Señales de infección grave (como fiebre alta, escalofríos graves, dolor de garganta persistente)
- Vacuidad de la piel, cambios en el color de la piel, pérdida del cabello y erupciones cutáneas.
- El picor inducido por la cloroquina es muy común entre los africanos negros (70%), pero mucho menos común en otras razas. Aumenta con la edad, y es tan severo como para detener el cumplimiento de la terapia con drogas. Se incrementa durante la fiebre al paludismo; su gravedad se correlaciona con la carga del parásito de malaria en sangre. Algunas evidencias indican que tiene una base genética y está relacionada con la acción de cloroquina con los receptores de opiáceos central o periféricamente.
- Sabor metálico desagradable
- Esto podría evitarse por formulaciones de liberación "mascada y controlada" como múltiples emulsiones.
- Cloroquina retinopatía
- Cambios electrocardiográficos
- Esto se manifiesta como alteraciones de conducción (bloque de granel-branch, bloqueo auriculoventricular) o Cardiomiopatía – a menudo con hipertrofia, fisiología restrictiva y insuficiencia cardíaca congestiva. Los cambios pueden ser irreversibles. Sólo se han reportado dos casos que requieren trasplante cardíaco, lo que sugiere que este riesgo particular es muy bajo. Microscopía electrónica de biopsias cardíacas muestran cuerpos de inclusión citoplasmática patognomónica.
- Pancytopenia, anemia aplásica, agranulocitosis reversible, plaquetas de sangre bajas, neutropenia.
Embarazo
No se ha demostrado que la cloroquina tenga efectos dañinos en el feto cuando se usa en las dosis recomendadas para la profilaxis de la malaria. Pequeñas cantidades de cloroquina se excretan en la leche materna de las mujeres lactantes. Sin embargo, este medicamento se puede recetar de forma segura a bebés y sus efectos no son perjudiciales. Los estudios con ratones muestran que la cloroquina marcada radiactivamente pasó a través de la placenta rápidamente y se acumuló en los ojos del feto, que permaneció presente cinco meses después de que la droga fue eliminada del resto del cuerpo. Se sigue aconsejando a las mujeres que están embarazadas o que planean quedar embarazadas que no viajen a regiones con riesgo de malaria.
Anciano
No hay evidencia suficiente para determinar si es seguro administrar cloroquina a personas de 65 años o más. Dado que se elimina por los riñones, la toxicidad debe controlarse cuidadosamente en personas con función renal deficiente.
Interacciones medicamentosas
La cloroquina tiene una serie de interacciones entre medicamentos que podrían ser motivo de preocupación clínica:
- Los niveles de ampicillina pueden reducirse mediante cloroquina;
- Los antiácidos pueden reducir la absorción de cloroquina;
- La cimetidina puede inhibir el metabolismo de la cloroquina; aumentar los niveles de cloroquina en el cuerpo;
- Los niveles de ciclosporina pueden aumentarse por cloroquina; y
- La mefloquina puede aumentar el riesgo de convulsiones.
Sobredosis
La cloroquina, en sobredosis, tiene un riesgo de muerte de alrededor del 20%. Se absorbe rápidamente en el intestino y los síntomas aparecen generalmente en una hora. Los síntomas de una sobredosis pueden incluir somnolencia, cambios en la visión, convulsiones, interrupción de la respiración y problemas cardíacos como fibrilación ventricular y presión arterial baja. También puede producirse un nivel bajo de potasio en sangre.
Si bien la dosis habitual de cloroquina utilizada en el tratamiento es de 10 mg/kg, la toxicidad comienza a ocurrir con 20 mg/kg y la muerte puede ocurrir con 30 mg/kg. En los niños, tan solo un comprimido puede causar problemas.
Las recomendaciones de tratamiento incluyen ventilación mecánica temprana, monitorización cardíaca y carbón activado. Es posible que se requieran líquidos intravenosos y vasopresores, siendo la epinefrina el vasopresor de elección. Las convulsiones pueden tratarse con benzodiazepinas. Es posible que se requiera cloruro de potasio intravenoso; sin embargo, esto puede provocar niveles altos de potasio en sangre más adelante en el curso de la enfermedad. No se ha encontrado que la diálisis sea útil.
Farmacología
La absorción de cloroquina es rápida y ocurre principalmente en el tracto gastrointestinal. Está ampliamente distribuido en los tejidos corporales. La unión a proteínas en plasma oscila entre el 46% y el 79%. Su metabolismo es parcialmente hepático, dando lugar a su principal metabolito, la desetilcloroquina. Su excreción es ≥50% como fármaco inalterado en la orina, donde la acidificación de la orina aumenta su eliminación. Tiene un volumen de distribución muy alto, ya que se difunde en el tejido adiposo del cuerpo.
La acumulación del fármaco puede provocar depósitos que pueden provocar visión borrosa y ceguera. Este y las quininas relacionadas se han asociado con casos de toxicidad retiniana, particularmente cuando se administran en dosis más altas durante períodos más prolongados. Con dosis prolongadas, se recomiendan visitas rutinarias a un oftalmólogo.
La cloroquina también es un agente lisosomotrópico, lo que significa que se acumula preferentemente en los lisosomas de las células del cuerpo. El pKa del nitrógeno quinoleínico de la cloroquina es 8,5, lo que significa que está desprotonado aproximadamente en un 10 % a pH fisiológico (según la ecuación de Henderson-Hasselbalch). Esto disminuye a aproximadamente 0,2% a un pH lisosomal de 4,6. Debido a que la forma desprotonada es más permeable a la membrana que la forma protonada, se puede realizar una "atrapamiento" del compuesto en los lisosomas.
Mecanismo de acción

Malaria
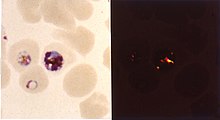
Se cree que el carácter lisosomotrópico de la cloroquina explica gran parte de su actividad antipalúdica; el fármaco se concentra en la vacuola alimentaria ácida del parásito e interfiere con los procesos esenciales. Sus propiedades lisosomotrópicas permiten además su uso en experimentos in vitro relacionados con enfermedades relacionadas con lípidos intracelulares, autofagia y apoptosis.
Dentro de los glóbulos rojos, el parásito de la malaria, que entonces se encuentra en su etapa de ciclo de vida asexual, debe degradar la hemoglobina para adquirir aminoácidos esenciales, que el parásito necesita para construir su propia proteína y para el metabolismo energético. La digestión se lleva a cabo en una vacuola de la célula parásita.
La hemoglobina se compone de una unidad proteica (digerida por el parásito) y una unidad hemo (no utilizada por el parásito). Durante este proceso, el parásito libera la molécula tóxica y soluble hemo. La fracción hemo consta de un anillo de porfirina llamado Fe (II) -protoporfirina IX (FP). Para evitar la destrucción por esta molécula, el parásito biocristaliza el hemo para formar hemozoína, una molécula no tóxica. La hemozoína se acumula en la vacuola digestiva en forma de cristales insolubles.
La cloroquina ingresa a los glóbulos rojos por difusión simple, inhibiendo la célula del parásito y la vacuola digestiva. La cloroquina (CQ) luego se protona (a CQ2+), ya que se sabe que la vacuola digestiva es ácida (pH 4,7); la cloroquina entonces no puede salir por difusión. La cloroquina recubre las moléculas de hemozoína para evitar una mayor biocristalización del hemo, lo que conduce a su acumulación. La cloroquina se une al hemo (o FP) para formar el complejo FP-cloroquina; este complejo es muy tóxico para la célula y altera la función de la membrana. La acción de los tóxicos FP-cloroquina y FP produce la lisis celular y, en última instancia, la autodigestión de las células del parásito. Por tanto, los parásitos que no forman hemozoína son resistentes a la cloroquina.
Resistencia en la malaria
Desde la primera documentación de P. falciparum a la cloroquina en la década de 1950, han aparecido cepas resistentes en África oriental y occidental, el sudeste asiático y América del Sur. La eficacia de la cloroquina contra P. falciparum ha disminuido a medida que evolucionaron cepas resistentes del parásito.
Los parásitos resistentes pueden eliminar rápidamente la cloroquina de la vacuola digestiva mediante una bomba transmembrana. Los parásitos resistentes a la cloroquina bombean cloroquina a una velocidad 40 veces mayor que los parásitos sensibles a la cloroquina; la bomba está codificada por el P. falciparum gen transportador de resistencia a la cloroquina (PfCRT). La función natural de la bomba de cloroquina es transportar péptidos: las mutaciones en la bomba que le permiten bombear cloroquina perjudican su función como bomba de péptidos y tienen un costo para el parásito, haciéndolo menos apto.
Los parásitos resistentes también suelen tener mutaciones en el transportador ABC P. falciparum gen de resistencia a múltiples fármacos (PfMDR1), aunque se cree que estas mutaciones son de importancia secundaria en comparación con PfCRT. Una proteína transportadora de cloroquina alterada, CG2, se ha asociado con la resistencia a la cloroquina, pero también parecen estar implicados otros mecanismos de resistencia.
Se ha descubierto que el verapamilo, un bloqueador de los canales de Ca2+, restaura tanto la capacidad de concentración de cloroquina como la sensibilidad a este fármaco. Otros agentes que han demostrado revertir la resistencia a la cloroquina en la malaria son la clorfeniramina, gefitinib, imatinib, tariquidar y zosuquidar.
A partir de 2014, la cloroquina sigue siendo eficaz contra la malaria avícola en Tailandia. Sohsuebngarm et al. Prueba 2014 P. gallinaceum en la Universidad de Chulalongkorn y descubrieron que el parásito no es resistente. La sertralina, la fluoxetina y la paroxetina revierten la resistencia a la cloroquina, haciendo que los biotipos resistentes sean susceptibles si se usan en un tratamiento conjunto.
Antivirales
La cloroquina tiene efectos antivirales contra algunos virus. Aumenta el pH endosómico tardío y lisosomal, lo que resulta en una liberación deficiente del virus desde el endosoma o lisosoma; la liberación del virus requiere un pH bajo. Por tanto, el virus no puede liberar su material genético en la célula y replicarse.
La cloroquina también parece actuar como un ionóforo de zinc que permite que el zinc extracelular ingrese a la célula e inhiba la ARN polimerasa viral dependiente de ARN.
Otro
La cloroquina inhibe la absorción de tiamina. Actúa específicamente sobre el transportador SLC19A3.
Contra la artritis reumatoide, actúa inhibiendo la proliferación de linfocitos, la fosfolipasa A2, la presentación de antígenos en las células dendríticas, la liberación de enzimas de los lisosomas, la liberación de especies reactivas de oxígeno de los macrófagos y la producción de IL-1.
Historia
En Perú, los indígenas extraían la corteza del árbol Cinchona (Cinchona officinalis) y utilizaban el extracto para combatir los escalofríos y la fiebre en el siglo XVII. En 1633, esta medicina herbaria se introdujo en Europa, donde se le dio el mismo uso y también se empezó a utilizar contra la malaria. La quinolina, un fármaco antipalúdico, se aisló del extracto en 1820.
Después de la Primera Guerra Mundial, el gobierno alemán buscó alternativas a la quinina. La cloroquina, un análogo sintético con el mismo mecanismo de acción, fue descubierta en 1934 por Hans Andersag y sus compañeros de trabajo de los laboratorios Bayer, quienes la llamaron Resochin. Fue ignorado durante una década porque se consideraba demasiado tóxico para el uso humano. En cambio, en la Segunda Guerra Mundial, el Cuerpo Africano Alemán utilizó el análogo de la cloroquina 3-metil-cloroquina, conocido como Sontochin. Después de que las fuerzas aliadas llegaron a Túnez, Sontochin cayó en manos de los estadounidenses, quienes enviaron el material a Estados Unidos para su análisis, lo que generó un renovado interés en la cloroquina. Los ensayos clínicos patrocinados por el gobierno de los Estados Unidos para el desarrollo de fármacos antipalúdicos demostraron inequívocamente que la cloroquina tiene un valor terapéutico significativo como fármaco antipalúdico. Se introdujo en la práctica clínica en 1947 para el tratamiento profiláctico de la malaria.
Síntesis química
La primera síntesis de cloroquina se reveló en una patente presentada por IG Farben en 1937. En el paso final, se hizo reaccionar 4,7-dicloroquinolina con 1-dietilamino-4-aminopentano.
En 1949, se habían establecido procesos de fabricación de cloroquina para permitir su uso generalizado.
Sociedad y cultura

Formulaciones
La cloroquina viene en forma de tabletas como sales de fosfato, sulfato y clorhidrato. La cloroquina generalmente se dispensa como fosfato.
Nombres
Las marcas incluyen Cloroquina FNA, Resochin, Dawaquin y Lariago.
Otros animales
La cloroquina, en diversas formas químicas, se utiliza para tratar y controlar el crecimiento superficial de anémonas y algas, y muchas infecciones por protozoos en acuarios, p. el parásito de los peces Amyloodinium ocellatum. También se utiliza en la malaria de las aves de corral.
Investigación
La cloroquina se propuso como tratamiento para el SARS, con pruebas in vitro que inhibían el coronavirus del síndrome respiratorio agudo grave (SARS-CoV). En octubre de 2004, un informe publicado afirmó que la cloroquina actúa como un inhibidor eficaz de la replicación del SARS-CoV in vitro. En agosto de 2005, un estudio revisado por pares confirmó y amplió los resultados.
La cloroquina se estaba considerando en 2003, en modelos preclínicos, como un agente potencial contra la fiebre chikungunya.
COVID-19

La cloroquina e hidroxicloroquina son medicamentos antimaláricos también utilizados contra algunas enfermedades autoinmunitarias. La cloroquina, junto con la hidroxicloroquina, fue un tratamiento experimental temprano para el COVID-19. Ninguno de los medicamentos evita la infección por SARS-CoV-2.
La proteína de espiga SARS-CoV-2 S2 requerida para la entrada viral en las células puede ser realizada por proteasasas TMPRSS2 ubicadas en la membrana celular, o por catepsinas (principalmente cathepsin L) en en endolysosomes. Hydroxychloroquine inhibe la acción de la cathepsin L en endolysosomes, but because cathepsin L cleavage is minor compared to TMPRSS2 cleavage, hydroxychloroquine does little tohibi SARS-CoV-2 infection.
Varios países utilizaron inicialmente cloroquina o hidroxicloroquina para el tratamiento de las personas hospitalizadas con COVID-19 (en marzo de 2020), aunque el medicamento no fue aprobado formalmente a través de ensayos clínicos. De abril a junio de 2020, hubo una autorización de uso de emergencia para su uso en los Estados Unidos, y fue utilizado fuera de la etiqueta para el posible tratamiento de la enfermedad. On 24 April 2020, citing the risk of "serious heart ritmo problems", the FDA posted a warning against using the drug for COVID-19 "outside of the hospital setting or a clinic trial".
Su uso fue retirado como un posible tratamiento para la infección COVID-19 cuando demostró no tener ningún beneficio para pacientes hospitalizados con enfermedad grave COVID-19 en el ensayo internacional de solidaridad y el ensayo de RECOVERY del Reino Unido. El 15 de junio de 2020, la FDA revocó su autorización de uso de emergencia, afirmando que "ya no era razonable creer" que la droga era efectiva contra COVID-19 o que sus beneficios superaron "riesgos conocidos y potenciales". En el otoño de 2020, los Institutos Nacionales de Salud emitieron directrices de tratamiento que recomendaban contra el uso de hidroxicloroquina para COVID-19 excepto como parte de un ensayo clínico.
En 2021, la hidroxicloroquina formaba parte del tratamiento recomendado para casos leves en la India.
En 2020, el uso especulativo de hidroxicloroquina para COVID-19 amenazó su disponibilidad para personas con indicaciones establecidas (malaria y enfermedades autoinmunes).
Los investigadores estiman que el uso de hidroxicloroquina en hospitales durante la primera fase de la pandemia causó 17.000 muertes en todo el mundo.Otro
Las propiedades radiosensibilizantes y quimiosensibilizantes de la cloroquina se están evaluando como estrategias anticancerígenas en humanos. En la ciencia biomedicinal, la cloroquina se utiliza en experimentos in vitro para inhibir la degradación lisosomal de productos proteicos. La cloroquina y sus formas modificadas también se han evaluado como opciones de tratamiento para afecciones inflamatorias como la artritis reumatoide y la enfermedad inflamatoria intestinal.