Clorocromato de piridinio

Clorocromato de piridinio (PCC) es una sal de color amarillo anaranjado con la fórmula [C5H5 NH]+[CrO3Cl]-. Es un reactivo en síntesis orgánica utilizado principalmente para la oxidación de alcoholes para formar carbonilos. Se conocen una variedad de compuestos relacionados con reactividad similar. El PCC ofrece la ventaja de la oxidación selectiva de alcoholes a aldehídos o cetonas, mientras que muchos otros reactivos son menos selectivos.
Estructura y preparación
PCC consiste en una cación de piridinio, [C5H5NH]+, y un anión tetraedral de clorocromato, [CrO3Cl]−. También se conocen sales relacionadas, como clorocromato de 1-butilpiridinio, [C5H5N(C)4H9[CrO]3Cl] y clorocromato de potasio.
PCC está disponible comercialmente. Descubrido por accidente, el reactivo se preparó originalmente mediante la adición de piridina en una solución fría de trióxido de cromo en ácido clorhídrico concentrado:
- C5H5N + HCl + CrO3 [C]5H5NH][CrO]3Cl]
En un método alternativo, la formación de vapores de cloruro de cromilo (CrO2Cl2) durante la preparación de la solución antes mencionada se minimizó simplemente cambiando el orden de adición: Se añadió una solución fría de piridina en ácido clorhídrico concentrado a trióxido de cromo sólido con agitación.
Usos
Oxidación de alcoholes
PCC se utiliza como oxidante. En particular, ha demostrado ser altamente eficaz en la oxidación de alcoholes primarios y secundarios a aldehídos y cetonas, respectivamente. El reactivo es más selectivo que el reactivo de Jones relacionado, por lo que hay pocas posibilidades de sobre-oxidación para formar ácidos carboxílicos si el permanganato de potasio acidificado se utiliza mientras el agua no está presente en la mezcla de reacción. Una oxidación típica de PCC implica la adición de un alcohol a una suspensión de PCC en el diclorometano. La reacción general es:
- 2 [C5H5NH][CrO]3Cl] + 3 R2CHOH → 2 [C5H5NH]Cl + Cr2O3 + 3 R2C=O + 3 H2O
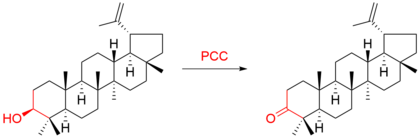
Por ejemplo, el triterpeno lupeol se oxidó a lupenona:
Oxidación de Babler
Con los alcoholes terciarios, el éster de cromato formado a partir de PCC puede isomerizarse vía una reacción [3,3]-sigmatrópica y, tras la oxidación, producir una enona, en una reacción conocida como oxidación de Babler:

Este tipo de reacción de transposición oxidativa se ha utilizado sintéticamente, por ejemplo para la síntesis de morfina.
El uso de otros oxidantes comunes en lugar del PCC generalmente provoca deshidratación, porque dichos alcoholes no se pueden oxidar directamente.
Otras reacciones
El PCC también convierte alcoholes y aldehídos insaturados adecuados en ciclohexenonas. Esta vía, una ciclación catiónica oxidativa, se ilustra mediante la conversión de (-)-citronelol en (-)-pulegona.
El PCC también produce oxidaciones alílicas, por ejemplo, en la conversión de dihidrofuranos en furanonas.
Reactivos relacionados
Otros reactivos más convenientes o menos tóxicos para oxidar alcoholes incluyen el dimetilsulfóxido, que se utiliza en las oxidaciones de Swern y Pfitzner-Moffatt, y compuestos de yodo hipervalentes, como el periodinano de Dess-Martin.
Seguridad
Una desventaja del uso de PCC es su toxicidad, que comparte con otros compuestos de cromo hexavalente.