Claudina

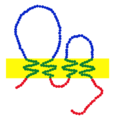
Las claudinas son una familia de proteínas que, junto con la ocludina, son los componentes más importantes de las uniones estrechas (zonulae occludentes). Las uniones estrechas establecen la barrera paracelular que controla el flujo de moléculas en el espacio intercelular entre las células de un epitelio. Tienen cuatro dominios transmembrana, con el extremo N-terminal y el extremo C-terminal en el citoplasma.
Estructura
Las claudinas son proteínas transmembrana pequeñas (20–24/27 kilodalton (kDa)) que se encuentran en muchos organismos, desde los nematodos hasta los seres humanos. Todas tienen una estructura muy similar. Las claudinas atraviesan la membrana celular cuatro veces, con el extremo N-terminal y el extremo C-terminal ubicados ambos en el citoplasma, y dos bucles extracelulares que muestran el mayor grado de conservación.
Las claudinas tienen interacciones cis y trans entre las membranas celulares. Las interacciones cis se dan cuando las claudinas de la misma membrana interactúan, una de las formas en que lo hacen es mediante interacciones moleculares en el dominio transmembrana. La interacción trans se da cuando las claudinas de células vecinas interactúan a través de sus bucles extracelulares. Las interacciones cis también se conocen como interacciones lado a lado y las interacciones trans también se conocen como interacciones cabeza a cabeza.
En general, la unión estrecha se caracteriza por su impermeabilidad. Sin embargo, dependiendo del tipo de claudina y sus interacciones, existe una permeabilidad selectiva. Esto incluye la selectividad de carga y la selectividad de tamaño.
N-terminal
El extremo N-terminal suele ser muy corto (1-10 aminoácidos). Se encuentra en el citoplasma, donde se cree que contribuye a la señalización celular, la organización del citoesqueleto y otras posibles funciones.
C-terminal
El extremo C-terminal tiene una cadena más larga y se encuentra en el citoplasma. Su longitud varía de 21 a 63 y es necesario para la localización de estas proteínas en las uniones estrechas. Se cree que puede desempeñar un papel en la señalización celular. Todas las claudinas humanas (con excepción de la claudina 12) tienen dominios que les permiten unirse a los dominios PDZ de las proteínas de andamiaje.
Dominio Transmembrane
El dominio transmembrana son los aminoácidos que atraviesan la membrana celular. El dominio transmembrana es importante para la interacción cis de las claudinas.
Primer bucle extracelular
El primer bucle extracelular tiene un rango de 42 a 56 aminoácidos y es más largo que el segundo bucle extracelular. Se sospecha que las cisteínas que se encuentran en el primer bucle extracelular forman enlaces disulfuro. Este bucle tiene aminoácidos cargados que pueden ser el predictor de la selectividad de carga de las uniones estrechas. El primer bucle extracelular desempeña un papel en la transinteracción de las claudinas de las células adyacentes.
Segundo bucle extracelular
El segundo bucle extracelular es más corto que el primero. En esta corta cadena de aminoácidos hay tres residuos hidrófobos. Se sospecha que estos tres residuos contribuyen a la transinteracción de proteínas entre células adyacentes.
Historia
Las claudinas fueron nombradas por primera vez en 1998 por los investigadores japoneses Mikio Furuse y Shoichiro Tsukita de la Universidad de Kioto. El nombre claudin proviene de la palabra latina claudere ("cerrar"), lo que sugiere el papel de barrera de estas proteínas.
Estudios
Una revisión reciente analiza la evidencia sobre la estructura y función de las proteínas de la familia de las claudinas utilizando un enfoque de sistemas para comprender la evidencia generada por técnicas de proteómica.
Se sintetizó una claudina quimérica para ayudar a mejorar la comprensión tanto de la estructura como de la función de la unión estrecha.
El modelado computacional es otra técnica que se utiliza para ayudar a mejorar la investigación sobre la estructura y las funciones de las claudinas.
Genes
En el genoma humano se encuentran 23 genes que codifican para las proteínas claudinas y hay 27 dominios transmembrana en los mamíferos. La conservación no se observa a nivel genético. A pesar de que el nivel genético no se conserva en las claudinas, su conservación estructural es muy similar.
- CLDN1, CLDN2, CLDN3, CLDN4, CLDN5, CLDN6, CLDN7, CLDN8, CLDN9, CLDN10, CLDN11, CLDN12, CLDN13, CLDN14, CLDN15, CLDN16, CLDN17, CLDN18, CLDN19, CLDN20, CLDN21, CLDN22, CLDN23
Véase también
- Occludin
Imágenes adicionales
Referencias
- ^ a b Hou J, Konrad M (2010-01-01). "Capítulo 7 - Claudins and Renal Magnesium Handling". En Yu AS (ed.). Temas actuales en Membranes. Vol. 65. Academic Press. pp. 151–176. doi:10.1016/s1063-5823(10)65007-7. ISBN 9780123810397.
- ^ Furuse M (2010-01-01). "Capítulo 1 - Introducción: Claudins, Tight Junctions, and the Paracellular Barrier". En Yu AS (ed.). Temas actuales en Membranes. Vol. 65. Academic Press. pp. 1–19. doi:10.1016/s1063-5823(10)65001-6. ISBN 9780123810397.
- ^ Szaszi K, Amoozadeh Y (2014-01-01-01). "Capítulo Seis - Nuevas visiones en funciones, regulaciones y roles patológicos de las interacciones de la lucha en el epitelio tubular del riñón". En Jeon KW (ed.). International Review of Cell and Molecular BiologyVol. 308. Academic Press. pp. 205–271. doi:10.1016/b978-0-12-800097-7.00006-3. ISBN 9780128000977. PMID 24411173.
- ^ Otani T, Nguyen TP, Tokuda S, Sugihara K, Sugawara T, Furuse K, et al. (Octubre 2019). "Claudins y JAM-A regulan coordinadamente la formación de unión estrecha y la polaridad epitelial". The Journal of Cell Biology. 218 (10): 3372–3396. doi:10.1083/jcb.201812157. PMC 6781433. PMID 31467165.
- ^ Greene C, Campbell M, Janigro D (2019-01-01-01). "Capítulo 1 - Fundamentos de la Anatomía del Cerebro y Funciones Globales". En Lonser RR, Sarntinoranont M, Bankiewicz K (eds.). Nervous System Drug Delivery. Academic Press. pp. 3–20. doi:10.1016/b978-0-12-813997-4.00001-3. ISBN 978-0-12-813997-4. S2CID 198273920.
- ^ Haseloff RF, Piontek J, Blasig IE (2010-01-01). "Capítulo 5 - La investigación de cis- y las interacciones entre Claudins". En Yu AS (ed.). Temas actuales en Membranes. Vol. 65. Academic Press. pp. 97–112. doi:10.1016/s1063-5823(10)65005-3. ISBN 9780123810397.
- ^ a b c d Günzel D, Yu AS (abril de 2013). "Claudins and the modulation of tight junction permeability". Fisiológica Reseñas. 93 (2): 525-569. doi:10.1152/physrev.00019.2012 PMC 3768107. PMID 23589827.
- ^ a b c "Crystal Structures of claudins: insights into their intermolecular interactions". Annals of the New York Academy of Sciences. 1205. Septiembre de 2010. doi:10.1111/nyas.2010.1205.issue-s1. ISSN 0077-8923.
- ^ a b Fuladi S, Jannat RW, Shen L, Weber CR, Khalili-Araghi F (enero 2020). "Modificación computacional de la estructura y función de Claudin". International Journal of Molecular Sciences. 21 3): 742. doi:10.3390/ijms21030742. PMC 7037046. PMID 31979311.
- ^ a b Rüffer C, Gerke V (mayo de 2004). "La cola citoplasmática C-terminal de las grietas 1 y 5 pero no su motivo de unión PDZ es requerido para la localización apical en las uniones estrechas epiteliales y endoteliales". European Journal of Cell Biology. 83 (4): 135-144. doi:10.1078/0171-9335-00366. PMID 15260435.
- ^ a b c Tsukita S, Tanaka H, Tamura A (febrero 2019). "Los Claudins: De las interacciones de la Tight a los sistemas biológicos". Tendencias en Ciencias Bioquímicas. 44 (2): 141–152. doi:10.1016/j.tibs.2018.09.008. PMID 30665499. S2CID 58640701.
- ^ Furuse M, Fujita K, Hiiragi T, Fujimoto K, Tsukita S (junio de 1998). "Claudin-1 y -2: nuevas proteínas integrales de membrana localizando en uniones estrechas sin semejanza secuencial a occludin". The Journal of Cell Biology. 141 (7): 1539–1550. doi:10.1083/jcb.141.7.1539. PMC 2132999. PMID 9647647.
- ^ Liu F, Koval M, Ranganathan S, Fanayan S, Hancock WS, Lundberg EK, et al. (Febrero 2016). "Systems Proteomics View of the Endogenous Human Claudin Protein Family". Journal of Proteome Research. 15 (2): 339–359. doi:10.1021/acs.jproteome.5b00769. PMC 4777318. PMID 26680015.
- ^ a b Taylor A, Warner M, Mendoza C, Memmott C, LeCheminant T, Bailey S, et al. (Mayo 2021). "Chimeric Claudins: Una nueva herramienta para estudiar la estructura y función de la articulación de la lucha". International Journal of Molecular Sciences. 22 (9): 4947. doi:10.3390/ijms22094947. PMC 8124314. PMID 34066630.
- ^ Hou J (2019-01-01). "Capítulo 7 - Canal Paracelular en Sistema de Órganos". En Hou J (ed.). El Canal Paracelular. Academic Press. pp. 93–141. doi:10.1016/b978-0-12-814635-4.00007-3. ISBN 978-0-12-814635-4. S2CID 90477792.
- ^ Hou J (2019-01-01). "Capítulo 8 - Canal Paracelular en Enfermedad Humana". En Hou J (ed.). El Canal Paracelular. Academic Press. pp. 143–173. doi:10.1016/b978-0-12-814635-4.00008-5. ISBN 978-0-12-814635-4. S2CID 90122806.