Ciclosporina
ciclosporina, también conocida como ciclosporina y ciclosporina, es un inhibidor de la calcineurina que se utiliza como medicamento inmunosupresor. Se toma por vía oral o intravenosa para la artritis reumatoide, la psoriasis, la enfermedad de Crohn, el síndrome nefrótico y en trasplantes de órganos para prevenir el rechazo. También se usa como colirio para la queratoconjuntivitis sicca (ojos secos).
Los efectos secundarios comunes incluyen presión arterial alta, dolor de cabeza, problemas renales, aumento del crecimiento del vello y vómitos. Otros efectos secundarios graves incluyen un mayor riesgo de infección, problemas hepáticos y un mayor riesgo de linfoma. Se deben controlar los niveles sanguíneos del medicamento para disminuir el riesgo de efectos secundarios. El uso durante el embarazo puede provocar un parto prematuro; sin embargo, la ciclosporina no parece causar defectos de nacimiento.
Se cree que la ciclosporina funciona al disminuir la función de los linfocitos. Lo hace formando un complejo con la ciclofilina para bloquear la actividad de la fosfatasa de la calcineurina, lo que a su vez disminuye la producción de citocinas inflamatorias por parte de los linfocitos T.
La ciclosporina se aisló en 1971 del hongo Tolypocladium inflatum y comenzó a usarse en medicina en 1983. Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud. En 2020, fue el 212º medicamento más recetado en los Estados Unidos, con más de 2 millones de recetas. Está disponible como medicamento genérico.
Usos médicos
La ciclosporina está indicada para tratar y prevenir la enfermedad de injerto contra huésped en el trasplante de médula ósea y para prevenir el rechazo de trasplantes de riñón, corazón e hígado. También está aprobado en los EE. UU. para el tratamiento de la artritis reumatoide y la psoriasis, la queratitis numular persistente después de la queratoconjuntivitis adenoviral y como colirio para tratar la sequedad ocular provocada por el síndrome de Sjögren y la disfunción de las glándulas de Meibomio.
Además de estas indicaciones, la ciclosporina también se utiliza en la dermatitis atópica grave, la enfermedad de Kimura, el pioderma gangrenoso, la urticaria crónica, la mastocitosis sistémica aguda y la uveítis posterior o intermedia de causa no infecciosa. También se usa, aunque con poca frecuencia, en la artritis reumatoide grave y enfermedades relacionadas.
La ciclosporina también se ha utilizado en personas con colitis ulcerosa grave aguda y urticaria que no responden al tratamiento con esteroides.
Efectos secundarios
Los efectos secundarios de la ciclosporina pueden incluir agrandamiento de las encías, aumento del crecimiento del vello, convulsiones, úlceras pépticas, pancreatitis, fiebre, vómitos, diarrea, confusión, aumento del colesterol, dificultad para respirar, entumecimiento y hormigueo (particularmente en los labios), picazón, presión arterial, retención de potasio (que posiblemente conduce a hiperpotasemia), disfunción renal y hepática, sensación de ardor en las yemas de los dedos y una mayor vulnerabilidad a las infecciones virales y fúngicas oportunistas. La ciclosporina causa hipertensión al inducir vasoconstricción en los riñones y aumentar la reabsorción de sodio. El aumento de la presión arterial puede provocar eventos cardiovasculares; por lo tanto, se recomienda utilizar la dosis efectiva más baja para las personas que requieren un tratamiento a largo plazo.
El uso de ciclosporina después de un trasplante de riñón se asocia con niveles elevados de ácido úrico en la sangre y, en algunos casos, con gota. Esto se debe a la disminución de la tasa de filtración glomerular, lo que conduce a la retención de ácido úrico. Se ha demostrado que el uso de azatioprina como alternativa reduce la incidencia de artritis gotosa.
La ciclosporina figura como carcinógeno del Grupo 1 de la IARC (es decir, hay suficiente evidencia de carcinogenicidad en humanos), lo que conduce específicamente al cáncer de piel de células escamosas y al linfoma no Hodgkin.
Farmacología
Mecanismo de acción
El efecto principal de la ciclosporina es disminuir la actividad de las células T; lo hace inhibiendo la calcineurina en la vía calcineurina-fosfatasa y evitando que se abra el poro de transición de la permeabilidad mitocondrial. La ciclosporina se une a la proteína citosólica ciclofilina (inmunofilina) de los linfocitos, especialmente de las células T. Este complejo ciclosporina-ciclofilina inhibe la calcineurina, que normalmente es responsable de activar la transcripción de la interleucina 2. En las células T, la activación del receptor de células T normalmente aumenta el calcio intracelular, que actúa a través de la calmodulina para activar la calcineurina. Luego, la calcineurina desfosforila el factor de transcripción NF-AT (factor nuclear de células T activadas), que se mueve hacia el núcleo de las células T y aumenta la transcripción de genes para IL-2 y citoquinas relacionadas. La ciclosporina, al impedir la desfosforilación de NF-AT, reduce la función de las células T efectoras; no afecta la actividad citostática.
La ciclosporina también se une a la proteína ciclofilina D que constituye parte del poro de transición de permeabilidad mitocondrial (MPTP), evitando así la apertura de MPTP. El MPTP se encuentra en la membrana mitocondrial de las células del músculo cardíaco. La apertura del MPTP significa un cambio repentino en la permeabilidad de la membrana mitocondrial interna, lo que permite que los protones y otros iones y solutos de un tamaño de hasta ~1,5 kDa atraviesen la membrana interna. Este cambio de permeabilidad se considera una catástrofe celular, que conduce a la muerte celular. Sin embargo, las breves aperturas de poros de transición de permeabilidad mitocondrial desempeñan un papel fisiológico esencial en el mantenimiento de una homeostasis mitocondrial saludable.
Farmacocinética
La ciclosporina es un péptido cíclico de 11 aminoácidos; contiene un solo D-aminoácido, que rara vez se encuentra en la naturaleza. A diferencia de la mayoría de los péptidos, los ribosomas no sintetizan la ciclosporina.
La ciclosporina se metaboliza mucho en humanos y animales después de la ingestión. Los metabolitos, que incluyen ciclosporina B, C, D, E, H y L, tienen menos del 10 % de actividad inmunosupresora de ciclosporina y están asociados con una mayor toxicidad renal. Se han aislado y caracterizado metabolitos individuales de ciclosporina, pero no parece que se hayan estudiado de forma exhaustiva.
Biosíntesis
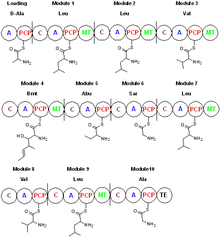
La ciclosporina es sintetizada por una péptido sintetasa no ribosomal, la ciclosporina sintetasa. La enzima contiene un dominio de adenilación, un dominio de tiolación, un dominio de condensación y un dominio de N-metiltransferasa. El dominio de adenilación es responsable del reconocimiento y la activación del sustrato, mientras que el dominio de tiolación une covalentemente los aminoácidos adenilados a la fosfopanteteína y el dominio de condensación alarga la cadena peptídica. Los sustratos de la ciclosporina sintetasa incluyen L-valina, L-leucina, L-alanina, glicina, ácido 2-aminobutírico, 4-metiltreonina y D-alanina, que es el aminoácido inicial en el proceso biosintético. Con el dominio de adenilación, la ciclosporina sintetasa genera los aminoácidos acil-adenilados y luego une covalentemente el aminoácido a la fosfopanteteína a través de un enlace tioéster. Algunos de los sustratos de aminoácidos se vuelven N-metilados por la S-adenosil metionina. El paso de ciclación libera ciclosporina de la enzima. Los aminoácidos como D-Ala y butenil-metil-L-treonina (Bmt) indican que la ciclosporina sintetasa requiere la acción de otras enzimas. La racemización de L-Ala a D-Ala por la alanina racemasa depende del fosfato de piridoxal. La formación de butenil-metil-L-treonina se realiza mediante una policétido sintasa Bmt que utiliza acetato/malonato como material de partida.
Grupo de genes
Tolypocladium inflatum, la especie utilizada actualmente para la producción masiva de ciclosporina, tiene los genes biosintéticos dispuestos en un grupo de 12 genes. De estos 12 genes, SimA (Q09164) es la ciclosporina sintetasa, SimB (CAA02484.1) es la alanina racemasa y SimG (similar a ATQ39432.1) es la policétido sintasa. Estos genes están asociados con un retrotransposón activo. Aunque estas secuencias están mal anotadas en GenBank y otras bases de datos, se pueden encontrar secuencias similares en un 90 % para la Beauveria felina productora de ciclosporina (o Amphichorda ~). SimB tiene dos parálogos en el mismo organismo con funciones diferentes pero superpuestas gracias a su baja especificidad.
Historia
En 1970, empleados de Sandoz (ahora Novartis) en Basilea, Suiza, aislaron nuevas cepas de hongos de muestras de suelo tomadas de Noruega y de Wisconsin en los EE. UU. Ambas cepas produjeron una familia de productos naturales llamados ciclosporinas. Se aislaron dos componentes relacionados que tenían actividad antifúngica a partir de extractos de estos hongos. La cepa noruega, Tolypocladium inflatum Gams, se utilizó más tarde para la fermentación a gran escala de ciclosporina.
El efecto inmunosupresor del producto natural ciclosporina se descubrió el 31 de enero de 1972 en una prueba de detección de inmunosupresión diseñada e implementada por Hartmann F. Stähelin en Sandoz. La estructura química de la ciclosporina se determinó en 1976, también en Sandoz. R.Y. Calne y colegas de la Universidad de Cambridge, y en trasplantes de hígado realizados por Thomas Starzl en el Hospital de la Universidad de Pittsburgh. El primer paciente, el 9 de marzo de 1980, era una mujer de 28 años. En los Estados Unidos, la Administración de Drogas y Alimentos (FDA) aprobó la ciclosporina para uso clínico en 1983.
Sociedad y cultura
Nombre
El producto natural fue llamado ciclosporina por los científicos de habla alemana que lo aislaron por primera vez y la ciclosporina cuando se tradujo al inglés. De acuerdo con las pautas de las denominaciones comunes internacionales (INN) para medicamentos, la y se reemplazó por i para que la INN del medicamento se escriba ciclosporina.
La ciclosporina es la INN y el nombre británico aprobado (BAN), mientras que la ciclosporina es el nombre adoptado en los Estados Unidos (USAN) y la ciclosporina es una antigua BAN.
Formularios disponibles
La ciclosporina presenta una solubilidad muy baja en agua y, como consecuencia, se han desarrollado formas de suspensión y emulsión del medicamento para administración oral e inyección. La ciclosporina fue originalmente lanzada al mercado por Sandoz (ahora Novartis), bajo la marca Sandimmune, que está disponible en forma de cápsulas de gelatina blanda, una solución oral y una formulación para administración intravenosa. Todas estas son composiciones no acuosas. Una formulación de microemulsión administrada por vía oral más nueva, Neoral, está disponible como una solución y como cápsulas de gelatina blanda. Las composiciones de Neoral están diseñadas para formar microemulsiones en contacto con el agua.
Las preparaciones genéricas de ciclosporina se han comercializado con varios nombres comerciales, incluidos Cicloral (de Sandoz/Hexal), Gengraf (de Abbott) y Deximune (de Dexcel Pharma). Desde 2002, una emulsión tópica de ciclosporina para el tratamiento de la inflamación causada por la queratoconjuntivitis sicca (síndrome del ojo seco) se comercializa con el nombre comercial Restasis. Ikervis es una formulación similar con una concentración del 0,1%. Las formulaciones de ciclosporina inhalada están en desarrollo clínico e incluyen una solución en propilenglicol y dispersiones de liposomas.
Investigación
Neuroprotección
La ciclosporina se encuentra actualmente en un estudio clínico de fase II/III (adaptativo) en Europa para determinar su capacidad para mejorar el daño celular neuronal y la lesión por reperfusión (fase III) en lesiones cerebrales traumáticas. Este estudio multicéntrico está siendo organizado por NeuroVive Pharma y el Consorcio Europeo de Lesiones Cerebrales usando la formulación de ciclosporina de NeuroVive llamada NeuroSTAT (también conocida por su nombre comercial de cardioprotección de CicloMulsion). Esta formulación utiliza una base de emulsión de lípidos en lugar de cremóforo y etanol. NeuroSTAT se comparó con Sandimmune en un estudio de fase I y se encontró que era bioequivalente. En este estudio, NeuroSTAT no mostró las reacciones anafilácticas y de hipersensibilidad que se encuentran en los productos a base de cremophor y etanol.
La ciclosporina se ha investigado como un posible agente neuroprotector en condiciones como una lesión cerebral traumática y se ha demostrado en experimentos con animales que reduce el daño cerebral asociado con una lesión. La ciclosporina bloquea la formación del poro de transición de la permeabilidad mitocondrial, que se ha descubierto que causa gran parte del daño asociado con lesiones en la cabeza y enfermedades neurodegenerativas. Las propiedades neuroprotectoras de la ciclosporina se descubrieron por primera vez a principios de la década de 1990, cuando dos investigadores (Eskil Elmér e Hiroyuki Uchino) realizaban experimentos de trasplante de células. Un hallazgo no deseado fue que la ciclosporina A era fuertemente neuroprotectora cuando cruzaba la barrera hematoencefálica. Este mismo proceso de destrucción mitocondrial a través de la apertura del poro MPT está implicado en el empeoramiento de las lesiones cerebrales traumáticas.
Enfermedad cardiaca
La ciclosporina se ha usado experimentalmente para tratar la hipertrofia cardíaca (un aumento en el volumen celular).
La apertura inadecuada del poro de transición de la permeabilidad mitocondrial (MPTP) se manifiesta en la isquemia (restricción del flujo sanguíneo al tejido) y lesión por reperfusión (daño que ocurre después de la isquemia cuando el flujo sanguíneo regresa al tejido), después de un infarto de miocardio (ataque cardíaco) y cuando se producen mutaciones en la ADN polimerasa mitocondrial se producen. El corazón intenta compensar el estado de enfermedad aumentando el Ca2+
para aumentar las tasas de ciclos de contractilidad. Niveles constitutivamente altos de mitocondrial Ca2+
causar una apertura inapropiada del MPTP que conduce a una disminución en el rango de función cardiaca, lo que lleva a una hipertrofia cardiaca como un intento de compensar el problema.
Se ha demostrado que la ciclosporina A disminuye la hipertrofia cardíaca al afectar a los miocitos cardíacos de muchas maneras. La ciclosporina A se une a la ciclofilina D para bloquear la apertura de MPTP y, por lo tanto, disminuye la liberación de la proteína citocromo C, que puede causar la muerte celular programada. CypD es una proteína dentro del MPTP que actúa como puerta; la unión de la ciclosporina A disminuye la cantidad de apertura inapropiada de MPTP, lo que disminuye el Ca2+
. Ca2+
permite revertir la hipertrofia cardíaca causada en la respuesta cardíaca original. La disminución de la liberación de citocromo C provocó una disminución de la muerte celular durante lesiones y enfermedades. La ciclosporina A también inhibe la vía de la fosfatasa calcineurina (14). Se ha demostrado que la inhibición de esta vía reduce la hipertrofia miocárdica.
Uso veterinario
El medicamento está aprobado en los Estados Unidos para el tratamiento de la dermatitis atópica en perros. A diferencia de la forma humana del medicamento, las dosis más bajas que se usan en los perros significan que el fármaco actúa como un inmunomodulador y tiene menos efectos secundarios que en los humanos. Los beneficios de usar este producto incluyen la reducción de la necesidad de terapias simultáneas para controlar la afección. Está disponible como un ungüento oftálmico para perros llamado Optimmune, fabricado por Intervet, que forma parte de Merck. También se usa para tratar la adenitis sebácea (respuesta inmunitaria contra las glándulas sebáceas), el pénfigo foliáceo (enfermedad cutánea ampollar autoinmune), la enfermedad intestinal inflamatoria, la furunculosis anal (enfermedad inflamatoria anal) y la miastenia gravis (una enfermedad neuromuscular).
Contenido relacionado
Etano
Artturi Ilmari Virtanen
Medicina Veterinaria