Ciclo visual
El ciclo visual es un proceso que se lleva a cabo en la retina y que repone la molécula retinal para su uso en la visión. El retinal es el cromóforo de la mayoría de las opsinas visuales, lo que significa que captura los fotones para iniciar la cascada de fototransducción. Cuando el fotón es absorbido, el 11-cis retinal se fotoisomeriza en todo-trans retinal al ser expulsado de la proteína opsina. Cada molécula de retinal debe viajar desde la célula fotorreceptora hasta el epitelio pigmentario de la retina y viceversa para renovarse y combinarse con otra opsina. Esta vía enzimática cerrada del 11-cis retinal a veces se denomina ciclo visual de Wald en honor a George Wald (1906–1997), quien recibió el Premio Nobel en 1967 por su trabajo en pos de su descubrimiento.
Retinal
El retinal es un cromóforo que forma proteínas fotosensibles de retinilideno cuando se une covalentemente a proteínas llamadas opsinas. El retinal puede fotoisomerizarse por sí solo, pero necesita estar unido a una proteína opsina para activar la cascada de fototransducción y ajustar la sensibilidad espectral a longitudes de onda más largas, que permiten la visión en color.
El retinal es una especie de retinoide y la forma aldehído de la vitamina A. El retinal es interconvertible con el retinol, la forma de transporte y almacenamiento de la vitamina A. Durante el ciclo visual, el retinal se mueve entre varios isómeros diferentes y también se convierte en retinol y éster de retinilo. Los retinoides pueden derivar de la oxidación de carotenoides como el betacaroteno o pueden consumirse directamente. Para llegar a la retina, se une a la proteína transportadora de retinol (RBP) y a la transtiretina, lo que evita su filtración en los glomérulos.
Al igual que en el transporte a través de la vía RBP-Transtiretina, los retinoides siempre deben estar unidos a moléculas de chaperonas por varias razones. Los retinoides son tóxicos, insolubles en soluciones acuosas y propensos a la oxidación, por lo que deben estar unidos y protegidos cuando se encuentran dentro del cuerpo. El cuerpo utiliza una variedad de chaperonas, particularmente en la retina, para transportar los retinoides.
Sinopsis
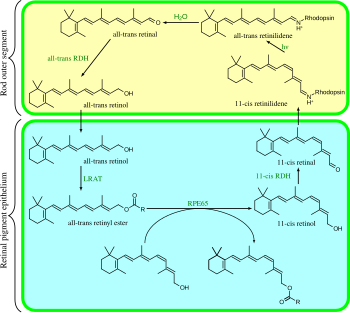
El ciclo visual es consistente en los mamíferos y se resume de la siguiente manera:
- all-trans-retinyl ester + H2O → 11-cis-retinol + ácido graso; isomerohidrolas RPE65;
- 11-cis-retinol + NAD+ → 11-cis-retina + NADH + H+; 11-cis-retinol deshidrogenasa;
- 11-cis-retinal + aporhodopsin → rhodopsin + H2O; formas Schiff base linkage to lysine, -CH=N+H-;
- rhodopsin + hν → metarhodopsin II (es decir, 11-cis fotoisomeriza a todos...trans):
- (rhodopsin + hν → photorhodopsin → bathorhodopsin → lumirhodopsin → metarhodopsin I → metarhodopsin II);
- metarhodopsin II + H2O → aporhodopsin + all-trans-retina;
- all-trans-retinal + NADPH + H+ → all-trans-retinol + NADP+; all-trans-retinol deshidrogenasa;
- Todo...trans-retinol + ácido graso → all-trans-retinil ester + H2O; lecithin retinol acyltransferases (LRATs).
Los pasos 3, 4, 5 y 6 ocurren en los segmentos externos de las células bastón; los pasos 1, 2 y 7 ocurren en las células del epitelio pigmentario de la retina (EPR).
Descripción
Cuando se absorbe un fotón, el 11-cis-retinal se transforma en todo-trans-retinal y se desplaza hacia el sitio de salida de la rodopsina. No abandonará la proteína opsina hasta que otro cromóforo nuevo venga a reemplazarlo, excepto en la vía ABCR. Mientras todavía está unido a la opsina, el todo-trans-retinal se transforma en todo-trans-retinol por acción de la todo-trans-retinol deshidrogenasa. Luego avanza hacia la membrana celular del bastón, donde es acompañado hasta el epitelio pigmentario de la retina (EPR) por la proteína de unión a retinoides interfotorreceptora (IRBP). Luego ingresa a las células del EPR y se transfiere a la chaperona de la proteína de unión a retinol celular (CRBP).
Cuando se encuentra dentro de la célula epitelial pigmentaria (EPR), unido a CRBP, el retinol all-trans es esterificado por la lecitina retinol aciltransferasa (LRAT) para formar un éster de retinilo. Los ésteres de retinilo del EPR están acompañados por una proteína conocida como RPE65. Es en esta forma que el EPR almacena la mayoría de sus retinoides, ya que el EPR almacena de 2 a 3 veces más retinoides que la propia retina neural. Cuando se necesita más cromóforo, la isomerohidrolasa actúa sobre los ésteres de retinilo para producir 11-cis-retinol, que se transfiere a la proteína de unión al retinaldehído celular (CRALBP). El 11-cis-retinol se transforma en 11-cis retinal por la 11-cis-retinol deshidrogenasa, y luego se envía de vuelta a las células fotorreceptoras a través de IRBP. Allí, reemplaza el cromóforo gastado en las moléculas de opsina, volviéndola fotosensible.
Carretera de ABCR
En circunstancias normales, el cromóforo gastado se descarga de la proteína mediante un cromóforo entrante "recargado". Sin embargo, a veces el cromóforo gastado puede abandonar la proteína opsina antes de su reemplazo, cuando se une a la proteína ABCA4 (también conocida como ABCR). En esta etapa, también se transforma en todo-trans-retinol, y luego sale del segmento externo del fotorreceptor a través de la chaperona IRBP. Luego sigue el ciclo visual convencional. Es a partir de esta vía que se puede explicar la presencia de opsina sin un cromóforo.
RGR regulation
El ciclo visual puede ser regulado por el sistema del receptor acoplado a proteína G de la retina (opsina RGR). Cuando la luz activa la opsina RGR, se acelera el reciclaje del cromóforo en el epitelio pigmentario de la retina. Este mecanismo proporciona cromóforo adicional después de blanqueamientos intensos y puede considerarse un mecanismo importante en las primeras fases de adaptación a la oscuridad y reposición de cromóforos.
Ciclos alternativos
Ciclo visual específico
Se cree que existe un ciclo visual alternativo, que utiliza células gliales de Müller en lugar del epitelio pigmentario de la retina. En esta vía, los conos reducen el retinal all-trans a retinol all-trans a través de la deshidrogenasa del retinol all-trans y luego transportan el retinol all-trans a las células de Müller. Allí, se transforma en 11-cis retinol por la isomerasa del retinol all-trans y puede almacenarse como ésteres de retinilo dentro de las células de Müller o transportarse de regreso a los fotorreceptores de los conos, donde se transforma de 11-cis retinol a 11-cis retinal por la deshidrogenasa del retinol 11-cis. Esta vía ayuda a explicar la rápida adaptación a la oscuridad en el sistema de los conos y la presencia de la deshidrogenasa del retinol 11-cis en los fotorreceptores de los conos, ya que no se encuentra en los bastones, solo en el epitelio pigmentario de la retina.
Ciclo visual de Melanopsin
La melanopsina es una opsina visual presente en las células ganglionares de la retina intrínsecamente fotosensibles (ipRGC) que también tienen un cromáforo retiniano. Sin embargo, a diferencia de los pigmentos de los conos y bastones, la melanopsina tiene la capacidad de actuar como fotopigmento excitable y como fotoisomerasa. Por lo tanto, la melanopsina es capaz de isomerizar el todo-trans-retinal en el propio 11-cis-retinal cuando se estimula con otro fotón. Por lo tanto, una ipRGC no depende de las células de Müller y/o de las células del epitelio pigmentario de la retina para esta conversión.
Leber's congenital amaurosis
Se ha propuesto como posible mecanismo de la amaurosis congénita de Leber la deficiencia de RPE65. Sin la proteína RPE65, el epitelio pigmentario de la retina no puede almacenar ésteres de retinilo y, por lo tanto, el ciclo visual se interrumpe. En las primeras etapas de la enfermedad, las células cono no se ven afectadas, ya que pueden depender del ciclo visual alternativo de las células de Müller. Sin embargo, los bastones no tienen acceso a esta alternativa y se vuelven inertes. La amaurosis congénita de Leber se manifiesta, por lo tanto, como nictalopía (ceguera nocturna). En las últimas etapas de la enfermedad, se observa una retinopatía general a medida que los bastones pierden su capacidad de señalizar. Como resultado, los bastones secretan continuamente glutamato, un neurotransmisor, a un ritmo que las células de Müller no pueden absorber. Los niveles de glutamato se acumularán dentro de la retina, donde alcanzarán niveles neurotóxicos. La deficiencia de RPE65 sería de origen genético y es solo una de las muchas posibles fisiopatologías propuestas para la enfermedad. Sin embargo, existe una terapia génica retiniana para reintroducir los genes RPE65 normales que ha sido aprobada por la FDA desde 2017.
Véase también
- Fototransducción visual
- Sistema visual
Referencias
- ^ Moiseyev, Gennadiy; Chen, Ying; Takahashi, Yusuke; Wu, Bill X.; Ma, Jian-xing (2005). "RPE65 es el isomerohidrolase en el ciclo visual retinoide". Actas de la Academia Nacional de Ciencias. 102 (35): 12413–12418. Bibcode:2005PNAS..10212413M. doi:10.1073/pnas.0503460102. PMC 1194921. PMID 16116091.
- ^ Jin, Minghao; Yuan, Quan; Li, Songhua; Travis, Gabriel H. (2007). "Role of LRAT on the Retinoid Isomerase Activity and Membrane Association of Rpe65". Journal of Biological Chemistry. 282 (29): 20915–20924. doi:10.1074/jbc.M701432200. PMC 2747659. PMID 17504753.
- ^ Wang, Jin-Shan; Kefalov, Vladimir J. (marzo de 2011). "El ciclo visual específico de Cone". Progress in Retinal and Eye Research. 30 2): 115 –128. doi:10.1016/j.preteyeres.2010.11.001. PMC 3073571. PMID 21111842.
- ^ Kolb H, Fernandez E, Nelson R (1995-01-01). "Melanopsin-expressing, Intrínsecamente Fotosensible Retinal Ganglion Cells (IpRGCs)". En Kolb H, Fernandez E, Nelson R (eds.). Webvision: La Organización del Sistema Retina y Visual. University of Utah Health Sciences Center. PMID 21413389.
- ^ "Productos aprobados – Luxturna". FDA Center for Biologics Evaluation and Research. 19 de diciembre de 2017.