Cianogeno
Cianógeno es el compuesto químico de fórmula (CN)2. El nitruro de carbono estable más simple, es un gas incoloro y altamente tóxico con un olor acre. La molécula es un pseudohalógeno. Las moléculas de cianógeno constan de dos grupos CN, análogos a las moléculas de halógeno diatómico, como el Cl2, pero mucho menos oxidantes. Los dos grupos ciano están unidos entre sí por sus átomos de carbono: N≡C‒C≡N, aunque se han detectado otros isómeros. El nombre también se usa para el radical CN y, por lo tanto, se usa para compuestos como el bromuro de cianógeno (NCBr) (pero consulte también Radical ciano).
El cianógeno es el anhídrido de la oxamida:
- H2NC(O)C(O)NH2 → NCCN + 2 H2O
aunque la oxamida se fabrica a partir de cianógeno mediante hidrólisis:
- NCCN + 2 H2O → H2NC(O)C(O)NH2
Preparación
El cianógeno generalmente se genera a partir de compuestos de cianuro. Un método de laboratorio implica la descomposición térmica del cianuro de mercurio:
- 2 Hg(CN)2 → (CN)2 + Hg2(CN)2
Alternativamente, se pueden combinar soluciones de sales de cobre (II) (como sulfato de cobre (II)) con cianuros; Se forma un cianuro de cobre (II) inestable que se descompone rápidamente en cianuro de cobre (I) y cianógeno.
- 2 CuSO4 + 4 KCN → (CN)2 + 2 CuCN + 2 K2SO4
Industrialmente, se crea mediante la oxidación de cianuro de hidrógeno, generalmente usando cloro sobre un catalizador de dióxido de silicio activado o dióxido de nitrógeno sobre una sal de cobre. También se forma cuando el nitrógeno y el acetileno reaccionan mediante una chispa o descarga eléctrica.
Isómeros
Did you mean:Cyanogen is NCCN. There are less stable isomers in which the order of the atoms differs. Isocyanogen (or cyano isocyanogen) is NCNC, isocyanogen is CNBC, and diazodicarbon is CCNN.
Paracianógeno
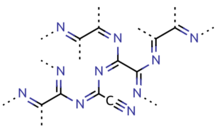
El paracianógeno es un polímero de cianógeno. La mejor manera de prepararlo es calentando cianuro de mercurio. También se puede preparar calentando cianuro de plata, cianato de plata, yoduro de cianógeno o yoduro cianúrico. También se puede preparar mediante la polimerización de cianógeno de 300 a 500 °C (572 a 932 °F) en presencia de trazas de impurezas. El paracianógeno también se puede convertir nuevamente en cianógeno calentándolo a 800 °C (1470 °F). Según la evidencia experimental, se cree que la estructura de este material polimérico es bastante irregular, siendo la mayoría de los átomos de carbono del tipo sp2 y dominios localizados de conjugación π.
Historia
El cianógeno fue sintetizado por primera vez en 1815 por Joseph Louis Gay-Lussac, quien determinó su fórmula empírica y le puso nombre. Gay-Lussac acuñó la palabra "cianógeno" de las palabras griegas κυανός (kyanos, azul) y γεννάω (gennao, creo), porque el químico sueco Carl Wilhelm Scheele aisló por primera vez el cianuro a partir del pigmento "azul de Prusia". En la década de 1850, los fotógrafos utilizaban jabón de cianógeno para eliminar las manchas de plata de sus manos. Alcanzó importancia con el crecimiento de la industria de fertilizantes a finales del siglo XIX y sigue siendo un intermediario importante en la producción de muchos fertilizantes. También se utiliza como estabilizador en la producción de nitrocelulosa.
El cianógeno se encuentra comúnmente en los cometas. En 1910, un análisis espectroscópico del cometa Halley encontró cianógeno en la cola del cometa, lo que hizo temer entre el público que la Tierra se envenenara al pasar por la cola. La gente en Nueva York usaba máscaras antigás y los comerciantes vendían "píldoras cometas" para tratamientos curanderos. Se afirma que neutraliza el envenenamiento. Debido a la naturaleza extremadamente difusa de la cola, no hubo ningún efecto cuando el planeta pasó a través de ella.
Seguridad
Al igual que otros cianuros, el cianógeno es muy tóxico, ya que se reduce fácilmente a cianuro, lo que envenena el complejo citocromo c oxidasa, interrumpiendo así la cadena de transferencia de electrones mitocondrial. El gas cianógeno es irritante para los ojos y el sistema respiratorio. La inhalación puede provocar dolor de cabeza, mareos, pulso rápido, náuseas, vómitos, pérdida del conocimiento, convulsiones y muerte, según la exposición. La dosis letal por inhalación suele oscilar entre 100 y 150 miligramos (1,5 a 2,3 granos).
El cianógeno produce la segunda llama natural más caliente conocida (después del subnitruro de carbono) con una temperatura de más de 4525 °C (8177 °F) cuando se quema en oxígeno.
En la cultura popular
En la serie de Doctor Who "El cerebro de Morbius" (la quinta serie de la temporada 13), el Doctor sintetiza cianógeno usando cianuro de hidrógeno como material de partida y lo ventila a través de una tubería para evitar que Solon realice una cirugía en el cerebro del cuerpo de Morbius, sin embargo, la completa poco después. muere por envenenamiento con cianógeno.
Showing translation forIn Dragnet (1987) Friday (Dan Aykroyd) and Streebek (Tom Hanks) are tracking down the villain who stole "the pseudo halogenic compound cyanogen#34;.
Contenido relacionado
Metilisotiazolinona
Reacción de adición de halógeno
Inosinato de disodio