Célula artificial
Una célula artificial, célula sintética o célula mínima es una partícula diseñada que imita una o varias funciones de una célula biológica. A menudo, las células artificiales son membranas biológicas o poliméricas que encierran materiales biológicamente activos. Como tales, los liposomas, los polimerosomas, las nanopartículas, las microcápsulas y una serie de otras partículas pueden considerarse células artificiales.
Los términos "célula artificial" y "célula sintética" se utilizan en diversos campos y pueden tener distintos significados, como se refleja también en las distintas secciones de este artículo. Algunas definiciones más estrictas se basan en el supuesto de que el término "célula" se relaciona directamente con las células biológicas y que, por lo tanto, estas estructuras tienen que estar vivas (o ser parte de un organismo vivo) y, además, que el término "artificial" implica que estas estructuras se construyen artificialmente desde abajo hacia arriba, es decir, a partir de componentes básicos. Por lo tanto, en el área de la biología sintética, una célula artificial puede entenderse como una célula hecha completamente de forma sintética que puede capturar energía, mantener gradientes iónicos, contener macromoléculas, así como almacenar información y tener la capacidad de replicarse. Este tipo de célula artificial aún no se ha creado.
Sin embargo, en otros casos, el término "artificial" no implica que toda la estructura sea hecha por el hombre, sino que puede referirse a la idea de que ciertas funciones o estructuras de las células biológicas pueden modificarse, simplificarse, reemplazarse o complementarse con una entidad sintética.
En otros campos, el término "célula artificial" puede referirse a cualquier compartimento que se parezca un poco a una célula biológica en tamaño o estructura, pero que esté hecho sintéticamente, o incluso hecho completamente a partir de componentes no biológicos. El término "célula artificial" también se utiliza para estructuras con aplicaciones directas, como compartimentos para la administración de fármacos. La microencapsulación permite el metabolismo dentro de la membrana, el intercambio de moléculas pequeñas y la prevención del paso de sustancias grandes a través de ella. Las principales ventajas de la encapsulación incluyen un mejor mimetismo en el cuerpo, una mayor solubilidad de la carga y una menor respuesta inmunitaria. Cabe destacar que las células artificiales han tenido éxito clínico en la hemoperfusión.
Ingeniería de base de células artificiales vivientes
El patólogo alemán Rudolf Virchow propuso la idea de que no sólo la vida surge de las células, sino que cada célula proviene de otra célula; "Omnis cellula e cellula". Hasta ahora, la mayoría de los intentos de crear una célula artificial sólo han creado un paquete que puede imitar ciertas tareas de la célula. Los avances en las reacciones de transcripción y traducción sin células permiten la expresión de muchos genes, pero estos esfuerzos están lejos de producir una célula completamente operativa.
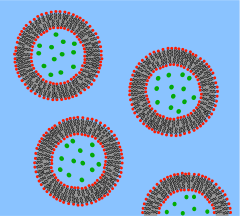
Un enfoque ascendente para construir una célula artificial implicaría crear una protocélula de novo, completamente a partir de materiales no vivos. Como implica el término "célula", un requisito previo es la generación de algún tipo de compartimento que defina una unidad celular individual. Las membranas de fosfolípidos son una opción obvia como límites de compartimentación, ya que actúan como barreras selectivas en todas las células biológicas vivas. Los científicos pueden encapsular biomoléculas en vesículas de fosfolípidos del tamaño de una célula y, al hacerlo, observar que estas moléculas actúan de manera similar a como lo hacen en las células biológicas y, de ese modo, recrear ciertas funciones celulares. De manera similar, los bloques de construcción biológicos funcionales se pueden encapsular en estos compartimentos lipídicos para lograr la síntesis de células artificiales (por rudimentarias que sean).
Se propone crear una vesícula de bicapa fosfolipídica con ADN capaz de autorreproducirse utilizando información genética sintética. Los tres elementos principales de estas células artificiales son la formación de una membrana lipídica, la replicación del ADN y el ARN mediante un proceso de plantilla y la recolección de energía química para el transporte activo a través de la membrana. Los principales obstáculos previstos y encontrados con esta protocélula propuesta son la creación de un ADN sintético mínimo que contenga toda la información suficiente para la vida y la reproducción de componentes no genéticos que son fundamentales para el desarrollo celular, como la autoorganización molecular. Sin embargo, se espera que este tipo de enfoque de abajo hacia arriba proporcione información sobre las cuestiones fundamentales de las organizaciones a nivel celular y los orígenes de la vida biológica. Hasta ahora, no se ha sintetizado ninguna célula completamente artificial capaz de autorreproducirse utilizando las moléculas de la vida, y este objetivo aún está en un futuro lejano, aunque varios grupos están trabajando actualmente para lograrlo.
Otro método propuesto para crear una protocélula se asemeja más a las condiciones que se cree que estuvieron presentes durante la evolución, conocidas como la sopa primordial. Se podrían encapsular varios polímeros de ARN en vesículas y, en condiciones límite tan pequeñas, se podrían probar reacciones químicas.
Ética y controversia
La investigación sobre protocélulas ha generado controversia y opiniones encontradas, incluidas críticas por la vaga definición de "vida artificial". La creación de una unidad básica de vida es la preocupación ética más urgente. La preocupación más extendida sobre las protocélulas es su posible amenaza a la salud humana y al medio ambiente a través de una replicación descontrolada. Sin embargo, es mucho más probable que las células artificiales creadas mediante un enfoque de arriba hacia abajo, o cualquier otra forma manipulada de células vivas existentes, puedan existir y reproducirse fuera de un laboratorio y, por lo tanto, representen una amenaza.
International Research Community
A mediados de la década de 2010, la comunidad científica comenzó a reconocer la necesidad de unificar el campo de la investigación de células sintéticas, reconociendo que la tarea de construir un organismo vivo completo a partir de componentes no vivos estaba fuera del alcance de los recursos de un solo país.
En 2017, se inició la colaboración internacional de investigación a gran escala Build-a-Cell, financiada por la NSF, para la construcción de células vivas sintéticas. Build-a-Cell ha llevado a cabo nueve eventos de talleres interdisciplinarios, abiertos a todos los interesados, para debatir y orientar el futuro de la comunidad de células sintéticas. A Build-a-Cell le siguieron organizaciones nacionales de células sintéticas en varios otros países. Entre esas organizaciones nacionales se incluyen FabriCell, MaxSynBio y BaSyC. Los esfuerzos europeos en materia de células sintéticas se unificaron en 2019 como la iniciativa SynCellEU.
Enfoque de arriba abajo para crear una célula de vida mínima
Los miembros del Instituto J. Craig Venter han utilizado un enfoque computacional de arriba hacia abajo para eliminar genes de un organismo vivo y reducirlos a un conjunto mínimo de genes. En 2010, el equipo logró crear una cepa replicante (denominada Mycoplasma laboratorium) de Mycoplasma mycoides utilizando ADN creado sintéticamente, considerado el requisito mínimo para la vida, que se insertó en una bacteria genómicamente vacía. Se espera que el proceso de biosíntesis de arriba hacia abajo permita la inserción de nuevos genes que realicen funciones rentables, como la generación de hidrógeno para combustible o la captura del exceso de dióxido de carbono en la atmósfera. Las innumerables redes reguladoras, metabólicas y de señalización no están completamente caracterizadas. Estos enfoques de arriba hacia abajo tienen limitaciones para la comprensión de la regulación molecular fundamental, ya que los organismos hospedadores tienen una composición molecular compleja e incompletamente definida. En 2019 se publicó un modelo computacional completo de todas las vías en la célula Mycoplasma Syn3.0, lo que representa el primer modelo in silico completo para un organismo mínimo vivo.
Grandes empresas, como ExxonMobil, han realizado grandes inversiones en biología, al asociarse con Synthetic Genomics Inc., la empresa de biosintéticos del propio Craig Venter, para desarrollar combustible a partir de algas.
A partir de 2016, Mycoplasma genitalium es el único organismo utilizado como punto de partida para la ingeniería de una célula mínima, ya que posee el genoma más pequeño conocido que se puede cultivar en condiciones de laboratorio; la variedad de tipo salvaje tiene 482, y la eliminación de exactamente 100 genes considerados no esenciales dio como resultado una cepa viable con tasas de crecimiento mejoradas. La Escherichia coli de genoma reducido se considera más útil, y se han desarrollado cepas viables con el 15% del genoma eliminado.
Se ha creado una variante de una célula artificial en la que se ha introducido un genoma completamente sintético en células huésped vaciadas genómicamente. Aunque no es completamente artificial porque se conservan los componentes citoplasmáticos y la membrana de la célula huésped, la célula diseñada está bajo el control de un genoma sintético y es capaz de replicarse.
Células artificiales para aplicaciones médicas
Historia
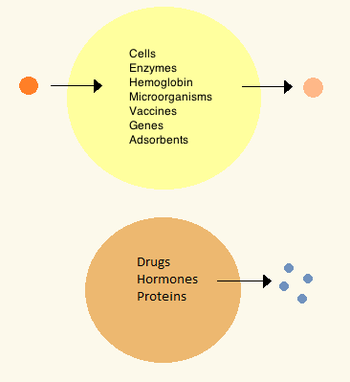
En la década de 1960, Thomas Chang desarrolló microcápsulas que más tarde llamaría "células artificiales", ya que eran compartimentos del tamaño de una célula fabricados con materiales artificiales. Estas células consistían en membranas ultrafinas de nailon, colodión o proteína reticulada cuyas propiedades semipermeables permitían la difusión de pequeñas moléculas dentro y fuera de la célula. Estas células tenían un tamaño micrométrico y contenían células, enzimas, hemoglobina, materiales magnéticos, adsorbentes y proteínas.
Las células artificiales posteriores han tenido dimensiones que van desde los cientos de micrómetros hasta los nanómetros y pueden transportar microorganismos, vacunas, genes, fármacos, hormonas y péptidos. El primer uso clínico de las células artificiales fue en la hemoperfusión mediante la encapsulación de carbón activado.
En la década de 1970, los investigadores pudieron introducir enzimas, proteínas y hormonas en microcápsulas biodegradables, lo que más tarde condujo al uso clínico en enfermedades como el síndrome de Lesch-Nyhan. Aunque la investigación inicial de Chang se centró en glóbulos rojos artificiales, recién a mediados de la década de 1990 se desarrollaron glóbulos rojos artificiales biodegradables. Las células artificiales en encapsulación celular biológica se utilizaron por primera vez en la clínica en 1994 para el tratamiento de un paciente diabético y desde entonces se han encapsulado otros tipos de células como hepatocitos, células madre adultas y células modificadas genéticamente y se están estudiando para su uso en la regeneración de tejidos.
Materiales
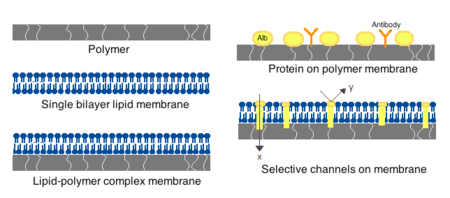
Las membranas para células artificiales pueden estar hechas de polímeros simples, proteínas reticuladas, membranas lipídicas o complejos polímero-lípido. Además, las membranas pueden diseñarse para presentar proteínas de superficie como albúmina, antígenos, portadores de Na/K-ATPasa o poros como canales iónicos. Los materiales comúnmente utilizados para la producción de membranas incluyen polímeros de hidrogel como alginato, celulosa y polímeros termoplásticos como metacrilato de hidroxietilo-metacrilato de metilo (HEMA-MMA), poliacrilonitrilo-cloruro de polivinilo (PAN-PVC), así como variaciones de los mencionados anteriormente. El material utilizado determina la permeabilidad de la membrana celular, que para el polímero depende de la importancia para determinar la difusión adecuada de nutrientes, desechos y otras moléculas críticas. Los polímeros hidrófilos tienen el potencial de ser biocompatibles y pueden fabricarse en una variedad de formas que incluyen micelas de polímero, mezclas sol-gel, mezclas físicas y partículas reticuladas y nanopartículas. De especial interés son los polímeros sensibles a estímulos que responden a cambios de pH o temperatura para su uso en la administración dirigida. Estos polímeros pueden administrarse en forma líquida a través de una inyección macroscópica y solidificarse o gelificarse in situ debido a la diferencia de pH o temperatura. Las preparaciones de nanopartículas y liposomas también se utilizan rutinariamente para la encapsulación y administración de materiales. Una ventaja importante de los liposomas es su capacidad de fusionarse con las membranas celulares y de orgánulos.
Preparación
Se han desarrollado muchas variantes para la preparación y encapsulación de células artificiales. Normalmente, se sintetizan vesículas como nanopartículas, polímerosomas o liposomas. Normalmente, se elabora una emulsión mediante el uso de equipos de alta presión, como un homogeneizador de alta presión o un microfluidizador. A continuación, también se describen dos métodos de microencapsulación para nitrocelulosa.
homogeneización de alta presión
En un homogeneizador de alta presión, dos líquidos en suspensión de aceite/líquido pasan a través de un pequeño orificio bajo una presión muy alta. Este proceso divide los productos y permite la creación de partículas extremadamente finas, de hasta 1 nm.
Microfluidización
Esta técnica utiliza un microfluidizador patentado para obtener una mayor cantidad de suspensiones homogéneas que pueden crear partículas más pequeñas que los homogeneizadores. Primero se utiliza un homogeneizador para crear una suspensión gruesa que luego se bombea al microfluidizador a alta presión. Luego, el flujo se divide en dos corrientes que reaccionarán a velocidades muy altas en una cámara de interacción hasta que se obtenga el tamaño de partícula deseado. Esta técnica permite la producción a gran escala de liposomas de fosfolípidos y las posteriores nanoencapsulaciones de material.
Método de goteo
En este método, una solución celular se incorpora gota a gota a una solución de colodión de nitrato de celulosa. A medida que la gota se desplaza a través del colodión, se recubre con una membrana gracias a las propiedades de polimerización interfacial del colodión. La célula se sedimenta posteriormente en parafina, donde se fija la membrana, que luego se suspende utilizando una solución salina. El método de la gota se utiliza para la creación de células artificiales de gran tamaño que encapsulan células biológicas, células madre y células madre modificadas genéticamente.
Método de emulsión
El método de emulsión se diferencia en que el material a encapsular suele ser más pequeño y se coloca en el fondo de una cámara de reacción donde se añade el colodión en la parte superior y se centrifuga o se revuelve de otro modo para crear una emulsión. Luego, el material encapsulado se dispersa y se suspende en una solución salina.
Importancia clínica
Liberación y entrega de drogas
Las células artificiales que se utilizan para la administración de fármacos se diferencian de otras células artificiales en que su contenido está destinado a difundirse fuera de la membrana o ser engullido y digerido por una célula huésped diana. A menudo se utilizan células artificiales de membrana lipídica submicrónicas que pueden denominarse nanocápsulas, nanopartículas, polimerosomas u otras variaciones del término.
Se ha desarrollado un sistema sensible a la temperatura que utiliza termómetros de ARN para controlar el momento y la ubicación de la liberación de la carga de las células artificiales. Esto se logra haciendo que las células artificiales expresen una proteína formadora de poros (alfa hemolisina) bajo el control de un termómetro de ARN, lo que permite que la liberación de la carga se acople a los cambios de temperatura.
Terapia enzima
La terapia enzimática se está estudiando activamente para las enfermedades metabólicas genéticas en las que una enzima está sobreexpresada, subexpresada, defectuosa o inexistente. En el caso de subexpresión o expresión de una enzima defectuosa, se introduce una forma activa de la enzima en el cuerpo para compensar el déficit. Por otro lado, una sobreexpresión enzimática puede contrarrestarse mediante la introducción de una enzima no funcional competidora; es decir, una enzima que metabolice el sustrato en productos no activos. Cuando se colocan dentro de una célula artificial, las enzimas pueden realizar su función durante un período mucho más largo en comparación con las enzimas libres y pueden optimizarse aún más mediante la conjugación de polímeros.
La primera enzima estudiada en el marco de la encapsulación de células artificiales fue la asparaginasa para el tratamiento del linfosarcoma en ratones. Este tratamiento retrasó la aparición y el crecimiento del tumor. Estos hallazgos iniciales condujeron a una mayor investigación sobre el uso de células artificiales para la administración de enzimas en melanomas dependientes de tirosina. Estos tumores tienen una mayor dependencia de la tirosina que las células normales para su crecimiento, y la investigación ha demostrado que la reducción de los niveles sistémicos de tirosina en ratones puede inhibir el crecimiento de los melanomas. El uso de células artificiales en la administración de tirosinasa, una enzima que digiere la tirosina, permite una mejor estabilidad de la enzima y se ha demostrado que es eficaz en la eliminación de tirosina sin los graves efectos secundarios asociados con la privación de tirosina en la dieta.
La terapia enzimática con células artificiales también es interesante para la activación de profármacos como la ifosfamida en ciertos tipos de cáncer. Las células artificiales que encapsulan la enzima citocromo p450, que convierte este profármaco en el fármaco activo, pueden adaptarse para acumularse en el carcinoma pancreático o implantarse cerca del lugar del tumor. En este caso, la concentración local de la ifosfamida activada será mucho mayor que en el resto del cuerpo, lo que evitará la toxicidad sistémica. El tratamiento tuvo éxito en animales y mostró una duplicación de la supervivencia media entre los pacientes con cáncer de páncreas en etapa avanzada en ensayos clínicos de fase I/II, y una triplicación de la tasa de supervivencia a un año.
Terapia genética
En el tratamiento de enfermedades genéticas, la terapia génica tiene como objetivo insertar, alterar o eliminar genes dentro de las células de un individuo afectado. La tecnología depende en gran medida de vectores virales, lo que genera inquietudes sobre la mutagénesis insercional y la respuesta inmunitaria sistémica que han provocado muertes humanas y el desarrollo de leucemia en ensayos clínicos. Eludir la necesidad de vectores mediante el uso de ADN desnudo o plasmídico como su propio sistema de administración también plantea problemas como la baja eficiencia de transducción y la mala focalización tisular cuando se administra sistémicamente.
Se han propuesto células artificiales como un vector no viral mediante el cual células no autólogas modificadas genéticamente se encapsulan e implantan para administrar proteínas recombinantes in vivo. Se ha demostrado que este tipo de inmunoaislamiento es eficaz en ratones mediante la administración de células artificiales que contienen hormona de crecimiento de ratón, lo que rescató un retraso del crecimiento en ratones mutantes. Se han realizado algunas estrategias para ensayos clínicos en humanos para el tratamiento del cáncer de páncreas, la esclerosis lateral y el control del dolor.
Hemoperfusión
El primer uso clínico de células artificiales fue en la hemoperfusión mediante la encapsulación de carbón activado. El carbón activado tiene la capacidad de adsorber muchas moléculas grandes y desde hace mucho tiempo se sabe que tiene la capacidad de eliminar sustancias tóxicas de la sangre en caso de intoxicación o sobredosis accidental. Sin embargo, la perfusión mediante la administración directa de carbón es tóxica, ya que provoca embolias y daños en las células sanguíneas, seguidos de su eliminación por las plaquetas. Las células artificiales permiten que las toxinas se difundan en la célula mientras mantienen la carga peligrosa dentro de su membrana ultrafina.
La hemoperfusión de células artificiales se ha propuesto como una opción de desintoxicación menos costosa y más eficiente que la hemodiálisis, en la que el filtrado de la sangre se lleva a cabo únicamente a través de la separación por tamaño mediante una membrana física. En la hemoperfusión, miles de células artificiales adsorbentes se retienen dentro de un pequeño recipiente mediante el uso de dos pantallas en cada extremo a través de las cuales se perfunde la sangre del paciente. A medida que la sangre circula, las toxinas o los medicamentos se difunden en las células y son retenidos por el material absorbente. Las membranas de las células artificiales son mucho más delgadas que las utilizadas en diálisis y su pequeño tamaño significa que tienen una gran superficie de membrana. Esto significa que una porción de célula puede tener una transferencia de masa teórica que es cien veces mayor que la de una máquina de riñón artificial completa. El dispositivo se ha establecido como un método clínico de rutina para pacientes tratados por envenenamiento accidental o suicida, pero también se ha introducido como terapia en la insuficiencia hepática y renal al realizar parte de la función de estos órganos. También se ha propuesto la hemoperfusión de células artificiales para su uso en inmunoadsorción, mediante la cual se pueden eliminar anticuerpos del cuerpo mediante la adhesión de un material inmunoadsorbente, como la albúmina, a la superficie de las células artificiales. Este principio se ha utilizado para eliminar anticuerpos de grupos sanguíneos del plasma para el trasplante de médula ósea y para el tratamiento de la hipercolesterolemia mediante anticuerpos monoclonales para eliminar las lipoproteínas de baja densidad. La hemoperfusión es especialmente útil en países con una industria manufacturera de hemodiálisis débil, ya que los dispositivos tienden a ser más baratos allí y se utilizan en pacientes con insuficiencia renal.
Células encapsuladas

El método más común de preparación de células artificiales es mediante la encapsulación celular. Las células encapsuladas se logran típicamente mediante la generación de gotitas de tamaño controlado a partir de una suspensión celular líquida que luego se solidifican o gelifican rápidamente para proporcionar estabilidad adicional. La estabilización se puede lograr mediante un cambio de temperatura o mediante la reticulación de materiales. El microambiente que ve una célula cambia tras la encapsulación. Normalmente pasa de estar en una monocapa a estar en suspensión en un armazón de polímero dentro de una membrana polimérica. Un inconveniente de la técnica es que encapsular una célula disminuye su viabilidad y capacidad de proliferar y diferenciarse. Además, después de algún tiempo dentro de la microcápsula, las células forman grupos que inhiben el intercambio de oxígeno y desechos metabólicos, lo que conduce a la apoptosis y la necrosis, lo que limita la eficacia de las células y activa el sistema inmunológico del huésped. Las células artificiales han tenido éxito en el trasplante de varias células, incluidos los islotes de Langerhans para el tratamiento de la diabetes, las células paratiroideas y las células de la corteza suprarrenal.
Hepatocitos encapsulados
La escasez de donantes de órganos hace que las células artificiales sean actores clave en las terapias alternativas para la insuficiencia hepática. El uso de células artificiales para el trasplante de hepatocitos ha demostrado viabilidad y eficacia en la provisión de función hepática en modelos de enfermedad hepática animal y dispositivos de hígado bioartificial. La investigación surgió de experimentos en los que los hepatocitos se adhirieron a la superficie de un microtransportador y evolucionaron hasta convertirse en hepatocitos que están encapsulados en una matriz tridimensional en microgotas de alginato cubiertas por una capa exterior de polilisina. Una ventaja clave de este método de administración es la elusión de la terapia de inmunosupresión durante la duración del tratamiento. Se han propuesto encapsulaciones de hepatocitos para su uso en un hígado bioartificial. El dispositivo consiste en una cámara cilíndrica incrustada con hepatocitos aislados a través de la cual circula el plasma del paciente extracorpóreamente en un tipo de hemoperfusión. Debido a que las microcápsulas tienen una alta relación área de superficie a volumen, proporcionan una gran superficie para la difusión del sustrato y pueden acomodar una gran cantidad de hepatocitos. El tratamiento de ratones con insuficiencia hepática inducida mostró un aumento significativo en la tasa de supervivencia. Los sistemas de hígado artificial todavía están en una etapa temprana de desarrollo, pero muestran potencial para pacientes que esperan un trasplante de órgano o mientras el hígado del propio paciente se regenera lo suficiente para recuperar su función normal. Hasta ahora, los ensayos clínicos que utilizan sistemas de hígado artificial y trasplante de hepatocitos en enfermedades hepáticas terminales han demostrado una mejora de los marcadores de salud, pero aún no han mejorado la supervivencia. La corta longevidad y la agregación de hepatocitos artificiales después del trasplante son los principales obstáculos encontrados. Los hepatocitos coencapsulados con células madre muestran una mayor viabilidad en cultivo y después de la implantación y la implantación de células madre artificiales solas también han demostrado regeneración hepática. Por ello, ha surgido el interés en el uso de células madre para la encapsulación en la medicina regenerativa.
Células bacterianas encapsuladas
Se ha propuesto la ingestión oral de colonias de células bacterianas vivas y actualmente se utiliza en terapias para la modulación de la microflora intestinal, la prevención de enfermedades diarreicas, el tratamiento de infecciones por H. Pylori, inflamaciones atópicas, intolerancia a la lactosa y modulación inmunológica, entre otras. El mecanismo de acción propuesto no se entiende completamente, pero se cree que tiene dos efectos principales. El primero es el efecto nutricional, en el que las bacterias compiten con las bacterias productoras de toxinas. El segundo es el efecto sanitario, que estimula la resistencia a la colonización y estimula la respuesta inmunológica. La administración oral de cultivos bacterianos es a menudo un problema porque son el objetivo del sistema inmunológico y a menudo se destruyen cuando se ingieren por vía oral. Las células artificiales ayudan a abordar estos problemas al proporcionar mimetismo en el cuerpo y una liberación selectiva o a largo plazo, lo que aumenta la viabilidad de las bacterias que llegan al sistema gastrointestinal. Además, la encapsulación de células bacterianas vivas se puede diseñar para permitir la difusión de pequeñas moléculas, incluidos péptidos, en el cuerpo con fines terapéuticos. Las membranas que han demostrado ser exitosas para la administración bacteriana incluyen acetato de celulosa y variantes de alginato. Otros usos que han surgido de la encapsulación de células bacterianas incluyen la protección contra el ataque de M. tuberculosis y la regulación positiva de las células secretoras de Ig del sistema inmunológico. La tecnología está limitada por el riesgo de infecciones sistémicas, actividades metabólicas adversas y el riesgo de transferencia de genes. Sin embargo, el mayor desafío sigue siendo la entrega de suficientes bacterias viables al sitio de interés.
Células de sangre artificiales como portadores de oxígeno
Los transportadores de oxígeno de tamaño nanométrico se utilizan como un tipo de sustitutos de los glóbulos rojos, aunque carecen de otros componentes de los glóbulos rojos. Están compuestos por un polímero sintético o una membrana artificial que rodea la hemoglobina animal, humana o recombinante purificada. En general, la administración de hemoglobina sigue siendo un desafío porque es altamente tóxica cuando se administra sin ninguna modificación. En algunos ensayos clínicos, se han observado efectos vasopresores.
Células de sangre rojas artificiales
El interés de la investigación en el uso de células artificiales para la sangre surgió después del pánico por el SIDA en los años 80. Además de evitar la transmisión potencial de enfermedades, los glóbulos rojos artificiales son deseables porque eliminan los inconvenientes asociados con las transfusiones de sangre alogénica, como la tipificación sanguínea, las reacciones inmunológicas y su corta vida útil de almacenamiento de 42 días. Un sustituto de la hemoglobina se puede almacenar a temperatura ambiente y no bajo refrigeración durante más de un año. Se han hecho intentos para desarrollar un glóbulo rojo funcional completo que comprenda carbónico no solo como transportador de oxígeno sino también las enzimas asociadas con la célula. El primer intento se realizó en 1957 reemplazando la membrana del glóbulo rojo por una membrana polimérica ultradelgada, seguida de una encapsulación a través de una membrana lipídica y, más recientemente, una membrana polimérica biodegradable. Una membrana biológica de glóbulo rojo que incluya lípidos y proteínas asociadas también se puede utilizar para encapsular nanopartículas y aumentar el tiempo de residencia in vivo evitando la captación de macrófagos y la depuración sistémica.
Leucopolímeros artificiales
Un leucopolimerosoma es un polimerosoma diseñado para tener las propiedades adhesivas de un leucocito. Los polimerosomas son vesículas compuestas por una lámina bicapa que puede encapsular muchas moléculas activas, como fármacos o enzimas. Al agregar las propiedades adhesivas de un leucocito a sus membranas, se puede hacer que se desaceleren o rueden a lo largo de las paredes epiteliales dentro del sistema circulatorio de rápido flujo.
Tipos no convencionales de células artificiales
Celda artificial electrónica
El concepto de célula electrónica artificial se ha ampliado en una serie de tres proyectos de la UE coordinados por John McCaskill entre 2004 y 2015.
La Comisión Europea patrocinó el desarrollo del programa Programmable Artificial Cell Evolution (PACE) de 2004 a 2008, cuyo objetivo era sentar las bases para la creación de "entidades autónomas microscópicas autoorganizadas, autorreplicantes y evolutivas construidas a partir de sustancias orgánicas e inorgánicas simples que pueden programarse genéticamente para realizar funciones específicas" para su eventual integración en sistemas de información. El proyecto PACE desarrolló la primera Omega Machine, un sistema de soporte vital microfluídico para células artificiales que podría complementar las funcionalidades químicas faltantes (como propusieron originalmente Norman Packard, Steen Rasmussen, Mark Beadau y John McCaskill). El objetivo final era lograr una célula híbrida evolutiva en un entorno programable complejo a microescala. Las funciones de la Omega Machine podrían entonces eliminarse paso a paso, lo que plantea una serie de desafíos evolutivos solucionables para la química de la célula artificial. El proyecto logró la integración química hasta el nivel de pares de las tres funciones básicas de las células artificiales (un subsistema genético, un sistema de contención y un sistema metabólico), y generó nuevos entornos microfluídicos programables con resolución espacial para la integración de la contención y la amplificación genética. El proyecto condujo a la creación del centro europeo de tecnología viva.
A raíz de esta investigación, en 2007, John McCaskill propuso centrarse en una célula artificial complementada electrónicamente, llamada célula química electrónica. La idea clave era utilizar una matriz masivamente paralela de electrodos acoplados a circuitos electrónicos dedicados localmente, en una película delgada bidimensional, para complementar la funcionalidad química celular emergente. La información electrónica local que define los circuitos de conmutación y detección de electrodos podría servir como un genoma electrónico, complementando la información secuencial molecular en los protocolos emergentes. Una propuesta de investigación tuvo éxito con la Comisión Europea y un equipo internacional de científicos que se superponía parcialmente con el consorcio PACE comenzó a trabajar entre 2008 y 2012 en el proyecto Células químicas electrónicas. El proyecto demostró, entre otras cosas, que el transporte local controlado electrónicamente de secuencias específicas podría utilizarse como un sistema de control espacial artificial para la proliferación genética de futuras células artificiales, y que los procesos centrales del metabolismo podrían ser administrados por matrices de electrodos adecuadamente recubiertos.
La principal limitación de este enfoque, aparte de las dificultades iniciales para dominar la electroquímica y la electrocinética a microescala, es que el sistema electrónico está interconectado como una pieza rígida y no autónoma de hardware macroscópico. En 2011, McCaskill propuso invertir la geometría de la electrónica y la química: en lugar de colocar sustancias químicas en un medio electrónico activo, colocar electrónica autónoma microscópica en un medio químico. Organizó un proyecto para abordar una tercera generación de células artificiales electrónicas a escala de 100 μm que podrían autoensamblarse a partir de dos semiceldas ('lablets') para encerrar un espacio químico interno y funcionar con la ayuda de electrónica activa alimentada por el medio en el que están inmersas. Estas células pueden copiar tanto su contenido electrónico como químico y serán capaces de evolucionar dentro de las limitaciones proporcionadas por sus bloques de construcción microscópicos presintetizados especiales. En septiembre de 2012, se comenzó a trabajar en este proyecto.
Neuronas artificiales
Hay investigación y desarrollo en neuronas físicas artificiales – orgánicas e inorgánicas.
Por ejemplo, algunas neuronas artificiales pueden recibir y liberar dopamina (señales químicas en lugar de señales eléctricas) y comunicarse con músculo de rata natural y células cerebrales, con potencial de uso en BCIs/protesis.
Los medidores biocompatibles de baja potencia pueden permitir la construcción de neuronas artificiales que funcionan a voltajes de potenciales de acción biológica y pueden utilizarse para procesar directamente señales de biosensación, para computación neuromorfónica y/o comunicación directa con neuronas biológicas.
Los circuitos neuromorficos orgánicos hechos de polímeros, recubiertos con un gel rico en iones para permitir que un material lleve una carga eléctrica como neuronas reales, se han incorporado en un robot, lo que le permite aprender sensorimotormente dentro del mundo real, en lugar de mediante simulaciones o virtualmente. Además, las neuronas de araña artificial hechas de materia blanda (polímeros) pueden operar en entornos biológicamente relevantes y permitir la comunicación sinérgica entre los dominios artificiales y biológicos.Jeewanu
Las protocélulas Jeewanu son partículas químicas sintéticas que poseen una estructura similar a la de las células y parecen tener algunas propiedades funcionales de vida. Sintetizadas por primera vez en 1963 a partir de minerales simples y compuestos orgánicos básicos mientras se exponían a la luz solar, todavía se informa que tienen algunas capacidades metabólicas, la presencia de una membrana semipermeable, aminoácidos, fosfolípidos, carbohidratos y moléculas similares al ARN. Sin embargo, la naturaleza y las propiedades de las Jeewanu aún están por esclarecer.
Células de cyborg semiartificiales
Véase también
- Protocell
- Biología sintética
- Vida artificial
- Entrega de drogas dirigida
- Respirocyte
- Chemoton
- Jeewanu
Referencias
- ^ Buddingh' BC, van Hest JC (abril de 2017). "Células artificiales: Compartimientos sintéticos con Funcionalidad y Adaptividad similares a la vida". Accounts of Chemical Research. 50 (4): 769–777. doi:10.1021/acs.accounts.6b00512. PMC 5397886. PMID 28094501.
- ^ Deamer D (julio de 2005). "¿Un paso gigante hacia la vida artificial?". Tendencias en la Biotecnología. 23 (7): 336–338. doi:10.1016/j.tibtech.2005.05.008. PMID 15935500.
- ^ a b c d e f g h i Chang TM (2007). Células artificiales: biotecnología, nanomedicina, medicina regenerativa, sustitutos de sangre, bioencapsulación, terapia celular/tem. Hackensack, N.J.: World Scientific. ISBN 978-981-270-576-1.
- ^ a b c d e f h i j k l Prakash S (2007). Células artificiales, ingeniería celular y terapia. Boca Raton, Fl: Woodhead Publishing Limited. ISBN 978-1-84569-036-6.
- ^ Gebelein CG (1983). Materiales poliméricos y órganos artificiales basados en un simposio patrocinado por la División de Química Orgánica y Plástico en la 185a Reunión de la Sociedad Química Americana. Washington, D.C.: American Chemical Society. ISBN 978-0-8412-1084-4.
- ^ Virchow RL (1858). Die cellularpathologie in ihrer begründung auf fisilogische und pathologische gewebelehre [Patología celular en su justificación de la histología fisiológica y patológica]. Zwanzig Vorlesungen gehalten wahrend der Monate Februar, Marz und April 1858 (in German). Berlín: Verlag von August Hirschwald. p. xv.
- ^ Kamiya K, Takeuchi S (agosto de 2017). "La formación de liposomas verdes hacia la síntesis de células artificiales bien definidas". Journal of Materiales Chemistry B. 5 (30): 5911–5923. doi:10.1039/C7TB01322A. PMID 32264347.
- ^ Litschel T, Schwille P (mayo 2021). "Reconstitución de proteínas dentro de gigantes Unilamellar Vesicles". Examen anual de la biofísica. 50: 525-548. doi:10.1146/annurev-biophys-100620-114132. PMID 33667121. S2CID 232131463.
- ^ Szostak JW, Bartel DP, Luisi PL (enero de 2001). "Synthesizing life". Naturaleza. 409 (6818): 387-390. doi:10.1038/35053176PMID 11201752. S2CID 4429162.
- ^ Pohorille A, Deamer D (marzo de 2002). "Células artificiales: perspectivas de biotecnología". Tendencias en la Biotecnología. 20 (3): 123–128. doi:10.1016/S0167-7799(02)01909-1. hdl:2060/20020043286. PMID 11841864.
- ^ Noireaux V, Maeda YT, Libchaber A (marzo de 2011). "Desarrollo de una célula artificial, desde la autoorganización hasta la computación y auto-reproducción". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 108 (9): 3473–3480. código:2011PNAS..108.3473N. doi:10.1073/pnas.1017075108. PMC 3048108. PMID 21317359.
- ^ Rasmussen S, Chen L, Nilsson M, Abe S (Summer 2003). "Bridging nonliving and living matter". Vida artificial. 9 (3): 269-316. CiteSeerX 10.1.1.101.1606. doi:10.1162/106454603322392479. PMID 14556688. S2CID 6076707.
- ^ Gilbert W (20 de febrero de 1986). "Origin of life: The RNA world". Naturaleza. 319 (6055): 618. Bibcode:1986Natur.319..618G. doi:10.1038/319618a0. S2CID 8026658.
- ^ Bedau M, Church G, Rasmussen S, Caplan A, Benner S, Fussenegger M, et al. (Mayo 2010). "Vida después de la célula sintética". Naturaleza. 465 (7297): 422-424. código:2010Natur.465..422. doi:10.1038/465422a. PMID 20495545. S2CID 27471255.
- ^ a b Parke EC (2009). Beadau MA (ed.). La ética de las protocellas implicaciones morales y sociales de crear vida en el laboratorio ([Online-Ausg.] ed.). Cambridge, Mass.: MIT Prensa. ISBN 978-0-262-51269-5.
- ^ Swetlitz, Ike (28 de julio de 2017). "De los productos químicos a la vida: los científicos tratan de construir células desde cero". Stat. Retrieved 4 de diciembre 2019.
- ^ "Build-a-Cell". Retrieved 4 de diciembre 2019.
- ^ "FabriCell". Retrieved 8 de diciembre 2019.
- ^ "MaxSynBio - Max Planck Research Network in Synthetic Biology". Retrieved 8 de diciembre 2019.
- ^ "BaSyC". Retrieved 8 de diciembre 2019.
- ^ "SynCell EU". Retrieved 8 de diciembre 2019.
- ^ a b c Gibson DG, Glass JI, Lartigue C, Noskov VN, Chuang RY, Algire MA, et al. (Julio 2010). "Creación de una célula bacteriana controlada por un genoma sintetizado químicamente". Ciencia. 329 (5987): 52–56. Código:2010Sci...329...52G. doi:10.1126/ciencia.1190719. PMID 20488990. S2CID 7320517.
- ^ Armstrong R (septiembre de 2014). "Diseñar con protocells: aplicaciones de una nueva plataforma técnica". Vida. 4 (3): 457-490. Bibcode:2014Life....4..457A. doi:10.3390/vida4030457. PMC 4206855. PMID 25370381.
- ^ Breuer M, Earnest TM, Merryman C, Wise KS, Sun L, Lynott MR, et al. (enero 2019). "El metabolismo esencial para una célula mínima". eLife. 8. doi:10.7554/eLife.36842. PMC 6609329. PMID 30657448.
- ^ Sheridan C (septiembre de 2009). "Big dólares de petróleo por algas". Nature Biotechnology. 27 (9): 783. doi:10.1038/nbt090909-783. PMID 19741613. S2CID 205270805.
- ^ EU Directorate-General for Health and Consumers (2016-02-12). Opinión sobre la biología sintética II: metodologías de evaluación de riesgos y aspectos de seguridad. Oficina de Publicaciones. doi:10.2772/63529. ISBN 9789279439162.
- ^ Chang TM (octubre de 1964). "Micápsulas semipermeables". Ciencia. 146 (3643): 524–525. Código Civil:1964Sci...146..524C. doi:10.1126/ciencia.146.3643.524. PMID 14190240. S2CID 40740134.
- ^ a b c Chang TM (1996). "Editorial: perspectivas pasadas, presentes y futuras sobre el 40 aniversario de sustitutos de glóbulos rojos basados en la hemoglobina". Células artificiales Blood Substit Immobil Biotechnol. 24: ixxxvi. NAID 10005526771.
- ^ Palmour RM, Goodyer P, Reade T, Chang TM (septiembre 1989). "Microencapsulado xanthine oxidase como terapia experimental en la enfermedad de Lesch-Nyhan". Lancet. 2 (8664): 687-688. doi:10.1016/s0140-6736(89)90939-2. PMID 2570944. S2CID 39716068.
- ^ Chang TM (1997). Sustitutos de sangre. Basel: Karger. ISBN 978-3-8055-6584-4.
- ^ Pronto-Shiong P, Heintz RE, Merideth N, Yao QX, Yao Z, Zheng T, et al. (abril de 1994). "Independencia de la insulina en un paciente diabético tipo 1 después del trasplante de islote encapsulado". Lancet. 343 (8903): 950–951. doi:10.1016/S0140-6736(94)90067-1. PMID 7909011. S2CID 940319.
- ^ Liu ZC, Chang TM (junio de 2003). "Coencapsulación de hepatocitos y células madre de médula ósea: conversión in vitro de amoníaco y reducción in vivo de bilirubin en ratas de Gunn hiperbilirubemia". The International Journal of Artificial Organs. 26 (6): 491-497. doi:10.1177/039139880302600607. PMID 12894754. S2CID 12447199.
- ^ Aebischer P, Schluep M, Déglon N, Joseph JM, Hirt L, Heyd B, et al. (junio de 1996). "Entrega intratecal de CNTF usando células xenógenas modificadas genéticamente encapsuladas en pacientes de esclerosis lateral amiotrófica". Nature Medicine. 2 (6): 696–699. doi:10.1038/nm0696-696. PMID 8640564. S2CID 8049662.
- ^ Vivier A, Vuillemard JC, Ackermann HW, Poncelet D (1992). "Producción sustitutiva de sangre a escala alta usando un microfluidizador". Biotecnología de biomateriales, células artificiales e inmovilización. 20 (2–4): 377–397. doi:10.3109/10731199209119658. PMID 1391454.
- ^ Jakaria MG, Sorkhdini P, Yang D, Zhou Y, Meenach SA (Febrero 2022). " nanopartículas de membrana celular pulmonar capaces de mejorar la internalización y la translocación en células epiteliales pulmonares". International Journal of Pharmaceutics. 613: 121418. doi:10.1016/j.ijpharm.2021.121418. PMC 8792290. PMID 34954003.
- ^ a b Monck, Carolina; Elani, Yuval; Ceroni, Francesca (2024-07-05). "Células sintéticas programadas genéticamente para síntesis de proteínas termoresponsivas y liberación de carga". Nature Chemical Biology: 1–7. doi:10.1038/s41589-024-01673-7. ISSN 1552-4469.
- ^ Park et al. 1981
- ^ Chang TM (enero de 1971). "Los efectos in vivo de microcapsules semipermeables que contienen L-asparaginasa en linfocitosarcoma 6C3HED". Naturaleza. 229 (5280): 117–118. Bibcode:1971Natur.229..117C. doi:10.1038/229117a0. PMID 4923094. S2CID 4261902.
- ^ Yu B, Chang TM (abril de 2004). "Efectos de la administración oral a largo plazo de microcápsulas poliméricas que contienen tirosinasa en mantener la disminución de los niveles sistémicos de tirosina en ratas". Journal of Pharmaceutical Sciences. 93 (4): 831-837. doi:10.1002/jps.10593. PMID 14999721.
- ^ Meadows GG, Pierson HF, Abdallah RM, Desai PR (agosto de 1982). "Influencia diplomática de tirosina y fenilalanina en la respuesta del melanoma B16 a la quimioterapia del metil ester de carbidopa-levodopa". Cancer Research. 42 (8): 3056–3063. PMID 7093952.
- ^ Chang TM (Febrero de 2004). "La bioencapsulación de células artísticas en dimensiones macro, micro, nano y moleculares: conferencia principal". Células artificiales, sustitutos de sangre y biotecnología. 32 (1): 1–23. doi:10.1081/bio-120028665. PMID 15027798. S2CID 37799530.
- ^ a b Löhr M, Hummel F, Faulmann G, Ringel J, Saller R, Hain J, et al. (mayo de 2002). "Células microencapsuladas, CYP2B1-transfectadas activando ifosfamida en el sitio del tumor: las balas mágicas del siglo XXI". Quimioterapia y Farmacología. 49 (Supl 1): S21–S24. doi:10.1007/s00280-002-0448-0. PMID 12042985. S2CID 10329480.
- ^ Kröger JC, Benz S, Hoffmeyer A, Bago Z, Bergmeister H, Günzburg WH, et al. (1999). "Inculcación intraarterial de células microencapsuladas, activadoras de Ifosfamide en el páncreas de cerdo para el blanco quimioterapéutico". Pancreatology. 3 (1): 55–63. doi:10.1159/000069147. PMID 12649565. S2CID 23711385.
- ^ Carmen IH (abril de 2001). "Muerte en el laboratorio: la política del Gelsinger secuela". Terapia molecular. 3 (4): 425-428. doi:10.1006/mthe.2001.0305. PMID 11319902.
- ^ Raper SE, Chirmule N, Lee FS, Wivel NA, Bagg A, Gao GP, et al. (1 de septiembre de 2003). "Síndrome de respuesta inflamatoria sistémica fetal en un paciente deficiente de ornitina transcarbamylase tras la transferencia genética adenoviral". Genética molecular y metabolismo. 80 (1–2): 148–158. doi:10.1016/j.ymgme.2003.08.016. PMID 14567964.
- ^ Cavazzana-Calvo M, Hacein-Bey S, de Saint Basile G, Gross F, Yvon E, Nusbaum P, et al. (abril de 2000). "Terapia genérica de la enfermedad humana grave combinada de inmunodeficiencia (SCID)-X1". Ciencia. 288 (5466): 669–672. Código:2000Sci...288..669C. doi:10.1126/ciencia.288.5466.669. PMID 10784449.
- ^ Hacein-Bey-Abina S, Von Kalle C, Schmidt M, McCormack MP, Wulffraat N, Leboulch P, et al. (octubre de 2003). "LMO2-asociado clonal Proliferación de células T en dos pacientes después de la terapia de genes para SCID-X1". Ciencia. 302 (5644): 415-419. Código:2003...302..415H. doi:10.1126/ciencia.1088547. PMID 14564000. S2CID 9100335.
- ^ Chang PL, Van Raamsdonk JM, Hortelano G, Barsoum SC, MacDonald NC, Stockley TL (febrero de 1999). "La entrega in vivo de proteínas heterologosas por células recombinantes microencapsuladas". Tendencias en la Biotecnología. 17 (2): 78–83. doi:10.1016/S0167-7799(98)01250-5. PMID 10087608.
- ^ al-Hendy A, Hortelano G, Tannenbaum GS, Chang PL (febrero de 1995). "Corrección del defecto de crecimiento en ratones enanos con mioblastos microencapsulados no autónomos, un enfoque alternativo a la terapia genética somática". Human Gene Terapia. 6 (2): 165–175. doi:10.1089/hum.1995.6.2-165. PMID 7734517.
- ^ Dunea G, Kolff WJ (1965). "Experiencia clínica con el Riñón artificial de carbón de Yatzidis". Transacciones de la American Society for Artificial Internal Organs. 11: 178–182. doi:10.1097/00002480-196504000-00035. PMID 14329080.
- ^ Bensinger WI, Buckner CD, Clift RA (1985). "Inmunoadsorción de sangre total de anti-A o anticuerpos anti-B". Vox Sanguinis. 48 (6): 357–361. doi:10.1111/j.1423-0410.1985.tb00196.x. PMID 3892895. S2CID 12777645.
- ^ Yang L, Cheng Sí. Yan WR, Yu YT (2004). "Extracorpórea sangre entera inmunoadsorción de miastenia autoinmune gravis por celulosa tripptofan adsorbente". Células artificiales, sustitutos de sangre y biotecnología. 32 (4): 519-528. doi:10.1081/bio-200039610. PMID 15974179. S2CID 7269229.
- ^ Chang PL (1994). "Calcium Phosphate-Mediated DNA Transfection". En Wolff JA (ed.). Terapéutica Genética. Boston: Birkhauser. pp. 157–179. doi:10.1007/978-1-4684-6822-9. ISBN 978-1-4684-6822-9.
- ^ Ponce S, Orive G, Gascón AR, Hernández RM, Pedraz JL (abril de 2005). "Microcapsules preparado con diferentes biomateriales para inmovilizar GDNF secretando fibroblastos 3T3". International Journal of Pharmaceutics. 293 (1–2): 1–10. doi:10.1016/j.ijpharm.2004.10.028. PMID 15778039.
- ^ Kizilel S, Garfinkel M, Opara E (diciembre de 2005). "El páncreas bioartificial: progreso y desafíos". Tecnología de la diabetes " Terapéutica. 7 (6): 968–985. doi:10.1089/dia.2005.7.968. PMID 16386103.
- ^ a b Dixit V, Gitnick G (27 de noviembre de 2003). "El hígado bioartificial: el estado del arte". El European Journal of Surgery. Suplemento. 164 (582): 71–76. doi:10.1080/11024159850191481. PMID 10029369.
- ^ Demetriou AA, Whiting JF, Feldman D, Levenson SM, Chowdhury NR, Moscioni AD, et al. (septiembre de 1986). "Reemplazamiento de la función hepática en ratas por trasplante de hepatocitos unidos a microcarrier". Ciencia. 233 (4769): 1190–1192. Bibcode:1986Sci...233.1190D. doi:10.1126/science.2426782. PMID 2426782.
- ^ Sgroi A, Serre-Beinier V, Morel P, Bühler L (febrero de 2009). "¿Qué alternativas clínicas al trasplante de hígado entero? Situación actual de dispositivos artificiales y trasplante de hepatocitos". Trasplante. 87 (4): 457-466. doi:10.1097/TP.0b013e3181963ad3. PMID 19307780.
- ^ Liu ZC, Chang TM (marzo de 2002). "Una mayor viabilidad de los hepatocitos trasplantados cuando los hepatocitos son co-encapsulados con células madre de médula ósea utilizando un método nuevo". Células artificiales, Sustitutos de Sangre e Inmovilización Biotecnología. 30 (2): 99–112. doi:10.1081/bio-120003191. PMID 12027231. S2CID 26667880.
- ^ Pedraz JL, Orive G, eds. (2010). Aplicaciones terapéuticas de microencapsulación celular (Online-Ausg. ed.). Nueva York: Springer Science+Business Media. ISBN 978-1-4419-5785-6.
- ^ Mattila-Sandholm T, Blum S, Collins JK, Crittenden R, De Vos W, Dunne C, et al. (1 de diciembre de 1999). "Probióticos: para demostrar eficacia". Tendencias en Ciencia y Tecnología de la Alimentación. 10 (12): 393–399. doi:10.1016/S0924-2244(00)00029-7.
- ^ Huang JS, Bousvaros A, Lee JW, Diaz A, Davidson EJ (noviembre de 2002). "Eficacia del uso probiótico en diarrea aguda en niños: un metaanálisis". Enfermedades y Ciencias Digestivas. 47 11): 2625–2634. doi:10.1023/A:1020501202369. PMID 12452406. S2CID 207559325.
- ^ Isolauri E, Arvola T, Sütas Y, Moilanen E, Salminen S (noviembre de 2000). "Probióticos en la gestión del eczema atópico". Alergía clínica y experimental. 30 11): 1604-1610. doi:10.1046/j.1365-2222.2000.00943.x. PMID 11069570. S2CID 13524021.
- ^ Lin MY, Yen CL, Chen SH (enero de 1998). "Management of lactose maldigestion by consuming milk containing lactobacilli". Enfermedades y Ciencias Digestivas. 43 (1): 133–137. doi:10.1023/A:1018840507952. PMID 9508514. S2CID 22890925.
- ^ Gill HS (1 de mayo de 1998). "Estimulación del Sistema Inmunitario por las Culturas Lácticas". International Dairy Journal. 8 (5–6): 535–544. doi:10.1016/S0958-6946(98)00074-0.
- ^ Aldwell FE, Tucker IG, de Lisle GW, Buddle BM (enero de 2003). "La entrega oral de Mycobacterium bovis BCG en una formulación lipídica induce resistencia a la tuberculosis pulmonar en ratones". Infección e inmunidad. 71 (1): 101–108. doi:10.1128/IAI.71.1.101-108.2003. PMC 143408. PMID 12496154.
- ^ Park JH, Um JI, Lee BJ, Goh JS, Park SY, Kim WS, Kim PH (septiembre de 2002). "Encapsulado Bifidobacterium bifidum potentiates intestinal IgA production". Inmunología celular. 219 (1): 22–27. doi:10.1016/S0008-8749(02)00579-8. PMID 12473264.
- ^ Kim HW, Greenburg AG (septiembre de 2004). "Líneas de oxígeno artificial como sustitutos de glóbulos rojos: una revisión seleccionada y estado actual". Órganos artificiales. 28 (9): 813–828. doi:10.1111/j.1525-1594.2004.07345.x. PMID 15320945.
- ^ Nelson DJ (1998). "Blood and HemAssistTM (DCLHb): Posiblemente un equipo terapéutico complementario". En Chang TM (ed.). Sustitutos de sangre: principios, métodos, productos y ensayos clínicos. Vol. 2. Basel: Karger. pp. 39–57.
- ^ Burhop KE, Estep TE (2001). "Hemoglobina indujo lesiones miocárdicas". Células artificiales, sustitutos de sangre y biotecnología. 29 (2): 101-106. doi:10.1080/10731190108951271. PMC 3555357.
- ^ "30 aniversario en Investigación Célula Roja Artificial". Células artificiales, sustitutos de sangre y biotecnología. 16 (1–3): 1–9. 1o de enero de 1988. doi:10.3109/10731198809132551.
- ^ Djordjevich L, Miller IF (mayo de 1980). "Eritrocitos sintéticos de hemoglobina encapsulada de lípidos". Hematología experimental. 8 (5): 584–592. PMID 7461058.
- ^ Hu CM, Zhang L, Aryal S, Cheung C, Fang RH, Zhang L (Julio 2011). "Nan nanopartículas poliméricas de cauflaje de membrana eritrocito como plataforma de entrega biomimética". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 108 (27): 10980–10985. Código:2011PNAS..10810980H. doi:10.1073/pnas.1106634108. PMC 3131364. PMID 21690347.
- ^ Hammer DA, Robbins GP, Haun JB, Lin JJ, Qi W, Smith LA, et al. (1 de enero de 2008). "Leuko-polymersomes". Faraday Discussions. 139: 129–41, discusión 213–28, 419–20. Código:2008FaDi..139..129H. doi:10.1039/B717821B. PMC 2714229. PMID 19048993.
- ^ a b c "Revolución de células artificiales programables" (PACE)". Consorcio PACE.
- ^ "Centro europeo para la tecnología viviente". European Center for Living Technology. Archivado desde el original el 14 de septiembre de 2011.
- ^ "Microscale Chemically Reactive Electronic Agents". Ruhr Universität Bochum.
- ^ Kleiner, Kurt (25 de agosto de 2022). "Making chips de computadora actúan más como células cerebrales". Revista Conocida Silencio Reseñas Anuales. doi:10.1146/knowable-082422-1. Retrieved 23 de septiembre 2022.
- ^ Keene, Scott T.; Lubrano, Claudia; Kazemzadeh, Setareh; Melianas, Armantas; Tuchman, Yaakov; Polino, Giuseppina; Scognamiglio, Paola; Cinà, Lucio; Salleo, Alberto; van de Burgt, Yoeri; Santoro, Francesca (septiembre 2020). "Sinapsis biohibrida con plasticidad mediada por neurotransmisor". Material de la naturaleza. 19 (9): 969–973. código:2020NatMa..19..969K. doi:10.1038/s41563-020-0703-y. ISSN 1476-4660. PMID 32541935. S2CID 219691307.
- Comunicado de prensa de la Universidad: "Los investigadores desarrollan sinapsis artificial que funciona con células vivas". Universidad de Stanford via medicalxpress.com. Retrieved 23 de septiembre 2022.
- ^ "La neurona artificial intercambia dopamina con células cerebrales de rata como una verdadera". Nuevo Científico. Retrieved 16 de septiembre 2022.
- ^ Wang, Ting; Wang, Ming; Wang, Jianwu; Yang, Le; Ren, Xueyang; Song, Gang; Chen, Shisheng; Yuan, Yuehui; Liu, Ruiqing; Pan, Liang; Li, Zheng; Leow, Wan Ru; Luo, Yifei; Ji, Shaobo; Cui, Zequn; He, Ke; Zhang, Feilong; Lv, Fengting; Tian, Yuanyuan; Cai, Kaiyu; Yang, Bowen; Niu, Jingyi; Zou, Haochen; Liu, Songrui; Xu, Guoliang; Fan, Xing; Hu, Benhui; Loh, Xian Jun; Wang, Lianhui; Chen, Xiaodong (8 de agosto 20). "Una neurona artificial mediada químicamente". Nature Electronics. 5 (9): 586–595. doi:10.1038/s41928-022-00803-0. hdl:10356/163240. ISSN 2520-1131. S2CID 251464760.
- ^ "Los científicos crean pequeños dispositivos que funcionan como el cerebro humano". The Independent20 de abril de 2020. Archivado desde el original el 24 de abril de 2020. Retrieved 17 de mayo, 2020.
- ^ "Los investigadores revelan electrónica que imitan al cerebro humano en un aprendizaje eficiente". phys.org. Archivado desde el original el 28 de mayo de 2020. Retrieved 17 de mayo, 2020.
- ^ Fu, Tianda; Liu, Xiaomeng; Gao, Hongyan; Ward, Joy E.; Liu, Xiaorong; Yin, Bing; Wang, Zhongrui; Zhuo, Ye; Walker, David J. F.; Joshua Yang, J.; Chen, Jianhan; Lovley, Derek R.; Yao, Jun (20 de abril de 2020). "Memrisadores bio voltaje inspirados". Nature Communications. 11 (1): 1861. Bibcode:2020NatCo..11.1861F. doi:10.1038/s41467-020-15759-y. PMC 7171104. PMID 32313096.
- ^ Bolakhe, Saugat. "Lego Robot con un "Brain" orgánico aprende a navegar un laberinto". Scientific American. Retrieved 1o de febrero 2022.
- ^ Krauhausen, Imke; Koutsouras, Dimitrios A.; Melianas, Armantas; Keene, Scott T.; Lieberth, Katharina; Ledanseur, Hadrien; Sheelamanthula, Rajendar; Giovannitti, Alexander; Torricelli, Fabrizio; Mcculloch, Iain; Blom, Paul W. M.; Salleoide, Alberto "Electrónico neuromorfico orgánico para la integración sensorimotor y el aprendizaje en robótica". Avances científicos. 7 (50): eabl5068. Bibcode:2021SciA....7.5068K doi:10.1126/sciadv.abl5068. hdl:10754/673986. PMC 8664264. PMID 34890232. S2CID 245046482.
- ^ Sarkar, Tanmoy; Lieberth, Katharina; Pavlou, Aristea; Frank, Thomas; Mailaender, Volker; McCulloch, Iain; Blom, Paul W. M.; Torriccelli, Fabrizio; Gkoupidenis, Paschalis (7 de noviembre de 2022). "Una neurona artificial orgánica para la detección neuromorfónica in situ y la biointerfacción". Nature Electronics. 5 (11): 774–783. doi:10.1038/s41928-022-00859-y. hdl:10754/686016. ISSN 2520-1131. S2CID 253413801.
- ^ "Las neuronas artificiales emulan contrapartes biológicas para permitir el funcionamiento sinérgico". Nature Electronics. 5 (11): 721–722. 10 noviembre 2022. doi:10.1038/s41928-022-00862-3. ISSN 2520-1131. S2CID 253469402.
- ^ a b c Grote M (septiembre 2011). "Jeewanu, o las "partículas de la vida". El enfoque de Krishna Bahadur en el siglo XX origen de la investigación de la vida". Journal of Biosciences. 36 (4): 563–570. doi:10.1007/s12038-011-9087-0. PMID 21857103. S2CID 19551399.
- ^ Caren LD, Ponnamperuma C (1967). Una revisión de algunos experimentos sobre la síntesis de 'Jeewanu'. NASA Technical Memorandum X-1439. National Aeronautics and Space Administration. CiteSeerX 10.1.1.691.9322. OCLC 761398715.
- ^ "Engineers Made Themselves Some Cyborg Cells". Mecánica popular. 2023-01-11. Retrieved 2023-01-13.
- ^ "Las bacterias de Cyborg ofrecen fuente de combustible verde a la luz solar". BBC Noticias. 2017-08-22. Retrieved 2023-01-13.
- ^ Peplow, Mark (2005-10-17). "Las células de Cyborg sienten humedad". Naturaleza. doi:10.1038/news051017-3. ISSN 1476-4687.
- ^ Berry, Vikas; Saraf, Ravi F. (2005-10-21). "Assembly of Nanoparticles on Live Bacterium: An Avenue to Fabricate Electronic Devices". Angewandte Chemie International Edition. 44 (41): 6668–6673. doi:10.1002/anie.200501711. ISSN 1433-7851. PMID 16215974. S2CID 15662656.
- ^ "Las bacterias Cyborg superan las plantas al convertir la luz solar en compuestos útiles (video)". American Chemical Society. Retrieved 2023-01-13.
- ^ Sakimoto, Kelsey K.; Wong, Andrew Barnabas; Yang, Peidong (2016-01-01). "Autofotosensibilización de bacterias no fotosintéticas para la producción solar-química". Ciencia. 351 (6268): 74–77. Código:2016...351...74S. doi:10.1126/science.aad3317. ISSN 0036-8075. PMID 26721997. S2CID 206642914.
- ^ Kornienko, Nikolay; Sakimoto, Kelsey K.; Herlihy, David M.; Nguyen, Son C.; Alivisatos, A. Paul; Harris, Harris Charles. B.; Schwartzberg, Adam; Yang, Peidong (2016-10-18). "Elucidación espectroscópica de la transferencia de energía en organismos híbridos inorgánicos-biológicos para la producción solar-química". Actas de la Academia Nacional de Ciencias. 113 (42): 11750–11755. código:2016PNAS..11311750K. doi:10.1073/pnas.1610554113. ISSN 0027-8424. PMC 5081607. PMID 27698140.
- ^ Contreras-Llano, Luis E.; Liu, Yu-Han; Henson, Tanner; Meyer, Conary C.; Baghdasaryan, Ofelya; Khan, Shahid; Lin, Chi-Long; Wang, Aijun; Hu, Che-Ming J.; Tan, Cheemeng (2023-01-11). "Engineering Cyborg Bacteria Through Intracellular Hydrogelation". Advanced Science. 10 (9): 2204175. doi:10.1002/advs.202204175. ISSN 2198-3844. 10037956. PMID 36628538. S2CID 255593443.