Celda de combustible

Una celda de combustible o pila electroquímica es una celda electroquímica que convierte la energía química de un combustible (a menudo hidrógeno) y un agente oxidante (a menudo oxígeno) en electricidad a través de un par de reacciones redox. Las celdas de combustible se diferencian de la mayoría de las baterías en que requieren una fuente continua de combustible y oxígeno (generalmente del aire) para sostener la reacción química, mientras que en una batería la energía química generalmente proviene de los metales y sus iones u óxidos que comúnmente ya están presentes en el batería, excepto en baterías de flujo. Las celdas de combustible pueden producir electricidad continuamente mientras se les suministre combustible y oxígeno.
Las primeras celdas de combustible fueron inventadas por Sir William Grove en 1838. El primer uso comercial de las celdas de combustible se produjo más de un siglo después de la invención de la celda de combustible de hidrógeno-oxígeno por Francis Thomas Bacon en 1932. La celda de combustible alcalina, también conocida como la celda de combustible Bacon en honor a su inventor, se ha utilizado en los programas espaciales de la NASA desde mediados de la década de 1960 para generar energía para satélites y cápsulas espaciales. Desde entonces, las pilas de combustible se han utilizado en muchas otras aplicaciones. Las celdas de combustible se utilizan para energía primaria y de respaldo para edificios comerciales, industriales y residenciales y en áreas remotas o inaccesibles. También se utilizan para impulsar vehículos de pila de combustible, como carretillas elevadoras, automóviles, autobuses, trenes, barcos, motocicletas y submarinos.
Hay muchos tipos de celdas de combustible, pero todas consisten en un ánodo, un cátodo y un electrolito que permite que los iones, a menudo iones de hidrógeno cargados positivamente (protones), se muevan entre los dos lados de la celda de combustible. En el ánodo, un catalizador hace que el combustible experimente reacciones de oxidación que generan iones (a menudo iones de hidrógeno con carga positiva) y electrones. Los iones se mueven del ánodo al cátodo a través del electrolito. Al mismo tiempo, los electrones fluyen del ánodo al cátodo a través de un circuito externo, produciendo electricidad de corriente continua. En el cátodo, otro catalizador hace que iones, electrones y oxígeno reaccionen, formando agua y posiblemente otros productos. Las pilas de combustible se clasifican por el tipo de electrolito que utilizan y por la diferencia en el tiempo de arranque que va desde 1 segundo para las pilas de combustible de membrana de intercambio de protones (pilas de combustible PEM, o PEMFC) a 10 minutos para celdas de combustible de óxido sólido (SOFC). Una tecnología relacionada son las baterías de flujo, en las que el combustible se puede regenerar mediante recarga. Las celdas de combustible individuales producen potenciales eléctricos relativamente pequeños, alrededor de 0,7 voltios, por lo que las celdas se "apilan" o se colocan en serie para crear suficiente voltaje para cumplir con los requisitos de una aplicación.Además de electricidad, las celdas de combustible producen agua, calor y, dependiendo de la fuente de combustible, cantidades muy pequeñas de dióxido de nitrógeno y otras emisiones. La eficiencia energética de una pila de combustible está generalmente entre el 40 y el 60 %; sin embargo, si el calor residual se captura en un esquema de cogeneración, se pueden obtener eficiencias de hasta el 85%.
Historia
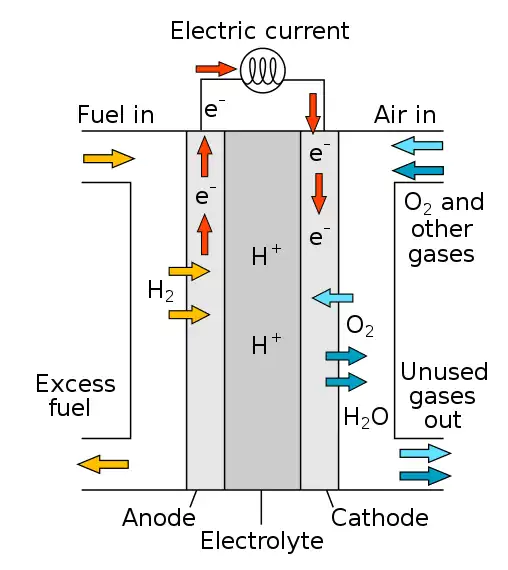
Las primeras referencias a las pilas de combustible de hidrógeno aparecieron en 1838. En una carta fechada en octubre de 1838 pero publicada en la edición de diciembre de 1838 de The London and Edinburgh Philosophical Magazine and Journal of Science, el físico y abogado galés Sir William Grove escribió sobre el desarrollo de su primera celdas de combustible crudo. Usó una combinación de láminas de hierro, cobre y porcelana, y una solución de sulfato de cobre y ácido diluido. En una carta a la misma publicación escrita en diciembre de 1838 pero publicada en junio de 1839, el físico alemán Christian Friedrich Schönbein habló sobre la primera celda de combustible crudo que había inventado. Su carta discutía la corriente generada a partir de hidrógeno y oxígeno disueltos en agua.Grove luego esbozó su diseño, en 1842, en la misma revista. La pila de combustible que fabricó utilizó materiales similares a los de la pila de combustible de ácido fosfórico actual.
En 1932, Francis Thomas Bacon inventó una celda de combustible que obtenía energía del hidrógeno y el oxígeno. Esto fue utilizado por la NASA para encender luces, aire acondicionado y comunicaciones.
Los británicos que impulsaron los alunizajes, Archivos de la BBC.
En 1932, el ingeniero inglés Francis Thomas Bacon desarrolló con éxito una celda de combustible estacionaria de 5 kW. La celda de combustible alcalina (AFC), también conocida como celda de combustible Bacon en honor a su inventor, es una de las tecnologías de celdas de combustible más desarrolladas, que la NASA ha utilizado desde mediados de la década de 1960.
En 1955, W. Thomas Grubb, un químico que trabajaba para General Electric Company (GE), modificó aún más el diseño original de la pila de combustible utilizando una membrana de intercambio iónico de poliestireno sulfonado como electrolito. Tres años más tarde, otro químico de GE, Leonard Niedrach, ideó una forma de depositar platino en la membrana, que sirvió como catalizador para las reacciones necesarias de oxidación de hidrógeno y reducción de oxígeno. Esto se conoció como la "pila de combustible Grubb-Niedrach".GE pasó a desarrollar esta tecnología con la NASA y McDonnell Aircraft, lo que llevó a su uso durante el Proyecto Gemini. Este fue el primer uso comercial de una celda de combustible. En 1959, un equipo dirigido por Harry Ihrig construyó un tractor de pila de combustible de 15 kW para Allis-Chalmers, que se mostró en ferias estatales en todo Estados Unidos. Este sistema utilizaba hidróxido de potasio como electrolito e hidrógeno y oxígeno comprimidos como reactivos. Más tarde, en 1959, Bacon y sus colegas demostraron una unidad práctica de cinco kilovatios capaz de alimentar una máquina de soldar. En la década de 1960, Pratt & Whitney autorizó las patentes estadounidenses de Bacon para su uso en el programa espacial estadounidense para suministrar electricidad y agua potable (el hidrógeno y el oxígeno están fácilmente disponibles en los tanques de las naves espaciales). En 1991, Roger Billings desarrolló el primer automóvil con pila de combustible de hidrógeno.
UTC Power fue la primera empresa en fabricar y comercializar un gran sistema estacionario de celdas de combustible para su uso como planta de cogeneración de energía en hospitales, universidades y grandes edificios de oficinas.
En reconocimiento a la industria de las pilas de combustible y al papel de Estados Unidos en el desarrollo de las pilas de combustible, el Senado de los EE. UU. reconoció el 8 de octubre de 2015 como el Día Nacional del Hidrógeno y las Pilas de Combustible, al aprobar la S. RES 217. La fecha se eligió en reconocimiento al peso atómico del hidrógeno (1,008).
Tipos de celdas de combustible; diseño
Las celdas de combustible vienen en muchas variedades; sin embargo, todos funcionan de la misma manera general. Están formados por tres segmentos adyacentes: el ánodo, el electrolito y el cátodo. Dos reacciones químicas ocurren en las interfaces de los tres segmentos diferentes. El resultado neto de las dos reacciones es que se consume combustible, se crea agua o dióxido de carbono y se crea una corriente eléctrica, que puede usarse para alimentar dispositivos eléctricos, normalmente denominados carga.
En el ánodo, un catalizador oxida el combustible, normalmente hidrógeno, convirtiendo el combustible en un ion con carga positiva y un electrón con carga negativa. El electrolito es una sustancia diseñada específicamente para que los iones puedan atravesarlo, pero los electrones no. Los electrones liberados viajan a través de un cable creando la corriente eléctrica. Los iones viajan a través del electrolito hasta el cátodo. Una vez que llegan al cátodo, los iones se reúnen con los electrones y los dos reaccionan con un tercer químico, generalmente oxígeno, para crear agua o dióxido de carbono.
Las características de diseño en una celda de combustible incluyen:
- La sustancia electrolítica, que normalmente define el tipo de celda de combustible, puede estar hecha de varias sustancias como hidróxido de potasio, carbonatos de sal y ácido fosfórico.
- El combustible que se utiliza. El combustible más común es el hidrógeno.
- El catalizador del ánodo, generalmente polvo fino de platino, descompone el combustible en electrones e iones.
- El catalizador del cátodo, a menudo níquel, convierte los iones en productos químicos de desecho, siendo el agua el tipo de desecho más común.
- Capas de difusión de gas diseñadas para resistir la oxidación.
Una celda de combustible típica produce un voltaje de 0,6 a 0,7 V a plena carga nominal. El voltaje disminuye a medida que aumenta la corriente, debido a varios factores:
- Pérdida de activación
- Pérdida óhmica (caída de voltaje debido a la resistencia de los componentes e interconexiones de la celda)
- Pérdida de transporte de masa (agotamiento de los reactivos en los sitios del catalizador bajo altas cargas, lo que provoca una rápida pérdida de voltaje).
Para entregar la cantidad deseada de energía, las celdas de combustible se pueden combinar en serie para generar un voltaje más alto y en paralelo para permitir que se suministre una corriente más alta. Tal diseño se llama pila de celdas de combustible. El área de la superficie de la celda también se puede aumentar para permitir una mayor corriente de cada celda.
Pilas de combustible de membrana de intercambio de protones
En el diseño arquetípico de celda de combustible de membrana de intercambio de protones de óxido de hidrógeno (PEMFC), una membrana de polímero conductor de protones (típicamente nafion) contiene la solución de electrolito que separa los lados del ánodo y el cátodo. Esto se denominó celda de combustible de electrolito de polímero sólido (SPEFC) a principios de la década de 1970, antes de que se entendiera bien el mecanismo de intercambio de protones. (Observe que los sinónimos membrana electrolítica de polímero y mecanismo de intercambio de protones dan como resultado el mismo acrónimo).
En el lado del ánodo, el hidrógeno se difunde al catalizador del ánodo donde luego se disocia en protones y electrones. Estos protones a menudo reaccionan con los oxidantes, lo que hace que se conviertan en lo que comúnmente se conoce como membranas de protones con múltiples facilitadores. Los protones se conducen a través de la membrana hasta el cátodo, pero los electrones se ven obligados a viajar en un circuito externo (suministrando energía) porque la membrana es eléctricamente aislante. En el catalizador del cátodo, las moléculas de oxígeno reaccionan con los electrones (que han viajado por el circuito externo) y los protones para formar agua.
Además de este tipo de hidrógeno puro, existen combustibles de hidrocarburos para celdas de combustible, que incluyen diesel, metanol (ver: celdas de combustible de metanol directo y celdas de combustible de metanol indirecto) e hidruros químicos. Los productos de desecho con este tipo de combustible son dióxido de carbono y agua. Cuando se usa hidrógeno, el CO 2 se libera cuando el metano del gas natural se combina con vapor, en un proceso llamado reformado de metano con vapor, para producir hidrógeno. Esto puede tener lugar en una ubicación diferente a la celda de combustible, lo que podría permitir que la celda de combustible de hidrógeno se use en interiores, por ejemplo, en montacargas.
Los diferentes componentes de un PEMFC son
- placas bipolares,
- electrodos,
- Catalizador,
- membrana, y
- el hardware necesario como colectores de corriente y juntas.
Los materiales utilizados para las diferentes partes de las celdas de combustible difieren según el tipo. Las placas bipolares pueden estar hechas de diferentes tipos de materiales, como metal, metal revestido, grafito, grafito flexible, compuesto C-C, compuestos de polímero de carbono, etc. El conjunto de electrodos de membrana (MEA) se conoce como el corazón de el PEMFC y generalmente está hecho de una membrana de intercambio de protones intercalada entre dos papeles de carbón recubiertos con catalizador. El platino y/o un tipo similar de metales nobles se utilizan normalmente como catalizador para PEMFC, y estos pueden estar contaminados con monóxido de carbono, lo que requiere un combustible de hidrógeno relativamente puro. El electrolito podría ser una membrana de polímero.
Problemas de diseño de celdas de combustible de membrana de intercambio de protones
CostoEn 2013, el Departamento de Energía estimó que se podrían lograr costos del sistema de celdas de combustible para automóviles de 80 kW de USD 67 por kilovatio, asumiendo una producción en volumen de 100 000 unidades automotrices por año y USD 55 por kilovatio, asumiendo una producción en volumen de 500,000 unidades. por año. Muchas empresas están trabajando en técnicas para reducir los costos de varias maneras, incluida la reducción de la cantidad de platino necesaria en cada celda individual. Ballard Power Systems ha experimentado con un catalizador mejorado con seda de carbono, que permite una reducción del 30 % (1,0–0,7 mg/cm) en el uso de platino sin reducción del rendimiento. La Universidad de Monash, Melbourne, utiliza PEDOT como cátodo. Un estudio publicado en 2011documentó el primer electrocatalizador sin metal utilizando nanotubos de carbono dopados relativamente económicos, que cuestan menos del 1% del costo del platino y tienen un rendimiento igual o superior. Un artículo publicado recientemente demostró cómo cambian las cargas ambientales cuando se utilizan nanotubos de carbono como sustrato de carbono para el platino.Gestión del agua y el aire (en PEMFC)En este tipo de celda de combustible, la membrana debe hidratarse, lo que requiere que el agua se evapore exactamente a la misma velocidad que se produce. Si el agua se evapora demasiado rápido, la membrana se seca, la resistencia a través de ella aumenta y eventualmente se agrietará, creando un "cortocircuito" de gas donde el hidrógeno y el oxígeno se combinan directamente, generando calor que dañará la celda de combustible. Si el agua se evapora demasiado lentamente, los electrodos se inundarán, evitando que los reactivos lleguen al catalizador y deteniendo la reacción. Se están desarrollando métodos para gestionar el agua en las células, como bombas electroosmóticas centradas en el control del flujo. Al igual que en un motor de combustión, es necesaria una proporción constante entre el reactivo y el oxígeno para mantener la celda de combustible funcionando de manera eficiente.Gestión de la temperaturaSe debe mantener la misma temperatura en toda la celda para evitar la destrucción de la celda por carga térmica. Esto es particularmente desafiante ya que la reacción 2H 2 + O 2 → 2H 2 O es altamente exotérmica, por lo que se genera una gran cantidad de calor dentro de la celda de combustible.Durabilidad, vida útil y requerimientos especiales para algún tipo de celdasLas aplicaciones de celdas de combustible estacionarias generalmente requieren más de 40 000 horas de operación confiable a una temperatura de -35 °C a 40 °C (-31 °F a 104 °F), mientras que las celdas de combustible automotrices requieren una vida útil de 5000 horas (el equivalente a 240.000 km (150.000 mi)) bajo temperaturas extremas. La vida útil actual es de 2500 horas (alrededor de 75 000 millas). Los motores automotrices también deben poder arrancar de manera confiable a -30 °C (-22 °F) y tener una alta relación potencia-volumen (típicamente 2,5 kW/L).Tolerancia limitada al monóxido de carbono de algunos cátodos (no PEDOT).
Pila de combustible de ácido fosfórico
Las celdas de combustible de ácido fosfórico (PAFC) fueron diseñadas e introducidas por primera vez en 1961 por GV Elmore y HA Tanner. En estas celdas, el ácido fosfórico se utiliza como electrolito no conductor para pasar iones de hidrógeno positivos del ánodo al cátodo. Estas celdas comúnmente trabajan en temperaturas de 150 a 200 grados centígrados. Esta alta temperatura causará pérdida de calor y energía si el calor no se elimina y utiliza correctamente. Este calor se puede aprovechar para producir vapor para sistemas de aire acondicionado o cualquier otro sistema que consuma energía térmica. El uso de este calor en la cogeneración puede mejorar la eficiencia de las celdas de combustible de ácido fosfórico de un 40 a un 50 % a aproximadamente un 80 %.El ácido fosfórico, el electrolito utilizado en los PAFC, es un ácido líquido no conductor que obliga a los electrones a viajar del ánodo al cátodo a través de un circuito eléctrico externo. Dado que la tasa de producción de iones de hidrógeno en el ánodo es pequeña, se utiliza platino como catalizador para aumentar esta tasa de ionización. Una desventaja clave de estas celdas es el uso de un electrolito ácido. Esto aumenta la corrosión u oxidación de los componentes expuestos al ácido fosfórico.
Pila de combustible de ácido sólido
Las pilas de combustible de ácido sólido (SAFC) se caracterizan por el uso de un material ácido sólido como electrolito. A bajas temperaturas, los ácidos sólidos tienen una estructura molecular ordenada como la mayoría de las sales. A temperaturas más cálidas (entre 140 y 150 °C para CsHSO 4), algunos ácidos sólidos experimentan una transición de fase para convertirse en estructuras "superprotónicas" altamente desordenadas, lo que aumenta la conductividad en varios órdenes de magnitud. Los primeros SAFC de prueba de concepto se desarrollaron en 2000 utilizando sulfato de hidrógeno de cesio (CsHSO 4). Los sistemas SAFC actuales utilizan fosfato de dihidrógeno de cesio (CsH 2 PO 4) y han demostrado una vida útil de miles de horas.
Celda de combustible alcalina
La celda de combustible alcalina (AFC) o celda de combustible de hidrógeno y oxígeno fue diseñada y demostrada públicamente por primera vez por Francis Thomas Bacon en 1959. Se utilizó como fuente principal de energía eléctrica en el programa espacial Apolo. La celda consta de dos electrodos de carbono poroso impregnados con un catalizador adecuado como Pt, Ag, CoO, etc. El espacio entre los dos electrodos se llena con una solución concentrada de KOH o NaOH que sirve como electrolito. El gas H 2 y el gas O 2 se burbujean en el electrolito a través de los electrodos de carbón poroso. Por lo tanto, la reacción general implica la combinación de hidrógeno gaseoso y oxígeno gaseoso para formar agua. La celda funciona continuamente hasta que se agota el suministro de reactivo. Este tipo de celda opera eficientemente en el rango de temperatura 343–413 K y proporciona un potencial de aproximadamente 0,9 V. La celda de combustible de membrana de intercambio de aniones alcalinos (AAEMFC) es un tipo de AFC que emplea un electrolito de polímero sólido en lugar de hidróxido de potasio (KOH) acuoso y es superior al AFC acuoso.
Pilas de combustible de alta temperatura
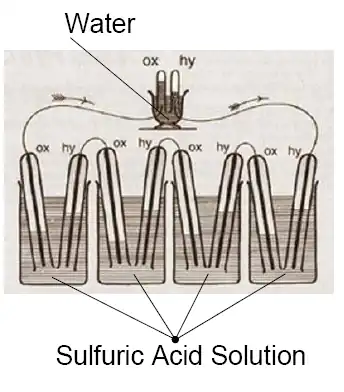
Pila de combustible de óxido sólido
Las celdas de combustible de óxido sólido (SOFC) utilizan un material sólido, más comúnmente un material cerámico llamado zirconio estabilizado con itria (YSZ), como electrolito. Debido a que las SOFC están hechas completamente de materiales sólidos, no se limitan a la configuración plana de otros tipos de celdas de combustible y, a menudo, se diseñan como tubos laminados. Requieren altas temperaturas de funcionamiento (800–1000 °C) y pueden funcionar con una variedad de combustibles, incluido el gas natural.
Las SOFC son únicas ya que en ellas, los iones de oxígeno cargados negativamente viajan desde el cátodo (lado positivo de la celda de combustible) al ánodo (lado negativo de la celda de combustible) en lugar de los iones de hidrógeno cargados positivamente que viajan del ánodo al cátodo, como es el caso en todos los demás tipos de celdas de combustible. El gas oxígeno se alimenta a través del cátodo, donde absorbe electrones para crear iones de oxígeno. Los iones de oxígeno luego viajan a través del electrolito para reaccionar con gas hidrógeno en el ánodo. La reacción en el ánodo produce electricidad y agua como subproductos. El dióxido de carbono también puede ser un subproducto según el combustible, pero las emisiones de carbono de un sistema SOFC son menores que las de una planta de combustión de combustibles fósiles. Las reacciones químicas para el sistema SOFC se pueden expresar de la siguiente manera:Reacción del ánodo: 2H 2 + 2O → 2H 2 O + 4eReacción del cátodo: O 2 + 4e → 2OReacción total de la celda: 2H 2 + O 2 → 2H 2 O
Los sistemas SOFC pueden funcionar con combustibles que no sean gas hidrógeno puro. Sin embargo, dado que el hidrógeno es necesario para las reacciones enumeradas anteriormente, el combustible seleccionado debe contener átomos de hidrógeno. Para que la celda de combustible funcione, el combustible debe convertirse en gas hidrógeno puro. Las SOFC son capaces de reformar internamente hidrocarburos ligeros como el metano (gas natural), el propano y el butano. Estas celdas de combustible se encuentran en una etapa temprana de desarrollo.
Existen desafíos en los sistemas SOFC debido a sus altas temperaturas de funcionamiento. Uno de esos desafíos es la posibilidad de que se acumule polvo de carbono en el ánodo, lo que ralentiza el proceso de reformado interno. La investigación para abordar este problema de "coquización de carbono" en la Universidad de Pensilvania ha demostrado que el uso de cermet a base de cobre (materiales resistentes al calor hechos de cerámica y metal) puede reducir la coquización y la pérdida de rendimiento.Otra desventaja de los sistemas SOFC es el lento tiempo de inicio, lo que hace que las SOFC sean menos útiles para las aplicaciones móviles. A pesar de estas desventajas, una temperatura de operación alta brinda una ventaja al eliminar la necesidad de un catalizador de metal precioso como el platino, lo que reduce el costo. Además, el calor residual de los sistemas SOFC se puede capturar y reutilizar, lo que aumenta la eficiencia general teórica hasta un 80-85 %.
La alta temperatura de funcionamiento se debe en gran medida a las propiedades físicas del electrolito YSZ. A medida que disminuye la temperatura, también lo hace la conductividad iónica de YSZ. Por tanto, para obtener un rendimiento óptimo de la pila de combustible, se requiere una alta temperatura de funcionamiento. Según su sitio web, Ceres Power, un fabricante de pilas de combustible SOFC del Reino Unido, ha desarrollado un método para reducir la temperatura de funcionamiento de su sistema SOFC a 500–600 grados Celsius. Reemplazaron el electrolito YSZ de uso común con un electrolito CGO (óxido de cerio y gadolinio). La temperatura de operación más baja les permite usar acero inoxidable en lugar de cerámica como sustrato de la celda, lo que reduce el costo y el tiempo de puesta en marcha del sistema.
Celda de combustible de carbonato fundido
Las celdas de combustible de carbonato fundido (MCFC) requieren una temperatura de funcionamiento alta, 650 °C (1200 °F), similar a las SOFC. Las MCFC usan sal de carbonato de litio y potasio como electrolito, y esta sal se licua a altas temperaturas, lo que permite el movimiento de carga dentro de la celda, en este caso, iones de carbonato negativos.
Al igual que las SOFC, las MCFC son capaces de convertir el combustible fósil en un gas rico en hidrógeno en el ánodo, lo que elimina la necesidad de producir hidrógeno externamente. El proceso de reforma genera emisiones de CO 2. Los combustibles compatibles con MCFC incluyen gas natural, biogás y gas producido a partir del carbón. El hidrógeno del gas reacciona con los iones de carbonato del electrolito para producir agua, dióxido de carbono, electrones y pequeñas cantidades de otras sustancias químicas. Los electrones viajan a través de un circuito externo creando electricidad y regresan al cátodo. Allí, el oxígeno del aire y el dióxido de carbono reciclado del ánodo reaccionan con los electrones para formar iones de carbonato que reponen el electrolito, completando el circuito. Las reacciones químicas para un sistema MCFC se pueden expresar de la siguiente manera:Reacción del ánodo: CO 3 + H 2 → H 2 O + CO 2 + 2eReacción del cátodo: CO 2 + ½O 2 + 2e → CO 3Reacción total de la celda: H 2 + ½O 2 → H 2 O
Al igual que con las SOFC, las desventajas de las MCFC incluyen tiempos de inicio lentos debido a su alta temperatura de funcionamiento. Esto hace que los sistemas MCFC no sean adecuados para aplicaciones móviles, y esta tecnología probablemente se utilizará para fines de celdas de combustible estacionarias. El principal desafío de la tecnología MCFC es la corta vida útil de las células. El electrolito de carbonato y alta temperatura conduce a la corrosión del ánodo y el cátodo. Estos factores aceleran la degradación de los componentes MCFC, disminuyendo la durabilidad y la vida útil de la celda. Los investigadores están abordando este problema explorando materiales resistentes a la corrosión para los componentes, así como diseños de celdas de combustible que puedan aumentar la vida útil de las celdas sin disminuir el rendimiento.
Las MCFC tienen varias ventajas sobre otras tecnologías de celdas de combustible, incluida su resistencia a las impurezas. No son propensos a la "coquización de carbono", que se refiere a la acumulación de carbono en el ánodo que da como resultado un rendimiento reducido al ralentizar el proceso de reformado interno del combustible. Por lo tanto, los combustibles ricos en carbono, como los gases derivados del carbón, son compatibles con el sistema. El Departamento de Energía de los Estados Unidos afirma que el carbón, en sí mismo, podría incluso ser una opción de combustible en el futuro, suponiendo que el sistema pueda hacerse resistente a las impurezas como el azufre y las partículas que resultan de convertir el carbón en hidrógeno.Los MCFC también tienen eficiencias relativamente altas. Pueden alcanzar una eficiencia de combustible a electricidad del 50%, considerablemente más alta que la eficiencia del 37-42% de una planta de celdas de combustible de ácido fosfórico. Las eficiencias pueden llegar al 65 % cuando la celda de combustible se combina con una turbina, y al 85 % si el calor se captura y utiliza en un sistema combinado de calor y energía (CHP).
FuelCell Energy, un fabricante de celdas de combustible con sede en Connecticut, desarrolla y vende celdas de combustible MCFC. La compañía dice que sus productos MCFC van desde sistemas de 300 kW a 2,8 MW que logran una eficiencia eléctrica del 47 % y pueden utilizar la tecnología CHP para obtener eficiencias generales más altas. Un producto, el DFC-ERG, se combina con una turbina de gas y, según la empresa, alcanza una eficiencia eléctrica del 65%.
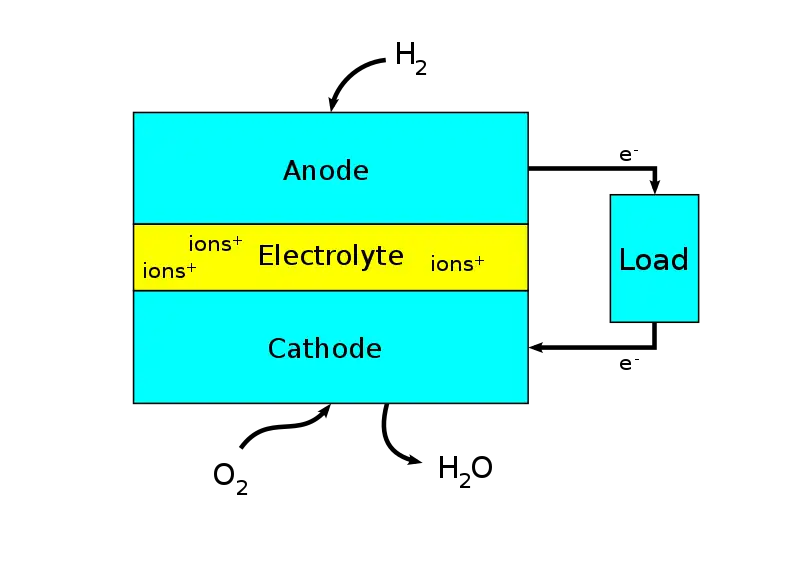
Celda de combustible de almacenamiento eléctrico
La celda de combustible de almacenamiento eléctrico es una batería convencional que se carga mediante la entrada de energía eléctrica, utilizando el efecto electroquímico convencional. Sin embargo, la batería incluye además entradas de hidrógeno (y oxígeno) para cargar alternativamente la batería químicamente.
Comparación de tipos de pilas de combustible
| nombre de la pila de combustible | Electrólito | Potencia cualificada (W) | Temperatura de trabajo (°C) | Eficiencia | Estado | Costo (USD/W) | |
|---|---|---|---|---|---|---|---|
| Celúla | Sistema | ||||||
| Pila de combustible de hidruro metálico | Solución alcalina acuosa | > −20(50 % P pico a 0 °C) | Comercial / Investigación | ||||
| Pila de combustible electrogalvánica | Solución alcalina acuosa | < 40 | Comercial / Investigación | ||||
| Celda de combustible de ácido fórmico directo (DFAFC) | Membrana polimérica (ionómero) | < 50W | < 40 | Comercial / Investigación | |||
| Batería de zinc-aire | Solución alcalina acuosa | < 40 | Producción en masa | ||||
| pila de combustible microbiana | Membrana polimérica o ácido húmico | < 40 | Investigar | ||||
| Celda de combustible microbiana de flujo ascendente (UMFC) | < 40 | Investigar | |||||
| Celda de combustible regenerativa | Membrana polimérica (ionómero) | < 50 | Comercial / Investigación | ||||
| Celda de combustible de borohidruro directo | Solución alcalina acuosa | 70 | Comercial | ||||
| Celda de combustible alcalina | Solución alcalina acuosa | 10–200 kilovatios | < 80 | 60–70% | 62% | Comercial / Investigación | |
| Celda de combustible de metanol directo | Membrana polimérica (ionómero) | 100 mW – 1 kW | 90–120 | 20-30% | 10-25% | Comercial / Investigación | 125 |
| Celda de combustible de metanol reformada | Membrana polimérica (ionómero) | 5 W – 100 kW | 250–300 (reformador)125–200 (PBI) | 50–60% | 25–40% | Comercial / Investigación | |
| Celda de combustible de etanol directo | Membrana polimérica (ionómero) | < 140 mW/cm² | > 25? 90–120 | Investigar | |||
| Celda de combustible de membrana de intercambio de protones | Membrana polimérica (ionómero) | 1 W – 500 kW | 50–100 (Nación)120–200 (PBI) | 50–70% | 30–50% | Comercial / Investigación | 50–100 |
| Celda de combustible redox (RFC) | Electrolitos líquidos con lanzadera redox y membrana polimérica (ionómero) | 1kW – 10MW | Investigar | ||||
| Pila de combustible de ácido fosfórico | Ácido fosfórico fundido (H 3 PO 4) | < 10 megavatios | 150–200 | 55% | 40%Cogeneración: 90% | Comercial / Investigación | 4.00–4.50 |
| Pila de combustible de ácido sólido | Sal de oxianión conductora de hidrógeno (ácido sólido) | 10 W – 1 kW | 200–300 | 55–60% | 40-45% | Comercial / Investigación | |
| Celda de combustible de carbonato fundido | Carbonato alcalino fundido | 100 megavatios | 600–650 | 55% | 45–55% | Comercial / Investigación | |
| Pila de combustible de óxido sólido tubular (TSOFC) | Óxido cerámico conductor de O | < 100 megavatios | 850–1100 | 60–65% | 55–60% | Comercial / Investigación | |
| Pila de combustible de cerámica protónica | Óxido cerámico conductor de hidrógeno | 700 | Investigar | ||||
| Pila de combustible de carbono directo | Varios diferentes | 700–850 | 80% | 70% | Comercial / Investigación | ||
| Celda de combustible de óxido sólido planar | Óxido cerámico conductor de O | < 100 megavatios | 500–1100 | 60–65% | 55–60% | Comercial / Investigación | |
| Células de biocombustible enzimáticas | Cualquiera que no desnaturalice la enzima. | < 40 | Investigar | ||||
| Celda de combustible de magnesio-aire | Agua salada | −20 a 55 | 90% | Comercial / Investigación |
Glosario de términos en la tabla:ÁnodoEl electrodo en el que tiene lugar la oxidación (pérdida de electrones). Para las celdas de combustible y otras celdas galvánicas, el ánodo es el terminal negativo; para las celdas electrolíticas (donde ocurre la electrólisis), el ánodo es el terminal positivo.Solución acuosaDe, relativo a, o parecido al aguaHecho de, con o por agua.CatalizadorSustancia química que aumenta la velocidad de una reacción sin consumirse; después de la reacción, puede recuperarse potencialmente de la mezcla de reacción y no cambia químicamente. El catalizador reduce la energía de activación requerida, lo que permite que la reacción avance más rápidamente oa una temperatura más baja. En una celda de combustible, el catalizador facilita la reacción de oxígeno e hidrógeno. Por lo general, está hecho de polvo de platino recubierto muy finamente sobre papel carbón o tela. El catalizador es áspero y poroso, por lo que la superficie máxima del platino puede estar expuesta al hidrógeno o al oxígeno. El lado recubierto de platino del catalizador mira hacia la membrana en la celda de combustible.CátodoEl electrodo en el que se produce la reducción (una ganancia de electrones). Para celdas de combustible y otras celdas galvánicas, el cátodo es el terminal positivo; para las celdas electrolíticas (donde ocurre la electrólisis), el cátodo es el terminal negativo.ElectrólitoSustancia que conduce iones cargados de un electrodo al otro en una celda de combustible, batería o electrolizador.Pila de celdas de combustiblePilas de combustible individuales conectadas en serie. Las celdas de combustible se apilan para aumentar el voltaje.Matrizalgo dentro o a partir del cual otra cosa se origina, desarrolla o toma forma.MembranaLa capa de separación en una celda de combustible que actúa como electrolito (un intercambiador de iones), así como también como una película de barrera que separa los gases en los compartimientos de ánodo y cátodo de la celda de combustible.Celda de combustible de carbonato fundido (MCFC)Un tipo de celda de combustible que contiene un electrolito de carbonato fundido. Los iones de carbonato (CO 3) se transportan del cátodo al ánodo. Las temperaturas de funcionamiento suelen rondar los 650 °C.Pila de combustible de ácido fosfórico (PAFC)Tipo de pila de combustible en la que el electrolito consiste en ácido fosfórico concentrado (H 3 PO 4). Los protones (H+) se transportan del ánodo al cátodo. El rango de temperatura de funcionamiento es generalmente de 160 a 220 °C.Celda de combustible de membrana de intercambio de protones (PEM)Una pila de combustible que incorpora una membrana de polímero sólido utilizada como electrolito. Los protones (H+) se transportan del ánodo al cátodo. El rango de temperatura de funcionamiento es generalmente de 60 a 100 °C para celdas de combustible de membrana de intercambio de protones de baja temperatura (LT-PEMFC). La celda de combustible PEM con una temperatura de funcionamiento de 120-200 °C se denomina celda de combustible de membrana de intercambio de protones de alta temperatura (HT-PEMFC).Pila de combustible de óxido sólido (SOFC)Tipo de celda de combustible en la que el electrolito es un óxido de metal sólido no poroso, normalmente óxido de circonio (ZrO 2) tratado con Y 2 O 3, y el O se transporta desde el cátodo al ánodo. Cualquier CO en el gas de reformado se oxida a CO 2 en el ánodo. Las temperaturas de funcionamiento suelen oscilar entre 800 y 1000 °C.SoluciónActo o proceso por el cual una sustancia sólida, líquida o gaseosa se mezcla homogéneamente con un líquido o, a veces, con un gas o un sólido.Una mezcla homogénea formada por este proceso; especialmente: un sistema líquido monofásico.La condición de ser disuelto.
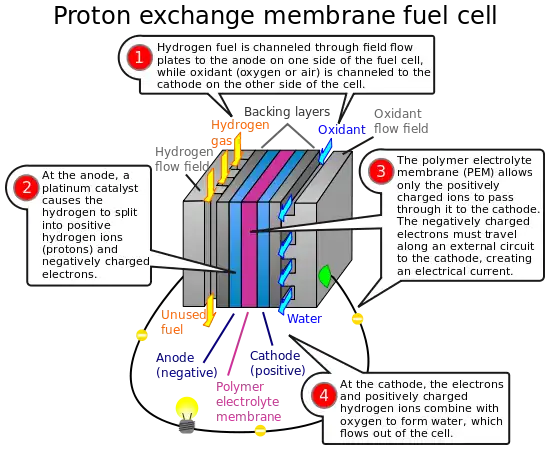
Eficiencia de los principales tipos de celdas de combustible
Máxima eficiencia teórica
La eficiencia energética de un sistema o dispositivo que convierte energía se mide por la relación entre la cantidad de energía útil emitida por el sistema ("energía de salida") y la cantidad total de energía que se introduce ("energía de entrada") o por la energía útil de salida como porcentaje de la energía total de entrada. En el caso de las pilas de combustible, la energía útil de salida se mide en energía eléctrica producida por el sistema. La energía de entrada es la energía almacenada en el combustible. Según el Departamento de Energía de EE. UU., las celdas de combustible generalmente tienen entre un 40 y un 60 % de eficiencia energética. Esto es más alto que algunos otros sistemas para la generación de energía. Por ejemplo, el motor de combustión interna típico de un automóvil tiene una eficiencia energética de alrededor del 25 %. Las plantas de energía de vapor generalmente alcanzan eficiencias de 30-40%mientras que las plantas de ciclo combinado de turbinas de gas y vapor pueden alcanzar eficiencias de hasta el 60%. En los sistemas combinados de calor y electricidad (CHP), el calor residual producido por el ciclo de energía primario, ya sea una celda de combustible, la fisión nuclear o la combustión, se captura y se utiliza, lo que aumenta la eficiencia del sistema hasta un 85-90 %.
La eficiencia máxima teórica de cualquier tipo de sistema de generación de energía nunca se alcanza en la práctica, y no considera otros pasos en la generación de energía, como la producción, el transporte y el almacenamiento de combustible y la conversión de la electricidad en energía mecánica. Sin embargo, este cálculo permite la comparación de diferentes tipos de generación de energía. La eficiencia máxima teórica de una pila de combustible se acerca al 100%, mientras que la eficiencia máxima teórica de los motores de combustión interna es de aproximadamente el 58%.
En la práctica
En un vehículo de pila de combustible, la eficiencia del tanque a la rueda es superior al 45 % con cargas bajas y muestra valores medios de alrededor del 36 % cuando se utiliza como procedimiento de prueba un ciclo de conducción como el NEDC (New European Driving Cycle). El valor NEDC comparable para un vehículo diésel es del 22 %. En 2008, Honda lanzó un vehículo eléctrico de pila de combustible de demostración (el Honda FCX Clarity) con una pila de combustible que aseguraba una eficiencia del 60% del tanque a la rueda.
También es importante tener en cuenta las pérdidas debidas a la producción, el transporte y el almacenamiento de combustible. Los vehículos con celdas de combustible que funcionan con hidrógeno comprimido pueden tener una eficiencia de la central eléctrica a la rueda del 22 % si el hidrógeno se almacena como gas a alta presión y del 17 % si se almacena como hidrógeno líquido. Las celdas de combustible no pueden almacenar energía como una batería, excepto como hidrógeno, pero en algunas aplicaciones, como plantas de energía independientes basadas en fuentes discontinuas como la energía solar o eólica, se combinan con electrolizadores y sistemas de almacenamiento para formar un sistema de almacenamiento de energía.. A partir de 2019, el 90 % del hidrógeno se usó para la refinación de petróleo, productos químicos y producción de fertilizantes (donde se requiere hidrógeno para el proceso Haber-Bosch), y el 98 % del hidrógeno se produce mediante el reformado de metano con vapor, que emite dióxido de carbono.La eficiencia general (de electricidad a hidrógeno y de regreso a electricidad) de dichas plantas (conocida como eficiencia de ida y vuelta), que utilizan hidrógeno puro y oxígeno puro, puede ser "del 35 al 50 por ciento", según la densidad del gas y otras condiciones. El sistema electrolizador/célula de combustible puede almacenar cantidades indefinidas de hidrógeno y, por lo tanto, es adecuado para el almacenamiento a largo plazo.
Las pilas de combustible de óxido sólido producen calor a partir de la recombinación del oxígeno y el hidrógeno. La cerámica puede funcionar tan caliente como 800 grados centígrados. Este calor se puede capturar y utilizar para calentar agua en una aplicación de microcogeneración de calor y energía (m-CHP). Cuando se captura el calor, la eficiencia total puede alcanzar el 80-90 % en la unidad, pero no considera las pérdidas de producción y distribución. Actualmente se están desarrollando unidades CHP para el mercado interno europeo.
El profesor Jeremy P. Meyers, en la revista Interface de la Sociedad Electroquímica en 2008, escribió: "Si bien las celdas de combustible son eficientes en relación con los motores de combustión, no son tan eficientes como las baterías, principalmente debido a la ineficiencia de la reacción de reducción de oxígeno (y....la reacción de evolución del oxígeno, en caso de que el hidrógeno se forme por electrólisis del agua).... [E]stos tienen más sentido para el funcionamiento desconectado de la red, o cuando el combustible se puede proporcionar de forma continua.Para aplicaciones que requieren frecuentes y relativamente puestas en marcha rápidas... donde las emisiones cero son un requisito, como en espacios cerrados como almacenes, y donde el hidrógeno se considera un reactivo aceptable, una [pila de combustible PEM] se está convirtiendo en una opción cada vez más atractiva [si cambiar las baterías es un inconveniente] ".En 2013, las organizaciones militares estaban evaluando las celdas de combustible para determinar si podían reducir significativamente el peso de la batería que llevaban los soldados.
Aplicaciones
Energía
Las celdas de combustible estacionarias se utilizan para la generación de energía primaria y de respaldo comercial, industrial y residencial. Las celdas de combustible son muy útiles como fuentes de energía en lugares remotos, como naves espaciales, estaciones meteorológicas remotas, grandes parques, centros de comunicaciones, lugares rurales, incluidas estaciones de investigación, y en ciertas aplicaciones militares. Un sistema de pila de combustible que funcione con hidrógeno puede ser compacto y ligero, y no tener piezas móviles importantes. Debido a que las celdas de combustible no tienen partes móviles y no involucran combustión, en condiciones ideales pueden lograr hasta un 99.9999% de confiabilidad. Esto equivale a menos de un minuto de tiempo de inactividad en un período de seis años.
Dado que los sistemas de electrolizadores de celdas de combustible no almacenan combustible en sí mismos, sino que dependen de unidades de almacenamiento externas, se pueden aplicar con éxito en el almacenamiento de energía a gran escala, siendo las áreas rurales un ejemplo. Hay muchos tipos diferentes de celdas de combustible estacionarias, por lo que las eficiencias varían, pero la mayoría tiene entre un 40 % y un 60 % de eficiencia energética. Sin embargo, cuando el calor residual de la pila de combustible se utiliza para calentar un edificio en un sistema de cogeneración, esta eficiencia puede aumentar hasta el 85 %. Esto es significativamente más eficiente que las centrales eléctricas de carbón tradicionales, que son solo alrededor de un tercio de eficiencia energética. Suponiendo una producción a escala, las celdas de combustible podrían ahorrar entre un 20 % y un 40 % en costos de energía cuando se usan en sistemas de cogeneración.Las celdas de combustible también son mucho más limpias que la generación de energía tradicional; una planta de energía de pila de combustible que utilice gas natural como fuente de hidrógeno generaría menos de una onza de contaminación (aparte del CO 2) por cada 1000 kW·h producidos, en comparación con las 25 libras de contaminantes generados por los sistemas de combustión convencionales. Las pilas de combustible también producen un 97 % menos de emisiones de óxido de nitrógeno que las centrales eléctricas de carbón convencionales.
Uno de esos programas piloto está operando en Stuart Island en el estado de Washington. Allí, la Iniciativa de Energía de Stuart Island ha construido un sistema completo de circuito cerrado: los paneles solares alimentan un electrolizador, que produce hidrógeno. El hidrógeno se almacena en un tanque de 500 galones estadounidenses (1,900 L) a 200 libras por pulgada cuadrada (1,400 kPa), y hace funcionar una celda de combustible ReliOn para proporcionar respaldo eléctrico completo a la residencia fuera de la red. Otro bucle de sistema cerrado se dio a conocer a fines de 2011 en Hempstead, Nueva York.
Las celdas de combustible se pueden usar con gas de baja calidad de vertederos o plantas de tratamiento de aguas residuales para generar energía y reducir las emisiones de metano. Se dice que una planta de celdas de combustible de 2,8 MW en California es la más grande de su tipo. Se están desarrollando celdas de combustible a pequeña escala (por debajo de 5kWhr) para su uso en despliegues residenciales fuera de la red.
Cogeneración
Los sistemas de celdas de combustible de calor y energía combinados (CHP), incluidos los sistemas micro combinados de calor y energía (MicroCHP), se utilizan para generar electricidad y calor para los hogares (ver celda de combustible para el hogar), edificios de oficinas y fábricas. El sistema genera energía eléctrica constante (vendiendo el exceso de energía a la red cuando no se consume), y al mismo tiempo produce aire caliente y agua a partir del calor residual. Como resultado, los sistemas CHP tienen el potencial de ahorrar energía primaria ya que pueden utilizar el calor residual que generalmente es rechazado por los sistemas de conversión de energía térmica. Un rango de capacidad típico de una celda de combustible doméstica es de 1–3 kW el, 4–8 kW th. Los sistemas CHP vinculados a enfriadores de absorción utilizan su calor residual para la refrigeración.
El calor residual de las pilas de combustible se puede desviar durante el verano directamente al suelo, lo que proporciona una mayor refrigeración, mientras que el calor residual durante el invierno se puede bombear directamente al edificio. La Universidad de Minnesota posee los derechos de patente de este tipo de sistema.
Los sistemas de cogeneración pueden alcanzar una eficiencia del 85 % (40-60 % eléctrica y el resto térmica). Las celdas de combustible de ácido fosfórico (PAFC) comprenden el segmento más grande de productos CHP existentes en todo el mundo y pueden proporcionar eficiencias combinadas cercanas al 90%. El carbonato fundido (MCFC) y las celdas de combustible de óxido sólido (SOFC) también se utilizan para la generación combinada de calor y energía y tienen eficiencias de energía eléctrica de alrededor del 60%. Las desventajas de los sistemas de cogeneración incluyen velocidades lentas de aumento y disminución, alto costo y corta vida útil. También su necesidad de tener un tanque de almacenamiento de agua caliente para suavizar la producción de calor térmico fue una seria desventaja en el mercado doméstico donde el espacio en las propiedades domésticas es muy importante.
Los consultores de Delta-ee afirmaron en 2013 que con el 64% de las ventas globales, los microcombinados de calor y electricidad de pila de combustible superaron a los sistemas convencionales en ventas en 2012. El proyecto japonés ENE FARM afirmó que se instalaron 34.213 PEMFC y 2.224 SOFC en el período 2012 –2014, 30.000 unidades en GNL y 6.000 en GLP.
Vehículos eléctricos de pila de combustible (FCEV)
Automóviles
A fines de 2019, se habían arrendado o vendido alrededor de 18,000 FCEV en todo el mundo. Se han presentado tres vehículos eléctricos de pila de combustible para arrendamiento comercial y venta: el Honda Clarity, el Toyota Mirai y el Hyundai ix35 FCEV. Los modelos de demostración adicionales incluyen el Honda FCX Clarity y el Mercedes-Benz F-Cell. Hasta junio de 2011, los FCEV de demostración habían recorrido más de 4 800 000 km (3 000 000 mi), con más de 27 000 recargas de combustible. Los vehículos eléctricos de pila de combustible tienen una autonomía media de 314 millas entre recargas de combustible. Se pueden repostar en menos de 5 minutos. El Programa de Tecnología de Celdas de Combustible del Departamento de Energía de EE. UU. establece que, a partir de 2011, las celdas de combustible lograron una eficiencia del 53 al 59 % a un cuarto de potencia y una eficiencia del vehículo del 42 al 53 % a plena potencia.y una durabilidad de más de 120 000 km (75 000 millas) con menos del 10 % de degradación. En un análisis de simulación de Well-to-Wheels de 2017 que "no abordó las limitaciones económicas y del mercado", General Motors y sus socios estimaron que por milla recorrida, un vehículo eléctrico de celda de combustible que funciona con hidrógeno gaseoso comprimido producido a partir de gas natural podría usar aproximadamente 40% menos de energía y emite un 45% menos de gases de efecto invernadero que un vehículo de combustión interna.
En 2015, Toyota presentó su primer vehículo de celda de combustible, el Mirai, a un precio de $57,000. Hyundai presentó el Hyundai ix35 FCEV de producción limitada bajo un contrato de arrendamiento. En 2016, Honda comenzó a arrendar el Honda Clarity Fuel Cell. En 2020, Toyota presentó la segunda generación de su marca Mirai, mejorando la eficiencia de combustible y ampliando el rango en comparación con el modelo Sedan 2014 original.
Crítica
Algunos comentaristas creen que los automóviles con celdas de combustible de hidrógeno nunca serán económicamente competitivos con otras tecnologías o que les tomará décadas volverse rentables. Elon Musk, CEO del fabricante de vehículos eléctricos a batería Tesla Motors, afirmó en 2015 que las celdas de combustible para uso en automóviles nunca serán comercialmente viables debido a la ineficiencia de producir, transportar y almacenar hidrógeno y la inflamabilidad del gas, entre otras razones.
En 2012, Lux Research, Inc. emitió un informe que decía: "El sueño de una economía de hidrógeno... no está más cerca". Concluyó que "el costo de capital... limitará la adopción a solo 5,9 GW" para 2030, proporcionando "una barrera casi insuperable para la adopción, excepto en aplicaciones de nicho". El análisis concluyó que, para 2030, el mercado estacionario de PEM alcanzará los 1.000 millones de dólares, mientras que el mercado de vehículos, incluidos los montacargas, alcanzará un total de 2.000 millones de dólares. Otros análisis citan la falta de una infraestructura extensa de hidrógeno en los EE. UU. como un desafío continuo para la comercialización de vehículos eléctricos de celda de combustible.
En 2014, Joseph Romm, autor de The Hype About Hydrogen (2005), dijo que los FCV aún no habían superado el alto costo de combustible, la falta de infraestructura de suministro de combustible y la contaminación causada por la producción de hidrógeno. "Se necesitarían varios milagros para superar todos esos problemas simultáneamente en las próximas décadas". Concluyó que la energía renovable no puede usarse económicamente para producir hidrógeno para una flota de FCV "ni ahora ni en el futuro". El analista de Greentech Media llegó a conclusiones similares en 2014. En 2015, Clean Technica enumeró algunas de las desventajas de los vehículos con celdas de combustible de hidrógeno. Lo mismo hizo Car Throttle.
Un video de 2019 de Real Engineering señaló que, a pesar de la introducción de vehículos que funcionan con hidrógeno, el uso de hidrógeno como combustible para automóviles no ayuda a reducir las emisiones de carbono del transporte. El 95 % del hidrógeno que todavía se produce a partir de combustibles fósiles libera dióxido de carbono, y producir hidrógeno a partir del agua es un proceso que consume energía. Almacenar hidrógeno requiere más energía, ya sea para enfriarlo hasta el estado líquido o para colocarlo en tanques a alta presión, y entregar el hidrógeno a las estaciones de servicio requiere más energía y puede liberar más carbono. El hidrógeno necesario para mover un FCV por kilómetro cuesta aproximadamente 8 veces más que la electricidad necesaria para mover un BEV la misma distancia.Una evaluación de 2020 concluyó que los vehículos de hidrógeno siguen siendo solo un 38 % eficientes, mientras que los vehículos eléctricos con batería tienen una eficiencia del 80 %.
Autobuses
En agosto de 2011, había alrededor de 100 autobuses de pila de combustible en servicio en todo el mundo. La mayoría de estos fueron fabricados por UTC Power, Toyota, Ballard, Hydrogenics y Proton Motor. Los autobuses de UTC habían recorrido más de 970 000 km (600 000 millas) en 2011. Los autobuses de pila de combustible tienen un ahorro de combustible de un 39 % a un 141 % mayor que los autobuses diésel y los autobuses de gas natural.
A partir de 2019, el NREL estaba evaluando varios proyectos de autobuses de celdas de combustible actuales y planificados en los EE. UU.
Trenes
En 2018, los primeros trenes propulsados por pilas de combustible, las unidades múltiples Alstom Coradia iLint, comenzaron a circular en la línea Buxtehude–Bremervörde–Bremerhaven–Cuxhaven en Alemania. Estos trenes ofrecen las ventajas de los trenes eléctricos sobre las locomotoras diésel y las DMU en la eliminación de las emisiones de chimeneas de los propios trenes sin el uso de electrificación por infraestructura de catenaria aérea. Dichos trenes se han pedido o se están probando en Suecia y el Reino Unido.
Camiones
En diciembre de 2020, Toyota y Hino Motors, junto con Seven-Eleven (Japón), FamilyMart y Lawson anunciaron que acordaron considerar conjuntamente la introducción de camiones eléctricos de celda de combustible de servicio ligero (FCET de servicio ligero). Lawson comenzó a probar la entrega a baja temperatura a fines de julio de 2021 en Tokio, utilizando un Hino Dutro en el que se implementa la celda de combustible Toyota Mirai. FamilyMart comenzó a realizar pruebas en la ciudad de Okazaki.
En agosto de 2021, Toyota anunció su plan para fabricar módulos de celdas de combustible en su planta de ensamblaje de automóviles de Kentucky para su uso en camiones grandes de cero emisiones y vehículos comerciales pesados. Planean comenzar a ensamblar los dispositivos electroquímicos en 2023.
En octubre de 2021, el camión basado en celdas de combustible de Daimler Truck recibió la aprobación de las autoridades alemanas para su uso en vías públicas.
Carretillas elevadoras
Una carretilla elevadora de pila de combustible (también llamada carretilla elevadora de pila de combustible) es una carretilla elevadora industrial impulsada por pila de combustible que se utiliza para levantar y transportar materiales. En 2013, se utilizaron más de 4000 carretillas elevadoras de pila de combustible en la manipulación de materiales en los EE. UU., de las cuales 500 recibieron financiación del DOE (2012). Las flotas de celdas de combustible son operadas por varias compañías, incluidas Sysco Foods, FedEx Freight, GENCO (en Wegmans, Coca-Cola, Kimberly Clark y Whole Foods) y HEB Grocers. Europa demostró 30 carretillas elevadoras de pila de combustible con Hylift y las amplió con HyLIFT-EUROPE a 200 unidades, con otros proyectos en Francia y Austria. Pike Research proyectó en 2011 que las carretillas elevadoras impulsadas por celdas de combustible serían el mayor impulsor de la demanda de combustible de hidrógeno para 2020.
La mayoría de las empresas en Europa y EE. UU. no utilizan carretillas elevadoras de petróleo, ya que estos vehículos trabajan en interiores donde se deben controlar las emisiones y, en su lugar, utilizan carretillas elevadoras eléctricas. Los montacargas alimentados por celdas de combustible pueden brindar beneficios sobre los montacargas alimentados por batería, ya que pueden reabastecerse de combustible en 3 minutos y pueden usarse en almacenes refrigerados, donde su rendimiento no se ve afectado por temperaturas más bajas. Las unidades FC a menudo se diseñan como reemplazos directos.
Motocicletas y bicicletas
En 2005, un fabricante británico de pilas de combustible impulsadas por hidrógeno, Intelligent Energy (IE), produjo la primera motocicleta funcional impulsada por hidrógeno llamada ENV (Emission Neutral Vehicle). La motocicleta tiene suficiente combustible para funcionar durante cuatro horas y viajar 160 km (100 millas) en un área urbana, a una velocidad máxima de 80 km / h (50 mph). En 2004, Honda desarrolló una motocicleta de pila de combustible que utilizaba el Honda FC Stack.
Otros ejemplos de motocicletas y bicicletas que usan celdas de combustible de hidrógeno incluyen el scooter de la compañía taiwanesa APFCT que usa el sistema de combustible de la italiana Acta SpA y el scooter Suzuki Burgman con una celda de combustible IE que recibió la aprobación de tipo de vehículo completo de la UE en 2011. Suzuki Motor Corp. y IE ha anunciado una empresa conjunta para acelerar la comercialización de vehículos de cero emisiones.
Aviones
En 2003, voló el primer avión propulsado por hélice del mundo que funcionaba completamente con una pila de combustible. La celda de combustible era un diseño de pila que permitía integrar la celda de combustible con las superficies aerodinámicas del avión. Los vehículos aéreos no tripulados (UAV) propulsados por celdas de combustible incluyen un UAV de celdas de combustible Horizon que estableció el récord de distancia volada para un UAV pequeño en 2007. Los investigadores de Boeing y los socios de la industria en toda Europa realizaron pruebas de vuelo experimentales en febrero de 2008 de un avión tripulado propulsado únicamente por una pila de combustible y baterías ligeras. El avión de demostración de pila de combustible, como se le llamó, utilizó un sistema híbrido de pila de combustible/batería de iones de litio de membrana de intercambio de protones (PEM) para impulsar un motor eléctrico, que estaba acoplado a una hélice convencional.
En 2009, el Ion Tiger del Laboratorio de Investigación Naval (NRL) utilizó una celda de combustible impulsada por hidrógeno y voló durante 23 horas y 17 minutos. Las celdas de combustible también se están probando y considerando para proporcionar energía auxiliar en los aviones, reemplazando los generadores de combustibles fósiles que se usaban anteriormente para arrancar los motores y satisfacer las necesidades eléctricas a bordo, al tiempo que reducen las emisiones de carbono.En 2016, un dron Raptor E1 realizó un vuelo de prueba exitoso utilizando una celda de combustible que era más liviana que la batería de iones de litio que reemplazó. El vuelo duró 10 minutos a una altitud de 80 metros (260 pies), aunque, según los informes, la celda de combustible tenía suficiente combustible para volar durante dos horas. El combustible estaba contenido en aproximadamente 100 gránulos sólidos de 1 centímetro cuadrado (0,16 pulgadas cuadradas) compuestos de un químico patentado dentro de un cartucho sin presión. Los gránulos son físicamente robustos y funcionan a temperaturas de hasta 50 °C (122 °F). La celda era de Arcola Energy.
Lockheed Martin Skunk Works Stalker es un UAV eléctrico propulsado por una celda de combustible de óxido sólido.
Barcos
El primer barco de pila de combustible del mundo, HYDRA, utilizó un sistema AFC con una potencia neta de 6,5 kW. Ámsterdam introdujo barcos impulsados por celdas de combustible que transportan personas por los canales de la ciudad.
Submarinos
Los submarinos Tipo 212 de las armadas alemana e italiana utilizan pilas de combustible para permanecer sumergidos durante semanas sin necesidad de salir a la superficie.
El U212A es un submarino no nuclear desarrollado por el astillero naval alemán Howaldtswerke Deutsche Werft. El sistema consta de nueve celdas de combustible PEM, que proporcionan entre 30 kW y 50 kW cada una. El barco es silencioso, lo que le da una ventaja en la detección de otros submarinos. Un documento naval ha teorizado sobre la posibilidad de un híbrido de celda de combustible nuclear mediante el cual la celda de combustible se usa cuando se requieren operaciones silenciosas y luego se repone desde el reactor nuclear (y agua).
Sistemas de energía portátiles
Los sistemas portátiles de celdas de combustible se clasifican generalmente como aquellos que pesan menos de 10 kg y proporcionan una potencia de menos de 5 kW. El tamaño del mercado potencial para las celdas de combustible más pequeñas es bastante grande, con una tasa de crecimiento potencial de hasta el 40% anual y un tamaño de mercado de alrededor de $ 10 mil millones, lo que lleva a que se dedique una gran cantidad de investigación al desarrollo de celdas de energía portátiles. Dentro de este mercado se han identificado dos grupos. El primero es el mercado de las celdas de microcombustible, en el rango de 1 a 50 W para alimentar dispositivos electrónicos más pequeños. El segundo es la gama de generadores de 1 a 5 kW para la generación de energía a mayor escala (por ejemplo, puestos militares avanzados, yacimientos petrolíferos remotos).
Las celdas de microcombustible están destinadas principalmente a penetrar en el mercado de teléfonos y computadoras portátiles. Esto se puede atribuir principalmente a la densidad de energía ventajosa proporcionada por las celdas de combustible sobre una batería de iones de litio, para todo el sistema. Para una batería, este sistema incluye el cargador y la propia batería. Para la celda de combustible, este sistema incluiría la celda, el combustible necesario y los accesorios periféricos. Teniendo en cuenta el sistema completo, se ha demostrado que las pilas de combustible proporcionan 530 Wh/kg en comparación con los 44 Wh/kg de las baterías de iones de litio. Sin embargo, aunque el peso de los sistemas de celdas de combustible ofrece una clara ventaja, los costos actuales no están a su favor. mientras que un sistema de batería generalmente costará alrededor de $ 1.20 por Wh, los sistemas de celdas de combustible cuestan alrededor de $ 5 por Wh, lo que los coloca en una desventaja significativa.
A medida que aumenta la demanda de energía para los teléfonos celulares, las celdas de combustible podrían convertirse en opciones mucho más atractivas para una mayor generación de energía. La demanda de mayor tiempo de funcionamiento en teléfonos y computadoras es algo que los consumidores exigen a menudo, por lo que las celdas de combustible podrían comenzar a avanzar en los mercados de computadoras portátiles y teléfonos celulares. El precio seguirá bajando a medida que se siga acelerando el desarrollo de las pilas de combustible. Las estrategias actuales para mejorar las micropilas de combustible son mediante el uso de nanotubos de carbono. Fue demostrado por Girishkumar et al. que depositar nanotubos en las superficies de los electrodos permite un área de superficie sustancialmente mayor aumentando la tasa de reducción de oxígeno.
Las celdas de combustible para uso en operaciones a mayor escala también son muy prometedoras. Los sistemas de energía portátiles que usan celdas de combustible se pueden usar en el sector del ocio (es decir, vehículos recreativos, cabañas, marinos), el sector industrial (es decir, energía para ubicaciones remotas, incluidos pozos de gas/petróleo, torres de comunicación, seguridad, estaciones meteorológicas) y en el sector militar. SFC Energy es un fabricante alemán de celdas de combustible de metanol directo para una variedad de sistemas de energía portátiles. Ensol Systems Inc. es un integrador de sistemas de energía portátiles que utiliza SFC Energy DMFC.La principal ventaja de las pilas de combustible en este mercado es la gran generación de energía por peso. Si bien las celdas de combustible pueden ser costosas, para ubicaciones remotas que requieren energía confiable, las celdas de combustible tienen una gran potencia. Para una excursión de 72 h, la comparación en peso es sustancial, con una celda de combustible que solo pesa 15 libras en comparación con las 29 libras de baterías necesarias para la misma energía.
Otras aplicaciones
- Suministro de energía para estaciones base o sitios celulares
- Generación distribuida
- Los sistemas de energía de emergencia son un tipo de sistema de pila de combustible, que puede incluir iluminación, generadores y otros aparatos, para proporcionar recursos de respaldo en una crisis o cuando fallan los sistemas regulares. Encuentran usos en una amplia variedad de entornos, desde hogares residenciales hasta hospitales, laboratorios científicos, centros de datos,
- Equipos de telecomunicaciones y buques de guerra modernos.
- Una fuente de alimentación ininterrumpida (UPS) proporciona energía de emergencia y, según la topología, también proporciona regulación de línea a los equipos conectados mediante el suministro de energía desde una fuente separada cuando la energía de la red pública no está disponible. A diferencia de un generador de reserva, puede brindar protección instantánea contra una interrupción momentánea de energía.
- Centrales eléctricas de carga base
- Vehículos híbridos, combinando la celda de combustible con un ICE o una batería.
- Computadoras portátiles para aplicaciones donde la carga de CA puede no estar disponible.
- Bases de carga portátiles para dispositivos electrónicos pequeños (por ejemplo, un clip para el cinturón que carga un teléfono celular o una PDA).
- Teléfonos inteligentes, portátiles y tabletas.
- Pequeños aparatos de calefacción
- Conservación de alimentos, lograda agotando el oxígeno y manteniendo automáticamente el agotamiento de oxígeno en un contenedor de envío que contiene, por ejemplo, pescado fresco.
- Alcoholímetros, donde la cantidad de voltaje generado por una celda de combustible se usa para determinar la concentración de combustible (alcohol) en la muestra.
- Detector de monóxido de carbono, sensor electroquímico.
Estaciones de servicio
Según FuelCellsWorks, un grupo industrial, a fines de 2019, 330 estaciones de servicio de hidrógeno estaban abiertas al público en todo el mundo. En junio de 2020, había 178 estaciones de hidrógeno disponibles públicamente en funcionamiento en Asia. 114 de estos estaban en Japón. Había al menos 177 estaciones en Europa, y aproximadamente la mitad de ellas estaban en Alemania. Había 44 estaciones de acceso público en los EE. UU., 42 de las cuales estaban ubicadas en California.
La construcción de una estación de combustible de hidrógeno cuesta entre $ 1 millón y $ 4 millones.
Mercados y economia
En 2012, los ingresos de la industria de celdas de combustible superaron el valor de mercado de $ 1 mil millones en todo el mundo, y los países del Pacífico asiático enviaron más de 3/4 de los sistemas de celdas de combustible en todo el mundo. Sin embargo, a partir de enero de 2014, ninguna empresa pública de la industria se había vuelto rentable. Se enviaron 140 000 pilas de celdas de combustible a nivel mundial en 2010, frente a los 11 000 envíos de 2007, y de 2011 a 2012, los envíos de celdas de combustible en todo el mundo tuvieron una tasa de crecimiento anual del 85 %. Tanaka Kikinzoku amplió sus instalaciones de fabricación en 2011. Aproximadamente el 50% de los envíos de celdas de combustible en 2010 fueron celdas de combustible estacionarias, frente a un tercio en 2009, y los cuatro productores dominantes en la industria de celdas de combustible fueron Estados Unidos, Alemania, Japón y Corea del Sur.La Alianza de Conversión de Energía de Estado Sólido del Departamento de Energía encontró que, a partir de enero de 2011, las celdas de combustible estacionarias generaron energía a aproximadamente $724 a $775 por kilovatio instalado. En 2011, Bloom Energy, un importante proveedor de celdas de combustible, dijo que sus celdas de combustible generaban energía a 9-11 centavos por kilovatio-hora, incluido el precio del combustible, el mantenimiento y el hardware.
Los grupos de la industria predicen que hay suficientes recursos de platino para la demanda futura y, en 2007, una investigación en el Laboratorio Nacional de Brookhaven sugirió que el platino podría reemplazarse por un recubrimiento de oro y paladio, que puede ser menos susceptible al envenenamiento y, por lo tanto, mejorar la vida útil de la celda de combustible. Otro método usaría hierro y azufre en lugar de platino. Esto reduciría el costo de una celda de combustible (ya que el platino en una celda de combustible regular cuesta alrededor de US $ 1,500, y la misma cantidad de hierro cuesta solo alrededor de US $ 1,50). El concepto estaba siendo desarrollado por una coalición del Centro John Innes y la Universidad de Milán-Bicocca. Los cátodos PEDOT son inmunes al envenenamiento por monóxido.
En 2016, Samsung "decidió abandonar los proyectos comerciales relacionados con las pilas de combustible, ya que las perspectivas del mercado no son buenas".
Investigación y desarrollo
- 2005: Los investigadores del Instituto de Tecnología de Georgia utilizaron triazol para elevar la temperatura de funcionamiento de las celdas de combustible PEM de menos de 100 °C a más de 125 °C, alegando que esto requerirá menos purificación de monóxido de carbono del combustible de hidrógeno.
- 2008: la Universidad de Monash, Melbourne, utilizó PEDOT como cátodo.
- 2009: Investigadores de la Universidad de Dayton, en Ohio, demostraron que conjuntos de nanotubos de carbono de crecimiento vertical podrían usarse como catalizadores en celdas de combustible. El mismo año, se demostró un catalizador a base de bisdifosfina de níquel para pilas de combustible.
- 2013: la firma británica ACAL Energy desarrolló una celda de combustible que, según dijo, puede funcionar durante 10,000 horas en condiciones de conducción simuladas. Afirmó que el costo de la construcción de celdas de combustible puede reducirse a $40/kW (aproximadamente $9,000 por 300 HP).
- 2014: Investigadores del Imperial College London desarrollaron un nuevo método para la regeneración de PEFC contaminados con sulfuro de hidrógeno. Recuperaron entre el 95 y el 100 % del rendimiento original de un PEFC contaminado con sulfuro de hidrógeno. También lograron rejuvenecer un PEFC contaminado con SO 2. Este método de regeneración es aplicable a varias pilas de celdas.
Contenido relacionado
Bohrio
Microfluidos
Cuasicristal