Catecolamina
| Catecolaminas |
|---|
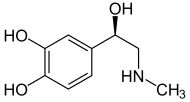 Epinefrina (Adrenalina) |
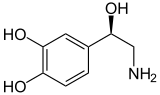 Norepinefrina (Noradrenalina) |
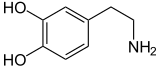 Dopamina |
Una catecolamina (abreviada CA) es un neurotransmisor monoamínico, un compuesto orgánico que tiene un catecol (benceno con dos grupos laterales hidroxilo uno al lado del otro) y un lado -amina de cadena.
El catecol puede ser una molécula libre o un sustituyente de una molécula más grande, donde representa un grupo 1,2-dihidroxibenceno.
Las catecolaminas se derivan del aminoácido tirosina, que se deriva de fuentes dietéticas y de la síntesis de fenilalanina. Las catecolaminas son hidrosolubles y se unen en un 50% a las proteínas plasmáticas en circulación.
Entre las catecolaminas se incluyen la epinefrina (adrenalina), la norepinefrina (noradrenalina) y la dopamina. La liberación de las hormonas epinefrina y norepinefrina de la médula suprarrenal de las glándulas suprarrenales es parte de la respuesta de lucha o huida.
La tirosina se crea a partir de la fenilalanina mediante la hidroxilación de la enzima fenilalanina hidroxilasa. La tirosina también se ingiere directamente de las proteínas de la dieta. Las células secretoras de catecolaminas utilizan varias reacciones para convertir la tirosina en serie en L-DOPA y luego en dopamina. Dependiendo del tipo de célula, la dopamina puede convertirse en norepinefrina o incluso convertirse en epinefrina.
Varias drogas estimulantes (como varias anfetaminas sustituidas) son análogos de catecolaminas.
Estructura
Las catecolaminas tienen la estructura distinta de un anillo de benceno con dos grupos hidroxilo, una cadena de etilo intermedia y un grupo amino terminal. Las feniletanolaminas como la norepinefrina tienen un grupo hidroxilo en la cadena de etilo.
Producción y degradación
Vías biosintéticas para las catecolaminas y las aminas traza en el cerebro humano L-Phenylalanine se convierte en L-tirosina por una enzima aminoácida aminoácida (AAAH) (fenilalanina 4-hidroxilasa), con oxígeno molecular (O2) y tetrahidrobiopterina como cofactores. L-La pirosina se convierte en L-DOPA por otra enzima AAAH (tyrosina 3-hidroxilase) con tetrahidrobiopterina, O2, y hierro ferroso (Fe2+Como cofactores. L-DOPA se convierte en dopamina por la enzima aromática L-aminoácido decarboxilasa (AADC), con fosfato piridoxal como cofactor. La dopamina también se utiliza como precursor en la síntesis de los neurotransmisores norepinefrina y epinefrina. La dopamina se convierte en norepinefrina por la enzima dopamina β-hidroxilasa (DBH), con O2 y ácido L-ascórbico como cofactores. La norepinefrina se convierte en epinefrina por la enzima feniletanoolamina N-metilransferasa (PNMT) con S-adenosyl-L-metionina como cofactor. |
Ubicación
Las catecolaminas son producidas principalmente por las células cromafines de la médula suprarrenal y las fibras posganglionares del sistema nervioso simpático. La dopamina, que actúa como neurotransmisor en el sistema nervioso central, se produce principalmente en los cuerpos celulares neuronales en dos áreas del tronco encefálico: el área tegmental ventral y la sustancia negra, la última de las cuales contiene neuronas pigmentadas con neuromelanina. Los cuerpos celulares del locus coeruleus, igualmente pigmentados con neuromelanina, producen norepinefrina. La epinefrina se produce en pequeños grupos de neuronas en el cerebro humano que expresan su enzima sintetizadora, la feniletanolamina N-metiltransferasa; estas neuronas se proyectan desde un núcleo adyacente (ventrolateral) al área postrema y desde un núcleo en la región dorsal del tracto solitario.
Biosíntesis
La dopamina es la primera catecolamina sintetizada a partir de DOPA. A su vez, la norepinefrina y la epinefrina se derivan de una modificación metabólica adicional de la dopamina. La enzima dopamina hidroxilasa requiere cobre como cofactor (no se muestra en el diagrama) y la DOPA descarboxilasa requiere PLP (no se muestra en el diagrama). El paso limitante de la velocidad en la biosíntesis de catecolaminas a través de la ruta metabólica predominante es la hidroxilación de L-tirosina a L-DOPA.
La síntesis de catecolaminas es inhibida por la alfa-metil-p-tirosina (AMPT), que inhibe la tirosina hidroxilasa.
Los aminoácidos fenilalanina y tirosina son precursores de las catecolaminas. Ambos aminoácidos se encuentran en altas concentraciones en el plasma sanguíneo y el cerebro. En los mamíferos, la tirosina se puede formar a partir de la fenilalanina de la dieta mediante la enzima fenilalanina hidroxilasa, que se encuentra en grandes cantidades en el hígado. Cantidades insuficientes de fenilalanina hidroxilasa dan como resultado fenilcetonuria, un trastorno metabólico que conduce a déficits intelectuales a menos que se trate con manipulación dietética. Generalmente se considera que la síntesis de catecolaminas comienza con la tirosina. La enzima tirosina hidroxilasa (TH) convierte el aminoácido L-tirosina en 3,4-dihidroxifenilalanina (L-DOPA). La hidroxilación de L-tirosina por TH da como resultado la formación del precursor DA L-DOPA, que es metabolizado por la L-aminoácido descarboxilasa aromática (AADC; ver Cooper et al. al., 2002) al transmisor dopamina. Este paso ocurre tan rápidamente que es difícil medir L-DOPA en el cerebro sin inhibir primero el AADC. En las neuronas que usan DA como transmisor, la descarboxilación de L-DOPA a dopamina es el paso final en la formación del transmisor; sin embargo, en aquellas neuronas que utilizan norepinefrina (noradrenalina) o epinefrina (adrenalina) como transmisores, también está presente la enzima dopamina β-hidroxilasa (DBH), que convierte la dopamina en norepinefrina. En otras neuronas en las que la epinefrina es el transmisor, una tercera enzima, la feniletanolamina N-metiltransferasa (PNMT), convierte la norepinefrina en epinefrina. Por lo tanto, una célula que usa epinefrina como transmisor contiene cuatro enzimas (TH, AADC, DBH y PNMT), mientras que las neuronas de norepinefrina contienen solo tres enzimas (que carecen de PNMT) y las células dopaminérgicas solo dos (TH y AADC).
Degradación
Las catecolaminas tienen una vida media de unos pocos minutos cuando circulan en la sangre. Pueden ser degradados por metilación por catecol-O-metiltransferasas (COMT) o por desaminación por monoaminooxidasas (MAO).
Los IMAO se unen a la MAO, evitando así que descomponga las catecolaminas y otras monoaminas.
El catabolismo de las catecolaminas está mediado por dos enzimas principales: la catecol-O-metiltransferasa (COMT), que está presente en la hendidura sináptica y el citosol de la célula, y la monoaminooxidasa (MAO), que se encuentra en la membrana mitocondrial. Ambas enzimas requieren cofactores: COMT usa Mg2+ como cofactor mientras que MAO usa FAD. El primer paso del proceso catabólico está mediado por MAO o COMT, que depende del tejido y la ubicación de las catecolaminas (por ejemplo, la degradación de las catecolaminas en la hendidura sináptica está mediada por COMT porque MAO es una enzima mitocondrial). Los siguientes pasos catabólicos en la vía involucran alcohol deshidrogenasa, aldehído deshidrogenasa y aldehído reductasa. El producto final de la epinefrina y la norepinefrina es el ácido vanililmandélico (VMA), que se excreta en la orina. El catabolismo de la dopamina conduce a la producción de ácido homovanílico (HVA).
Función
Modalidad
Dos catecolaminas, la norepinefrina y la dopamina, actúan como neuromoduladores en el sistema nervioso central y como hormonas en la circulación sanguínea. La catecolamina norepinefrina es un neuromodulador del sistema nervioso simpático periférico, pero también está presente en la sangre (principalmente a través de 'desbordamiento' de las sinapsis del sistema simpático).
Los niveles altos de catecolaminas en la sangre están asociados con el estrés, que puede ser inducido por reacciones psicológicas o factores estresantes ambientales, como niveles elevados de sonido, luz intensa o niveles bajos de azúcar en la sangre.
Los niveles extremadamente altos de catecolaminas (también conocidos como toxicidad por catecolaminas) pueden ocurrir en un traumatismo del sistema nervioso central debido a la estimulación o daño de los núcleos del tronco encefálico, en particular, aquellos núcleos que afectan el sistema nervioso simpático. En la medicina de urgencias, este hecho se conoce ampliamente como un "vertedero de catecolaminas".
Los niveles extremadamente altos de catecolaminas también pueden ser causados por tumores neuroendocrinos en la médula suprarrenal, una afección tratable conocida como feocromocitoma.
Los niveles altos de catecolaminas también pueden ser causados por la deficiencia de monoaminooxidasa A (MAO-A), conocida como síndrome de Brunner. Como MAO-A es una de las enzimas responsables de la degradación de estos neurotransmisores, su deficiencia aumenta considerablemente la biodisponibilidad de estos neurotransmisores. Ocurre en ausencia de feocromocitoma, tumores neuroendocrinos y síndrome carcinoide, pero se parece al síndrome carcinoide con síntomas como enrojecimiento facial y agresión.
La porfiria aguda puede causar niveles elevados de catecolaminas.
Efectos
Las catecolaminas provocan cambios fisiológicos generales que preparan el cuerpo para la actividad física (la respuesta de lucha o huida). Algunos efectos típicos son aumentos en el ritmo cardíaco, la presión arterial, los niveles de glucosa en sangre y una reacción general del sistema nervioso simpático. Algunas drogas, como la tolcapona (un inhibidor central de la COMT), elevan los niveles de todas las catecolaminas. El aumento de las catecolaminas también puede provocar un aumento de la frecuencia respiratoria (taquipnea) en los pacientes.
La catecolamina se secreta en la orina después de descomponerse y su nivel de secreción se puede medir para el diagnóstico de enfermedades asociadas con los niveles de catecolamina en el cuerpo. La prueba de orina para catecolaminas se usa para detectar feocromocitoma.
Función en las plantas
"Se han encontrado en 44 familias de plantas, pero no se ha establecido ninguna función metabólica esencial para ellas. Son precursores de benzo[c]phenanthridine alkaloids, que son los ingredientes principales activos de muchos extractos de plantas medicinales. Los CA han sido implicados para tener un posible papel protector contra depredadores de insectos, lesiones y desintoxicación de nitrógeno. Se ha demostrado que promueven el crecimiento del tejido vegetal, la embrigenesis somática de culturas in vitro y la floración. Las CA inhiben la oxidación del ácido indole-3-acetico y aumentan la biosíntesis de etileno. También se ha demostrado que aumentan los efectos sinérgicos de los gibberellins".
Prueba de catecolaminas
Las catecolaminas son secretadas por células en tejidos de diferentes sistemas del cuerpo humano, principalmente por los sistemas nervioso y endocrino. Las glándulas suprarrenales secretan ciertas catecolaminas en la sangre cuando la persona está estresada física o mentalmente y esta suele ser una respuesta fisiológica saludable. Sin embargo, el exceso agudo o crónico de catecolaminas circulantes puede potencialmente aumentar la presión arterial y la frecuencia cardíaca a niveles muy altos y eventualmente provocar efectos peligrosos. Las pruebas de metanefrinas libres en plasma fraccionadas o las metanefrinas en orina se utilizan para confirmar o descartar ciertas enfermedades cuando el médico identifica signos de hipertensión y taquicardia que no responden adecuadamente al tratamiento. Cada una de las pruebas mide la cantidad de metabolitos de adrenalina y noradrenalina, llamados respectivamente metanefrina y normetanefrina.
También se realizan análisis de sangre para analizar la cantidad de catecolaminas presentes en el organismo.
Las pruebas de catecolaminas se realizan para identificar tumores raros en la glándula suprarrenal o en el sistema nervioso. Las pruebas de catecolaminas brindan información relativa a tumores como: feocromocitoma, paraganglioma y neuroblastoma.
Contenido relacionado
Carbonato de litio
4-fenil-4-(1-piperidinil)ciclohexanol
Arturo aikin

