Carnitina palmitoiltransferasa I
La carnitina palmitoiltransferasa I (CPT1), también conocida como carnitina aciltransferasa I, CPTI, CAT1, CoA:carnitina acil transferasa (CCAT) o palmitoilCoA transferasa I, es una enzima mitocondrial responsable de la formación de acil carnitinas al catalizar la transferencia del grupo acilo de un acil-CoA graso de cadena larga desde la coenzima A a la l-carnitina. El producto suele ser palmitoilcarnitina (de ahí el nombre), pero otros ácidos grasos también pueden ser sustratos. Forma parte de una familia de enzimas llamadas carnitina aciltransferasas. Esta "preparación" permite el movimiento posterior de la acil carnitina desde el citosol al espacio intermembrana de las mitocondrias.
Actualmente se conocen tres isoformas de CPT1: CPT1A, CPT1B y CPT1C. La CPT1 está asociada a la membrana mitocondrial externa. Esta enzima puede ser inhibida por el malonil CoA, el primer intermediario comprometido que se produce durante la síntesis de ácidos grasos. Su papel en el metabolismo de los ácidos grasos hace que la CPT1 sea importante en muchos trastornos metabólicos como la diabetes. Dado que no se conoce su estructura cristalina, su mecanismo de acción exacto aún está por determinar.
Estructura

CPT1 es una proteína de membrana integral que existe en tres isoformas en los tejidos de los mamíferos: CPT1A, CPT1B y CPT1C. Las dos primeras se expresan en la membrana mitocondrial externa de la mayoría de los tejidos, pero sus proporciones relativas varían entre tejidos. CPT1A predomina en tejidos lipogénicos como el hígado, mientras que CPT1B predomina en tejidos como el corazón y el músculo esquelético que tienen una alta capacidad oxidativa de ácidos grasos (células adiposas marrones). Ambas isoformas son proteínas integrales de la membrana mitocondrial externa a través de dos regiones transmembrana en la cadena peptídica. La topología de membrana de CPT1A fue descrita por Fraser et al. en 1997. Es politópica, con los extremos N y C expuestos en el aspecto citosólico de la membrana mitocondrial externa, con un bucle corto que une los dos dominios transmembrana que sobresale hacia el espacio intermembrana mitocondrial.
La tercera isoforma (CPT1C) fue identificada en 2002 y se expresa tanto en las mitocondrias como en el retículo endoplasmático. Normalmente se expresa sólo en las neuronas (cerebro), aunque su expresión está alterada en ciertos tipos de células cancerosas.
Aún no se ha determinado la estructura exacta de ninguna de las isoformas de CPT1, aunque se han creado diversos modelos in silico para CPT1 basados en carnitina aciltransferasas estrechamente relacionadas, como la carnitina acetiltransferasa (CRAT).
Una diferencia estructural importante entre CPT1 y CPT2, CRAT y carnitina octanoiltransferasa (COT) es que CPT1 contiene un dominio adicional en su extremo N-terminal que consta de unos 160 aminoácidos. Se ha determinado que este dominio N-terminal adicional es importante para la molécula inhibidora clave de CPT1, malonil-CoA, y actúa como un interruptor que hace que CPT1A sea más o menos sensible a la inhibición de malonil-CoA.
Se ha propuesto que existen dos sitios de unión distintos en CPT1A y CPT1B. El "sitio A" o "sitio CoA" parece unir tanto malonil-CoA como palmitoil-CoA, así como otras moléculas que contienen coenzima A, lo que sugiere que la enzima se une a estas moléculas a través de la interacción con la fracción de coenzima A. Se ha sugerido que malonil-CoA puede comportarse como un inhibidor competitivo de CPT1A en este sitio. Se ha propuesto un segundo "sitio O" para unir malonil-CoA con más fuerza que el sitio A. A diferencia del sitio A, el sitio O se une a malonil-CoA a través del grupo dicarbonilo de la fracción malonato de malonil-CoA. La unión de malonil-CoA a cualquiera de los sitios A y O inhibe la acción de CPT1A al excluir la unión de carnitina a CPT1A. Dado que aún no se ha aislado ni obtenido imágenes de la estructura cristalina de CPT1A, su estructura exacta aún está por dilucidar.
Función
Enzyme mechanism
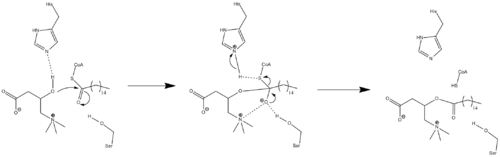
Debido a que actualmente no se dispone de datos sobre la estructura cristalina, no se conoce el mecanismo exacto de la CPT1. Se han postulado un par de mecanismos posibles diferentes para la CPT1, ambos de los cuales incluyen el residuo de histidina 473 como residuo catalítico clave. A continuación se muestra uno de estos mecanismos basado en un modelo de carnitina acetiltransferasa, en el que la His 473 desprotona la carnitina mientras que un residuo de serina cercano estabiliza el intermedio oxianión tetraédrico.
Se ha propuesto un mecanismo diferente que sugiere que una tríada catalítica compuesta por los residuos Cys-305, His-473 y Asp-454 lleva a cabo el paso de transferencia de acilo de la catálisis. Este mecanismo catalítico implica la formación de un intermediario covalente tioacilo-enzima con Cys-305.
Función biológica
El sistema de la palmitoiltransferasa de carnitina es un paso esencial en la betaoxidación de los ácidos grasos de cadena larga. Este sistema de transferencia es necesario porque, mientras que los ácidos grasos se activan (en forma de un enlace tioéster a la coenzima A) en la membrana mitocondrial externa, los ácidos grasos activados deben oxidarse dentro de la matriz mitocondrial. Los ácidos grasos de cadena larga, como el palmitoil-CoA, a diferencia de los ácidos grasos de cadena corta y media, no pueden difundirse libremente a través de la membrana interna mitocondrial y requieren un sistema de transporte para ser transportados a la matriz mitocondrial.

La carnitina palmitoiltransferasa I es el primer componente y el paso limitante de la velocidad del sistema de la carnitina palmitoiltransferasa, que cataliza la transferencia del grupo acilo de la coenzima A a la carnitina para formar palmitoilcarnitina. Luego, una translocasa transporta la acilcarnitina a través de la membrana mitocondrial interna, donde se convierte nuevamente en palmitoil-CoA.
Al actuar como aceptor de grupos acilo, la carnitina también puede desempeñar la función de regular la relación CoA:acilo-CoA intracelular.
Reglamento
La CPT1 es inhibida por el malonil-CoA, aunque el mecanismo exacto de inhibición sigue siendo desconocido. Se ha demostrado que la isoforma de CPT1 del músculo esquelético y del corazón, CPT1B, es entre 30 y 100 veces más sensible a la inhibición del malonil-CoA que la CPT1A. Esta inhibición es un buen objetivo para futuros intentos de regular la CPT1 para el tratamiento de trastornos metabólicos.
La acetil-CoA carboxilasa (ACC), la enzima que cataliza la formación de malonil-CoA a partir de acetil-CoA, es importante en la regulación del metabolismo de los ácidos grasos. Los científicos han demostrado que los ratones knock out de ACC2 tienen una grasa corporal y un peso reducidos en comparación con los ratones de tipo salvaje. Esto es resultado de una menor actividad de ACC que provoca una posterior disminución de las concentraciones de malonil-CoA. Estos niveles reducidos de malonil-CoA a su vez impiden la inhibición de CPT1, lo que provoca un aumento final de la oxidación de los ácidos grasos. Dado que las células del músculo esquelético y del corazón tienen una baja capacidad para la síntesis de ácidos grasos, la ACC puede actuar puramente como una enzima reguladora en estas células.
Significado clínico
La forma "CPT1A" está asociada con la deficiencia de carnitina palmitoiltransferasa I. Este trastorno poco común conlleva riesgo de encefalopatía hepática, hipoglucemia hipocetósica, convulsiones y muerte súbita inesperada en la infancia.
La CPT1 está asociada con la diabetes tipo 2 y la resistencia a la insulina. Estas enfermedades, junto con muchos otros problemas de salud, hacen que los niveles de ácidos grasos libres (AGL) en los seres humanos aumenten, la grasa se acumule en el músculo esquelético y disminuya la capacidad de los músculos para oxidar los ácidos grasos. La CPT1 se ha visto implicada en la contribución a estos síntomas. Los niveles elevados de malonil-CoA causados por la hiperglucemia y la hiperinsulinemia inhiben la CPT1, lo que provoca una disminución posterior en el transporte de ácidos grasos de cadena larga a las mitocondrias de los músculos y el corazón, lo que disminuye la oxidación de los ácidos grasos en dichas células. La desviación de los AGCL fuera de las mitocondrias conduce al aumento observado en los niveles de AGL y la acumulación de grasa en el músculo esquelético.
Su importancia en el metabolismo de los ácidos grasos hace que la CPT1 sea una enzima potencialmente útil en la que centrarse también en el desarrollo de tratamientos para muchos otros trastornos metabólicos.
Interacciones
Se sabe que la CPT1 interactúa con muchas proteínas, incluidas las de la familia NDUF, PKC1 y ENO1.
En el VIH, la proteína Vpr aumenta la expresión del ARNm de la PDK4, carnitina palmitoiltransferasa I (CPT1) inducida por PPARbeta/delta en las células. La eliminación de CPT1A mediante el análisis de bibliotecas de shRNA inhibe la replicación del VIH-1 en células T Jurkat cultivadas.
Véase también
- Carnitina palmitoiltransferas II
Referencias
- ^ a b c GRCh38: Ensembl release 89: ENSG00000110090 – Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00024900 – Ensembl, May 2017
- ^ "Human PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ van der Leij FR, Huijkman NC, Boomsma C, Kuipers JR, Bartelds B (2000). "Genomics of the human carnitine acyltransferase genes". Genética molecular y metabolismo. 71 ()1 –2): 139 –53. doi:10.1006/mgme.2000.3055. PMID 11001805.
- ^ Bonnefont JP, Djouadi F, Prip-Buus C, Gobin S, Munnich A, Bastin J (2004). "Carnitina palmitoiltransferas 1 y 2: aspectos bioquímicos, moleculares y médicos". Aspectos moleculares de la medicina. 25 ()5 –6): 495 –520. doi:10.1016/j.mam.2004.06.004. PMID 15363638.
- ^ a b Jogl G, Tong L (Jan 2003). "Crystal structure of carnitine acetyltransferase and implications for the catalytic mechanism and fatty acid transport". Celular. 112 1): 113–22. doi:10.1016/S0092-8674(02)01228-X. PMID 12526798. S2CID 18633987.
- ^ Brown NF, Hill JK, Esser V, Kirkland JL, Corkey BE, Foster DW, McGarry JD (Oct 1997). "Adipocitos blancos y células 3T3-L1 muestran un patrón anómalo de la palmitoiltransferasa carnitina (CPT) Esoformo expresión durante la diferenciación. Expresión inter-tissue e inter-species de enzimas CPT I y CPT II". The Biochemical Journal. 327 1): 225 –31. doi:10.1042/bj3270225. PMC 1218784. PMID 9355756.
- ^ Lee J, Ellis JM, Wolfgang MJ (Jan 2015). "La oxidación del ácido graso adiposo es necesaria para la termogénesis y potencia la inflamación causada por el estrés oxidativo". Cell Reports. 10 2): 266–279. doi:10.1016/j.celrep.2014.12.023. PMC 4359063. PMID 25578732.
- ^ Fraser F, Corstorphine, CG, Zammit, VA (mayo de 1997). "Topología de la palmitoiltransferasa carnitina I en la membrana exterior mitocondrial". Biochemical Journal. 323 3): 711 –718. doi:10.1042/bj3230711. PMC 1218374. PMID 1218374.
- ^ Precio N, van der Leij F, Jackson V, Corstorphine C, Thomson R, Sorensen A, Zammit V (Oct 2002). "Una nueva proteína exprimida por el cerebro relacionada con la palmitoiltransferasa de carnitina I". Genómica. 80 4): 433 –442. doi:10.1006/geno.2002.6845. PMID 12376098.
- ^ Casals N, Zammit VA, Herrero L, Fado R, Rodríguez R, Serra D (Dec 2016). "Carnitina palmitoiltransferasa 1C: De Cognición a Cáncer" (PDF). Prog Lipid Res. 61: 134 –148. doi:10.1016/j.plipres.2015.11.004. PMID 26708865.
- ^ Ezzeddini R, Taghikhani M, Salek Farrokhi A, Somi MH, Samadi N, Esfahani A, Rasaee, MJ (Mayo 2021). "Downregulation of fatty acid oxidation by involvement of HIF-1α and PPARγ in human gastric adenocarcinoma and its related clinic significance". Journal of Physiology and Biochemistry. 77 2): 249 –260. doi:10.1007/s13105-021-00791-3. S2CID 232300877.
- ^ Morillas M, López-Viñas E, Valencia A, Serra D, Gómez-Puertas P, Hegardt FG, Asins G (mayo de 2004). "Modelo estructural de la palmitoiltransferasa carnitina basado en el cristal de acetilransferasa carnitina". The Biochemical Journal. 379 (Pt 3): 777 –784. doi:10.1042/BJ20031373. PMC 1224103. PMID 14711372.
- ^ Rao JN, Warren GZ, Estolt-Povedano S, Zammit VA, Ulmer TS (2011). "Un interruptor estructural dependiente del medio ambiente se basa en la regulación de la palma carnitina 1A". J Biol Chem. 286 (49): 42545 –42554. doi:10.1074/jbc.M111.306951. PMC 3234983. PMID 21990363.
- ^ López-Viñas E, Bentebibel A, Gurunathan C, Morillas M, de Arriaga D, Serra D, Asins G, Hegardt FG, Gómez-Puertas P (Jun 2007). "Definición por análisis funcional y estructural de dos sitios malonyl-CoA en palma carnitina 1A". El Diario de Química Biológica. 282 (25): 18212–24. doi:10.1074/jbc.M700885200. PMID 174523.
- ^ Liu H, Zheng G, Treber M, Dai J, Woldegiorgis G (Feb 2005). "Cysteine-scanning mutagenesis of muscular carnitine palmitoyltransferase I revela un solo residuo de cisteína (Cys-305) es importante para la catalisis". El Diario de Química Biológica. 280 (6): 4524 –4531. doi:10.1074/jbc.M400893200. PMID 15579906.
- ^ Berg JM, Tymoczo JL, Stryer L, "Biochemistry", 6a edición 2007
- ^ Jogl G, Hsiao YS, Tong L (Nov 2004). "Strutura y función de aciltransferas de carnitina". Annals of the New York Academy of Sciences. 1033 1): 17 –29. Bibcode:2004NYASA1033...17J. doi:10.1196/annals.1320.002. PMID 15591000. S2CID 24466239.
- ^ Shi J, Zhu H, Arvidson DN, Woldegiorgis G (Feb 2000). "Los primeros 28 residuos de aminoácidos N-terminales de carnitina del músculo del corazón humano palmitoiltransferasa Soy esencial para la sensibilidad de malonyl CoA y la unión de alta afinidad". Bioquímica. 39 4): 712 –717. doi:10.1021/bi9918700. PMID 10651636.
- ^ Abu-Elheiga L, Oh W, Kordari P, Wakil SJ (Sep 2003). "Acetyl-CoA carboxylase 2 ratones mutantes están protegidos contra la obesidad y la diabetes inducidas por dietas altas en grasa/carbohidratos". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 100 (18): 10207–10212. Código:2003PNAS..10010207A. doi:10.1073/pnas.1733877100. PMC 193540. PMID 12920182.
- ^ Ogawa E, Kanazawa M, Yamamoto S, Ohtsuka S, Ogawa A, Ohtake A, Takayanagi M, Kohno Y (2002). "Expresión de análisis de dos mutaciones en la deficiencia de carnitina palmitoiltransferase IA". Journal of Human Genetics. 47 (7): 342 –7. doi:10.1007/s100380200047. PMID 12111367.
- ^ Collins SA, Sinclair G, McIntosh S, Bamforth F, Thompson R, Sobol I, Osborne G, Corriveau A, Santos M, Hanley B, Greenberg CR, Vallance H, Arbour L (2010). "Carnitina palmitoiltransferase 1A (CPT1A) Prevalencia de P479L en recién nacidos vivos en Yukón, Territorios del Noroeste y Nunavut". Genética molecular y metabolismo. 101 ()2-3): 200 –204. doi:10.1016/j.ymgme.2010.07.013. PMID 20696606.
- ^ Rasmussen BB, Holmbäck UC, Volpi E, Morio-Liondore B, Paddon-Jones D, Wolfe RR (Dec 2002). "Malonyl coenzyme A and the regulation of functional carnitine palmitoyltransferase-1 activity and fat oxidation in human skeletal muscular". The Journal of Clinical Investigation. 110 (11): 1687 –93. doi:10.1172/JCI15715. PMC 151631. PMID 12464674.
- ^ McGarry JD, Mills SE, Long CS, Foster DW (Jul 1983). "Observaciones sobre la afinidad para el carnitina, y la sensibilidad malonyl-CoA, de la palmitoiltransferasa carnitina I en los tejidos animales y humanos. Demostración de la presencia de malonyl-CoA en tejidos no hepáticos de la rata". The Biochemical Journal. 214 1): 21 –8. doi:10.1042/bj2140021. PMC 1152205. PMID 6615466.
- ^ Schreurs M, Kuipers F, van der Leij FR (2010). "Enzimas reguladoras de la beta-oxidación mitocondrial como objetivos para el tratamiento del síndrome metabólico". Reseñas de obesidad. 11 5): 380 –8. doi:10.1111/j.1467-789X.2009.00642.x. PMID 19694967. S2CID 24954036.
- ^ Havugimana PC, Hart GT, Nepusz T, Yang H, Turinsky AL, Li Z, Wang PI, Boutz DR, Fong V, Phanse S, Babu M, Craig SA, Hu P, Wan C, Vlasblom J, Dar VU, Bezginov A, Clark GW, Wu GC, Wodak SJ, Tillier ER, Paccanaro A, Marco EMtte, Emili A (Ago 2012). "Un censo de complejos de proteínas solubles humanos". Celular. 150 5): 1068–81. doi:10.1016/j.cell.2012.08.011. PMC 3477804. PMID 22939629.
- ^ Shrivastav S, Zhang L, Okamoto K, Lee H, Lagranha C, Abe Y, Balasubramanyam A, Lopaschuk GD, Kino T, Kopp JB (Sep 2013). "HIV-1 Vpr mejora la transcripción mediada PPARβ/δ, aumenta la expresión PDK4 y reduce la actividad PDC". Endocrinología molecular. 27 (9): 1564–76. doi:10.1210/me.-13201270. PMC 3753422. PMID 23842279.
- ^ Yeung ML, Houzet L, Yedavalli VS, Jeang KT (Jul 2009). "Un peinado corto en todo el genoma RNA de células T yrkat para proteínas humanas que contribuyen a la reproducción productiva del VIH-1". El Diario de Química Biológica. 284 (29): 19463–73. doi:10.1074/jbc.M109.010033. PMC 2740572. PMID 19460752.
Enlaces externos
- GeneReviews/NCBI/NIH/UW entrada en Carnitine Palmitoyltransferase 1A Deficiencia