Cardiografía de impedancia
La cardiografía de impedancia (ICG) es una tecnología no invasiva que mide la conductividad eléctrica total del tórax y sus cambios en el tiempo para procesar de forma continua una serie de parámetros cardiodinámicos, como el volumen sistólico (VS), la frecuencia cardíaca (FC), el gasto cardíaco (GC), el tiempo de eyección ventricular (VET) y el período de preeyección, y se utiliza para detectar los cambios de impedancia causados por una corriente de alta frecuencia y baja magnitud que fluye a través del tórax entre dos pares adicionales de electrodos ubicados fuera del segmento medido. Los electrodos sensores también detectan la señal del ECG, que se utiliza como reloj de sincronización del sistema.
Introducción
La cardiografía de impedancia (ICG), también conocida como pletismografía de impedancia eléctrica (EIP) o bioimpedancia eléctrica torácica (TEB), se ha investigado desde la década de 1940. La NASA ayudó a desarrollar la tecnología en la década de 1960. El uso de la cardiografía de impedancia en la investigación psicofisiológica fue pionero con la publicación de un artículo de Miller y Horvath en 1978. Posteriormente, las recomendaciones de Miller y Horvath fueron confirmadas por un grupo de estándares en 1990. Una lista completa de referencias está disponible en ICG Publications. Con ICG, se utiliza la colocación de cuatro sensores desechables dobles en el cuello y el pecho para transmitir y detectar cambios eléctricos y de impedancia en el tórax, que se utilizan para medir y calcular parámetros cardiodinámicos.
Proceso
- Cuatro pares de electrodos se colocan en el cuello y el nivel de diafragma, delineando el tórax
- Alta frecuencia, la corriente de baja magnitud se transmite a través del pecho en una dirección paralela con la columna vertebral del conjunto de pares externos
- La corriente busca un camino de menor resistencia: la aorta llena de sangre (la señal de fase sistólica) y la vena cava superior e inferior (la señal de fase diastólica, principalmente relacionada con la respiración)
- Los pares interiores, colocados en los hitos anatómicos delineando tórax, perciben las señales de impedancia y la señal ECG
- ICG mide la impedancia de referencia (resistencia) a esta corriente
- Con cada latido cardíaco, volumen de sangre y velocidad en el cambio de aorta
- ICG mide el cambio correspondiente en la impedancia y su calendario
- ICG atribuye los cambios en la impedancia a (a) la expansión volumétrica de la aorta (esta es la principal diferencia entre ICG y cardiometría eléctrica) y (b) a la alineación causada por la velocidad de la sangre de los eritrocitos como función de la velocidad de la sangre
- ICG utiliza la base de referencia y los cambios en la impedancia para medir y calcular los parámetros hemodinámicos
Hemodynamics
La hemodinámica es un subcapítulo de la fisiología cardiovascular que estudia las fuerzas generadas por el corazón y el movimiento resultante de la sangre a través del sistema cardiovascular. Estas fuerzas se manifiestan ante el médico como valores pareados del flujo sanguíneo y la presión arterial medidos simultáneamente en el nodo de salida del corazón izquierdo. La hemodinámica es una contraparte fluídica de la ley de Ohm en electrónica: la presión es equivalente al voltaje, el flujo a la corriente, la resistencia vascular a la resistencia eléctrica y el trabajo miocárdico a la potencia.

La relación entre los valores instantáneos de la presión arterial aórtica y el flujo sanguíneo a través de la válvula aórtica durante un intervalo de latido cardíaco y sus valores medios se representan en la figura 1. Sus valores instantáneos pueden utilizarse en investigación; en la práctica clínica, sus valores medios, PAM y VS, son adecuados.
Parámetros de flujo sanguíneo
Los parámetros del flujo sanguíneo sistémico (global) son: (a) el flujo sanguíneo por latido, el volumen sistólico, SV [ml/latido], y (b) el flujo sanguíneo por minuto, el gasto cardíaco, GC [l/min]. Existe una relación clara entre estos parámetros del flujo sanguíneo:
CO[l/min] (SV)[ml] Recursos humanos[bpm])/1000 {Eq.1}
donde FC es la frecuencia cardíaca (pulsaciones por minuto, ppm).
Dado que el valor normal de CO es proporcional a la masa corporal que debe perfundir, no puede existir un valor "normal" de SV y CO para todos los adultos. Todos los parámetros del flujo sanguíneo deben indexarse. La convención aceptada es indexarlos por el área de superficie corporal, BSA [m2], mediante la fórmula de DuBois y DuBois, una función de la altura y el peso:
BSA[m]2] = W0.425[kg] × H0,7525[cm] × 0,007184 {Eq.2}
Los parámetros indexados resultantes son el Índice sistólico, SI (ml/latido/m2) definido como
SI[ml/beat/m2] SV[ml]/BSA[m]2] {Eq.3}
y el índice cardíaco, IC (l/min/m2), definido como
CI[l/min/m2] CO[l/min]/BSA[m]2] {Eq.4}
Estos parámetros de flujo sanguíneo indexados presentan rangos típicos:
Para el índice sistólico: 35 < SItípico < 65 ml/latido/m2; para el índice cardíaco: 2,8 < ICtípico < 4,2 l/min/m2.
La ecuación 1 para los parámetros indexados cambia a
CI[l/min/m2] (SI)[ml/beat/m2] Recursos humanos[bpm])/1000 {Eq.1a}
Transporte de oxígeno
La función principal del sistema cardiovascular es el transporte de oxígeno: la sangre es el vehículo, el oxígeno es la carga. La tarea del sistema cardiovascular sano es proporcionar una perfusión adecuada a todos los órganos y mantener un equilibrio dinámico entre la demanda de oxígeno y el aporte de oxígeno. En una persona sana, el sistema cardiovascular siempre aumenta el flujo sanguíneo en respuesta al aumento de la demanda de oxígeno. En una persona hemodinámicamente comprometida, cuando el sistema no puede satisfacer una mayor demanda de oxígeno, el flujo sanguíneo a los órganos que se encuentran en una posición inferior en la lista de prioridades de aporte de oxígeno se reduce y estos órganos pueden, con el tiempo, fallar. Los trastornos digestivos, la impotencia masculina, el cansancio, el sonambulismo y la intolerancia a la temperatura ambiental son ejemplos clásicos de un estado de bajo flujo, que da lugar a una reducción del flujo sanguíneo.
Moduladores
La variabilidad de la SI y de la PAM se logran mediante la actividad de los moduladores hemodinámicos.

Los términos convencionales de la fisiología cardiovascular para los moduladores hemodinámicos son precarga, contractilidad y poscarga. Se ocupan de (a) las fuerzas de llenado inercial de la sangre que regresa a la aurícula (precarga), que estiran las fibras miocárdicas, almacenando así energía en ellas, (b) la fuerza por la cual las fibras del músculo cardíaco se acortan, liberando así la energía almacenada en ellas para expulsar parte de la sangre en el ventrículo hacia la vasculatura (contractilidad), y (c) las fuerzas que la bomba tiene que vencer para entregar un bolo de sangre a la aorta por cada contracción (poscarga). El nivel de precarga se evalúa actualmente a partir de la presión ocluida de la arteria pulmonar (PAOP) en un paciente cateterizado, o del índice diastólico final (EDI) mediante el uso de ultrasonido. La contractilidad no se evalúa de manera rutinaria; Con frecuencia, la inotropía y la contractilidad se intercambian como términos iguales. La poscarga se evalúa a partir del valor SVRI.
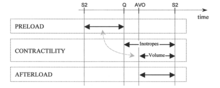
En lugar de utilizar los términos precarga, contractilidad y poscarga, la terminología y metodología preferenciales en hemodinámica por latido consisten en utilizar los términos para las herramientas de modulación hemodinámica reales, que el cuerpo utiliza o que el médico tiene en su caja de herramientas para controlar el estado hemodinámico:
La precarga y el nivel de contractilidad inducido (mecánicamente) por Frank-Starling se modulan mediante la variación del volumen intravascular (expansión de volumen o reducción de volumen/diuresis).
La modulación farmacológica de la contractilidad se realiza con agentes inotrópicos cardioactivos (inotrópicos positivos o negativos) presentes en el torrente sanguíneo que afectan la velocidad de contracción de las fibras miocárdicas.
La poscarga se modula variando el calibre de los esfínteres de entrada y salida de cada órgano, es decir, la resistencia vascular, con los agentes farmacológicos vasoactivos (vasoconstrictores o vasodilatadores y/o inhibidores de la ECA y/o ARA II) (ECA = enzima convertidora de angiotensina; ARA II = bloqueador del receptor de angiotensina). La poscarga también aumenta con el aumento de la viscosidad sanguínea, sin embargo, con excepción de pacientes extremadamente hemodiluidos o hemoconcentrados, este parámetro no se considera rutinariamente en la práctica clínica.
Con excepción de la expansión de volumen, que sólo puede lograrse por medios físicos (ingesta intravenosa u oral de líquidos), todas las demás herramientas de modulación hemodinámica son agentes farmacológicos, cardioactivos o vasoactivos.
La medición del IC y sus derivados permite a los médicos realizar evaluaciones, diagnósticos, pronósticos y decisiones de tratamiento oportunas para los pacientes. Se ha demostrado claramente que tanto los médicos capacitados como los no capacitados son incapaces de estimar el gasto cardíaco únicamente mediante una evaluación física.
Supervisión invasiva
La medición clínica del gasto cardíaco está disponible desde la década de 1970. Sin embargo, esta medición del flujo sanguíneo es altamente invasiva, ya que utiliza un catéter de termodilución dirigido por el flujo (también conocido como catéter de Swan-Ganz), lo que representa riesgos significativos para el paciente. Además, esta técnica es costosa (varios cientos de dólares por procedimiento) y requiere un médico experto y un entorno estéril para la inserción del catéter. Como resultado, se ha utilizado solo en estratos muy estrechos (menos del 2%) de pacientes gravemente enfermos y de alto riesgo en los que el conocimiento del flujo sanguíneo y el transporte de oxígeno superaban los riesgos del método. En los Estados Unidos, se estima que se realizan al menos dos millones de procedimientos de monitoreo de catéter de arteria pulmonar por año, con mayor frecuencia en pacientes quirúrgicos cardíacos y vasculares perioperatorios, insuficiencia cardíaca descompensada, insuficiencia multiorgánica y trauma.
Supervisión no invasiva
En teoría, una forma no invasiva de monitorizar la hemodinámica aportaría un valor clínico excepcional, ya que se podrían obtener datos similares a los métodos de monitorización hemodinámica invasiva con un coste mucho menor y sin riesgo. Aunque la monitorización hemodinámica no invasiva se puede utilizar en pacientes que antes requerían un procedimiento invasivo, el mayor impacto se puede conseguir en pacientes y entornos asistenciales en los que la monitorización hemodinámica invasiva no era posible ni justificaba el riesgo o el coste. Debido a su seguridad y a su bajo coste, la aplicabilidad de las mediciones hemodinámicas vitales podría extenderse a un número significativamente mayor de pacientes, incluidos los pacientes ambulatorios con enfermedades crónicas. La ICG se ha utilizado incluso en condiciones extremas, como el espacio exterior y una expedición al monte Everest. Los pacientes con insuficiencia cardíaca, hipertensión, marcapasos y disnea son cuatro enfermedades en las que la monitorización hemodinámica no invasiva ambulatoria puede desempeñar un papel importante en la evaluación, el diagnóstico, el pronóstico y el tratamiento. Algunos estudios han demostrado que el gasto cardíaco con ICG es preciso, mientras que otros estudios han demostrado que es inexacto. Se ha demostrado que el uso de ICG mejora el control de la presión arterial en la hipertensión resistente cuando lo utilizan tanto especialistas como médicos generales. También se ha demostrado que el ICG predice el empeoramiento del estado de la insuficiencia cardíaca.
Parámetros ICG
Las señales eléctricas y de impedancia se procesan para determinar puntos de referencia, que luego se utilizan para medir y calcular parámetros hemodinámicos, como el gasto cardíaco, el volumen sistólico, la resistencia vascular sistémica, el contenido de líquido torácico, el índice de aceleración y la relación del tiempo sistólico.
| Parámetro | Definición |
|---|---|
| Tasa de corazón | Número de latidos cardíacos cada minuto |
| Producto cardíaco | Cantidad de sangre bombeada por el ventrículo izquierdo cada minuto |
| Índice cardíaco | Salida cardiaca normalizada para superficie corporal |
| Volumen de descarga | Cantidad de sangre bombeada por el ventrículo izquierdo cada latido del corazón |
| Stroke Index | Volumen de troque normalizado para superficie corporal |
| Vascular sistémico Resistencia | La resistencia al flujo de sangre en la vasculatura (a menudo llamada "descarga") |
| Vascular sistémico Índice de resistencia | Resistencia vascular sistémica normalizada para superficie corporal |
| Índice de aceleración | Aceleración del flujo sanguíneo en la aorta |
| Índice de vulnerabilidad | Velocidad pico de flujo sanguíneo en la aorta |
| Contenido del fluido torácico | La conductividad eléctrica de la cavidad torácica, que se determina principalmente por los fluidos intravasculares, intraalveolares e intersticiales en el tórax |
| Trabajo cardíaco izquierdo | Un indicador de la cantidad de trabajo que el ventrículo izquierdo debe realizar para bombear sangre cada minuto |
| Índice de trabajo cardíaco izquierdo | Trabajo cardíaco izquierdo normalizado para superficie corporal |
| Relación de tiempo sistólica | La relación del sístolo eléctrico y mecánico |
| Pre Ejection Period | El intervalo de tiempo desde el comienzo de la estimulación eléctrica de los ventrículos hasta la apertura de la válvula aórtica (sístolo electrónico) |
| Hora de inyección ventricular izquierda | El intervalo de tiempo de la apertura al cierre de la válvula aórtica (sístolo mecánico) |
Referencias
- ^ a b "Qué es TEB y cómo funciona". Archivado desde el original en 2016-07-03. Retrieved 2015-05-01.
- ^ "25. Impedance Plethysmography". www.bem.fi.
- ^ Kubicek W.G., Witsoe, D.A., Patterson, R.P., Mosharrata, M.A., Karnegis, J.N., From, A.H.L. (1967). Las mejoras significativas de su exactitud clínica tuvieron lugar en los años 80 en BoMed Medical Manufacturing LTD bajo B. Bo Sramek con el producto NCCOM3. en 1992 la empresa fue renombrada a CDIC y el producto renombrado a BioZ. Desarrollo y evaluación de un sistema cardiográfico de impedancia para medir la producción cardíaca y el desarrollo de un sistema de computación de la tasa de consumo de oxígeno utilizando un espectrómetro de masa de cuádrupo. NASA-CR-92220, N68-32973.
- ^ "Transferencia tecnológica". 2016-09-15. Archivado desde el original el 19 de diciembre de 2002.
- ^ Miller, J. C., " Horvath, S. M. (1978). Cardiografía de impedancia. Psychophysiology, 15(1), 80–91.
- ^ Sherwood, A., Allen, M. T., Fahrenberg, J., Kelsey, R. M., Lovallo, W. R., " van Doornen, L. J. (1990). Directrices metodológicas para la cardiografía de impedancia. Psychophysiology, 27(1), 1–23.
- ^ WR Milnor: Hemodynamics, Williams & Wilkins, 1982
- ^ "Device Biomed Local Aiding NASA". 9 de enero de 2000.
- ^ Van De Water, Joseph M.; Miller, Timothy W.; Vogel, Robert L.; Mount, Bruce E.; Dalton, Martin L. (2003). "Impedance Cardiographya". Chest. 123 (6): 2028–2033. doi:10.1378/chest.123.6.2028. PMID 12796185.
- ^ Albert, Nancy M.; Ave, Melanie D.; Li, Jianbo; Young, James B. (2004). "Equivalencia de los métodos de bioimpedancia y termodilución para medir el rendimiento cardíaco en pacientes hospitalizados con insuficiencia cardíaca crónica avanzada y descompensada". American Journal of Critical Care. 13 (6): 469-479. doi:10.4037/ajcc2004.13.6.469. PMID 15568652.
- ^ Kamath SA, Drazner MH, Tasissa G, Rogers JG, Stevenson LW, Yancy CW (agosto de 2009). "Correlation of impedance cardiography with invasive hemodynamic measurements in patients with advanced heart failure: the BioImpedance CardioGraphy (BIG) substudy of the Evaluation Study of Congestive Heart Failure and Pulmonary Artery Catheterization Effectiveness (ESCAPE) Trial". Am. Heart J. 158 (2): 217–23. doi:10.1016/j.ahj.2009.06.002. PMC 2720805. PMID 19619697.
- ^ Taler, Sandra J.; Textor, Stephen C.; Augustine, Jo Ellen (2002). "Hipertensión resistente". Hipertensión. 39 (5): 982-988. doi:10.1161/01.HYP.0000016176.16042.2F. PMID 12019280.
- ^ Smith, Ronald D.; Levy, Pavel; Ferrario, Carlos M. (2006). "Valor de la hemodinámica no invasiva al control de presión arterial en sujetos hipertensivos". Hipertensión. 47 (4): 771–777. doi:10.1161/01.HYP.0000209642.11448.e0. PMID 16520405.
- ^ Packer, Milton; Abraham, William T.; Mehra, Mandeep R.; Yancy, Clyde W.; Lawless, Christine E.; Mitchell, Judith E.; Smart, Frank W.; Bijou, Rachel; o'Connor, Christopher M.; Massie, Barry M.; Pina, Ileana L.; Greenberg, Barry H.; Young, James B.; Fishbein, Daniel P.; Hauptman, Paul J.; Bourge, Robert C.; Strobeckali "Utility of Impedance Cardiography for the Identification of Short-Term Risk of Clinical Decompensation in Stable Patients with Chronic Heart Failure". Journal of the American College of Cardiology. 47 (11): 2245–2252. doi:10.1016/j.jacc.2005.12.071. PMID 16750691.
Enlaces externos
- http://bomed.us/teb.html Archivado 2016-07-03 en la máquina Wayback