Carborano
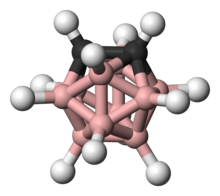
carboranos (o carboranos) son grupos deslocalizados por electrones (con enlaces no clásicos) compuestos de átomos de boro, carbono e hidrógeno. Como muchos de los hidruros de boro relacionados, estos grupos son poliedros o fragmentos de poliedros. Los carboranos son una clase de heteroboranos.
En términos de alcance, los carboranos pueden tener desde 5 hasta 14 átomos en la estructura de la jaula. La mayoría tiene dos átomos de carbono enjaulados. Los correspondientes análogos de alquilo C y B también se conocen en algunos casos.
Estructura y unión
Los carboranos y boranos adoptan geometrías de jaula tridimensionales (racimos) en marcado contraste con los compuestos orgánicos típicos. Las jaulas son compatibles con enlaces sigma deslocalizados, mientras que los hidrocarburos suelen ser cadenas o anillos.
Al igual que con otros grupos poliédricos deslocalizados por electrones, la estructura electrónica de estos compuestos de grupos puede describirse mediante las reglas de Wade-Mingos. Al igual que los hidruros de boro relacionados, estos grupos son poliedros o fragmentos de poliedros, y se clasifican de manera similar como closo-, nido-, arachno-, hypho-, hipercloso-, iso-, klado-, conjuncto- y megalo-, según si representan un poliedro completo (closo-) o un poliedro al que le faltan uno (nido-), dos (arachno-), tres ( hypho-), o más vértices. Los carboranos son un ejemplo notable de heteroboranos. En esencia, estas reglas enfatizan los vínculos deslocalizados y multicéntricos para las interacciones B-B, C-C y B-C.
Estructuralmente, se puede considerar que están relacionados con el icosaédrico (Ih) [B12H12]2− mediante el reemplazo formal de dos de sus BH− fragmentos con CH.
Isómeros
Los isómeros geométricos de los carboranos pueden existir en función de las distintas ubicaciones del carbono dentro de la jaula. Los isómeros requieren el uso de prefijos numéricos en el nombre de un compuesto. El closo-dicarbadecaborano puede existir en tres isómeros: 1,2-, 1,7- y 1,12-C2B10H12.
Preparación
Los carboranos se han preparado mediante muchas rutas, siendo la más común la adición de reactivos alquinílicos a grupos de hidruro de boro para formar carboranos dicarbonados. Por este motivo, la gran mayoría de los carboranos tienen dos vértices de carbono.
Derivados de monocarba
Losmonocarboranos son grupos con BnC jaulas. La derivada de 12 vértices es la que mejor se estudia, pero se conocen varias.
Por lo general, se preparan mediante la adición de reactivos de un carbono a grupos de hidruro de boro. Los reactivos de un carbono incluyen cianuro, isocianuros y formaldehído. Por ejemplo, monocarbadodecaborato ([CB11H12]−) se produce a partir de decaborano y formaldehído, seguido de la adición de dimetilsulfuro de borano. Los monocarboranos son precursores de aniones débilmente coordinantes.
Clústeres de Dicarba
Los dicarbaboranos se pueden preparar a partir de hidruros de boro utilizando alquinos como fuente de los dos centros de carbono. Además del closo-C2BnHn+2 serie mencionada anteriormente, Se conocen varias especies de dicarbonos de jaula abierta, incluida nido-C2B3H7 (isoestructural e isoelectrónico con B 5H9) y arachno- C2B7H13.
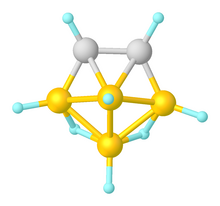
Síntesis de derivados icosaédricos closo-dicarbadodecaborano (R2C2B10H10) emplean alquinos como R2C2 fuente y decaborano (B10H14) para suministrar la unidad B10.
Clasificación por tamaño de jaula
La siguiente clasificación está adaptada del libro de Grimes sobre carboranos.
Carboranos pequeños y abiertos
Esta familia de clusters incluye las jaulas nido CB5H9, C2B4H8, C3B3H7, C4B2H6 y C2B3H7. Se ha dedicado relativamente poco trabajo a estos compuestos. El pentaborano[9] reacciona con acetileno para dar nido-1,2-C2B 4H8. Tras el tratamiento con hidruro de sodio, este último forma la sal [1,2-C2B4H7]−Na+.
Carboranos pequeños y cerrados
Esta familia de clusters incluye las jaulas closo C2B3H5, C2B4H6, C2B5H7 y CB5 H7. Esta familia de grupos también se estudia a la ligera debido a dificultades de síntesis. Como reflejo también de los desafíos sintéticos, muchos de estos compuestos son mejor conocidos como sus derivados alquílicos. 1,5-C2B3H 5 es el único isómero conocido de la jaula de cinco vértices. Se prepara a partir de la reacción del pentaborano (9) con acetileno en dos operaciones que comienzan con la condensación con acetileno seguida de pirólisis (craqueo) del producto:
- B5H9 + C2H2 → Nido-2,3-C2B4H8 + BH3
- C2B4H8 → closo-2,3-C2B3H5 + BH3
Carboranos de tamaño intermedio

Esta familia de clusters incluye las jaulas closo C2B6H8, C2B7H9, C2B8H10 y C2B9H11.
La isomería está bien establecida en esta familia: 1,2- y 1,6-C2B6H8, y 2,3- y 2,4-C2B5H7, así como en carboranos de jaula abierta como 2,3- y 2,4-C2B4H8 y 1,2 y 1,3-C2B9H13. En general, los isómeros que tienen átomos de carbono en la jaula no adyacentes son más estables térmicamente que aquellos con carbonos adyacentes, de modo que el calentamiento tiende a inducir la separación mutua de los átomos de carbono en la estructura.
Los carboranos de nuclearidad intermedia se generan de manera más eficiente mediante degradaciones que comienzan con carborano como se resume en estas ecuaciones, comenzando desde [C2B9H12]−:
- [C]2B9H12]− + H+ → C2B9H13
- C2B9H13 → C2B9H11 + H2
Por el contrario, los carboranos más pequeños suelen prepararse mediante la construcción de rutas, p. de pentaborano + alquino.
La oxidación con cromato de este grupo de 11 vértices da como resultado la deboronación, dando C2B7H13. De esa especie, otros grupos resultan por pirólisis, a veces en presencia de diborano: C2B6H8, C2B 8H10 y C 2B7H9.
Carboranos icosaédricos
Los closocarboranos icosaédricos de carga neutra, 1,2-, 1,7- y 1,12- C2 B10H12 (informalmente orto -, meta- y para-carborano) son particularmente estables y están disponibles comercialmente. El ortocarborano se forma primero tras la reacción de decarborano y acetileno. Se convierte cuantitativamente en metacarborano al calentarlo en una atmósfera inerte. La producción de metacarborano a partir de ortocarborano requiere 700 °C y se realiza en aprox. 25% de rendimiento.
[CB11H12] - también está bien establecido.
Reacciones
La metalación de los carboranos se ilustra mediante las reacciones de closo-C2B 3H5 con fuentes de carbonilo de hierro. Se obtienen dos productos que contienen closo Fe y Fe2, según a estas ecuaciones idealizadas:
- C2B3H5 + Fe2(CO)9 → C2B3H5Fe(CO)3 + Fe(CO)5 + CO
- C2B3H5Fe(CO)3 + Fe2(CO)9 → C2B3H5(Fe(CO)3)2 + Fe(CO)5 + CO
La degradación inducida por la base de los carboranos da derivados aniónicos nido , que también se pueden emplear como ligandos para metales de transición, que generan metalacarboranos, que son carboranos que contienen uno o más átomos de metal de transición o grupo principal en El marco de la jaula. Los más famosos son el Dicarbollide, complejos con la fórmula m 2+ [c 2 b 9 H 11 ] 2- , donde M significa metal.
Research
Los complejosde dicarbolida se han evaluado para muchas aplicaciones durante muchos años, pero las aplicaciones comerciales son raras. El bis (Dicarbollide) [CO (C 2 b 9 h 11 ) 2 ] - se ha utilizado como precipitante para la eliminación de 137cs + de Radiowastes.
Se han explorado las aplicaciones médicas de los carboranos. Los carboranos funcionalizados con C representan una fuente de boro para la terapia de captura de neutrones de boro.
El compuesto H (CHB 11 cl 11 ) es un Superacid, que forma una sal aislable con catión de benceno protonado, [c 6 h 7 ] + (catión de benzenio). La fórmula de esa sal es [c 6 h 7 ] + [chb 11 cl 11 ] - . El Superacid protona Fullerene, C 60 .