Calicreína
Las calicreínas son un subgrupo de las serina proteasas, enzimas capaces de escindir los enlaces peptídicos de las proteínas. En los seres humanos, la calicreína plasmática (codificada por el gen KLKB1) no tiene parálogo conocido, mientras que las peptidasas relacionadas con la calicreína tisular (KLK) codifican una familia de quince serina proteasas estrechamente relacionadas. Estos genes están localizados en el cromosoma 19q13 y forman el grupo contiguo más grande de proteasas dentro del genoma humano. Las calicreínas son responsables de la coordinación de varias funciones fisiológicas, entre ellas la presión arterial, la licuefacción del semen y la descamación de la piel.
Occurrence
En 1934, Eugen Werle informó que había encontrado una sustancia en el páncreas de seres humanos y de varios animales en cantidades tan grandes que se podía pensar que el páncreas era su lugar de origen. La denominó calicreína, palabra que deriva de la palabra griega para páncreas. Desde entonces, se han encontrado enzimas similares en los fluidos biológicos de seres humanos y otros mamíferos, así como en algunos venenos de serpientes.
Venom
La oruga conocida como Lagoa crispata contiene glándulas venenosas adheridas a espinas hipodérmicas, que producen e inyectan veneno que en la naturaleza se ha caracterizado como calicreína.
El veneno de los solenodontes y algunas musarañas como la musaraña de cola corta del norte consiste en múltiples copias de las serina proteasas calicreína 1 (KLK1). Las KLK1 son muy similares a las serina proteasas que se encuentran en serpientes venenosas como las víboras, y han evolucionado en paralelo a partir de un precursor de toxina común, que causa efectos hipotensores in vivo.
Plasma kallikrein
El gen KLKB1, que codifica la calicreína plasmática, se encuentra en el cromosoma 4q34-35. Se sintetiza como un precursor inactivo, la precalicreína, que debe sufrir un procesamiento proteolítico para activarse. Esto se facilita por el factor XII, la PRCP u otros estímulos.
La calicreína plasmática libera quininas (bradicinina y calidina) de los quininógenos, péptidos responsables de la regulación de la presión arterial y la activación de la inflamación. También es capaz de generar plasmina a partir del plasminógeno:
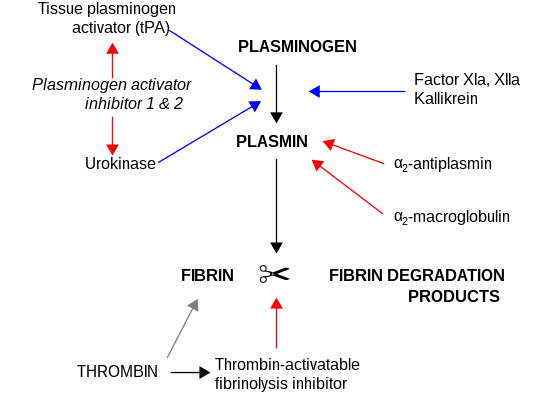
Estructura
La calicreína es homóloga del factor XI y consta de cuatro dominios de manzana y un dominio de serina proteasa.
Tissue kallikreins
A diferencia de la calicreína plasmática, las calicreínas tisulares (KLK) se expresan en todo el cuerpo humano y desempeñan diversas funciones fisiológicas. Como algunas calicreínas pueden catalizar la activación de otras, se han implicado varias cascadas que involucran a estas proteasas en la regulación de las funciones homeostáticas.
Función
De manera similar a KLKB1, tres calicreínas tisulares, KLK1, KLK2 y KLK12, también participan en la regulación de la presión arterial a través de la activación de la bradicinina. KLK2, KLK3, KLK4, KLK5 y KLK14 se expresan en la próstata y se cree que son responsables de regular la licuefacción del semen a través de la hidrólisis de la semenogelina. La descamación de la piel probablemente esté controlada por KLK5, KLK7 y KLK14, que se expresan en la capa más externa de la epidermis y escinden las proteínas de adhesión celular. Además, KLK6 y KLK8 están asociadas con la plasticidad neuronal en el sistema nervioso central.
Genes
Se conocen 15 calicreínas tisulares humanas: KLK1, KLK2, KLK3, KLK4, KLK5, KLK6, KLK7, KLK8, KLK9, KLK10, KLK11, KLK12, KLK13, KLK14, KLK15.
Significado clínico
Las peptidasas relacionadas con la calicreína son objeto de una activa investigación por parte de los investigadores de fármacos como posibles biomarcadores del cáncer.
El antígeno prostático específico (PSA; hk3, gen 3 de la calicreína humana) y la calicreína glandular humana (hK2) se utilizan como marcadores tumorales del cáncer de próstata.
Ecallantide, lanadelumab y berotralstat son medicamentos aprobados por la FDA que inhiben la calicreína y pueden utilizarse para tratar el angioedema hereditario.
Una variante sin sentido en KLK15 se ha asociado con el síndrome de Ehlers-Danlos hipermóvil.
Véase también
- Prekallikrein
- Sistema Kinin-kallikrein
- Kinin
- Aprotinina
- Lista de condiciones cutáneas
Referencias
- ^ Raspi G (septiembre de 1996). "Kallikrein and kallikrein-like proteinases: purification and determination by chromatographic and electrophoretic methods". Journal of Chromatography. B, Aplicaciones Biomédicas. 684 (1–2): 265–287. doi:10.1016/0378-4347(96)00144-2. PMID 8906477.
- ^ Lamdin JM, Howell DE, Kocan KM, Murphey DR, Arnold DC, Fenton AW, et al. (septiembre de 2000). "La estructura venomosa del cabello, el veneno y el ciclo de vida de Lagoa crispata, una oruga pus de Oklahoma". Toxicon. 38 (9): 1163–1189. doi:10.1016/s0041-0101(99)00195-6. PMID 10736472.
- ^ Casewell NR, Petras D, Card DC, Suranse V, Mychajliw AM, Richards D, et al. (diciembre 2019). "El genoma Solenodon revela la evolución convergente del veneno en los mamíferos eulipotyphlan". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 116 (51): 25745-25755. Código:2019PNAS..11625745C. doi:10.1073/pnas.1906117116. PMC 6926037. PMID 31772017.
- ^ Barua A, Koludarov I, Mikheyev AS (diciembre 2021). "Coopción de la misma familia de genes ancestrales dio lugar a toxinas mamíferas y reptilianas". BMC Biología. 19 (1): 268. doi:10.1186/s12915-021-01191-1. PMC 8705180. PMID 349491.
- ^ Kita M, Okumura Y, Ohdachi SD, Oba Y, Yoshikuni M, Nakamura Y, et al. (Febrero 2005). "Purificación y caracterización de la blarinasin, un nuevo tejido kallikrein-como la proteasa de la trilla corta Blarina brevicauda: estudios comparativos con la toxina blarina". Química Biológica. 386 (2): 177–182. doi:10.1515/BC.2005.022. Hdl:2115/7398. PMID 15843162. S2CID 2884850.
- ^ Bhoola KD, Figueroa CD, Worthy K (marzo de 1992). "Bioregulation of kinins: kallikreins, kininogens, and kininases". Pharmacological Reseñas. 44 (1): 1–80. PMID 1313585.
- ^ Stefan Offermanns; Walter Rosenthal (2008). Enciclopedia de Farmacología Molecular. Springer. pp. 673–. ISBN 978-3-540-38916-3. Retrieved 11 de diciembre 2010.
- ^ Giusti B, Serratì S, Margheri F, Papucci L, Rossi L, Poggi F, et al. (Noviembre 2005). "El patrón de kallikrein del tejido antígeno de las células endoteliales en la esclerosis sistémica". Artritis y reumatismo. 52 (11): 3618–3628. doi:10.1002/art.21383. PMID 16255054.
- ^ Michael IP, Pampalakis G, Mikolajczyk SD, Malm J, Sotiropoulou G, Diamandis EP (mayo de 2006). "El tejido humano kallikrein 5 es miembro de una vía de cascada proteolítica involucrada en la licuefacción seminal del coágulo y potencialmente en la progresión del cáncer de próstata". El Diario de Química Biológica. 281 (18): 12743–12750. doi:10.1074/jbc.M600326200. PMID 16517595.
- ^ Emami N, Diamandis EP (febrero de 2008). "Human kallikrein-related peptidase 14 (KLK14) es un nuevo componente activador de la cascada proteolítica KLK. Posible función en plasma y piel seminal". El Diario de Química Biológica. 283 (6): 3031–3041. doi:10.1074/jbc.M707253200. PMID 18056261.
- ^ Ovaere P, Lippens S, Vandenabeele P, Declercq W (septiembre de 2009). "Los papeles emergentes de las cascadas de serine protease en la epidermis". Tendencias en Ciencias Bioquímicas. 34 (9): 453–463. doi:10.1016/j.tibs.2009.08.001. PMID 19726197.
- ^ Tamura H, Ishikawa Y, Hino N, Maeda M, Yoshida S, Kaku S, Shiosaka S (febrero de 2006). "Neuropsin es esencial para los primeros procesos de adquisición de memoria y la potenciación colateral de Schaffer a largo plazo en el hipocampo del ratón adulto in vivo". The Journal of Physiology. 570 (Pt 3): 541-551. doi:10.1113/jphysiol.2005.098715. PMC 1479887. PMID 16308352.
- ^ Borgoño CA, Diamandis EP (noviembre 2004). "Los papeles emergentes de los tejidos humanos kallikreins en cáncer". Reseñas de la naturaleza. Cáncer. 4 11): 876-890. doi:10.1038/nrc1474. PMID 15516960. S2CID 382797.
- ^ Diamandis EP, Yousef GM (agosto de 2002). "Kallikreins de tejido humano: una familia de nuevos biomarcadores de cáncer". Química Clínica. 48 (8): 1198–1205. doi:10.1093/clinchem/48.8.1198. PMID 12142373.
- ^ "Variantes en la familia Kallikrein Gene y el síndrome de Hypermobile Ehlers-Danlos".
Enlaces externos
- La base de datos en línea MEROPS para peptidases y sus inhibidores: S01.212 Archivado 2020-05-27 en la máquina Wayback
- Kallikreins en la Biblioteca Nacional de Medicina de EE.UU.