Cadena de descomposición
En ciencia nuclear, la cadena de desintegración se refiere a una serie de desintegraciones radiactivas de diferentes productos de desintegración radiactiva como una serie secuencial de transformaciones. También se conoce como "cascada radiactiva". La mayoría de los radioisótopos no se desintegran directamente a un estado estable, sino que sufren una serie de desintegraciones hasta que finalmente se alcanza un isótopo estable.
Las etapas de descomposición se conocen por su relación con las etapas anteriores o posteriores. Un isótopo padre es aquel que se desintegra para formar un isótopo hijo. Un ejemplo de esto es el uranio (número atómico 92) que se descompone en torio (número atómico 90). El isótopo hijo puede ser estable o puede decaer para formar un isótopo hijo propio. El hijo de un isótopo hijo a veces se denomina isótopo nieto.
El tiempo que tarda un solo átomo padre en descomponerse en un átomo de su isótopo hijo puede variar ampliamente, no solo entre diferentes pares padre-hijo, sino también aleatoriamente entre parejas idénticas de isótopos padre e hijo. El decaimiento de cada átomo individual ocurre espontáneamente, y el decaimiento de una población inicial de átomos idénticos a lo largo del tiempo t, sigue una distribución exponencial decreciente, e−λt, donde λ se denomina constante de decaimiento. Una de las propiedades de un isótopo es su vida media, el tiempo en el que la mitad de un número inicial de radioisótopos originales idénticos han decaído en sus hijos, que está inversamente relacionado con λ. Se han determinado vidas medias en laboratorios para muchos radioisótopos (o radionúclidos). Estos pueden variar desde casi instantáneos (menos de 10−21 segundos) hasta más de 1019 años.
Cada una de las etapas intermedias emite la misma cantidad de radiactividad que el radioisótopo original (es decir, existe una relación de uno a uno entre el número de desintegraciones en etapas sucesivas), pero cada etapa libera una cantidad diferente de energía. Siempre y cuando se logre el equilibrio, cada isótopo hijo sucesivo estará presente en proporción directa a su vida media; pero como su actividad es inversamente proporcional a su vida media, cada nucleido en la cadena de decaimiento contribuye finalmente con tantas transformaciones individuales como la cabeza de la cadena, aunque no con la misma energía. Por ejemplo, el uranio-238 es débilmente radiactivo, pero la pechblenda, un mineral de uranio, es 13 veces más radiactivo que el uranio puro debido al radio y otros isótopos secundarios que contiene. Los isótopos de radio inestables no solo son importantes emisores de radiactividad, sino que, como siguiente etapa en la cadena de descomposición, también generan radón, un gas radiactivo pesado, inerte y natural. Las rocas que contienen torio y/o uranio (como algunos granitos) emiten gas radón que puede acumularse en lugares cerrados como sótanos o minas subterráneas.
La cantidad de isótopos en las cadenas de desintegración en un momento determinado se calcula con la ecuación de Bateman.
Historia
Todos los elementos e isótopos que se encuentran en la Tierra, con la excepción del hidrógeno, el deuterio, el helio, el helio-3 y quizás pequeñas cantidades de isótopos estables de litio y berilio que se crearon en el Big Bang, fueron creados por la s- El proceso o el proceso r en estrellas o colisiones estelares, y para que estos sean hoy parte de la Tierra, deben haber sido creados a más tardar hace 4.500 millones de años. Todos los elementos creados hace más de 4500 millones de años se denominan primordiales, lo que significa que fueron generados por los procesos estelares del universo. En el momento en que fueron creados, los que eran inestables comenzaron a decaer inmediatamente. Todos los isótopos que tienen vidas medias inferiores a 100 millones de años se han reducido a 2,8×10−12% o menos de las cantidades originales creadas y capturadas por la Tierra acreción; son trazas en la actualidad, o se han descompuesto por completo. Solo hay otros dos métodos para crear isótopos: artificialmente, dentro de un reactor hecho por el hombre (o tal vez natural), o a través de la descomposición de una especie isotópica original, el proceso conocido como decaimiento cadena.
Los isótopos inestables se descomponen en sus productos secundarios (que a veces pueden ser incluso más inestables) a un ritmo determinado; eventualmente, a menudo después de una serie de desintegraciones, se alcanza un isótopo estable: hay alrededor de 200 isótopos estables en el universo. En los isótopos estables, los elementos ligeros suelen tener una menor proporción de neutrones a protones en su núcleo que los elementos más pesados. Los elementos ligeros como el helio-4 tienen una relación neutrón:protón cercana a 1:1. Los elementos más pesados, como el plomo, tienen cerca de 1,5 neutrones por protón (por ejemplo, 1,536 en plomo-208). Ningún nucleido más pesado que el plomo-208 es estable; estos elementos más pesados tienen que perder masa para lograr la estabilidad, generalmente como desintegración alfa. El otro método de desintegración común para los isótopos con una alta proporción de neutrones a protones (n/p) es la desintegración beta, en la que el nucleido cambia de identidad elemental mientras mantiene la misma masa y reduce su proporción n/p. Para algunos isótopos con una relación n/p relativamente baja, existe una desintegración beta inversa, mediante la cual un protón se transforma en un neutrón, moviéndose así hacia un isótopo estable; sin embargo, dado que la fisión casi siempre produce productos que son pesados en neutrones, la emisión de positrones es relativamente rara en comparación con la emisión de electrones. Hay muchas cadenas de desintegración beta relativamente cortas, al menos dos (una desintegración beta pesada y una desintegración de positrones ligera) para cada peso discreto hasta alrededor de 207 y algunas más, pero para los elementos de mayor masa (isótopos más pesados que el plomo) hay son sólo cuatro caminos que abarcan todas las cadenas de descomposición. Esto se debe a que solo hay dos métodos principales de descomposición: la radiación alfa, que reduce la masa en 4 unidades de masa atómica (uma), y la beta, que no cambia la masa atómica en absoluto (solo el número atómico y la relación p/n). Los cuatro caminos se denominan 4n, 4n + 1, 4n + 2 y 4n + 3; el resto de dividir la masa atómica por cuatro da la cadena que el isótopo usará para desintegrarse. Hay otros modos de decaimiento, pero invariablemente ocurren con menor probabilidad que el decaimiento alfa o beta. (No debe suponerse que estas cadenas no tienen ramificaciones: el siguiente diagrama muestra algunas ramificaciones de cadenas, y en realidad hay muchas más, porque hay muchos más isótopos posibles de los que se muestran en el diagrama). Por ejemplo, el El tercer átomo de nihonio-278 sintetizado sufrió seis desintegraciones alfa hasta mendelevio-254, seguidas de una captura de electrones (una forma de desintegración beta) hasta fermio-254, y luego una séptima alfa hasta californio-250, sobre la cual habría seguido la cadena 4n + 2 como se indica en este artículo. Sin embargo, los nucleidos superpesados más pesados sintetizados no alcanzan las cuatro cadenas de desintegración, porque alcanzan un nucleido que se fisiona espontáneamente después de unas pocas desintegraciones alfa que terminan la cadena: esto es lo que sucedió con los dos primeros átomos de nihonio-278 sintetizados, así como con a todos los nucleidos más pesados producidos.
Tres de esas cadenas tienen un isótopo (o nucleido) de larga vida cerca de la parte superior; este isótopo de larga vida es un cuello de botella en el proceso a través del cual la cadena fluye muy lentamente y mantiene la cadena debajo de ellos 'viva'; con el flujo. Los tres nucleidos de vida larga son el uranio-238 (vida media = 4500 millones de años), el uranio 235 (vida media = 700 millones de años) y el torio-232 (vida media = 14000 millones de años). La cuarta cadena no tiene un isótopo de cuello de botella tan duradero, por lo que casi todos los isótopos en esa cadena se han descompuesto hace mucho tiempo hasta estar muy cerca de la estabilidad en la parte inferior. Cerca del final de esa cadena está el bismuto-209, que durante mucho tiempo se pensó que era estable. Sin embargo, recientemente se descubrió que el bismuto-209 es inestable con una vida media de 19 billones de billones de años; es el último paso antes del talio-205 estable. En el pasado distante, alrededor de la época en que se formó el sistema solar, había más tipos de isótopos inestables de alto peso disponibles, y las cuatro cadenas eran más largas con isótopos que desde entonces se han desintegrado. Hoy hemos fabricado isótopos extintos, que nuevamente toman sus lugares anteriores: el plutonio-239, el combustible de la bomba nuclear, como ejemplo principal, tiene una vida media de "solo" 24.500 años, y se desintegra por emisión alfa en uranio-235. En particular, a través de la producción a gran escala de neptunio-237 hemos resucitado con éxito la cuarta cadena hasta ahora extinta. Por lo tanto, las tablas a continuación comienzan las cuatro cadenas de descomposición en isótopos de californio con números de masa de 249 a 252.
Tipos de caries
Los cuatro modos más comunes de desintegración radiactiva son: desintegración alfa, desintegración beta, desintegración beta inversa (considerada como emisión de positrones y captura de electrones) y transición isomérica. De estos procesos de desintegración, solo la desintegración alfa cambia el número de masa atómica (A) del núcleo y siempre lo disminuye en cuatro. Debido a esto, casi cualquier desintegración dará como resultado un núcleo cuyo número de masa atómica tiene el mismo residuo mod 4, dividiendo todos los nucleidos en cuatro cadenas. Los miembros de cualquier cadena de descomposición posible deben extraerse enteramente de una de estas clases. Las cuatro cadenas también producen helio-4, ya que las partículas alfa son núcleos de helio-4.
En la naturaleza se observan tres cadenas principales de desintegración (o familias), comúnmente llamadas serie del torio, serie del radio o uranio y serie del actinio, que representan tres de estas cuatro clases y terminan en tres isótopos estables diferentes de plomo. El número de masa de cada isótopo en estas cadenas se puede representar como A = 4n, A = 4n + 2 y A = 4n + 3, respectivamente. Los isótopos iniciales de larga vida de estos tres isótopos, respectivamente torio-232, uranio-238 y uranio-235, han existido desde la formación de la tierra, ignorando los isótopos artificiales y sus desintegraciones creados desde la década de 1940.
Debido a la vida media relativamente corta de su isótopo inicial neptunio-237 (2,14 millones de años), la cuarta cadena, la serie de neptunio con A = 4n + 1, ya está extinto en la naturaleza, excepto por el último paso limitante de la velocidad, la descomposición del bismuto-209. Sin embargo, todavía se encuentran en la naturaleza trazas de 237Np y sus productos de desintegración como resultado de la captura de neutrones en el mineral de uranio. Ahora se sabe que el isótopo final de esta cadena es el talio-205. Algunas fuentes más antiguas dan el isótopo final como bismuto-209, pero recientemente se descubrió que es muy poco radiactivo, con una vida media de 2,01×1019 años.
También hay cadenas de descomposición no transuránicas de isótopos inestables de elementos ligeros, por ejemplo, las de magnesio-28 y cloro-39. En la Tierra, la mayoría de los isótopos iniciales de estas cadenas antes de 1945 fueron generados por radiación cósmica. Desde 1945, las pruebas y el uso de armas nucleares también han liberado numerosos productos de fisión radiactivos. Casi todos estos isótopos se desintegran por modos de desintegración β− o β+, cambiando de un elemento a otro sin cambiar la masa atómica. Estos productos secundarios posteriores, al estar más cerca de la estabilidad, generalmente tienen vidas medias más largas hasta que finalmente se descomponen en la estabilidad.
Cadenas de descomposición de actínidos alfa
| Actinides by decay chain | Media vida rango a) | Productos de fisión de 235U por rendimiento | ||||||
|---|---|---|---|---|---|---|---|---|
| 4n | 4n + 1 | 4n + 2 | 4n + 3 | 4.5–7% | 0,04–1,25% | 0,21 % | ||
| 228RaNo | 4 a 6 | 155Eu. | ||||||
| 244Cm. | 241Pu. | 250Cf | 227AcNo | 10–29 a | 90Sr | 85Kr | 113mCd. | |
| 232U. | 238Pu. | 243Cm. | 29–97 a | 137Cs | 151Sm. | 121mSn | ||
| 248Bk | 249Cf. | 242mAm. | 141–351 a | No hay productos de fisión semivida en el rango de 100 a 210 ka... | ||||
| 241Am. | 251Cf. | 430–900 a | ||||||
| 226RaNo | 247Bk | 1.3–1.6 ka | ||||||
| 240Pu | 229Th | 246Cm. | 243Am. | 4.7–7.4 ka | ||||
| 245Cm. | 250Cm | 8.3 a 8.5 ka | ||||||
| 239Pu. | 24.1 ka | |||||||
| 230ThNo | 231PaNo | 32-76 ka | ||||||
| 236Np. | 233U. | 234UNo | 150–250 ka | 99TcINGLES | 126Sn | |||
| 248Cm | 242Pu | 327–375 ka | 79SeINGLES | |||||
| 1.53 Ma | 93Zr | |||||||
| 237Np. | 2.1 a 6,5 Ma | 135CsINGLES | 107Pd | |||||
| 236U | 247Cm. | 15-24 Ma | 129IINGLES | |||||
| 244Pu | 80 Ma | ... ni más allá de 15.7 Ma | ||||||
| 232ThNo | 238UNo | 235UNo. | 0.7–14.1 Ga | |||||
| ||||||||
En las cuatro tablas siguientes, se omiten las ramificaciones menores de descomposición (con una probabilidad de ramificación inferior al 0,0001 %). La liberación de energía incluye la energía cinética total de todas las partículas emitidas (electrones, partículas alfa, cuantos gamma, neutrinos, electrones Auger y rayos X) y el núcleo de retroceso, asumiendo que el núcleo original estaba en reposo. La letra "a" representa un año (del latín annus).
En las tablas a continuación (excepto el neptunio), también se dan los nombres históricos de los nucleidos naturales. Estos nombres se utilizaron en el momento en que se descubrieron e investigaron por primera vez las cadenas de descomposición. A partir de estos nombres históricos se puede ubicar la cadena particular a la que pertenece el nucleido y reemplazarla con su nombre moderno.
Las tres cadenas de desintegración alfa de actínido de origen natural que se indican a continuación: torio, uranio/radio (del U-238) y actinio (del U-235), cada una termina con su propio isótopo de plomo específico (Pb-208, Pb -206 y Pb-207 respectivamente). Todos estos isótopos son estables y también están presentes en la naturaleza como nucleidos primordiales, pero sus cantidades en exceso en comparación con el plomo-204 (que solo tiene un origen primordial) pueden utilizarse en la técnica de datación de rocas con uranio-plomo.
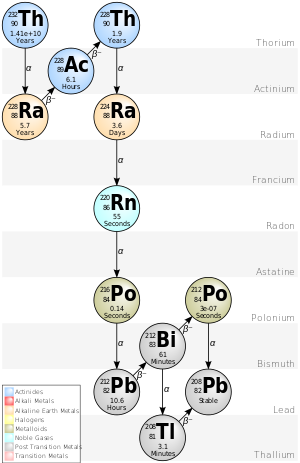
Serie de torio
La cadena 4n de Th-232 se denomina comúnmente "serie de torio" o "cascada de torio". Comenzando con el torio-232 natural, esta serie incluye los siguientes elementos: actinio, bismuto, plomo, polonio, radio, radón y talio. Todos están presentes, al menos transitoriamente, en cualquier muestra que contenga torio natural, ya sea metal, compuesto o mineral. La serie termina con plomo-208.
La energía total liberada del torio-232 al plomo-208, incluida la energía perdida por los neutrinos, es de 42,6 MeV.
| nuclide | nombre histórico (short) | nombre histórico (long) | modo de desintegración | semivida ()a=año) | energía liberada, MeV | producto de la desintegración |
|---|---|---|---|---|---|---|
| 252Cf | α | 2.645 a | 6.1181 | 248C m | ||
| 248Cm | α | 3.4×105 a | 5.162 | 244Pu | ||
| 244Pu | α | 8×107 a | 4.589 | 240U | ||
| 240U | β - | 14.1 h | .39 | 240Np | ||
| 240Np | β− | 1.032 h | 2.2 | 240Pu | ||
| 240Pu | α | 6561 a | 5.1683 | 236U | ||
| 236U | Thoruranium | α | 2.3×107 a | 4.494 | 232 Th | |
| 232Th | Th | Thorium | α | 1.405×1010 a | 4.081 | 228Ra |
| 228Ra | MsTh1 | Mesothorium 1 | β− | 5.75 a | 0,046 | 228Ac |
| 228Ac | MsTh2 | Mesothorium 2 | β− | 6.25 h | 2.124 | 228 |
| 228Th | RdTh | Radiothorium | α | 1.9116 a | 5.520 | 224Ra |
| 224Ra | ThX | Thorium X | α | 3.6319 d | 5.789 | 220Rn |
| 220Rn | Tn | Thoron, Thorium Emanation | α | 55,6 s | 6.404 | 216Po |
| 216Po | ThA | Thorium A | α | 0.145 s | 6.906 | 212Pb |
| 212Pb | ThB | Thorium B | β− | 10.64 h | 0,570 | 212B i |
| 212Bi | ThC | Thorium C | β− 64,06% α 35,94% | 60.55 min | 2.252 6.208 | 212Po 208Tl |
| 212Po | ThC | Thorium C′ | α | 299 ns | 8.784 | 208P b |
| 208Tl | ThC′ | Thorium C′ | β− | 3.053 min | 1.803 | 208Pb |
| 208Pb | ThD | Thorium D | estable | . | . | . |
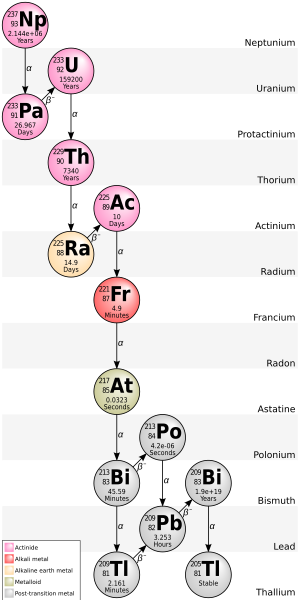
Serie de neptunio
La cadena 4n + 1 de 237 np se llama comúnmente la serie de neptunio " o " Cascade de Neptunium ". En esta serie, solo dos de los isótopos involucrados se encuentran naturalmente en cantidades significativas, a saber, los dos últimos: Bismuth-209 y Thallium-205. Algunos de los otros isótopos se han detectado en la naturaleza, que se originan en cantidades trazas de 237 np producido por la reacción de eliminación (n, 2n) en primordial 238 u. Un detector de humo que contiene una cámara de ionización de América-241 acumula una cantidad significativa de neptunio-237 a medida que su decaimiento de americio; Los siguientes elementos también están presentes, al menos transitoriamente, como productos de descomposición del neptunio: actinio, astatina, bismuto, francium, plomo, polonio, protactinio, radio, talio, torio y uranio. Dado que esta serie solo fue descubierta y estudiada en 1947-1948, sus nucleidos no tienen nombres históricos. Un rasgo único de esta cadena de descomposición es que el radón de gas noble solo se produce en una rama rara (no se muestra en la ilustración) pero no en la secuencia principal de decaimiento; Por lo tanto, el radón de esta cadena de descomposición no migra a través de la roca casi tanto como de los otros tres. Otro rasgo único de esta secuencia de descomposición es que termina en el talio en lugar de el plomo. Esta serie termina con el isótopo estable Thallium-205.
La energía total liberada de Californium-249 a Thallium-205, incluida la energía perdida por los neutrinos, es de 66.8 MeV.
| nuclide | modo de desintegración | semivida ()a=año) | energía liberada, MeV | producto de la desintegración |
|---|---|---|---|---|
| 249Cf | α | 351 a | 5.813+.388 | 245C m |
| 245Cm | α | 8500 a | 5.362+.175 | 241Pu |
| 241Pu | β - | 14.4 a | 0,021 | 241Am |
| 241Am | α | 432,7 a | 5.638 | 237Np |
| 237Np | α | 2.14·106 a | 4.959 | 233Pa |
| 233Pa | β− | 27,0 d | 0.571 | 233U |
| 233U | α | 1.592·105 a | 4.909 | 229 Th |
| 229Th | α | 7340 a | 5.168 | 225Ra |
| 225Ra | β− | 14.9 d | 0.36 | 225Ac |
| 225Ac | α | 10.0 d | 5.935 | 221Fr |
| 221Fr. | α 99.9952% β− 0,0048% | 4,8 min | 6.3 0.314 | 217At 221Ra |
| 221Ra | α | 28 s | 6.9 | 217Rn |
| 217At | α 99,992% β− 0,008% | 32 ms | 7.0 0.737 | 213Bi 217Rn |
| 217Rn | α | 540 μs | 7.9 | 213Po |
| 213Bi | β− 97,80% α 2.20% | 46,5 min | 1.423 5.87 | 213Po 209Tl |
| 213Po | α | 3.72 μs | 8.536 | 209P b |
| 209Tl | β− | 2.2 min | 3.99 | 209P b |
| 209Pb | β− | 3.25 h | 0.644 | 209 Bi |
| 209Bi | α | 1.9·1019 a | 3.137 | 205Tl |
| 205Tl | . | estable | . | . |
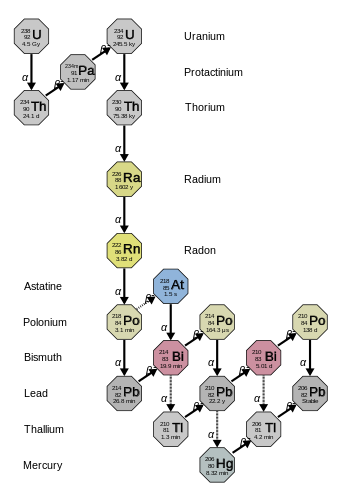
Serie de uranio
La cadena 4n+2 del uranio-238 se denomina "serie de uranio" o "serie de radio". Comenzando con el uranio-238 natural, esta serie incluye los siguientes elementos: astato, bismuto, plomo, polonio, protactinio, radio, radón, talio y torio. Todos están presentes, al menos transitoriamente, en cualquier muestra que contenga uranio natural, ya sea metal, compuesto o mineral. La serie termina con plomo-206.
La energía total liberada del uranio-238 al plomo-206, incluida la energía perdida por los neutrinos, es de 51,7 MeV.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
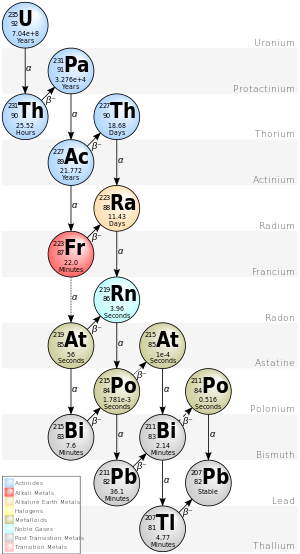
ACTINIO SERIE
La cadena 4n+3 de uranio-235 se llama comúnmente la serie de actinium " o " Actinium Cascade ". Comenzando con el isótopo U-235 natural, esta serie de descomposición incluye los siguientes elementos: Actinium, Astatine, Bismuth, Francium, Lead, Polonio, Protactinium, Radium, Radon, Thallium y Torio. Todos están presentes, al menos transitoriamente, en cualquier muestra que contenga uranio-235, ya sea metal, compuesto, mineral o mineral. Esta serie termina con el ISOTOPE estable LED-207.
La energía total liberada del uranio-235 al LED-207, incluida la energía perdida contra los neutrinos, es de 46.4 MeV.
| nuclide | nombre histórico (short) | nombre histórico (long) | modo de desintegración | semivida ()a=año) | energía liberada, MeV | producto de la desintegración |
|---|---|---|---|---|---|---|
| 251Cf | α | 900,6 a | 6.176 | 247Cm | ||
| 247C m | α | 1.56·107 a | 5.353 | 243Pu | ||
| 243Pu | β - | 4.95556 h | 0,5979 | 243Am | ||
| 243A m | α | 7388 a | 5.439 | 239Np | ||
| 239Np | β− | 2.3565 d | 0,722 | 239Pu | ||
| 239 Pu | α | 2.41·104 a | 5.244 | 235U | ||
| 235U | AcU | Actin Uranium | α | 7.04·108 a | 4.678 | 231 Th |
| 231Th | UY | Uranium Y | β− | 25.52 h | 0.391 | 231Pa |
| 231Pa | Pa | Protactinio | α | 32760 a | 5.150 | 227Ac |
| 227Ac | Ac | Actinium | β− 98,62% α 1.38% | 21.772 a | 0,045 5.042 | 227 Th 223Fr |
| 227Th | RdAc | Radioactinio | α | 18.68 d | 6.147 | 223Ra |
| 223Fr. | AcK | Actinium K | β− 99,994% α 0,006% | 22.00 min | 1.149 5.340 | 223Ra 219At |
| 223Ra | AcX | Actinio X | α | 11.43 d | 5.979 | 219Rn |
| 219At | α 97,00% β− 3.00% | 56 s | 6.275 1.700 | 215Bi 219Rn | ||
| 219Rn | An | Actinon, Actinium Emanation | α | 3.96 s | 6.946 | 215Po |
| 215Bi | β− | 7.6 min | 2.250 | 215Po | ||
| 215Po | AcA | Actinium A | α 99,99977% β− 0,00023% | 1.781 ms | 7.527 0,7515 | 211Pb 215At |
| 215At | α | 0,1 ms | 8.178 | 211Bi | ||
| 211Pb | AcB | Actinium B | β− | 36,1 min | 1.367 | 211Bi |
| 211Bi | AcC | Actinio C | α 99,724% β− 0,276% | 2.14 min | 6.751 0,575 | 207 Tl 211Po |
| 211Po | AcC ' | Actinium C' | α | 516 ms | 7.595 | 207P b |
| 207Tl | AcC" | Actinium C" | β− | 4.77 min | 1.418 | 207Pb |
| 207Pb | AcD | Actinium D | . | estable | . | . |
Contenido relacionado
TNT (desambiguación)
KL1
Ecolocalización