BRCA2
BRCA2 y BRCA2 () son un gen humano y su producto proteico, respectivamente. El símbolo oficial (BRCA2, cursiva para el gen, no cursiva para la proteína) y el nombre oficial (originalmente cáncer de mama 2; actualmente BRCA2, asociado a reparación del ADN) son mantenidos por el Comité de Nomenclatura Genética de HUGO. Un símbolo alternativo, FANCD1, reconoce su asociación con el complejo proteico FANC. Los ortólogos, denominados Brca2 y Brca2, son comunes en otras especies de vertebrados. BRCA2 es un gen supresor de tumores humanos (específicamente, un gen cuidador), que se encuentra en todos los seres humanos; su proteína, también llamada con el sinónimo proteína de susceptibilidad al cáncer de mama tipo 2, se encarga de reparar el ADN.
BRCA2 y BRCA1 normalmente se expresan en las células de la mama y otros tejidos, donde ayudan a reparar el ADN dañado o a destruir las células si el ADN no se puede reparar. Están implicados en la reparación de daños cromosómicos y desempeñan un papel importante en la reparación sin errores de roturas de doble cadena del ADN. Si el BRCA1 o el BRCA2 se dañan por una mutación de BRCA, el ADN dañado no se repara adecuadamente y esto aumenta el riesgo de cáncer de mama. BRCA1 y BRCA2 se han descrito como "genes de susceptibilidad al cáncer de mama" y "proteínas de susceptibilidad al cáncer de mama". El alelo predominante tiene una función supresora de tumores normal, mientras que las mutaciones de alta penetrancia en estos genes provocan una pérdida de la función supresora de tumores, lo que se correlaciona con un mayor riesgo de cáncer de mama.
El gen BRCA2 está ubicado en el brazo largo (q) del cromosoma 13 en la posición 12.3 (13q12.3). El gen humano de referencia BRCA2 contiene 27 exones y el ADNc tiene 10.254 pares de bases que codifican una proteína de 3.418 aminoácidos.
Función

Aunque las estructuras de las BRCA1 y BRCA2 los genes son muy diferentes, al menos algunas funciones están interrelacionadas. Las proteínas hechas por ambos genes son esenciales para reparar el ADN dañado (ver Figura de pasos de reparación recombinacional). BRCA2 une el ADN de una sola cadena e interactúa directamente con la recombinase RAD51 para estimular y mantener la invasión de hebras, un paso vital de recombinación homologosa. La localización de RAD51 a la ruptura doble de ADN requiere la formación del complejo BRCA1-PALB2-BRCA2. PALB2 (Partner and localizer of BRCA2) puede funcionar sinérgicamente con una quimera BRCA2 (termed piccolo, o piBRCA2) para promover aún más la invasión de hilos. Estos descansos pueden ser causados por radiación natural y médica u otras exposiciones ambientales, pero también ocurren cuando los cromosomas intercambian material genético durante un tipo especial de división celular que crea esperma y huevos (meiosis). Las roturas de doble cadena también se generan durante la reparación de enlaces cruzados de ADN. Mediante la reparación del ADN, estas proteínas desempeñan un papel en el mantenimiento de la estabilidad del genoma humano y la prevención de reorganizaciones genéticas peligrosas que pueden conducir a cánceres hematológicos y otros.
Se ha demostrado que BRCA2 posee un papel crucial en la protección contra la degradación nucleolítica dependiente de MRE11 de las horquillas invertidas que se forman durante la parada de la horquilla de replicación del ADN (causada por obstáculos como mutaciones, agentes intercalantes, etc.).
Al igual que BRCA1, BRCA2 probablemente regula la actividad de otros genes y desempeña un papel fundamental en el desarrollo embrionario.
Significado clínico
Ciertas variaciones del gen BRCA2 aumentan el riesgo de cáncer de mama como parte de un síndrome de cáncer de mama-ovario hereditario. Los investigadores han identificado cientos de mutaciones en el gen BRCA2, muchas de las cuales provocan un mayor riesgo de cáncer. Las mutaciones BRCA2 suelen ser inserciones o eliminaciones de una pequeña cantidad de pares de bases de ADN en el gen. Como resultado de estas mutaciones, el producto proteico del gen BRCA2 es anormal y no funciona correctamente. Los investigadores creen que la proteína defectuosa BRCA2 no puede reparar el daño del ADN que se produce en todo el genoma. Como resultado, hay un aumento en las mutaciones debido a la síntesis de translesiones propensa a errores después de un daño no reparado en el ADN, y algunas de estas mutaciones pueden hacer que las células se dividan de manera incontrolada y formen un tumor.
Las personas que tienen dos copias mutadas del gen BRCA2 tienen un tipo de anemia de Fanconi. Esta condición es causada por niveles extremadamente reducidos de la proteína BRCA2 en las células, lo que permite la acumulación de ADN dañado. Los pacientes con anemia de Fanconi son propensos a sufrir varios tipos de leucemia (un tipo de cáncer de células sanguíneas); tumores sólidos, particularmente de cabeza, cuello, piel y órganos reproductivos; y supresión de la médula ósea (producción reducida de células sanguíneas que provoca anemia). Las mujeres que han heredado un gen BRCA1 o BRCA2 defectuoso tienen riesgos de cáncer de mama y de ovario que son tan altos y parecen tan selectivos que muchas portadoras de mutaciones optan por someterse a una cirugía profiláctica. Ha habido muchas conjeturas para explicar esta especificidad tisular aparentemente sorprendente. Los principales determinantes de dónde se producen los cánceres hereditarios asociados a BRCA1 y BRCA2 están relacionados con la especificidad tisular del patógeno del cáncer, el agente que causa la inflamación crónica o el carcinógeno. El tejido diana puede tener receptores para el patógeno, quedar expuesto selectivamente a carcinógenos y a un proceso infeccioso. Un déficit genómico innato perjudica las respuestas normales y exacerba la susceptibilidad a enfermedades en los órganos diana. Esta teoría también se ajusta a los datos de varios supresores de tumores más allá de BRCA1 o BRCA2. Una ventaja importante de este modelo es que sugiere que existen algunas opciones además de la cirugía profiláctica.
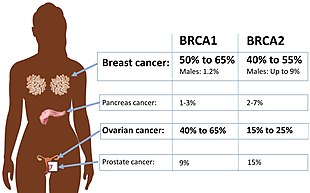
Además del cáncer de mama en hombres y mujeres, las mutaciones en BRCA2 también conducen a un mayor riesgo de cáncer de ovario, de trompas uterinas, de próstata y de páncreas. En algunos estudios, las mutaciones en la parte central del gen se han asociado con un mayor riesgo de cáncer de ovario y un riesgo menor de cáncer de próstata que las mutaciones en otras partes del gen. También se han observado varios otros tipos de cáncer en determinadas familias con mutaciones BRCA2.
En general, las mutaciones genéticas fuertemente heredadas (incluidas las mutaciones en BRCA2) representan sólo entre el 5 y el 10 % de los casos de cáncer de mama; El riesgo específico de padecer cáncer de mama u otro tipo de cáncer para cualquier persona que tenga una mutación BRCA2 depende de muchos factores.
Historia
| El gen BRCA2 fue descubierto en 1994. En 1996, Kenneth Offit y su grupo de investigación en Memorial Sloan Kettering Cancer Center identificaron con éxito la mutación más común en el gen asociado con cáncer de mama y ovario entre individuos de ascendencia judía ashkenazi.
El gen fue clonado por primera vez por científicos de Myriad Genetics, Endo Recherche, Inc., HSC Research " Development Limited Partnership, y la Universidad de Pennsylvania. Métodos para diagnosticar la probabilidad de un paciente con mutaciones en BRCA1 y BRCA2 Conseguir cáncer fue cubierto por patentes propiedad o controladas por Myriad Genetics. El modelo de negocio de Myriad de ofrecer exclusivamente la prueba diagnóstica liderada desde los inicios de Myriad como startup en 1994 a ser una empresa de comercio público con 1200 empleados y alrededor de $500M en ingresos anuales en 2012; también condujo a la polémica sobre precios altos de prueba y la indisponibilidad de segundas opiniones de otros laboratorios de diagnóstico, que a su vez llevó al hito Association for Molecular Pathology v. Myriad Genetics demanda. Mutaciones de Germline y efecto fundadorTodas las mutaciones de BRCA2 identificadas hasta la fecha han sido heredadas, lo que sugiere la posibilidad de un gran efecto "fundador" en el que una determinada mutación es común a un grupo poblacional bien definido y se puede rastrear teóricamente a un antepasado común. Dada la complejidad de la detección de mutaciones para BRCA2, estas mutaciones comunes pueden simplificar los métodos necesarios para la detección de mutaciones en ciertas poblaciones. El análisis de mutaciones que ocurren con alta frecuencia también permite el estudio de su expresión clínica. Un ejemplo llamativo de una mutación fundadora se encuentra en Islandia, donde una mutación BRCA2 (999del5) representa prácticamente todas las familias de cáncer de mama/ovarian. Esta mutación de cambio de marco conduce a un producto de proteína altamente truncado. En un estudio amplio que examina cientos de personas con cáncer y control, esta mutación 999del5 se encontró en el 0,6% de la población general. Cabe destacar que el 72% de los pacientes que fueron encontrados portadores tenían antecedentes familiares moderados o fuertes de cáncer de mama, el 28% tenía poco o ningún historial familiar de la enfermedad. Esto sugiere fuertemente la presencia de modificar genes que afectan la expresión fenotípica de esta mutación, o posiblemente la interacción de la mutación BRCA2 con factores ambientales. En el cuadro siguiente figuran ejemplos adicionales de mutaciones fundadoras en BRCA2.
MeiosisEn la planta Arabidopsis thaliana, pérdida de la BRCA2 homolog AtBRCA2 causa graves defectos en la meiosis masculina y en el desarrollo del gametocito femenino. La proteína AtBRCA2 es necesaria para la localización adecuada de la proteína compleja sinaptonómica AtZYP1 y las recombinasas AtRAD51 y AtDMC1. Además, AtBRCA2 es necesario para la correcta sinopsis meiotica. Así es probable que AtBRCA2 sea importante para la recombinación meiotica. Parece que AtBRCA2 actúa durante la meiosis para controlar los pasos de invasión de una sola carretera mediados por AtRAD51 y AtDMC1 que ocurren durante la reparación homologosa meocótica recombinacional de daños al ADN. Los Homologs de BRCA2 también son esenciales para la meiosis en el hongo Ustilago maydis, el gusano Caenorhabditis elegans, y la fruta Drosophila melanogaster. Los ratones que producen versiones truncadas de BRCA2 son viables pero estériles. Las ratas mutantes BRCA2 tienen un fenotipo de inhibición del crecimiento y esterilidad en ambos sexos. La aspermatogénesis en estas ratas mutantes se debe a un fracaso de la sinapsis cromosómica homologosa durante la meiosis. Secuencias de repetición BRCDMC1 (DNA meiotic recombinase 1) es un homolog específico de meiosis RAD51 que media el intercambio de hilos durante la reparación recombinacional homologosa. DMC1 promueve la formación de productos de invasión de cadenas de ADN (moléculas de unión) entre moléculas de ADN homologosas. El DMC1 humano interactúa directamente con cada una de una serie de secuencias de repetición en la proteína BRCA2 (llamadas repeticiones del BRC) que estimulan la formación de moléculas articulares por DMC1. Las repeticiones de BRC se conforman a un motivo que consiste en una secuencia de unos 35 aminoácidos altamente conservados que están presentes al menos una vez en todas las proteínas tipo BRCA2. El BRCA2 BRC repite estimulando la formación de moléculas articulares promoviendo la interacción del ADN monoestado (ssDNA) con DMC1. El ssDNA complejo con DMC1 puede emparejar con ssDNA homologous de otro cromosoma durante la etapa de sinopsis de la meiosis para formar una molécula conjunta, un paso central en la recombinación homologosa. Así, las secuencias de repetición BRC de BRCA2 parecen desempeñar un papel clave en la reparación recombinacional de los daños de ADN durante la recombinación meiotica. En general, parece que la recombinación homologosa durante las funciones de meiosis para reparar los daños de ADN, y que BRCA2 desempeña un papel clave en el desempeño de esta función. NeurogenesisBRCA2 es requerido en el ratón para la neurogénesis y la supresión de medulloblastoma. La pérdida de ‘BRCA2’ afecta profundamente a la neurogénesis, especialmente durante el desarrollo neural embrionario y postnatal. Estos defectos neurológicos surgen del daño del ADN. Control epigenéticoLas alteraciones epigenéticas en expresión de BRCA2 (causando sobreexpresión o subexpresión) son muy frecuentes en cánceres esporádicos (ver Tabla abajo) mientras que las mutaciones en BRCA2 raramente se encuentran. En el cáncer de pulmón de células no pequeñas, BRCA2 es reprimido epigemáticamente por la hipermetilación del promotor. En este caso, la hipermetilación promotora se asocia significativamente con la baja expresión de mRNA y la baja expresión de proteínas, pero no con la pérdida de heterocigosidad del gen. En el cáncer de ovario esporádico se encuentra un efecto opuesto. El promotor BRCA2 y las regiones de 5'-UTR tienen relativamente pocos o ningún dinucleótido CpG metilado en el ADN tumoral en comparación con el ADN no-tumor, y se encuentra una correlación significativa entre hipometilación y una sobreexpresión de BRCA2. Esto indica que la hipometilación del promotor BRCA2 y las regiones de 5'-UTR conduce a la sobreexpresión de BRCA2 mRNA. Un informe indicaba cierto control epigenético de la expresión BRCA2 por los microRNAs miR-146a y miR-148a. Expresión BRCA2 en cáncerEn los eucariotas, la proteína BRCA2 tiene un papel importante en la reparación recombinacional homologosa. En ratones y humanos, BRCA2 principalmente media el montaje ordenado de RAD51 sobre el ADN de una sola tirada (ss), la forma que es activa para la unión homologosa y la invasión de hebras. BRCA2 también redirige RAD51 del ADN doble y evita la disociación del SsDNA. Además, los cuatro paralogs de RAD51, que consisten en RAD51B (RAD51L1), RAD51C (RAD51L2), RAD51D (RAD51L3), XRCC2 forman un complejo llamado el complejo BCDX2 (ver Figura: Reparación Recombinacional de ADN). Este complejo participa en el reclutamiento o estabilización de RAD51 en los sitios de daños. El complejo BCDX2 parece actuar facilitando el montaje o la estabilidad del filamento de nucleoproteína RAD51. RAD51 cataliza la transferencia de hilo entre una secuencia rota y su homólogo no dañado para permitir la re-síntesis de la región dañada (ver modelos de recombinación homóloga). Algunos estudios sobre cánceres reportan sobreexpresados BRCA2 mientras que otros estudios reportan una subexpresión BRCA2. Al menos dos informes encontraron sobreexpresión en algunos tumores esporádicos de mama y subexpresión en otros tumores esporádicos de mama. (véase el cuadro). Muchos cánceres tienen deficiencias epigenéticas en varios genes de reparación de ADN (ver frecuencias de epimutaciones en genes de reparación de ADN en cánceres). Estas deficiencias de reparación probablemente causen mayores daños de ADN no correspondidos. La sobreexpresión de BRCA2 visto en muchos cánceres puede reflejar compensatorio BRCA2 sobreexpresión y mayor reparación recombinacional homologosa para al menos parcialmente lidiar con tales daños excesivos de ADN. Egawa et al. sugiere que el aumento de la expresión de BRCA2 puede explicarse por la inestabilidad genómica que se observa con frecuencia en cánceres, lo que induce la expresión BRCA2 mRNA debido a una creciente necesidad de BRCA2 para la reparación de ADN. Under-expression of BRCA2 en sí mismo llevaría a aumentar los daños no pagados de ADN. Los errores de replicación pasados de estos daños (ver síntesis de translesión) conducirían a mayores mutaciones y cáncer.
InteraccionesBRCA2 ha demostrado interactuar con
Arquitectura de dominioBRCA2 contiene una serie de 39 repeticiones de aminoácidos que son esenciales para la unión a RAD51 (una proteína clave en la reparación recombinacional de ADN) y la resistencia al tratamiento de metilmetanosulfonato. El dominio helicoidal BRCA2 adopta una estructura helicoidal, que consiste en un núcleo de cuatro-helix (alfa 1, alfa 8, alfa 9, alfa 10) y dos sucesivas beta-hairpins (beta 1 a beta 4). Un segmento de aproximadamente 50 aminoácidos que contiene cuatro helices cortos (alfa 2 a alfa 4), medias alrededor de la superficie de la estructura central. En BRCA2, los cálices alfa 9 y alfa 10 empacan con el dominio BRCA2 OB1 a través de contactos de van der Waals que involucran residuos hidrofóbicos y aromáticos, y también a través de bonos de hidrógeno de cadena lateral y columna vertebral. Este dominio se une a la proteína DSS1 de 70 aminoácidos (suprimida en el síndrome de las manos divididas/split pie), que fue identificada originalmente como uno de los tres genes que mapean a un locus de 1,5 Mb eliminado en un síndrome de malformación del desarrollo heredado. El dominio BRCA OB1 asume un pliegue OB, que consiste en una hoja de beta de cinco puntas muy curvada que se cierra sobre sí mismo para formar una beta-barrel. OB1 tiene un groove poco profundo formado por una cara de la hoja curvada y es demarcado por dos lazos, uno entre beta 1 y beta 2 y otro entre beta 4 y beta 5, que permite la unión débil de ADN de una sola cadena. El dominio también se une a la proteína DSS1 de 70 aminoácidos (deletado en la mano dividida/síndrome del pie del cuerpo). El dominio BRCA OB3 asume un pliegue OB, que consiste en una hoja de beta de cinco puntas muy curvada que se cierra sobre sí mismo para formar una beta-barrel. El OB3 tiene un groove pronunciado formado por una cara de la hoja curvada y es demarcado por dos lazos, uno entre beta 1 y beta 2 y otro entre beta 4 y beta 5, que permite la unión ssDNA fuerte. El dominio de la Torre adopta una estructura secundaria consistente en un par de largos, antiparalelos alfa-helices (el tallo) que soportan un paquete de tres-hijo (3HB) al final. El 3HB contiene un motivo helix-turn-helix y es similar a los dominios de unión de ADN de las recombinasas específicas del sitio bacteriano, y de los factores de transcripción eucariotas Myb y homeodomain. El dominio Torre tiene un papel importante en la función de supresor tumoral de BRCA2, y es esencial para la unión adecuada de BRCA2 al ADN. Estudios mostrados que la conformación de este dominio de torre es controlada al estestericamente por una pequeña proteína "DSS1", que interactúa con los dominios helical, OB1 y OB2 de BRCA2. Patentes, cumplimiento, litigio y controversiaLa Universidad de Utah, el Instituto Nacional de Ciencias de la Salud Ambiental (NIEHS) y Myriad Genetics en 1994 presentó una solicitud de patente para el gen y cáncer aislados BRCA1 que promueve mutaciones, así como métodos para diagnosticar la probabilidad de contraer cáncer de mama; en el próximo año, Myriad, en colaboración con otros investigadores, aisló y secuencia el gen BRCA2 e identificó mutaciones relevantes, y el primero presentó la patente. Myriad es el licenciatario exclusivo de estas patentes y las ha aplicado en los Estados Unidos contra laboratorios de diagnóstico clínico. Este modelo de negocio llevó de Myriad siendo una startup en 1994 a ser una empresa comercial pública con 1200 empleados y alrededor de $500M en ingresos anuales en 2012; también condujo a la controversia sobre altos precios y la incapacidad de obtener segundas opiniones de otros laboratorios de diagnóstico, que a su vez condujo a la histórica Asociación de Patología Molecular v. Myriad Genética demanda. Las patentes comienzan a expirar en 2014. Peter Meldrum, CEO de Myriad Genetics, ha reconocido que Myriad tiene "otras ventajas competitivas que pueden hacer que esa aplicación [patente] innecesaria" en Europa. Las decisiones legales relativas a las patentes BRCA1 y BRCA2 afectarán el campo de las pruebas genéticas en general. En junio de 2013, en Association for Molecular Pathology v. Myriad Genetics (No 12-398), la Corte Suprema de los Estados Unidos declaró unánimemente que "un segmento de ADN natural es un producto de la naturaleza y no patentado elegible simplemente porque ha sido aislado", invalidando las patentes de Myriad sobre los genes BRCA1 y BRCA2. Sin embargo, la Corte también sostuvo que la manipulación de un gen para crear algo que no se encuentra en la naturaleza todavía podría ser elegible para la protección de patentes. El Tribunal Federal de Australia llegó a la conclusión contraria, defendiendo la validez de una patente de Myriad Genetics de Australia sobre el gen BRCA1 en febrero de 2013, pero esta decisión está siendo apelada y la apelación incluirá el examen de la sentencia del Tribunal Supremo de los Estados Unidos. |