Boracina
Borazina, también conocida como borazol, es un compuesto inorgánico con la fórmula química B3H6. N3. En este compuesto cíclico se alternan las tres unidades BH y las tres unidades NH. El compuesto es isoelectrónico e isoestructural con el benceno. Por esta razón, a veces se hace referencia a la borazina como “benceno inorgánico”. Al igual que el benceno, la boracina es un líquido incoloro con olor aromático.
Síntesis
El compuesto fue descubierto en 1926 por los químicos Alfred Stock y Erich Pohland mediante una reacción de diborano con amoníaco.
La borazina se puede sintetizar mediante el tratamiento de diborane y amoníaco en una relación 1:2 a 250–300 °C con una conversión de 50%.
- 3 B2H6 + 6 NH3 → 2 B3H6N3 + 12 H2
Una ruta alternativa más eficiente comienza con borohidruro de sodio y sulfato de amonio:
- 6 NaBH4 + 3 (NH)4)2Así que...4 → 2 B3N3H6 + 3 Na2Así que...4 + 18 H2
En un proceso de dos pasos para obtener borazina, el tricloruro de boro se convierte primero en tricloroborazina:
- 3 BCl3 + 3 NH4Cl → Cl3B3H3N3 + 9 HCl
Los enlaces B-Cl se convierten posteriormente en enlaces B-H:
- 2 Cl3B3H3N3 + 6 NaBH4 → 2 B3H6N3 + 3 B2H6 + 6 NaCl
Estructura
La boracina es isoelectrónica con el benceno y tiene una conectividad similar, por lo que a veces se la denomina "benceno inorgánico". Esta comparación no es rigurosamente válida debido a la diferencia de electronegatividad entre el boro y el nitrógeno. Las determinaciones estructurales cristalográficas de rayos X muestran que las longitudes de los enlaces dentro del anillo de borazina son todas equivalentes a 1,429 Å, una propiedad compartida por el benceno. Sin embargo, el anillo de boracina no forma un hexágono perfecto. El ángulo de enlace es de 117,1° en los átomos de boro y de 122,9° en los nitrógenos, lo que le da a la molécula el grupo de puntos de simetría D3h.
La electronegatividad del boro (2,04 en la escala de Pauling) en comparación con la del nitrógeno (3,04) y también la deficiencia de electrones en el átomo de boro y el par solitario del nitrógeno favorecen estructuras mesoméricas alternativas para la borazina.
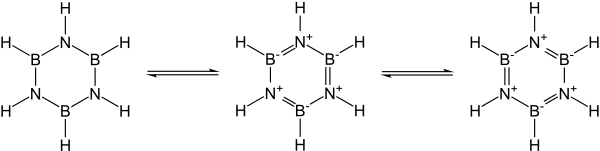
El boro se comporta como un ácido de Lewis y el nitrógeno se comporta como una base de Lewis.
Aromaticidad
Debido a sus similitudes con el benceno, se han realizado varios análisis computacionales y experimentales de la aromaticidad de la borazina. El número de electrones pi en la boracina obedece a la regla 4n + 2 y las longitudes de los enlaces B-N son iguales, lo que sugiere que el compuesto puede ser aromático. Sin embargo, la diferencia de electronegatividad entre el boro y el nitrógeno crea un reparto desigual de carga que da como resultado enlaces con mayor carácter iónico y, por lo tanto, se espera que tenga una deslocalización de electrones peor que el análogo totalmente de carbono. La boracina, con un cambio de entalpía estándar de formación ΔfH de −531 kJ/mol, es térmicamente muy estable.
Orbitales de enlace natural (NBO)
El análisis de los orbitales de enlace natural (NBO) sugiere una aromaticidad débil en la boracina. En el modelo NBO, los enlaces B-N en el anillo están ligeramente desplazados de los ejes nucleares, y B y N tienen grandes diferencias de carga. El análisis de blindaje químico natural (NCS) proporciona evidencia adicional de la aromaticidad basada en una contribución del enlace B-N π al blindaje magnético. Los cálculos basados en orbitales NBO muestran que este enlace π permite una corriente de anillo débil que contrarresta en cierta medida un campo magnético simulado en el centro del anillo de borazina. Una pequeña corriente anular sugiere cierta deslocalización.
Función de localización de electrones (ELF)
El análisis topológico del enlace de la boracina mediante la función de localización de electrones (ELF) indica que la boracina puede describirse como un compuesto aromático π. Sin embargo, el enlace en la boracina está menos deslocalizado que en el benceno debido a una diferencia en los valores de bifurcación de las cuencas electrónicas. Valores de bifurcación más grandes indican una mejor deslocalización de electrones, y se argumenta que cuando este valor de bifurcación es mayor que 0,70, la deslocalización es suficiente para designar un compuesto aromático. Para el benceno, este valor es 0,91, pero el sistema π de borazina se bifurca en el valor ELF de 0,682. Esto se debe a la diferencia de electronegatividad entre B y N, que produce una interacción de enlace más débil que la interacción C-C en el benceno, lo que lleva a una mayor localización de electrones en las unidades B-H y N-H. El valor de bifurcación está ligeramente por debajo del límite de 0,70, lo que sugiere una aromaticidad moderada.
Reactividad
Hidrólisis
La borazina se hidroliza fácilmente, produciendo ácido bórico, amoníaco e hidrógeno.
Polimerización

Calentar borazina a 70 °C expulsa hidrógeno con formación de poliborazileno:
- B3N3H6 → 1/n[B]3N3H4]n
Con halides de hidrógeno y halógenos
Con cloruro de hidrógeno forma un aducto.
- B3N3H6 + 3 HCl → B3N3H9Cl3
- Reacción de adición de borazina con cloruro de hidrógeno
- B3N3H9Cl3 + NaBH4 → (BH4N)3
- Reducción con sodio borohydride
La reacción de adición con bromo no requiere un catalizador. Las borazinas sufren un ataque nucleofílico en el boro y un ataque electrofílico en el nitrógeno.
Precursor cerámico
El nitruro de boro se puede preparar calentando poliborazileno a 1000 °C.
Las borazinas también son materiales de partida para otras cerámicas potenciales, como los carbonitruros de boro. La boracina también se puede utilizar como precursor para hacer crecer películas delgadas y capas individuales de nitruro de boro hexagonal (h-BN) en superficies catalíticas como cobre, platino, níquel, hierro y muchas más, con deposición química de vapor (CVD).

El poliborazileno se ha propuesto como medio de almacenamiento de hidrógeno reciclado para aplicaciones en vehículos con pilas de combustible de hidrógeno, utilizando un recipiente de un solo recipiente. Proceso de digestión y reducción para recrear borano de amoníaco.
Entre otros compuestos de tipo B-N, se ha predicho que las borazinas mixtas sustituidas con amino-nitro superan a los explosivos a base de carbono como el CL-20.
Compuestos relacionados
(C
2H
>2B
>2N
2) es un anillo aromático de seis miembros con dos átomos de carbono, dos átomos de nitrógeno y dos átomos de boro en pares opuestos.
1,2-Dihidro-1,2-azaborina (C
>4BNH
>6 ) es un anillo de seis miembros con cuatro átomos de carbono, un átomo de nitrógeno y un átomo de boro.
Lectura adicional
- Sneddon LG, Mirabelli MG, Lynch AT, Fazen PJ, Su K, Beck JS (1991). "Polímeros precursores de cerámica borona" (PDF). Puro Appl. Chem. 63 (3): 407-410. doi:10.1351/pac199163030407. S2CID 53629042.
- Jeon JK, Uchimaru Y, Kim DP (agosto de 2004). "Synthesis of novel amorphous boron carbonitride ceramics from the borazine derivative copolymer via hydroboration". Química Inorgánica. 43 (16): 4796–8. doi:10.1021/ic035254a. PMID 15285647.
- Paetzold P (1991). "Nuevas perspectivas en la química boron-ntrógeno - I" (PDF). Puro Appl. Chem. 63 (3): 345-350. doi:10.1351/pac199163030345. S2CID 53659373.
- Islas R (2007). "Borazine: ser o no ser aromático". Química Estructural. 18 (6): 833-839. doi:10.1007/s11224-007-9229-z. S2CID 95098134.