Bioelemento
Los bioelementos o elementos biogénicos son los elementos químicos presentes en los seres vivos. Si se analiza químicamente la materia viva se encuentra que está constituida por unos setenta elementos, casi todos los elementos estables que existen en la Tierra, salvo los gases nobles; sin embargo, alrededor del 99% de la masa de la mayoría de las células está constituida por cuatro elementos, carbono (C), hidrógeno (H), oxígeno (O), nitrógeno (N), que son mucho más abundantes en la materia viva que en la corteza terrestre.
Proporción de los bioelementos
La proporción de los diversos bioelementos es bastante diferente a la que encontramos en la atmósfera, la hidrosfera o en la corteza terrestre; esto nos indica que la vida ha seleccionado aquellos elementos que le son más adecuados para formar sus estructuras y realizar sus funciones. Por ejemplo, el carbono representa aproximadamente un 20% del peso de los organismos, pero su concentración en la atmósfera, en forma de dióxido de carbono es muy baja, por lo que los seres vivos extraen y concentran este elemento en sus tejidos.
La siguiente tabla muestra la proporción de algunos bioelementos en el cuerpo humano comparada con la que tienen en el resto de la Tierra:
| Elemento | Litosfera- atmósfera- hidrosfera (%) | Cuerpo humano (%) |
| Oxígeno (O) | 50,02 | 62,81 |
| Carbono (C) | 0,18 | 19,37 |
| Hidrógeno (H) | 0,95 | 9,31 |
| Nitrógeno (N) | 0,03 | 5,14 |
| Calcio (Ca) | 3,22 | 1,38 |
| Fósforo (P) | 0,11 | 0,64 |
| Azufre (S) | 0,11 | 0,63 |
| Sodio (Na) | 2,36 | 0,26 |
| Potasio (K) | 2,28 | 0,22 |
| Cloro (Cl) | 0,20 | 0,18 |
| Magnesio (Mg) | 2,08 | 0,04 |
| Flúor (F) | 0,10 | 0,009 |
| Hierro (Fe) | 4,18 | 0,005 |
| Aluminio (Al) | 7,30 | 0,001 |
| Manganeso (Mn) | 0,08 | 0,0001 |
| Silicio (Si) | 25,80 | - |
Según la segunda ley de la termodinámica en un sistema cerrado la entropía (desorden) tiende a incrementarse. Sin embargo, los seres vivos se mantienen ordenados respecto a su medio, "enriqueciéndose" en bioelementos relativamente poco abundantes en su medio mediante el gasto de energía.
Los bioelementos pueden clasificarse en primarios y secundarios.
Bioelementos primarios
Los bioelementos primarios son los elementos imprescindibles para formar las biomoléculas (glúcidos, lípidos, proteínas y ácidos nucleicos); son los mencionados anteriormente (C, H, O, N, P, S) y son claramente mayoritarios. El 90% corresponde al oxígeno (62%), carbono (20%) e hidrógeno (10%); el elevado porcentaje de hidrógeno y de oxígeno se explica por el hecho de que la materia viva está constituida principalmente por agua (H 2 O). La presencia de otros bioelementos primarios se explica porque sus propiedades son las idóneas para formar materia viva:
- Tienen una masa atómica relativamente pequeña que favorece la formación de enlaces covalentes estables entre sí. Son los elementos más ligeros con capacidad para formar enlaces covalentes.
- Dado que el oxígeno y el nitrógeno son muy electronegativos dan lugar a moléculas dipolares, que se disuelven bien en agua lo que facilita las reacciones metabólicas.
- El carbono, el oxígeno y el nitrógeno pueden compartir más de un par de electrones, formando enlaces dobles, lo que les dota de una gran versatilidad.
- Los compuestos formados por estos átomos se encuentran en estado muy reducido, de modo que tienden a oxidarse para formar moléculas de menor energía; la energía liberada en estas oxidaciones es aprovechada para realizar las funciones vitales de los organismos.
Carbono
Si descontamos el oxígeno y el hidrógeno del agua, el carbono es, de largo, el elemento más abundante en los seres vivos (le sigue de lejos el nitrógeno, con el 3%). Su abundancia en la materia viva se explica por sus propiedades:
- Tiene cuatro electrones en el último orbital lo que hace que tenga gran capacidad para formar enlaces covalentes estables con otros carbonos; los enlaces pueden ser simples (CC) y dobles (C=C) (raramente triples en la materia viva), formando anillos y largas cadenas estables, ramificadas o no (macromoléculas). Según el número de átomos de carbono, de enlaces simples y/o dobles y la presencia o no de anillos, cada macromolécula tiene propiedades distintas, de modo que, virtualmente, pueden existir un número ilimitado de ellas.
- Gran capacidad para unirse al hidrógeno, oxígeno, nitrógeno y azufre, aumentando enormemente la posibilidad de crear nuevos grupos funcionales (carbonilo (C=O), alcohol (C-OH), carboxilo (COOH), amina (C -NH 2 ), sulfhidrilo (C-SH), etc.) que, junto con la propiedad anterior, origina una extraordinaria diversidad de compuestos orgánicos.
- Debido a la configuración tetraédrica de los enlaces del átomo de carbono, los diferentes tipos de moléculas orgánicas tienen estructuras tridimensionales diferentes, de modo que una misma molécula, dependiendo de la posición en el espacio de sus átomos, tiene propiedades físico-químco- biológicas distintas, multiplicando así el número de compuestos con actividad biológica (por ejemplo, los estereoisómeros de los monosacáridos).
Por todos estos motivos, la materia viva está compuesta mayoritariamente por moléculas formadas por un esqueleto principal de átomos de carbono unidos entre sí que, a su vez, están enlazados con átomos de hidrógeno, oxígeno y nitrógeno. El azufre interviene en mucha menor proporción, unido también directamente a átomos de carbono; el fósforo está siempre en forma de fosfato inorgánico (PO 4 ) y no se enlaza directamente al carbono.
Hidrógeno
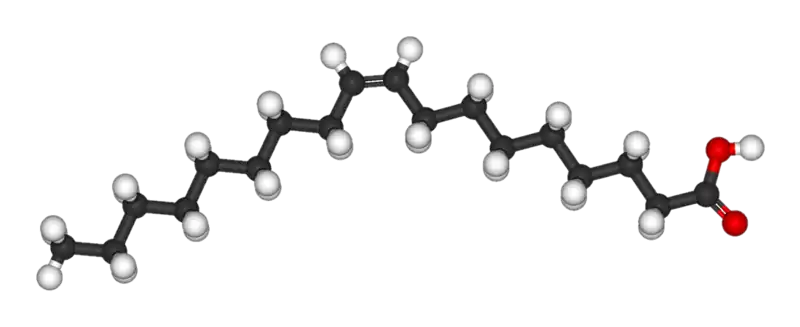
Aparte de ser uno de los componentes de la molécula de agua, el hidrógeno tiene una gran facilidad para formar enlaces covalentes con el carbono, lo suficientemente fuertes para ser estables, pero no tanto para impedir su ruptura, posibilitando así la síntesis de otras moléculas. De hecho, en las largas cadenas de carbono, el hidrógeno "llena" los enlaces que le quedan libres en el carbono; el ejemplo más evidente son los ácidos grasos, que son largas cadenas de hidrocarburos (hidrógeno + carbono) con un grupo carboxilo inicial.
El hidrógeno se combina también con el oxígeno para formar el grupo hidroxilo, muy extendido en todas las biomoléculas, ya sea formando el grupo alcohol (en glúcidos, esteroides, aminoácidos, etc.) o formando parte del grupo carboxilo (ácidos grasos), aminoácidos, grupos fosfato, etc.).
Oxígeno
El oxígeno, también componente del agua, es el bioelemento más electronegativo (con la salvedad del flúor que es muy poco abundante). Esto le hace idóneo para arrancar electrones a otros átomos, es decir, para oxidarlos; lo que conlleva la liberación de energía que puede ser aprovechada por la célula, por ejemplo, en la respiración aeróbica, que es la forma más extendida de obtener energía por parte de los seres vivos.
El esqueleto básico carbono-hidrógeno de las biomoléculas es apolar, por lo que es insoluble en agua; la presencia de oxígeno hace que las cadenas hechas de carbono e hidrógeno sean polares y se conviertan en solubles en agua, algo imprescindible para que se lleven a cabo las reacciones metabólicas.
Nitrógeno
El nitrógeno, de igual modo que el carbono y el azufre, muestra una gran facilidad al formar compuestos tanto con el hidrógeno (como el amoníaco, NH 3 ) como con el oxígeno (NO 2, NO 3 ) lo que permite la transformación de una forma a otra con liberación de energía. El nitrógeno se encuentra principalmente formando parte del grupo amino (-NH 2 ) de los aminoácidos (componentes de las proteínas) y de las bases nitrogenadas (componentes de los ácidos nucleicos). Cabe destacar que, a pesar de la gran abundancia de nitrógeno gas en la atmósfera (N 2 ), muy pocos organismos son capaces de aprovecharlo; casi todo el nitrógeno de la biosfera se incorpora a partir de nitrato (NO 3 ) inorgánico,
Azufre
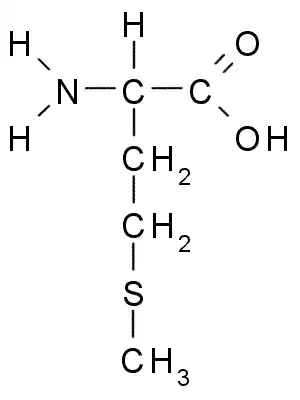
El azufre se encuentra básicamente en forma de radical sulfhidrilo (-SH) en algunos aminoácidos (como la cisteína) y coenzimas (por ejemplo, el coenzima-A). Los sulhidrilos de la cisteína pueden formar puentes disulfuro entre sí, enlaces covalentes fuertes que son clave en el establecimiento de la estructura terciaria plegada de muchas proteínas.
Fósforo
El fósforo se encuentra siempre en forma inorgánica, como ácido ortofosfórico (H 3 PO 4 ) o alguna de sus formas disociadas (fosfatos: (H 2 PO 4, HPO 4, PO 4 ), combinadas con moléculas orgánicas (como los fosfolípidos) de las membranas celulares, y los nucleótidos del ADN y ARN) Cabe destacar que los fosfatos pueden establecer enlaces ricos en energía (como el ATP), siendo claves en el intercambio de energía que se lleva a término en el metabolismo Las sales del ácido fosfórico (como el fosfato cálcico) forman parte de los huesos de los vertebrados y de los esqueletos calcáreos de algunos invertebrados.
Bioelementos secundarios
Los bioelementos secundarios son todo el resto de elementos químicos que se encuentran en la materia viva. Cuatro son relativamente abundantes (sodio (Na), potasio (K), magnesio (Mg), calcio (Ca); el resto se presentan en muy baja proporción y reciben el nombre de oligoelementos.
Sodio y potasio
El sodio y el potasio se encuentran en forma iónica, Na y K respectivamente, e intervienen en la homeostasis electrolítica de la célula y en el mantenimiento de la diferencia de potencial electroquímico a ambos lados de la membrana plasmática, donde existe una bomba de sodio-potasio que hace salir 3Na y hace entrar 2K en el citosol simultáneamente, con consumo de ATP.
Magnesio
El yo Mg es un cofactor de muchas enzimas. Es uno de los componentes de la clorofila, donde desempeña un papel central en el proceso de fotosíntesis, ya que capta dos electrones, reduciéndose de Mg a Mg, que son rápidamente arrancados por dos fotones, por lo que se vuelve a oxidar de Mg a Mg. Se podría decir que este ciclo reducción-oxidación del magnesio es el que soporta la vida en el planeta, ya que está en la base del aprovechamiento de la energía luminosa por parte de los organismos autótrofos.
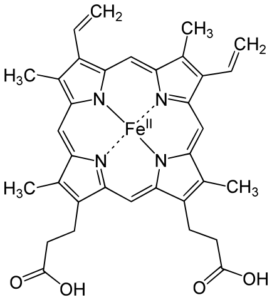
Hierro
El hierro se encuentra en prácticamente todos los seres vivos y cumple con numerosas y variadas funciones.
- Hay diferentes proteínas que contienen el grupo hemo, que consiste en el ligante porfirina con un átomo de hierro. Algunos ejemplos:
- La hemoglobina y la mioglobina; la primera transporta oxígeno, O 2, y la segunda lo almacena.
- Los citocromos; los citocromos c catalizan la reducción de oxígeno a agua. Los citocromos P450 catalizan la oxidación de compuestos hidrofóbicos, como fármacos o drogas, para que puedan ser excretados, y participan en la síntesis de distintas moléculas.
- Las peroxidasas y catalasas catalizan la oxidación de peróxidos, H 2 O 2, que son tóxicos.
- Las proteínas de hierro/azufre (Fe/S) participan en procesos de transferencia de electrones.
- También se pueden encontrar proteínas donde átomos de hierro se enlazan entre sí a través de enlaces puente de oxígeno. Se denominan proteínas Fe-O-Fe. Algunos ejemplos:
- Las bacterias metanotróficas, que emplean el metano, CH 4, como fuente de energía y de carbono, usan proteínas de este tipo, llamadas monooxigenasas, para catalizar la oxidación de este metano.
- La hemeritrina transporta oxígeno en algunos organismos marinos.
- Algunas ribonucleótido reductasas contienen hierro. Catalizan la formación de desoxinucleótidos.
Los animales para transportar el hierro dentro del cuerpo emplean unas proteínas llamadas transferrinas. Para almacenarlo emplean la ferritina y la hemoiderina. El hierro entra en el organismo al ser absorbido en el intestino delgado y es transportado o almacenado por esas proteínas. La mayor parte del hierro se reutiliza y poco se excreta.
Tanto el exceso como el defecto de hierro pueden provocar problemas en el organismo. El envenenamiento por hierro se llama hemocromatosis. En las transfusiones de sangre se emplean ligandos que forman con el hierro complejos de alta estabilidad para evitar que quede demasiado hierro libre.
Estos ligantes se conocen como sideróforos. Muchos microorganismos utilizan estos sideróforos para captar el hierro que necesitan. También se pueden utilizar como antibióticos, porque no dejan hierro libre disponible.
Yodo
El yodo es necesario para sintetizar las hormonas tiroideas, que regulan el metabolismo.
Zinc
Es abundante en el cerebro, órganos reproductores y páncreas.
Manganeso
El manganeso es cofactor de varias enzimas, entre las que destacan los encargados de degradar el superóxidos y peróxidos, moléculas muy tóxicas que se forman en ciertas reacciones metabólicas; también es un factor de crecimiento. Su deficiencia provoca el amarilleamiento de las hojas.
Cobre
El cobre forma parte de la hemocianina, el equivalente de la hemoglobina en algunos invertebrados, y actúa como cofactor de algunas enzimas oxidasas, como la citocromo c oxidasa, la lisil oxidasa y la superóxido dismutasa.
Cobalto
El cobalto forma parte de la vitamina B12 y de enzimas implicadas en la fijación de nitrógeno atmosférico.
Molibdeno
El molibdeno se encuentra en el llamado cofactor de molibdeno (COM) en distintas oxotransferasas, con la función de transferir átomos de oxígeno del agua a la vez que se produce la transferencia de dos electrones. Algunas de las enzimas que contienen este cofactor son la xantina oxidasa que oxida la xantina en ácido úrico, el aldehído oxidasa que oxida aldehídos, así como aminas y sulfuros en el hígado, la sulfito oxidasa que oxida sulfitos en el hígado, la nitrato importante en el ciclo del nitrógeno en las plantas, etc.
Contenido relacionado
Lista de tratados internacionales ambientales
Tamaño de la población
Bioma