Batrachochytrium dendrobatidis
Batrachochytrium dendrobatidis (bə-TRAY-koh-KIT-ree-əm DEN-droh-bə-ty-dis), también conocido como Bd u hongo quítrido de los anfibios, es un hongo que causa la enfermedad quitridiomicosis en los anfibios.
Desde su descubrimiento en 1998 por Lee Berger, la enfermedad devastó poblaciones de anfibios en todo el mundo, en un declive global hacia múltiples extinciones, parte de la extinción del Holoceno. Una segunda especie descrita recientemente, B. salamandrivorans, también causa quitridiomicosis y muerte en salamandras.
Los hongos patógenos que causan la enfermedad quitridiomicosis dañan la piel de ranas, sapos y otros anfibios, alterando su equilibrio de agua y sal y, finalmente, provocando insuficiencia cardíaca, según informa Nature. Algunas especies de anfibios parecen tener una capacidad innata para resistir la infección por quitridiomicosis debido a la simbiosis con Janthinobacterium lividum. Incluso dentro de las especies que generalmente sucumben, algunas poblaciones sobreviven, lo que posiblemente demuestre que estos rasgos o alelos de las especies están sujetos a la selección evolutiva.
Etymology
El nombre genérico se deriva de las palabras griegas batrachos (rana) y chytra (vasija de barro), mientras que el epíteto específico se deriva del género de ranas del que se realizó la confirmación original de patogenicidad (Dendrobates), dendrobatidis proviene del griego dendron, "árbol" y bates, "el que trepa", en referencia a un género de ranas venenosas dardo.
Sistemáticos
Batrachochytrium dendrobatidis se consideraba hasta hace poco la única especie del género Batrachochytrium. La clasificación inicial del patógeno como quitridio se basó en la ultraestructura de las zoosporas. El análisis de ADN del SSU-rDNA ha corroborado esta opinión, con la coincidencia más cercana a Chytridium confervae. En 2013 se descubrió una segunda especie de Batrachochytrium: B. salamandrivorans, que afecta principalmente a las salamandras y también causa quitridiomicosis. B. salamandrivorans se diferencia de B. dendrobatidis principalmente en la formación de tubos germinativos in vitro, la formación de talos coloniales con múltiples esporangios in vivo y una menor preferencia térmica.
Morfología

B. dendrobatidis infecta la piel queratinizada de los anfibios. El hongo de la epidermis tiene un talo que lleva una red de rizoides y esporangios de paredes lisas, aproximadamente esféricos e inoperculados (sin opérculo). Cada esporangio produce un solo tubo para descargar las esporas.
Estructura de los zoospore
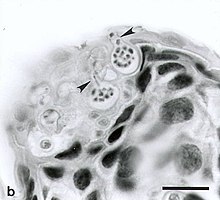
Las zoosporas de B. dendrobatidis, que suelen tener un tamaño de 3 a 5 μm, tienen un cuerpo alargado-ovoidal con un único flagelo posterior (de 19 a 20 μm de largo) y poseen un área central de ribosomas a menudo con esferas de ribosomas unidas a membranas dentro de la masa ribosómica principal. Se ha observado un pequeño espolón, ubicado en la parte posterior del cuerpo celular, adyacente al flagelo, pero esto puede ser un artefacto en las muestras fijadas con formalina. El área central de los ribosomas está rodeada por una única cisterna de retículo endoplasmático, dos a tres mitocondrias y un extenso complejo de microcuerpos y glóbulos lipídicos. Los microcuerpos se yuxtaponen y casi rodean de cuatro a seis glóbulos lipídicos (tres anteriores y uno a tres laterales), algunos de los cuales parecen estar unidos por una cisterna. Algunas zoosporas parecen contener más glóbulos lipídicos (esto puede haber sido resultado de un efecto de plano de corte, porque los glóbulos eran a menudo lobulados en las zoosporas examinadas). No se ha observado un rumposoma.
Estructura de Flagellum
Un centriolo no funcional se encuentra adyacente al cinetosoma. Nueve puntales interconectados unen el cinetosoma al plasmalema y hay una placa terminal en la zona de transición. Se ha observado una estructura similar a un anillo interno unido a los túbulos de los dobletes flagelares dentro de la zona de transición en la sección transversal. No se han observado raíces asociadas con el cinetosoma. En muchas zoosporas, el núcleo se encuentra parcialmente dentro de la agregación de ribosomas y estaba situado invariablemente lateralmente. Dentro del citoplasma, fuera del área ribosómica, se encontraron pequeñas vacuolas y un aparato de Golgi con cisternas apiladas. Las mitocondrias, que a menudo contienen una pequeña cantidad de ribosomas, están densamente teñidas con crestas discoidales.
Ciclo de vida
B. dendrobatidis tiene dos etapas de vida primarias: un zoosporangio sésil reproductivo y una zoospora móvil uniflagelada liberada del zoosporangio. Se sabe que las zoosporas están activas solo por un corto período de tiempo y pueden viajar distancias cortas de uno a dos centímetros. Sin embargo, las zoosporas son capaces de quimiotaxis y pueden moverse hacia una variedad de moléculas que están presentes en la superficie de los anfibios, como azúcares, proteínas y aminoácidos. B. dendrobatidis también contiene una variedad de enzimas proteolíticas y esterasas que lo ayudan a digerir células de anfibios y usar la piel de anfibios como fuente de nutrientes. Una vez que la zoospora llega a su huésped, forma un quiste debajo de la superficie de la piel e inicia la parte reproductiva de su ciclo de vida. Las zoosporas enquistadas se convierten en zoosporangios, que pueden producir más zoosporas que pueden reinfectar al huésped o liberarse en el entorno acuático circundante. Se ha demostrado que los anfibios infectados con estas zoosporas mueren de paro cardíaco.
Además de los anfibios, B. dendrobatidis también infecta a los cangrejos de río (Procambarus alleni, P. clarkii, Orconectes virilis y O. immunis), pero no a los peces mosquito (Gambusia holbrooki).
Fisiología
B. dendrobatidis puede crecer en un amplio rango de temperaturas (4-25 °C), siendo las temperaturas óptimas entre 17 y 25 °C. El amplio rango de temperaturas para el crecimiento, incluida la capacidad de sobrevivir a 4 °C, le da al hongo la capacidad de hibernar en sus huéspedes, incluso cuando las temperaturas en los ambientes acuáticos son bajas. La especie no crece bien a temperaturas superiores a 25 °C, y el crecimiento se detiene por encima de los 28 °C. Las ranas arbóreas de ojos rojos infectadas (Litoria chloris) se recuperaron de sus infecciones cuando se las incubó a una temperatura de 37 °C.
Varying forms
B. dendrobatidis se ha encontrado ocasionalmente en formas distintas de sus etapas tradicionales de zoospora y esporangios. Por ejemplo, antes de la ola de calor europea de 2003 que diezmó las poblaciones de la rana acuática Rana lessonae a causa de la quitridiomicosis, el hongo existía en los anfibios como organismos esféricos, unicelulares, confinados en parches diminutos (de 80 a 120 micrómetros de diámetro). Estos organismos, desconocidos en ese momento, fueron posteriormente identificados como B. dendrobatidis. Las características de los organismos sugerían zoosporas enquistadas; es posible que hayan incorporado una espora en reposo, un saprobio o una forma parasitaria del hongo que no es patógena.
Hábitat y relación con los anfibios
El hongo crece en la piel de los anfibios y produce zoosporas acuáticas. Está muy extendido y se distribuye desde los bosques de tierras bajas hasta las frías cimas de las montañas. A veces es un parásito no letal y posiblemente un saprófito. El hongo está asociado con la mortalidad del huésped en las tierras altas o durante el invierno, y se vuelve más patógeno a temperaturas más bajas.
Distribución geográfica
Se ha sugerido que B. dendrobatidis se originó en África o Asia y posteriormente se extendió a otras partes del mundo a través del comercio de ranas africanas con uñas (Xenopus laevis). En este estudio, se examinaron 697 especímenes archivados de tres especies de Xenopus, recolectadas previamente entre 1879 y 1999 en el sur de África. El primer caso de quitridiomicosis se encontró en un espécimen de X. laevis de 1938. El estudio también sugiere que la quitridiomicosis había sido una infección estable en el sur de África durante 23 años antes de encontrar a alguien infectado fuera de África. Hay información más reciente de que la especie se originó en la península de Corea y se extendió a través del comercio de ranas.
Se cree que las ranas toro americanas (Lithobates catesbeianus), también ampliamente distribuidas, también son portadoras de la enfermedad debido a su baja susceptibilidad inherente a la infección por B. dendrobatidis. La rana toro a menudo escapa del cautiverio y puede establecer poblaciones salvajes donde puede introducir la enfermedad en nuevas áreas. También se ha demostrado que B. dendrobatidis puede sobrevivir y crecer en suelo húmedo y en plumas de aves, lo que sugiere que B. dendrobatidis también puede propagarse en el medio ambiente a través de las aves y el transporte de tierra. Las infecciones se han relacionado con la mortalidad masiva de anfibios en América del Norte, América del Sur, América Central, Europa y Australia. B. dendrobatidis ha sido implicada en la extinción de la rana diurna de hocico puntiagudo (Taudactylus acutirostris) en Australia.
Se ha identificado una amplia variedad de huéspedes anfibios susceptibles a la infección por B. dendrobatidis, incluidas las ranas de bosque (Lithobates sylvatica), la rana de patas amarillas de montaña (Lithobates muscosa), la salamandra de dos líneas del sur (Eurycea cirrigera), la salamandra de San Marcos (Eurycea nana), la salamandra de Texas (Eurycea neotenes), la salamandra de los manantiales del río Blanco (Eurycea pterophila), la salamandra de los manantiales de Barton (Eurycea sosorum), la salamandra de la meseta de Jollyville (Eurycea tonkawae), el Ambystoma jeffersonianum, la rana coro occidental (Pseudacris triseriata), la rana grillo del sur (Acris gryllus), el sapo de espuelas oriental (Scaphiopus holbrooki), la rana leopardo del sur (Lithobates sphenocephala), la rana leopardo del Río Grande (Lithobates berlandieri) y el tritón sardo (Euproctus platycephalus). y especies de ranas endémicas, la rana de Beysehir en Turquía (Pelophylax caralitanus).
Asia sudoriental
Si bien la mayoría de los estudios sobre B. dendrobatidis se han realizado en varios lugares del mundo, la presencia del hongo en el sudeste asiático sigue siendo un desarrollo relativamente reciente. No se conoce el proceso exacto a través del cual se introdujo el hongo en Asia; sin embargo, como se mencionó anteriormente, se ha sugerido que el transporte de especies portadoras asintomáticas (por ejemplo, Lithobates catesbeianus, la rana toro americana) puede ser un componente clave en la diseminación del hongo, al menos en China. Los estudios iniciales demostraron la presencia del hongo en estados/países insulares como Hong Kong, Indonesia, Taiwán y Japón. Poco después, países de Asia continental como Tailandia, Corea del Sur y China informaron sobre la incidencia de B. dendrobatidis entre sus poblaciones de anfibios. Se ha dedicado mucho esfuerzo a clasificar la herpetofauna en países como Camboya, Vietnam y Laos, donde se descubren con frecuencia nuevas especies de ranas, sapos y otros anfibios y reptiles. Al mismo tiempo, los científicos toman muestras de la herpetofauna para determinar si estos animales recién descubiertos poseen rastros del hongo.
En Camboya, un estudio mostró que B. dendrobatidis prevalece en todo el país en áreas cercanas a Phnom Penh (en un pueblo a <5 km), Sihanoukville (ranas recolectadas del mercado local), Kratie (ranas recolectadas de las calles alrededor de la ciudad) y Siem Reap (ranas recolectadas de una reserva nacional: Centro Angkor para la Conservación de la Biodiversidad). Otro estudio en Camboya cuestionó el potencial impacto antropológico en la diseminación de B. dendrobatidis en las poblaciones locales de anfibios en 3 áreas diferentes en relación con la interacción humana: baja (un bosque aislado en la cima de una montaña que la gente rara vez visita), media (un camino forestal a ~15 km de un pueblo que se usa al menos una vez a la semana) y alta (un pequeño pueblo donde los humanos interactúan con su entorno a diario). Usando PCR cuantitativa, evidencia de B. Se encontró B. dendrobatidis en los tres sitios, con el mayor porcentaje de anfibios positivos para el hongo en el camino forestal (impacto medio; 50%), seguido del bosque de montaña (impacto bajo; 44%) y la aldea (impacto alto; 36%). La influencia humana probablemente explica la detección del hongo en las áreas medias y altas, sin embargo, no proporciona una explicación adecuada de por qué incluso anfibios aislados fueron positivos para B. dendrobatidis. Esto puede quedar sin respuesta hasta que se realicen más investigaciones sobre la transmisión del hongo a través de paisajes. Sin embargo, evidencia reciente sugiere que los mosquitos pueden ser un posible vector que puede ayudar a propagar B. dendrobatidis. Otro estudio en la Guayana Francesa informa una infección generalizada, con 8 de 11 sitios muestreados que dieron positivo para infección por B. dendrobatidis para al menos una especie. Este estudio sugiere que Bd está más extendido de lo que se pensaba anteriormente.
Efecto sobre los anfibios
Las poblaciones de anfibios en todo el mundo han estado en constante declive debido a un aumento en la enfermedad quitridiomicosis, causada por este hongo Bd. Bd puede introducirse en un anfibio principalmente a través de la exposición al agua, colonizando los dedos y las superficies ventrales del cuerpo del animal con mayor intensidad y extendiéndose por todo el cuerpo a medida que el animal madura. Los efectos potenciales de este patógeno son hiperqueratosis, hiperplasia epidérmica, úlceras y, lo más destacado, el cambio en la regulación osmótica que a menudo conduce a un paro cardíaco. La tasa de mortalidad de los anfibios depende de una variedad de factores, pero lo más importante es la intensidad de la infección. Algunas ranas adoptan el desprendimiento de piel como un mecanismo de defensa para B. dendrobatidis; sin embargo, esto no siempre es efectivo, ya que la mortalidad fluctúa entre especies. Por ejemplo, la rana Fletcher, a pesar de que se despoja de su piel, sufre una tasa de mortalidad especialmente alta cuando se infecta con la enfermedad en comparación con especies similares como Lim. peronii y Lim. tasmaniensis. Se ha descubierto que algunas especies de anfibios se adaptan a la infección después de una mortandad inicial, siendo las tasas de supervivencia de los individuos infectados y no infectados iguales.
Según un estudio de la Universidad Nacional de Australia, se estima que el hongo Bd ha causado la disminución de 501 especies de anfibios, aproximadamente el 6,5 por ciento del total mundial conocido. De ellas, 90 han desaparecido por completo y otras 124 especies han disminuido en más del 90 por ciento, y las probabilidades de que las especies afectadas se recuperen y alcancen una población saludable son dudosas. Sin embargo, estas conclusiones fueron criticadas por estudios posteriores, que propusieron que el Bd no era un factor tan importante de la disminución de los anfibios como se había descubierto en el estudio anterior.
Un anfibio en particular que ha sido afectado gravemente por Batrachochytrium dendrobatidis (Bd) es el Lithobates clamitans. El Bd mata a esta rana al interferir con el intercambio externo de agua, lo que provoca un desequilibrio en el intercambio iónico que conduce a una insuficiencia cardíaca.
Inmunity
Algunas especies de anfibios son inmunes al Bd o tienen protección biológica contra el hongo. Una de estas salamandras es la salamandra alpina o S. atra. Estas salamandras tienen varias subespecies, pero comparten un rasgo común: la toxicidad. Un estudio de 2012 demostró que ninguna salamandra alpina de la zona tenía la enfermedad, a pesar de su prevalencia en la zona. Las salamandras alpinas pueden producir productos alcaloides u otros péptidos tóxicos que pueden ser protectores contra los microbios.
Véase también
- hongos patógenos
- Declina en poblaciones anfibias
- Ranavirus
Referencias
- ^ Berger L, Speare R, Daszak P, Green DE, Cunningham AA, Goggin CL, Slocombe R, Ragan MA, Hyatt AD, McDonald KR, Hines HB, Lips KR, Marantelli G, Parkes H (julio de 1998). "La hitridiomycosis causa la mortalidad anfibia asociada a la disminución de la población en los bosques lluviosos de Australia y Centroamérica". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 95 (15): 9031–6. Código:1998PNAS...95.9031B. doi:10.1073/pnas.95.15.9031. PMC 21197. PMID 9671799.
- ^ a b c d Longcore JE, Pessier AP, Nichols DK (1999). "Batrachochytrium Dendrobatidis gen. et sp. nov, un patógeno chytrid a los anfibios". Mis disculpas. 91 (2): 219–227. doi:10.2307/3761366. JSTOR 3761366.
- ^ "Etymologia: Batrachochytrium salamandrivorans". Emerg Infect Dis. 22 (7): 1282. Julio 2016. doi:10.3201/eid2207.ET2207. PMC 4918143.
- ^ a b Martel, A.; Spitzen-van der Sluijs, A.; Blooi, M.; Bert, W.; Ducatelle, R.; Fisher, M. C.; Woeltjes, A.; Bosman, W.; Chiers, K.; Bossuyt, F.; Pasmans, F. (2013). "Batrachochytrium salamandrivorans sp. nov. causes lethal chytridiomycosis in anphibians". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 110 (38): 15325–15329. Código:2013PNAS..11015325M. doi:10.1073/pnas.1307356110. PMC 3780879. PMID 24003137.
- ^ a b Garner TW, Perkins MW, Govindarajulu P, Seglie D, Walker S, Cunningham AA, Fisher MC (septiembre de 2006). "El emergente patógeno anfibio Batrachochytrium dendrobatidis infecta globalmente a poblaciones de la rana de toros norteamericanos, Lithobates catesbeiana". Cartas de Biología. 2 (3): 455–459. doi:10.1098/rsbl.2006.0494. PMC 1686185. PMID 17148429.
- ^ Moss AS, Reddy NS, Dortaj IM, San Francisco MJ (2008). "Chemotaxis del patógeno anfibio Batrachochytrium dendrobatidis y su respuesta a una variedad de atacantes". Mis disculpas. 100 (1): 1–5. doi:10.3852/mycologia.100.1.1. PMID 18488347.
- ^ Symonds EP, Trott DJ, Bird PS, Mills P (2008). "Características del crecimiento y actividad enzimática Batrachochytrium dendrobatidis isolates". Mycopathologia. 166 (3): 143–147. doi:10.1007/s11046-008-9135-y. PMID 18568420. S2CID 8545084.
- ^ Berger L, Hyatt AD, Speare R, Longcore JE (diciembre de 2005). "Las etapas del ciclo de vida de los anfibios chytrid Batrachochytrium dendrobatidis". Enfermedades de los organismos acuáticos. 68 (1): 51–63. doi:10.3354/dao068051. PMID 16465834.
- ^ Voyles J, Young S, Berger L, Campbell C, Voyles WF, Dinudom A, Cook D, Webb R, Alford RA, Skerratt LF, Speare R (2009). "Patogénesis de quitritomcosis, causa de declives anfibios catastróficos". Ciencia. 326 (5952): 582-585. Código:2009Sci...326..582V. doi:10.1126/ciencia.1176765. PMID 19900897. S2CID 52850132.
- ^ McMahon, T. A.; Brannelly, L. A.; Chatfield, M. W.; Johnson, P. T.; Joseph, M. B.; McKenzie, V. J.; Richards-Zawacki, C. L.; Venesky, M. D.; Rohr, J. R. (2013). "McMahon, Taegan A. et al "Chytrid fungus Batrachochytrium dendrobatidis tiene anfitriones y libera químicos que causan patología en ausencia de infección". Actas de la Academia Nacional de Ciencias 110.1 (2013): 210-215. Web. 01 Nov. 2020". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 110 (1): 210-5. doi:10.1073/pnas.1200592110. PMC 3538220. PMID 23248288.
- ^ a b Piotrowski JS, Annis S, Longcore JE (2004). "Physiology of Batrachochytrium dendrobatidis, un patógeno quítrico de anfibios". Mis disculpas. 96 (1): 9–15. doi:10.2307/3761981. JSTOR 3761981. PMID 21148822.
- ^ Woodhams DC, Alford RA, Marantelli G (junio de 2003). "Enfermedad emergente de anfibios curada por temperatura corporal elevada". Dis. Aquat. Org. 55 (1): 65–7. doi:10.3354/dao055065. PMID 12887256.
- ^ Di Rosa I, y otros (2007). "¿La Causa Proximada de las Ranas?". Naturaleza. 447 (7144): E4–E5. Código:2007Natur.447....4R. doi:10.1038/nature05941. PMID 17538572. S2CID 4421285.
- ^ Ron SR (2005). "Predecir la distribución del patógeno anfibio B. dendrobatidis en el Nuevo Mundo". Biotropica. 37 (2): 209–221. doi:10.1111/j.1744-7429.2005.00028.x. S2CID 84272576.
- ^ Daszak P, Cuningham AA, Hyatt AD (2003). "La enfermedad de la infección y la población anfibia disminuye". Divers. Distrib. 9 (2): 141–150. Código:2003DivDi...9..141D. doi:10.1046/j.1472-4642.2003.00016.x. S2CID 16838374.
- ^ a b Weldon C, du Preez LH, Hyatt AD, Muller R, Spears R (diciembre de 2004). "Origin of the anphibian chytrid fungus". Infecto emergente. Dis. 10 (12): 2100-5. doi:10.3201/eid1012.030804. PMC 3323396. PMID 15663845.
- ^ "Frog-Killing Fungus encontrado para tener orígenes en la península coreana". El New York Times. 2018-05-10. ISSN 0362-4331. Retrieved 2018-05-20.
- ^ Kats LB, Ferrer RP (2003). "Depredadores extranjeros y declives anfibios: revisión de dos décadas de ciencia y transición a la conservación". Diversidad y distribuciones. 9 (2): 99–110. Código:2003DivDi...9...99K. doi:10.1046/j.1472-4642.2003.00013.x. S2CID 85969277.
- ^ Daszak P, Strieby A, Cunningham AA, Longcore JE, Brown CC, Porter D (2004). "Experimental evidence that the bullfrog (Rana catesbeiana) es un portador potencial de chytridiomycosis, una enfermedad fúngica emergente de anfibios". Herpetological Journal. 14: 201–207.
- ^ Johnson ML, Speare R (julio de 2005). "Posibles modos de difusión del quitrid anfibio Batrachochytrium dendrobatidis en el medio ambiente" (PDF). Dis. Aquat. Org. 65 (3): 181–6. doi:10.3354/dao065181. PMID 16119886.
- ^ Lips KR (1999). "La mortalidad materna y la declinación poblacional de los anuranos en un sitio continental en el oeste de Panamá". Conservation Biology. 13 (1): 117–125. Bibcode:1999ConBi..13..117L. doi:10.1046/j.1523-1739.1999.97185.x. S2CID 86205459.
- ^ Daszak P, Cunningham AA, Hyatt AD (2003). "La enfermedad infecciosa y la población anfibia disminuye" (PDF). Diversidad y distribuciones. 9 (2): 141–50. Código:2003DivDi...9..141D. doi:10.1046/j.1472-4642.2003.00016.x. S2CID 16838374. Archivado desde el original (PDF) el 2008-12-26.
- ^ Herrera RA, Steciow MM, Natale GS (2005). "Chytrid fungus parasitizing the wild anphibian Leptodactylus ocellatus (Anura: Leptodactylidae) in Argentina". Enfermedades de los organismos acuáticos. 64 (3): 247–52. doi:10.3354/dao064247. PMID 15997823.
- ^ Schloegel LM, Hero JM, Berger L, Speare R, McDonald K, Daszak P (2006). "El declive de la rana del día afilada (Taudactylus acutiostris): el primer caso documentado de extinción por infección en una especie de vida silvestre libre?". EcoHealth. 3: 35–40. CiteSeerX 10.1.1.602.3591. doi:10.1007/s10393-005-0012-6. S2CID 11114174.
- ^ Reeves MK (2008). "Batrachochytrium dendrobatidis en ranas de madera (Lithobates sylvatica) de Three National Wildlife Refuges in Alaska, USA". Herpetological Review. 39 (1): 68–70.
- ^ Andre SE, Parker J, Briggs CJ (2008). "Efecto de la temperatura en la respuesta del huésped a la infección de Batrachochytrium dendrobatidis en la rana de color amarillo de montaña (Lithobates muscosa)". Journal of Wildlife Diseases. 44 (3): 716-720. doi:10.7589/0090-3558-44.3.716. PMID 18689660.
- ^ Byrne MW, Davie EP, Gibbons JW (2008). "Batrachochytrium dendrobatidis sucesos Eurycea cirrigera". Sureste Naturalista. 7 (3): 551–555. doi:10.1656/1528-7092-7.3.551. S2CID 84713825.
- ^ Gaertner JP, Forstner MR, O'Donnell L, Hahn D (2009). "Detección de Batrachochytrium dendrobatidis en especies endémicas de salamandra del centro de Texas". EcoHealth. 6 (1): 20–26. doi:10.1007/s10393-009-0229-x. PMID 19424755. S2CID 23997421.
- ^ Brodman R, Briggler JT (2008). "Batrachochytrium dendrobatidis dentro Ambystoma jeffersonianum larvas en el sur de Indiana". Herpetological Review. 39 (3): 320-321.
- ^ a b Lehtinen RM, Kam Y-C Richards CL (2008). "Evaluaciones preliminares para Batrachochytrium dendrobatidis en Taiwán". Herpetological Review. 39 (3): 317-318.
- ^ Lovich R, Ryan MJ, Pessier AP, CLaypool B (2008). "Infección con el hongo Batrachochytrium dendrobatidis en un no nativo Lithobates berlandieri debajo del nivel del mar en el Valle de Coachella, California, USA". Herpetological Review. 39 (3): 315-317.
- ^ Bovero S, Sotgiu G, Angelini C, Doglio S, Gazzaniga E, Cunningham AA, Garner TW (2008). "Detección de chytridiomycosis causada por Batrachochytrium dendrobatidis en el nuevote sardiniano en peligro (Euproctus platycephalus), en el sur de Cerdeña, Italia". Journal of Wildlife Diseases. 44 (3): 712-715. doi:10.7589/0090-3558-44.3.712. PMID 18689659.
- ^ Erismis UC, Konuk M, Yoldas T, Agyar P, Yumuk D, Korcan SE (2014). "Vio de los anfibios endémicos de Turquía para el hongo chytrid Batrachochytrium dendrobatidis, en Turquía" (PDF). Journal of Wildlife Diseases. 111 (2): 153–157. doi:10.3354/dao02742. PMID 25266902.
- ^ Bai, C.; T. W. Garner & Y. Li (2010). "Primera evidencia de Batrachochytrium dendrobatidis en China: descubrimiento de chytridiomycosis en ranas toroamericanas introducidas y anfibios nativos en la provincia de Yunnan, China". Dis Aquat Org. 92 (1): 241–244. doi:10.1007/s10393-010-0307-0. PMID 20372969. S2CID 24321977.
- ^ Rowley J, Chan SK, Tang WS, Speare R, Skerratt LF, Alford RA, Cheung KS, Ho CY, Campbell R (2007). "Vivienda para el anfibioquítrido Batrachochytrium dendrobatidis en Hong Kong en anfibios nativos y en el comercio anfibio internacional". Enfermedades de los organismos acuáticos. 78 (2): 87–95. doi:10.3354/dao01861. PMID 18286805.
- ^ Kusrini MD, Skerratt LF, Garland S, Berger L, Endarwin W (2008). "Chytridiomycosis in frogs of Mount Gede Pangrango, Indonesia" (PDF). Enfermedades de los organismos acuáticos. 82 (3): 187–194. doi:10.3354/dao01981. PMID 19244970.
- ^ Fisher MC, Garner TW, Walker SF (2009). "Emergencia mundial Batrachochytrium dendrobatidis y anfibio chytridiomycosis inspace, time, and host". Examen anual de la microbiología. 63: 291–310. doi:10.1146/annurev.micro.091208.073435. PMID 19575560.
- ^ McLeod DS, Sheridan JA, Jiraungkoorskul W, Khonsue W (2008). "A survey for chytrid hongus in Thai anphibians". Raffles Bulletin of Zoology. 56: 199-204.
- ^ Yang H; H. Baek; R. Speare; R. Webb; S. Park; T. Kim; K.C. Lasat er; S. Shin; S. Son; J. Park; M. Min; Y. Kim; K. Na; H. Lee " S. Park (2008). "Primera detección del hongo anfibio chytrid Batrachochytrium dendrobatidis en poblaciones libres de anfibios en Asia continental: encuesta en Corea del Sur". Dis Aquat Org. 86 (1): 9–13. doi:10.3354/dao02098. PMID 19899344.
- ^ Wei, Y.; K. Xu; D.-Z. Zhu; X.-F. Chen " X.-L. Wang (2010). "Primer estudio de primera línea para Batrachochytrium dendrobatidis en Rana dybowskii salvaje en la provincia de Heilongjiang, China". Dis Aquat Org. 92 (3): 241–244. doi:10.3354/dao02172. PMID 21268987.
- ^ Gaertner JP, Mendoza JA, Forstner MR, Neang T, Hahn D (2011). "Detección de Batrachochytrium dendrobatidis en ranas de diferentes lugares en Camboya". Herpetological Review. 42: 546-548.
- ^ Mendoza JA, Gaertner JP, Holden J, Forstner MR, Hahn D (2011). "Detección de Batrachochytrium dendrobatidis on anphibians in Pursat Province, Cambodia". Herpetological Review. 42: 542-545.
- ^ Courtois EA, Gaucher P, Chave J, Schmeller DS (2015). "Occurrencia de Bd en Guayana Francesa, Sudamérica". PLOS ONE. 10 (4): e0125128. Bibcode:2015PLoSO..1025128C. doi:10.1371/journal.pone.0125128. PMC 4406614. PMID 25902035.
- ^ "Chytridiomycosis". www.amphibiaweb.org. Retrieved 2016-05-27.
- ^ Wu, Nicholas C. (abril 2023). "La carga patógena predice la perturbación funcional anfitriona: un metaanálisis de un panzoótico fungo anfibio". Ecología funcional. 37 (4): 900–914. Bibcode:2023FuEco...37..900W. doi:10.1111/1365-2435.14245. ISSN 0269-8463.
- ^ Wu, Nicholas C.; Cramp, Rebecca L.; Ohmer, Michel E. B.; Franklin, Craig E. (2019-01-27). "Epidérmica: desentrañar la patogénesis de la quitridimiocosis". Journal of Experimental Biology. 222 (Pt 2). doi:10.1242/jeb.191817. ISSN 1477-9145. PMID 30559300.
- ^ Wu, Nicholas C.; Cramp, Rebecca L.; Franklin, Craig E. (2018-02-27). "El tamaño del cuerpo influye en costos energéticos y osmoregulatorios en ranas infectadas con Batrachochytrium dendrobatidis". Scientific Reports. 8 (1): 3739. Bibcode:2018NatSR...8.3739W. doi:10.1038/s41598-018-22002-8. ISSN 2045-2322. 5829222. PMID 29487313.
- ^ DiRenzo, Graziella; Zipkin, Elise; Grant, Evan Campbell; Royle, J. Andrew; Longo, Ana; Zamudio, Kelly; Lips, Karen (3 de octubre de 2018). "El rescate evolutivo promueve la coexistencia entre los anfitriones y los patógenos". Aplicaciones ecológicas. 28 (8): 1948–1962. Código:2018EcoAp..28.1948D. doi:10.1002/eap.1792. PMID 30368999.
- ^ Yong, Ed (2019-03-28). "La peor enfermedad jamás grabada". El Atlántico. Retrieved 2019-03-28.
- ^ Lambert, Max R.; Womack, Molly C.; Byrne, Allison Q.; Hernández-Gómez, Obed; Noss, Clay F.; Rothstein, Andrew P.; Blackburn, David C.; Collins, James P.; Crump, Martha L.; Koo, Michelle S.; Nanjappa, Priya (2020-03-20). "El acuerdo sobre "la panzoótica fungosa anfibia causa una pérdida catastrófica y continua de la biodiversidad". Ciencia. 367 (6484): eaay1838. doi:10.1126/science.aay1838. ISSN 0036-8075. PMID 32193293.
- ^ Pereira, K. E.; Woodley, S. K. (2021-01-11). "Defensores de piel de salamandras norteamericanas contra un hongo mortal salamandra". Conservación de animales. 24 (4): 552-567. Bibcode:2021AnCon..24..552P. doi:10.1111/acv.12666. ISSN 1367-9430. S2CID 232030040.
- ^ a b R, Lötters, S Kielgast, J Sztatecsny, M Wagner, N Schulte, U Werner, P Rödder, D Dambach, J Reissner, T Hochkirch, A Schmidt, B (2012-04-30). Absence of infection with the anphibian chytrid fungus in the terrestrial Alpine salamander, Salamandra atra. Deutsche Gesellschaft für Herpetologie und Terrarienkunde (DGHT). OCLC 1030045649.
{{cite book}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ a b DE MEESTER, Gilles; ŠUNJE, Emina; PRINSEN, Els; VERBRUGGEN, Erik; VAN DAMME, Raoul (2020-10-13). "La variación toxina entre las poblaciones salamandra: discutir las causas potenciales y las direcciones futuras". Zoología Integrativa. 16 3): 336–353 doi:10.1111/1749-4877.12492. Hdl:10067/1718680151162165141. ISSN 1749-4877. PMID 32965720. S2CID 221862886.
- ^ Lüddecke, Tim; Schulz, Stefan; Steinfartz, Sebastian; Vences, Miguel (2018-09-04). "El arsenal tóxico de un salamandra: revisión de la diversidad de veneno de la piel y función en los verdaderos salamandras, género Salamandra". La Ciencia de la Naturaleza. 105 (9–10): 56. Bibcode:2018SciNa.105...56L. doi:10.1007/s00114-018-1579-4. ISSN 0028-1042. S2CID 253637272.
Más lectura
- Daszak, Peter; Berger L; Cunningham AA; Hyatt AD; Green DE; Speare R. (1999). "Las nuevas enfermedades infecciosas y la población anfibia descifran". Enfermedades Infecciosas Emergentes. 5 (6): 735–748. doi:10.3201/eid0506.990601. PMC 2640803. PMID 10603206.
- Johnson, Megan L.; Speare, Richard (agosto de 2003). "Survival of Batrachochytrium dendrobatidis in Water: Quarantine and Disease Control Implications". Enfermedades Infecciosas Emergentes. 9 (8): 915–921. doi:10.3201/eid0908.030145. PMC 3020615. PMID 12967488.
Enlaces externos
- Chytrid Fungi Online en la Universidad de Alabama
- Batrachochytrium dendrobatidis en MycoBank.
- Batrachochytrium dendrobatidis dentro Índice Fungorum