Astrovirus
Los astrovirus (Astroviridae) son un tipo de virus que se descubrió por primera vez en 1975 utilizando microscopios electrónicos después de un brote de diarrea en humanos. Además de los humanos, los astrovirus ahora se han aislado de numerosas especies animales mamíferas (y se clasifican como género Mamastrovirus) y de especies aviares como patos, pollos y pavitos (clasificados como género Avastrovirus). Los astrovirus son virus icosaédricos de 28 a 35 nm de diámetro que tienen una estructura superficial característica similar a una estrella de cinco o seis puntas cuando se observan con microscopio electrónico. Junto con Picornaviridae y Caliciviridae, Astroviridae comprende una tercera familia de virus sin envoltura cuyo genoma está compuesto de ARN monocatenario de sentido positivo. El astrovirus tiene un genoma de ARN monocatenario de sentido positivo no segmentado dentro de una cápside icosaédrica sin envoltura. Numerosos estudios han demostrado que los astrovirus humanos son una causa importante de gastroenteritis en niños pequeños en todo el mundo. En los animales, los astrovirus también causan infecciones del tracto gastrointestinal, pero también pueden provocar encefalitis (en humanos y ganado), hepatitis (aviar) y nefritis (aviar).
Microbiología
Taxonomía
Esta familia de virus consta de dos géneros: Avastrovirus (AAstV) y Mamastrovirus (MAstV).
El Comité Internacional de Taxonomía de Virus (ICTV) estableció a los Astroviridae como una familia viral en 1995. Se han reportado más de 50 astrovirus, aunque el ICTV reconoce oficialmente 22 especies. El género Avastrovirus comprende tres especies: astrovirus del pollo (virus de la nefritis aviar tipos 1-3), astrovirus del pato (astrovirus del pato C-NGB) y astrovirus del pavo (astrovirus del pavo 1). El género Mamastrovirus incluye los astrovirus bovinos 1 y 2, astrovirus humanos (tipos 1-8), astrovirus felino 1, astrovirus porcino 1, astrovirus del visón 1 y astrovirus ovino 1.
Estructura
Ciclo de vida
Morfología
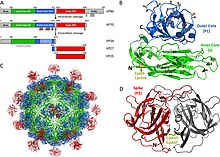
Los astrovirus son virus sin envoltura de 28-30 nm con simetría icosaédrica T-3. Tienen formas esféricas y constan de una cubierta proteica llamada cápside. Los astrovirus tienen proyecciones distintivas en forma de estrella de cinco o seis puntas en el 10% de los viriones (los otros viriones tienen superficies lisas). La cápside del virión se expresa a partir de un ARNm subgenómico y su precursor sufre múltiples escisiones para formar la proteína VP70. Las cápsides que están hechas de la proteína VP70 son escindidas por tripsina para formar partículas que son muy infecciosas (VP25/26, VP27/29 y VP34). Las espigas que crean la apariencia de estrella en la superficie del virión están hechas de dos proteínas estructurales (VP25 y VP27), mientras que la cubierta de la cápside está hecha de VP34.
Genome
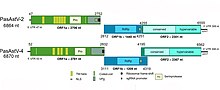
Los astrovirus tienen un genoma compuesto por una sola hebra de ARN de sentido positivo. La hebra tiene una cola de poli A en el extremo 3', pero no tiene capuchón 5' sino que está unida a una proteína VPg. Con la exclusión de la poliadenilación en el extremo 3', el genoma tiene entre 6,8 y 7,9 kb de longitud. El genoma está organizado en tres marcos de lectura abiertos (ORFs), con un solapamiento de aproximadamente 70 nucleótidos entre ORF1a y ORF1b. El ORF restante se conoce como ORF2. ORF2 codifica las proteínas estructurales, que son -al menos- VP26, VP29 y VP32, siendo la más antigénica e inmunogénica de estas VP26. Esta proteína probablemente esté involucrada en los primeros pasos de la infección viral, siendo un factor clave en el ciclo biológico de los astrovirus. Se ha estimado que la tasa de mutación del genoma del astrovirus humano es de 3,7 × 10−3 sustituciones de nucleótidos por sitio por año, con una tasa de cambios sinónimos de 2,8 × 10−3 sustituciones de nucleótidos por sitio por año. La capacidad de recombinación genética parece estar presente en los astrovirus humanos de tipo 3 y tipo 4, y en las cepas de astrovirus porcinos.
Replicación
La replicación de los astrovirus se produce en el citoplasma. El ARN de los astrovirus es infeccioso y funciona como ARN mensajero para ORF1a y ORF1b; se cree que la iniciación de la traducción está mediada por VPg, de forma similar a Caliciviridae. Un mecanismo de cambio de marco entre estos dos polipéptidos no estructurales traduce la ARN polimerasa dependiente de ARN (RdRp). En los complejos de replicación cerca de las membranas intracelulares, ORF1a y ORF1b se escinden para generar proteínas no estructurales individuales que participan en la replicación. RdRp transcribe el ARN subgenómico a partir del promotor subgenómico, lo que permite una mayor producción de proteínas estructurales. El ARN subgenómico contiene ORF2, que codifica la proteína precursora de la cápside (VP90). VP90 se escinde proteolíticamente durante el empaquetamiento y produce cápsides inmaduras formadas por VP70. Tras la encapsidación, las cápsides inmaduras se liberan de la célula sin lisis. Los viriones extracelulares son escindidos por la tripsina y forman viriones infecciosos maduros.
Evolución
La cápside de los Astroviridae está relacionada con la de los Tymoviridae. La región no estructural está relacionada con la de los Potyviridae. Parece que este grupo de virus puede haber surgido en algún momento del pasado como resultado de un evento de recombinación entre dos virus distintos y que esto incluso ocurrió en la unión de las regiones codificantes estructurales y no estructurales.
Especies infectadas
Avastrovirus

Los virus Avastrovirus 1-3 se asocian con infecciones entéricas en pavos, patos, pollos y gallinas de guinea. En los pavitos de 1 a 3 semanas de edad, algunos síntomas de enteritis incluyen diarrea, apatía, ingestión de hígado y nerviosismo. Estos síntomas suelen ser leves, pero en los casos de enteritis y síndrome de mortalidad de los pavitos (PEMS), que tiene como síntomas deshidratación, disfunción inmunológica y anorexia, la mortalidad es alta. El examen post mortem de los intestinos de las aves infectadas muestra intestinos llenos de líquido. También se observa hiperplasia de enterocitos en estudios histopatológicos. Sin embargo, a diferencia de otros virus entéricos, no hay suministro de vellosidades.
Las especies de avastrovirus suelen infectar sitios extraintestinales como el riñón o el hígado, lo que provoca hepatitis y nefritis. Las aves infectadas por el virus de la nefritis aviar suelen morir en las 3 semanas siguientes a la infección. Las partículas virales se pueden detectar en la materia fecal en el plazo de 2 días y la máxima eliminación del virus se produce entre 4 y 5 días después de la infección. El virus se puede encontrar en el riñón, el yeyuno, el bazo, el hígado y la bolsa sinovial de las aves infectadas. Los síntomas de esta enfermedad incluyen diarrea y pérdida de peso. Las necropsias muestran riñones hinchados y descoloridos y hay evidencia de muerte de las células epiteliales y nefritis intersticial linfocítica. Otro avastrovirus extraintestinal es el virus de la hepatitis aviar que infecta a los patos. La hepatitis en patos causada por este astrovirus del pato (DAstV) suele ser mortal.
En las aves, los avastrovirus se detectan mediante la técnica ELISA de captura de antígeno. En ausencia de vacunas, la higiene es la forma predominante de prevenir las infecciones por avastrovirus.
Mamastrovirus
Los mamastrovirus suelen causar gastroenteritis en los mamíferos infectados. En los animales, la gastroenteritis no suele diagnosticarse porque la mayoría de las infecciones por astrovirus son asintomáticas. Sin embargo, en los visones y los seres humanos, los astrovirus pueden causar diarrea y ser mortales. El período de incubación del mamastrovirus es de 1 a 4 días. Cuando aparecen síntomas, el período de incubación es seguido por diarrea durante varios días. En los visones, los síntomas incluyen un aumento de la secreción de las glándulas apocrinas. Los astrovirus humanos se asocian con gastroenteritis en niños y adultos inmunodeprimidos. Entre el 2 y el 8 % de las gastroenteritis agudas no bacterianas en niños se asocian con astrovirus humanos. Estas partículas virales suelen detectarse en las células epiteliales del duodeno. En las ovejas, se encontraron astrovirus ovinos en las vellosidades del intestino delgado.
Los mamastrovirus también causan enfermedades del sistema nervioso. Estas enfermedades se dan con mayor frecuencia en el ganado, los visones y los seres humanos. En el ganado, esto ocurre esporádicamente e infecta a animales individuales. Los síntomas de esta infección incluyen convulsiones, decúbito lateral y alteración de la coordinación. Los exámenes histológicos mostraron necrosis neuronal y gliosis de la corteza cerebral, el cerebelo, la médula espinal y el tronco encefálico.
Signos y síntomas en humanos
Las infecciones humanas suelen ser autolimitadas, pero también pueden propagarse sistemáticamente e infectar a personas inmunodeprimidas.
Los astrovirus causan con mayor frecuencia infecciones del tracto gastrointestinal, pero en algunos animales pueden causar encefalitis (en humanos y en ganado), hepatitis (en aves) y nefritis (en aves).
Diagnosis
Se han utilizado la microscopía electrónica, el enzimoinmunoensayo (ELISA), la inmunofluorescencia y la reacción en cadena de la polimerasa para detectar partículas virales, antígenos o ácidos nucleicos virales en las heces de personas infectadas. Se ha descrito un método que utiliza la RT-PCR en tiempo real, que puede detectar todos los genotipos de astrovirus humanos. Algunas técnicas de RT-qPCR pueden detectar simultáneamente astrovirus humanos y otros virus entéricos asociados con la gastroenteritis. También se utilizan microarrays para diferenciar entre los ocho serotipos diferentes de astrovirus humanos.
Patogenesis
Los astrovirus causan gastroenteritis al provocar la destrucción del epitelio intestinal, lo que conduce a la inhibición del mecanismo de absorción habitual, la pérdida de las funciones secretoras y la disminución de la permeabilidad epitelial en los intestinos. Se observó que las respuestas inflamatorias no afectaban la patogénesis de los astrovirus.
Epidemiología
La incidencia de infecciones por astrovirus varía según la estación. En los climas templados, la infección es mayor durante los meses de invierno, posiblemente debido a las temperaturas más bajas que mejoran la estabilidad del virus. Esto contrasta con las regiones tropicales, donde la prevalencia es mayor durante la estación lluviosa. La distribución estacional en los climas tropicales se puede explicar por el efecto de la lluvia, particularmente en el deterioro del saneamiento en los países en desarrollo.
Los astrovirus humanos se transmiten por vía fecal-oral. La principal vía de transmisión de los astrovirus es a través de alimentos y agua contaminados. Los niños pequeños que viven en guarderías o los adultos que viven en cuarteles militares son los más propensos a contraer la enfermedad. Los astrovirus humanos pueden liberarse en grandes cantidades en las heces de las personas infectadas y contaminar las aguas subterráneas, el agua dulce y el agua marina debido al tratamiento inadecuado de las aguas residuales. Las frutas y verduras cultivadas en aguas contaminadas también pueden actuar como fuentes de infección viral. Las malas prácticas de manipulación de alimentos, la mala higiene de las manos y la contaminación de objetos inanimados son otros factores que favorecen la transmisión de virus entéricos.
Los astrovirus también pueden transmitirse a los humanos a partir de otras especies animales. En comparación con las personas que no tuvieron contacto con pavos, los trabajadores de mataderos de pavos tenían tres veces más probabilidades de dar positivo en la prueba de anticuerpos contra astrovirus de pavos. Además, algunos astrovirus de humanos, patos, pollos y pavos están relacionados filogenéticamente y comparten características genéticas.
Prevención
Los astrovirus humanos pueden prevenirse mediante la detección e inactivación en alimentos y agua contaminados, además de la desinfección de fómites contaminados.
Tratamiento
Astrovirus Immunoglobulina
En un estudio realizado por Bjorkholm et al., a un paciente de 78 años diagnosticado con macroglobulinemia de Waldenström se le administraron 0,4 g/kg de inmunoglobulina contra astrovirus durante cuatro días y los síntomas desaparecieron, lo que llevó a una recuperación completa del astrovirus; sin embargo, aún se deben realizar más pruebas.
Achyrocline bogotensis terapia antiviral
En un estudio realizado por Tellez et al., se utilizaron extractos de una planta, Achyrocline bogotensis, para desarrollar una terapia antiviral tanto para el rotavirus como para el astrovirus. La Achyrocline bogotensis se utilizaba habitualmente para infecciones cutáneas y urinarias. La metodología de prueba del fármaco implicó la aplicación del extracto a las células para el pretratamiento (bloqueo), la actividad viral directa (evidencia de la eliminación del virus) y el tratamiento (una disminución de la carga viral después de que se establece una infección). El extracto demostró una actividad viral directa al eliminar los astrovirus directamente y un tratamiento al provocar una disminución de la carga viral después de una infección establecida. No se observó ningún efecto previo al tratamiento durante el experimento.
Timeline
1975: Appleton y Higgins descubrieron por primera vez el astrovirus en muestras de heces de niños que sufrían gastroenteritis mediante microscopía electrónica (ME).
1975: Madeley y Cosgrove denominaron Astrovirus a la partícula viral de 20-30 nm, basándose en su apariencia de estrella en la microscopía electrónica.
1976-1992: Lee y Kurtz serotipificaron 291 muestras de heces de astrovirus en Oxford; descubrieron los serotipos 6 y 7
1981: Lee y Kurtz lograron cultivar astrovirus en un cultivo de tejido dependiente de tripsina utilizando células de riñón de embrión humano (HEK)
1985: Lee y Kurtz descubren dos serotipos de astrovirus que se utilizan para tipificar 13 cepas de astrovirus adquiridos en la comunidad
1987: Gray et al. descubrieron que un brote de gastroenteritis que duró 22 días en un asilo de ancianos fue causado por astrovirus tipo 1 y calicivirus
1988: Hermann y Hudson utilizan la caracterización de antígenos de astrovirus cultivados con HEK para desarrollar anticuerpos monoclonales
1992: Cruz et al. analizaron 5.000 muestras de heces. El 7,5% de las enfermedades diarreicas encontradas en niños ambulatorios rurales de Guatemala fueron causadas por astrovirus.
1993: Jiang et al. secuencian el ARN del astrovirus y determinan la presencia de tres ORF y el desplazamiento del marco ribosómico
1993: Monroe et al. clasifican los datos subgenómicos de los astrovirus, lo que respalda su clasificación como una familia viral.
1994: Oishi et al. determinan que el astrovirus es la principal causa de gastroenteritis en las escuelas de la ciudad de Katano, Osaka, Japón
1995: Bjorkholm y col. llevaron a cabo un estudio clínico y trataron con éxito con inmunoglobulina intravenosa a un paciente de 78 años con macroglobulinemia de Waldenström y gastroenteritis asociada a astrovirus.
1995: Jonassen et al. utilizan PCR para detectar todos los serotipos conocidos (7) de astrovirus
1995: En su sexto informe, el ICTV establece a Astroviridae como una familia viral
1996: Glass et al. señalan un cambio epidemiológico con respecto a los astrovirus debido a las mejoras en la RT-PCT (PCR de transcripción inversa), los anticuerpos monoclonales y los inmunoensayos enzimáticos (EIA); los astrovirus ahora se consideran una de las principales causas de enfermedades diarreicas en todo el mundo.
1996: Palombo y Bishop, epidemiología de las infecciones por astrovirus en niños que sufren gastroenteritis en Melbourne, Australia (los datos recopilados incluyen incidencia total, diversidad genética y caracterización de serotipos)
1998: Unicomb et al. realizan un estudio clínico en Bangladesh y concluyen que las infecciones por astrovirus implican enfermedades diarreicas nosocomiales, agudas y persistentes.
1998: Gaggero et al. identifican al astrovirus humano tipo 1 como la principal causa de gastroenteritis aguda en niños chilenos
1999: Bon et al. descubren un astrovirus en un brote de gastroenteritis en Dijon, Francia
2001: Dennehy et al. recolectaron muestras de heces de niños hospitalizados que sufrían gastroenteritis aguda; se determinó que el astrovirus era la segunda causa principal de gastroenteritis después del rotavirus.
2002: Guix et al. completan un estudio epidemiológico sobre la presencia de astrovirus en Barcelona, España; la incidencia total de astrovirus en 2.347 muestras fue de 4,95 con un pico en el número de casos en el invierno
2003: Basu et al. descubrieron astrovirus en el 2,7% de las muestras de heces recogidas de 346 niños que padecían gastroenteritis en Gaborone, Botswana
2009: Finkbeiner et al. utilizaron la secuenciación de Sanger para descubrir un nuevo astrovirus en muestras de heces de niños que sufrieron un brote de gastroenteritis aguda en una guardería
2009: Kapoor et al., mediante RT-PCR, descubren nuevas cepas de astrovirus HMOAstV especies A, B y C que son muy similares a los astrovirus encontrados en especies de visones y ovinos; esto demostró que el virus puede tener la capacidad de saltar de una especie a otra.
Referencias
- ^ Madeley CR, Cosgrove BP (septiembre de 1975). "Carta: 28 partículas nm en heces en gastroenteritis infantil". Lancet. 2 (7932): 451–2. doi:10.1016/S0140-6736(75)90858-2. PMID 51251. S2CID 54289244.
- ^ a b c Brown DW, Gunning KB, Henry DM, Awdeh ZL, Brinker JP, Tzipori S, Herrmann JE (enero de 2008). "A DNA oligonucleotide microarray for detecting human astrovirus serotypes". Journal of Virological Métodos. 147 (1): 86–92. doi:10.1016/j.jviromet.2007.07.028. PMC 2238180. PMID 17905448.
- ^ Matsui SM, Kiang D, Ginzton N, Chew T, Geigenmüller-Gnirke U (2001). "Biología molecular de los astrovirus: Destacados seleccionados". Gastroenteritis Virus: Simposio de la Fundación Novartis 238. Novartis Foundation Symposia. Vol. 238. pp. 219–33, discussion 233–6. doi:10.1002/0470846534.ch13. ISBN 978-0-470-84653-7. PMID 11444028.
- ^ a b c d e f g h Maclachlan NJ, Dubovi EJ, Barthold SW, Swayne DE, Winton JR (2017). Veterinaria de Fenner Virología (Fifth ed.). Amsterdam: Elsevier/Academic Press. ISBN 978-0-12-800946-8.
- ^ Taxonomía de virus: clasificación y nomenclatura de virus: Noveno Informe del Comité Internacional de Taxonomía de Virus. (2012) Ed: King, A.M.Q., Adams, M.J., Carstens, E.B. y Lefkowitz, E.J. San Diego: Elsevier.
- ^ a b c Bosch A, Pintó RM, Guix S (2014). "Astrovirus humano". Microbiología clínica Reseñas. 27 (4): 1048-1074. doi:10.1128/CMR.00013-14. ISSN 0893-8512. PMC 4187635. PMID 25278582.
- ^ a b c d Bosch A, Pintó RM, Guix S (octubre de 2014). "Astrovirus humano". Microbiología clínica Reseñas. 27 (4): 1048–74. doi:10.1128/CMR.00013-14. PMC 4187635. PMID 25278582.
- ^ Krishna NK (2005). "Identificación de dominios estructurales involucrados en la biología astróvirus capsid". Inmunología Viral. 18 (1): 17–26. doi:10.1089/vim.2005.18.17 PMC 1393289. PMID 15802951.
- ^ "Zona Viral". ExPASy. Retrieved 12 de junio 2015.
- ^ Dong J, Dong L, Méndez E, Tao Y (agosto 2011). "La estructura Cristal del astrólogo humano capsid spike". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 108 (31): 12681–6. Bibcode:2011PNAS..10812681D. doi:10.1073/pnas.1104834108. PMC 3150915. PMID 21768348.
- ^ "Astroviridae ~ ViralZone". viralzone.expasy.org. Retrieved 21 de mayo 2021.
- ^ Geigenmüller U, Ginzton NH, Matsui SM (1o de febrero de 1997). "Construcción de un clon de cDNA de longitud genoma para el serotipo 1 del astrovirus humano y síntesis de transcripciones de ARN infecciosas". Journal of Virology. 71 (2): 1713-1717. doi:10.1128/JVI.71.2.1713-1717.1997. ISSN 0022-538X. 191237. PMID 8995706.
- ^ Marczinke B, Bloys AJ, Brown TD, Willcocks MM, Carter MJ, Brierley I (1 de septiembre de 1994). "La región de codificación de polimerasa dependiente del ARN dependiente del astrovirus humano se expresa por el cambio de marco ribosomal". Journal of Virology. 68 (9): 5588–5595. doi:10.1128/JVI.68.9.5588-5595.1994. ISSN 0022-538X. 236959. PMID 8057439.
- ^ Speroni S, Rohayem J, Nenci S, Bonivento D, Robel I, Barthel J, Luzhkov VB, Coutard B, Canard B, Mattevi A (17 de abril de 2009). "Análisis estructural y bioquímico del astrovirus patógeno humano Serine Protease en 2 Resolución". Journal of Molecular Biology. 387 (5): 1137–1152. doi:10.1016/j.jmb.2009.02.044. ISSN 0022-2836. PMID 19249313.
- ^ Arias CF, DuBois RM (19 enero 2017). "El Astrovirus Capsid: A Review". Viruses. 9 1): 15. doi:10.3390/v9010015. ISSN 1999-4915. PMC 5294984. PMID 28106836.
- ^ Willcocks MM, Brown TD, Madeley CR, Carter MJ (julio de 1994). "La secuencia completa de un astrovirus humano". El Diario de Virología General. 75 (7): 1785-8. doi:10.1099/0022-1317-75-7-1785. PMID 8021608.
- ^ Payne S (2017). Family Astroviridae. Prensa Académica. ISBN 9780128031094.
- ^ Royuela E, Sánchez-Fauquier A (enero de 2010). "La clonación molecular, la expresión y la primera caracterización antígena del astrovirus humano VP26 proteína estructural y una forma eliminada C-terminal". Inmunología comparada, microbiología y enfermedades infecciosas. 33 (1): 1–14. doi:10.1016/j.cimid.2008.07.010. PMID 18790534.
- ^ Babkin IV, Tikunov AY, Zhirakovskaia EV, Netesov SV, Tikunova NV (marzo de 2012). "La alta tasa evolutiva del astrovirus humano". Infección, genética y evolución. 12 (2): 435–42. Código:2012 InfGE..12..435B. doi:10.1016/j.meegid.2012.01.019. PMID 22326537.
- ^ Medici MC, Tummolo F, Martella V, Banyai K, Bonerba E, Chezzi C, et al. (junio 2015). "Heterogeneidad genética y recombinación en astrovirus humano tipo 3. " Infección, genética y evolución. 32: 156–60. Código: 2015 InfGE..32..156M. doi:10.1016/j.meegid.2015.03.011. Hdl:11586/158908. PMID 25784567.
- ^ Martella V, Medici MC, Terio V, Catella C, Bozzo G, Tummolo F, et al. (diciembre 2013). "Diversión de linaje y recombinación en astrovirus humano tipo 4. " Infección, genética y evolución. 20: 330–5. Código:2013 InfGE..20..330M. doi:10.1016/j.meegid.2013.09.015. Hdl:10447/88045. PMID 24084291.
- ^ Lv SL, Zhang HH, Li JY, Hu WQ, Song YT, Opriessnig T, Xiao CT (octubre 2019). "High genetic diversity and recombination events of porcine astrovirus strains identified from ill and asymptomatic pigs in 2017, Hunan Province, China". Virus Genes. 55 (5): 673–681. doi:10.1007/s11262-019-01692-w. Hdl:20.500.11820/5e7c9e5b-ce5c-4bfc-94dc-c490d04b159b. PMID 31372920. S2CID 199380888.
- ^ Dong J, Dong L, Méndez E, Tao Y (2 agosto 2011). "La estructura Cristal del astrólogo humano capsid spike". Actas de la Academia Nacional de Ciencias. 108 (31): 12681–12686. Código:2011PNAS..10812681D. doi:10.1073/pnas.1104834108. ISSN 0027-8424. PMC 3150915. PMID 21768348.
- ^ Geigenmüller U, Ginzton NH, Matsui SM (1o de febrero de 1997). "Construcción de un clon de cDNA de longitud genoma para el serotipo 1 del astrovirus humano y síntesis de transcripciones de ARN infecciosas". Journal of Virology. 71 (2): 1713-1717. doi:10.1128/JVI.71.2.1713-1717.1997. ISSN 0022-538X. 191237. PMID 8995706.
- ^ Méndez E, Murillo A, Velázquez R, Burnham A, Arias CF (7 septiembre 2012). "Ciclo de replicación de los Astrovirus". Astrovirus Research: 19–45 doi:10.1007/978-1-4614-4735-1_2. PMC 7121303.
- ^ Marczinke B, Bloys AJ, Brown TD, Willcocks MM, Carter MJ, Brierley I (1 de septiembre de 1994). "La región de codificación de polimerasa dependiente del ARN dependiente del astrovirus humano se expresa por el cambio de marco ribosomal". Journal of Virology. 68 (9): 5588–5595. doi:10.1128/JVI.68.9.5588-5595.1994. ISSN 0022-538X. 236959. PMID 8057439.
- ^ Speroni S, Rohayem J, Nenci S, Bonivento D, Robel I, Barthel J, Luzhkov VB, Coutard B, Canard B, Mattevi A (17 de abril de 2009). "Análisis estructural y bioquímico del astrovirus patógeno humano Serine Protease en 2 Resolución". Journal of Molecular Biology. 387 (5): 1137–1152. doi:10.1016/j.jmb.2009.02.044. ISSN 0022-2836. PMID 19249313.
- ^ Kelly AG, Netzler NE, White PA (octubre 2016). "Acontecimientos científicos de recombinación y los orígenes del virus de la hepatitis E". BMC Biología Evolutiva. 16 (1): 210. Código:2016BMCEE..16..210K. doi:10.1186/s12862-016-0785-y. PMC 5062859. PMID 27733122.
- ^ Jindal N, Patnayak DP, Ziegler AF, Lago A, Goyal SM (mayo de 2009). "Reproducción experimental del síndrome de enteritis de poult: hallazgos clínicos, respuesta al crecimiento y microbiología". Poultry Science. 88 (5): 949-58. doi:10.3382/ps.2008-00490. PMC 7107170. PMID 19359682.
- ^ Swayne DE, Glisson JR (2013). Enfermedades de la poesía. John Wiley & Sons, Incorporated. ISBN 9781118720028.
- ^ Fu Y, Pan M, Wang X, Xu Y, Xie X, Knowles NJ, et al. (mayo de 2009). "Secuencia completa de un astrovirus pato asociado con hepatitis fatal en patitos". El Diario de Virología General. 90 1104-1108. doi:10.1099/vir.0.008599-0. PMID 19264607.
- ^ Cortez V, Freiden P, Gu Z, Adderson E, Hayden R, Schultz-Cherry S (febrero de 2017). "Persistent Infections with Diverse Co-Circulating Astroviruses in Pediatric Oncology Patients, Memphis, Tennessee, USA". Enfermedades Infecciosas Emergentes. 23 (2): 288-290. doi:10.3201/eid2302.161436. PMC 5324824. PMID 28098537.
- ^ "Astroviridae - Virus de ARN de sentido positivo - Virus de ARN de sentido positivo (2011)". International Committee on Taxonomy of Viruses (ICTV). Retrieved 1 de mayo 2020.
- ^ Bouzalas IG, Wüthrich D, Walland J, Drögemüller C, Zurbriggen A, Vandevelde M, et al. (septiembre de 2014). Onderdonk AB (ed.). " Astrovirus neurotrópico en ganado con encefalitis no estimulante en Europa". Journal of Clinical Microbiology. 52 (9): 3318–24. doi:10.1128/JCM.01195-14. PMC 4313157. PMID 24989603.
- ^ Bouzalas IG, Wüthrich D, Walland J, Drögemüller C, Zurbriggen A, Vandevelde M, et al. (septiembre de 2014). " Astrovirus neurotrópico en ganado con encefalitis no estimulante en Europa". Journal of Clinical Microbiology. 52 (9): 3318–24. doi:10.1128/JCM.01195-14. PMC 4313157. PMID 24989603.
- ^ "La Epidemiología de los Astrovirus". web.stanford.edu. Retrieved 15 de octubre 2016.
- ^ "Astroviruses - Enfermedad Infecciosa y Agentes Antimicrobianos". www.antimicrobe.org. Retrieved 15 de octubre 2016.
- ^ "Astroviridae". web.stanford.edu. Retrieved 11 de noviembre 2016.
- ^ Wunderli W, Meerbach A, Guengoer T, Berger C, Greiner O, Caduff R, Trkola A, Bossart W, Gerlach D, Schibler M, Cordey S (11 de noviembre de 2011). "Astrovirus Infection in Hospitalized Infants with Severe Combined Immunodeficiency after Allogeneic Hematopoietic Stem Cell Transplantation". PLOS ONE. 6 (11): e27483. Bibcode:2011PLoSO...627483W. doi:10.1371/journal.pone.0027483. ISSN 1932-6203. PMC 3214048. PMID 22096580.
- ^ Dubovi EJ (30 noviembre 2016). Veterinaria de Fenner Virología (Fifth ed.). Elsevier Science. ISBN 978-0-12-800946-8.
- ^ Guix S, Bosch A, Pintó RM (2005). "El diagnóstico y la clasificación del astrovirus humano: perspectivas actuales y futuras". Cartas en Microbiología Aplicada. 41 (2): 103–5. doi:10.1111/j.1472-765X.2005.01759.x. PMID 16033504. S2CID 20344500.
- ^ Royuela E, Negredo A, Sánchez-Fauquier A (abril de 2006). "Desarrollo de un método RT-PCR en tiempo real para la detección sensible del astrovirus humano". Journal of Virological Métodos. 133 (1): 14–9. doi:10.1016/j.jviromet.2005.10.012. PMID 16321452.
- ^ Liu Y, Xu ZQ, Zhang Q, Jin M, Yu JM, Li JS, et al. (julio de 2012). "Detección simultánea de siete virus entericos asociados a la gastroenteritis aguda por un ensayo basado en Luminex múltiple". Journal of Clinical Microbiology. 50 (7): 2384–9. doi:10.1128/JCM.06790-11. PMC 3405628. PMID 22518865.
- ^ Bosch A, Pintó RM, Guix S (octubre de 2014). "Astrovirus humano". Microbiología clínica Reseñas. 27 (4): 1048–74. doi:10.1128/cmr.00013-14. PMC 4187635. PMID 25278582.
- ^ Monroe SS, Holmes JL, Belliot GM (2001). "Epídemiología molecular de los astrovirus humanos". Gastroenteritis Virus: Simposio de la Fundación Novartis 238. Novartis Foundation Symposia. Vol. 238. pp. 237–45, discussion 245–9. doi:10.1002/0470846534.ch14. ISBN 978-0-470-84653-7. PMID 11444029.
- ^ "Las enfermedades infecciosas en Inglaterra y Gales: enero a marzo de 1999". Informe sobre enfermedades transmisibles. CDR Suplemento. 9 (4): S1-20. Julio 1999. PMID 10434464.
- ^ a b Glass RI, Noel J, Mitchell D, Herrmann JE, Blacklow NR, Pickering LK y otros (1996). "La epidemiología cambiante de la gastroenteritis asociada al astrovirus: una revisión". Gastroenteritis viral. Archivos de Virología Suplemento. Vol. 12. pp. 287–300. doi:10.1007/978-3-7091-6553-9_31. ISBN 978-3-211-82875-5. PMID 9015126.
- ^ Koopmans MP, Bijen MH, Monroe SS, Vinjé J (enero de 1998). "Seroprevalencia de neutralización de anticuerpos a los tipos de astrovirus 1 a 7 en humanos en Holanda". Inmunología de laboratorio clínico y diagnóstico. 5 (1): 33–7. doi:10.1128/CDLI.5.1.33-37.1998. PMC 121387. PMID 9455876.
- ^ Midthun K, Greenberg HB, Kurtz JB, Gary GW, Lin FY, Kapikian AZ (abril de 1993). "Caracterización y seroepidemiología de un astrovirus tipo 5 asociado con un brote de gastroenteritis en el condado de Marin, California". Journal of Clinical Microbiology. 31 (4): 955–62. doi:10.1128/JCM.31.4.955-962.1993. PMC 263593. PMID 8385155.
- ^ Abad FX, Villena C, Guix S, Caballero S, Pintó RM, Bosch A (septiembre 2001). "Potential role of fomites in the vehicular transmission of human astroviruses". Microbiología aplicada y ambiental. 67 (9): 3904–7. Bibcode:2001 ApEnM.67.3904A. doi:10.1128/AEM.67.9.3904-3907.2001. PMC 93108. PMID 11525984.
- ^ Todd EC, Greig JD, Bartleson CA, Michaels BS (agosto de 2007). "Extrañas donde los trabajadores alimentarios han estado implicados en la propagación de la enfermedad alimentaria. Parte 2. Descripción de brotes por tamaño, gravedad y configuración". Journal of Food Protection. 70 (8): 1975–93. doi:10.4315/0362-028X-70.8.1975. PMID 17803160.
- ^ Meliopoulos VA, Kayali G, Burnham A, Oshansky CM, Thomas PG, Gray GC, et al. (14 de mayo de 2014). Kapoor A (ed.). "Detección de anticuerpos contra el astrovirus de Turquía en humanos". PLOS ONE. 9 (5): e96934. Bibcode:2014PLoSO...996934M. doi:10.1371/journal.pone.0096934. PMC 4020816. PMID 24826893.
- ^ Björkholm M, Celsing F, Runarsson G, Waldenström J (agosto de 1995). "Terapia de inmunoglobulina intravenosa exitosa para la gastroenteritis astrovirus severa y persistente después del tratamiento de la fludarabina en un paciente con la macroglobulinemia de Waldenström". International Journal of Hematology. 62 (2): 117–20. doi:10.1016/0925-5710(95)00396-A. PMID 8590772.
- ^ Téllez MA, Téllez AN, Vélez F, Ulloa JC (diciembre de 2015). "In vitro antiviral activity against rotavirus and astrovirus infection exerciseed by substances obtained from Achyrocline bogotensis (Kunth) DC. (Compositae)". BMC Medicina complementaria y alternativa. 15 (1): 428. doi:10.1186/s12906-015-0949-0. PMC 4668688. PMID 26630872.
Enlaces externos
- Viralzone: Astroviridae
- ICTV
- Enfermedades africanas de fauna y flora silvestres Archived 27 August 2016 at archive. hoy