Apoptosoma
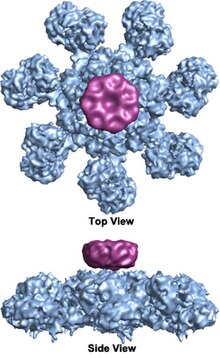
El apoptosoma es una gran estructura proteica cuaternaria formada en el proceso de apoptosis. Su formación se desencadena por la liberación de citocromo c de las mitocondrias en respuesta a un estímulo de muerte celular interno (intrínseco) o externo (extrínseco). Los estímulos pueden variar desde daño en el ADN e infección viral hasta señales de desarrollo como las que conducen a la degradación de la cola de un renacuajo.
En las células de mamíferos, una vez que se libera el citocromo c, se une a la proteína citosólica Apaf-1 para facilitar la formación de un apoptosoma. Un estudio bioquímico inicial sugiere una proporción de dos a uno de citocromo c a apaf-1 para la formación de apoptosomas. Sin embargo, estudios estructurales recientes sugieren que la proporción de citocromo c a apaf-1 es de uno a uno. También se ha demostrado que el nucleótido dATP como tercer componente se une a apaf-1, aunque su papel exacto aún se debate. El apoptosoma de los mamíferos nunca había cristalizado, pero en 2002 se obtuvieron imágenes de un apoptosoma humano APAF-1/citocromo-c con una resolución más baja (2 nm) mediante microscopía electrónica de transmisión criogénica, revelando una partícula heptamérica en forma de rueda con simetría de 7 veces. Recientemente, también se resolvió una estructura de resolución media (9,5 Ångström) del apoptosoma humano mediante microscopía crioelectrónica, lo que permite una inferencia inequívoca de las posiciones de todos los dominios APAF-1 (CARD, NBARC y WD40) y el citocromo c. Ahora también existe una estructura cristalina de la subunidad Apaf-1 monomérica e inactiva (PDB 3SFZ).
Una vez formado, el apoptosoma puede reclutar y activar la procaspasa-9 inactiva. Una vez activada, esta caspasa iniciadora puede activar las caspasas efectoras y desencadenar una cascada de eventos que conducen a la apoptosis.
Historia
El término apoptosoma se introdujo por primera vez en el artículo de 1998 de Yoshihide Tsujimoto "El papel de las proteínas de la familia Bcl-2 en la apoptosis: ¿apoptosomas o mitocondrias?". Sin embargo, el apoptosoma se conocía antes como un complejo ternario. Este complejo involucraba caspasa-9 y Bcl-XL, cada uno de los cuales se unía a un dominio Apaf-1 específico. Entonces se creía que la formación de este complejo desempeñaba un papel regulador en la muerte celular de los mamíferos. En diciembre del mismo año, se publicó otro artículo en The Journal of Biological Chemistry que afirmaba que Apaf-1 es el regulador de la apoptosis, mediante la activación de la procaspasa-9.
Los criterios para un apoptosoma se establecieron en 1999. En primer lugar, debe ser un complejo grande (más de 1,3 millones de daltons). En segundo lugar, su formación requiere la hidrólisis de un enlace de alta energía de ATP o dATP. Y por último debe activar la procaspasa-9 en su forma funcional. La formación de este complejo es el punto de no retorno y se producirá la apoptosis. El complejo multimérico estable APAF-1 y citocromo se ajusta a esta descripción y ahora se denomina apoptosoma.
Se pensaba que el apoptosoma era un complejo multimérico por dos razones. En primer lugar, acercar varias moléculas de procaspasa-9 para su escisión. Y en segundo lugar, para elevar el umbral de la apoptosis, por lo tanto la fuga inespecífica de citocromo c no daría lugar a la apoptosis.
Una vez que se estableció el apoptosoma como activador de la procaspasa-9, las mutaciones dentro de esta vía se convirtieron en un área de investigación importante. Algunos ejemplos incluyen células de leucemia humana, cáncer de ovario e infecciones virales. Las áreas de investigación actuales para esta vía se discutirán con más detalle. También existen rutas ocultas para la muerte celular, que son independientes de APAF-1 y, por tanto, del apoptosoma. Estas rutas también son independientes de las caspasas-3 y 9. Estas vías ocultas para la apoptosis son más lentas, pero pueden resultar útiles con más investigaciones.

(Yuan et al. 2010, Estructura de un complejo de CARD apoptosome-procaspase-9
Estructura
El apoptosoma es un complejo holoenzimático multimolecular ensamblado alrededor de la proteína adaptadora Apaf1 (factor activador de proteasa apoptótica 1) durante la apoptosis mediada por mitocondrias que debe ser estimulada por algún tipo de señal de estrés. La formación del apoptosoma requiere la presencia de ATP/dATP y citocromo c en el citosol. Un estímulo de estrés puede desencadenar la liberación de citocromo c en el citoplasma, que luego se unirá al extremo C de Apaf-1 dentro de una región que contiene múltiples repeticiones de WD-40. La oligomerización de Apaf-1 parece ir acompañada de un reclutamiento sincronizado de procaspasa-9 en el motivo CARD en el extremo N de Apaf-1. El apoptosoma desencadena la activación de caspasas en la vía intrínseca de la apoptosis.
El complejo heptamérico en forma de rueda con estructura de simetría séptuple del apoptosome fue revelado por primera vez a la resolución 27 Å por técnicas de criomicroscopia de electrones y tiene una masa calculada de aproximadamente 1 MDa (Acehan et al. 2002). Esta partícula tipo rueda tiene siete radios y un centro central. La región distal de la charla tiene una forma Y pronunciada. El dominio del hub está conectado al dominio Y por un brazo doblado. Cada uno El dominio Y comprende dos lóbulos (uno grande y uno pequeño) entre los cuales los sitios de unión cytochrome c. Debido a que la resolución de la estructura apoptosome era relativamente baja, se propusieron dos modelos controvertidos para la asamblea apoptosome. Un modelo sugiere que los dominios NOD forman el centro y los dominios CARD forman un anillo más libre en la parte superior de la región NOD. Otro modelo propone que Apaf-1 se organice de manera extendida, de tal manera que tanto la CARD N-terminal como la región de unión nucleótido forman el centro central del apoptoso, mientras que los 13 WD-40 repetidos constituyen los dos lóbulos. El lóbulo grande está formado por siete repeticiones y el lóbulo pequeño está formado por seis repeticiones. Cada caspase- 9 molécula une un dominio CARD en el centro central, formando una estructura en forma de cúpula. Esta controversia ha sido resuelta por una reciente estructura de alta resolución del complejo humano apoptosome-procaspase-9 CARD. Esta estructura demostró claramente que sólo las regiones del NOD forman el centro del apoptosome (ver imágenes), mientras que CARD está flexiblemente ligada a la plataforma del apoptosome y se vuelve desordenado en el estado del suelo apoptosome. Una vez que el apoptosome se une a procaspase-9, las CARDs Apaf-1 y procaspase-9 CARDs forman una estructura flexible similar al disco sentado sobre la plataforma. El número de repeticiones WD-40 también se ha demostrado que es de 15 en lugar de 13, y se compone de un beta-propeller 7-bladed y un beta-propeller de 8-neblados.

La evidencia de Wang y sus colegas indica que la relación estequiométrica de procaspasa-9 a Apaf-1 dentro del complejo es aproximadamente 1:1. Esto se demostró además mediante análisis de espectrometría de masas cuantitativa. Se ha demostrado que la estequiometría del citocromo c con respecto a Apaf-1 dentro del complejo es 1:1. Existen algunos debates sobre si se requiere la incorporación estable del citocromo c en el apoptosoma después de la oligomerización, pero datos estructurales recientes favorecen la idea de que el citocromo c estabiliza el apoptosoma humano oligomérico. Sin embargo, es posible que el citocromo c no sea necesario para el ensamblaje del apoptosoma en especies no mamíferas, como gusanos y moscas de la fruta. Además, se ha informado que varias otras moléculas, en particular la caspasa-3, se copurifican con el apoptosoma y se ha demostrado que la caspasa-3 puede unirse al complejo apoptosoma-procaspasa-9.
Apaf-1 forma la columna vertebral del apoptosoma. Tiene tres regiones distintas: el dominio de reclutamiento de caspasa N-terminal (CARD, residuos 1-90), una región central de oligomerización y unión de nucleótidos (NB-ARC/NOD, 128-586) y una región WD40 C-terminal ( 613-1248) que forman una proteína de aproximadamente 140 KDa.
- El dominio CARD de Apaf-1 interactúa con procaspase-9 e implicado en el reclutamiento dentro del apoptosome.
- La región NB-ARC/NOD presenta una similitud significativa de secuencia a la proteína C. elegans Ced-4.
- La región C-terminal WD40 de Apaf1 contiene 15 repeticiones WD-40 estructuradas en dos dominios en forma de b-propeller. Las repeticiones WD-40 son secuencias alrededor de 40 aminoácidos largos que terminan en Trp-Asp y suelen estar involucrados en la interacción proteína-proteína.
Un conector corto y dominios a/b de unión de nucleótidos (NBD) que contienen cajas Walker conservadas A (p-loop 155-161) y B (239-243) siguen al dominio CARD N-terminal. Las cajas Walker A/B son fundamentales para la unión de dATP/ATP y Mg2+. Después del NBD hay un pequeño dominio helicoidal (HD1), un segundo enlazador y un dominio de hélice alada conservado (WHD). La región NOD comprende NBD, HD1 y WHD, creando un dominio ATPasa que forma parte de la familia AAA+ de ATPasas. Hay un dominio súper helicoidal (HD2) presente en la unión entre las repeticiones NOD y WD-40. Las repeticiones de WD40 están en grupos de ocho y siete con enlazadores que las conectan.

Apoptosomas en otros organismos
Las descripciones anteriores son para el apoptosoma humano. Las estructuras complejas de apoptosomas de otros organismos tienen muchas similitudes, pero tienen tamaños y números de subunidades bastante diferentes, como se muestra en la figura. El sistema de la mosca de la fruta, llamado Dark, tiene un anillo de 8 subunidades (PDB 4V4L). El apoptosoma del nematodo, llamado CED-4, es octamérico pero mucho más pequeño (PDB 3LQQ) y no incluye las regiones que se unirían al citocromo C.
Mecanismo de acción
Iniciación
El inicio de la acción del apoptosoma se corresponde con los primeros pasos en la vía de muerte celular programada (PCD). En los animales, la apoptosis se puede catalizar de dos formas; la vía extrínseca implica la unión de ligandos extracelulares a receptores transmembrana, mientras que la vía intrínseca tiene lugar en las mitocondrias. Esta vía intrínseca implica la liberación de citocromo C de las mitocondrias y su posterior unión a la proteína citosólica Apaf-1. Por tanto, la liberación de citocromo c es necesaria para el inicio de la acción del apoptosoma; esta liberación se regula de varias maneras, la más importante mediante la detección de niveles de iones calcio.
Liberación de citocromo c
Se propone que la liberación del citocromo c se produzca de dos maneras. En primer lugar, el poro de transición de permeabilidad (PTP), cuando la mitocondria recibe una señal que induce la muerte y libera proteínas del espacio intermembrana (12). El PTP está compuesto por el canal aniónico dependiente de voltaje (VDAC), la proteína de la membrana interna translocadora de nucleótidos de adenina (AdNT) y la proteína de la matriz ciclofilina D (CyD) (12). Este poro hace que las mitocondrias se hinchen y la membrana mitocondrial externa se rompa (Diamond & McCabe, 2007). Con este cambio de permeabilidad, proteínas como el citocromo c se liberan al citosol (12). Este cambio probablemente causa la transición de la permeabilidad mitocondrial (MPT), donde el potencial transmembrana mitocondrial colapsa y cesa la producción de ATP (12). La inhibición de este método por el agente farmacéutico ciclosporina A (CsA) condujo al descubrimiento de la segunda vía (13). El segundo método de liberación de citocromo c es independiente del PTP e involucra únicamente al VDAC. Los miembros de la familia Bcl-2 de proteínas proapoptóticas pueden inducir la apertura del VDAC (12). Esto provocará que se produzca la misma liberación de proteínas del espacio intermembrana, incluido el citocromo c, y la posterior MPT (12).
Apaf-1
A. Ausencia de citocromo c
En ausencia del citocromo c, Apaf-1 existe en su forma monomérica; Se cree que el dominio WD-40 permanece plegado sobre la proteína, manteniendo a Apaf-1 en un estado autoinhibido. Además, varias áreas están tan estrechamente unidas que la proteína no puede unirse a ninguna otra cosa. Se ha determinado mediante espectrometría de masas que en las células autoinhibidas o "bloqueadas" En este estado, el ADP está unido al dominio ATPasa de Apaf-1. En este estado, esta proteína es singular e incapaz de activar ninguna caspasa.
B. Presencia de citocromo c
El citocromo c se une al dominio WD-40 de Apaf-1. Esto permite que el "bloqueo" para ser liberado, lo que significa que este dominio ya no está autoinhibido. Sin embargo, los dominios CARD y NB-ARC permanecen en estado autoinhibido. El dominio CARD sólo se liberará de este bloqueo cuando Apaf-1 esté vinculado a (d) ATP/ATP; cuando ATP se une, el dominio CARD podrá unirse a Caspasa-9. Cuando el ADP está en el dominio ATPasa, se inhibe la oligomerización. Por lo tanto, la unión de ATP también permite la oligomerización de Apaf-1 en la estructura heptagonal necesaria para la activación de caspasa aguas abajo. Las mutaciones en el dominio ATPasa inactivan la proteína; sin embargo, el método para controlar este intercambio ADP-ATP no está claro. Por lo tanto, la oligomerización sólo puede ocurrir en presencia de 7 moléculas de citocromo c, 7 proteínas Apaf-1 y suficiente (d) ATP/ATP. El dominio ATPasa pertenece a la familia AAA+ de ATPasas; esta familia es conocida por su capacidad para unirse a otros dominios ATPasa y formar hexa o heptámeros. Entonces, el apoptosoma se considera activo cuando hay siete moléculas de Apaf-1 dispuestas en una estructura de rueda, orientadas de manera que los dominios NB-ARC descansen en el centro.
Acción activa del apoptosoma
Este apoptosoma funcional puede proporcionar una activación de plataforma de caspasa 9. La caspasa 9 existe como zimógeno en el citosol y se cree que se encuentra a 20 nM en las células. Aunque se sabe que no es necesario escindir el zimógeno para volverse activo, la actividad de la procaspasa-9 puede aumentar significativamente una vez escindida. La primera hipótesis es que el apoptosoma proporciona un lugar para la dimerización de dos moléculas de caspasa 9 antes de la escisión; Esta hipótesis fue favorecida por Reidl & Salvasen en 2007. La segunda es que la escisión tiene lugar mientras la caspasa 9 todavía está en su forma monomérica. En cada caso, la activación de la caspasa 9 conduce a la activación de una cascada de caspasas completa y la posterior muerte celular. Se ha sugerido que la razón evolutiva por la que el complejo proteico multimérico activa la cascada de caspasas es garantizar que pequeñas cantidades de citocromo c no causen accidentalmente apoptosis.
Áreas de investigación
¿Qué sucede cuando ocurren mutaciones?
Si bien la apoptosis es necesaria para el funcionamiento natural del cuerpo, las mutaciones de la vía del apoptosoma causan efectos catastróficos y cambios en el cuerpo. Las mutaciones de la vía celular pueden promover la muerte celular o impedirla, creando una gran cantidad de enfermedades en el cuerpo. Las vías de apoptosis mutadas que causan enfermedades son abundantes y tienen una amplia gama, desde el cáncer, debido a la falta de actividad de los apoptosomas, la enfermedad de Alzheimer debido a demasiada actividad de los apoptosomas y muchas otras enfermedades neurodegenerativas como la enfermedad de Parkinson y Huntington. #39;s enfermedad. Las enfermedades neurodegenerativas como el Alzheimer, el Parkinson y el Huntington están relacionadas con la edad e implican un aumento de la apoptosis en el que mueren las células que aún pueden funcionar o que contribuyen a mantener la función del tejido. Apaf-1-ALT es un mutante de Apaf-1 que se encuentra en el cáncer de próstata y que no tiene residuos 339-1248. Estudios estructurales recientes del apoptosoma demuestran que Apaf-1-ALT no puede formar apoptosoma porque le faltan componentes estructurales clave para el ensamblaje.
Represión de la apoptosis que causa cáncer
Las anomalías genéticas y bioquímicas dentro de una célula normalmente desencadenan la muerte celular programada para librar al cuerpo de la función y el desarrollo irregulares de las células; sin embargo, las células cancerosas han adquirido mutaciones que les permiten reprimir la apoptosis y sobrevivir. Se han desarrollado quimioterapias como la radiación ionizante para activar estas vías de PCD reprimidas mediante hiperestimulación para promover la PCD normal.
Mutaciones P53 en Apoptosis
P53 funciona como un supresor de tumores que participa en la prevención del cáncer y se produce de forma natural en las vías apoptóticas. P53 hace que las células entren en apoptosis e interrumpan una mayor división celular, evitando así que la célula se vuelva cancerosa (16). En la mayoría de los cánceres, es la vía p53 la que ha mutado, lo que resulta en una falta de capacidad para terminar con las células disfuncionales. La función de P53 también puede ser responsable de una duración de vida limitada donde las mutaciones del gen p53 provocan la expresión de formas dominantes negativas que producen animales de larga vida. Por ejemplo, en un experimento con C. elegans, se descubrió que el aumento de la vida útil de los mutantes p53 dependía del aumento de la autofagia. En otro experimento con Drosophila, la mutación p53 tuvo efectos tanto positivos como negativos en la vida adulta, lo que concluyó un vínculo entre la diferenciación sexual, la PCD y el envejecimiento. Determinar cómo p53 afecta la esperanza de vida será un área importante para futuras investigaciones.
Dirigirse al apoptosoma para la terapia contra el cáncer
La inhibición de la apoptosis es una de las características clave del cáncer, por lo que encontrar formas de manipular y superar esta inhibición para formar el apoptosoma y activar las caspasas es importante en el desarrollo de nuevos tratamientos contra el cáncer. La capacidad de provocar directamente la activación del apoptosoma es valiosa en las terapias contra el cáncer porque los genes cancerosos infectados no pueden destruirse, lo que provoca que se forme una continuación del cáncer. Al activar el apoptosoma mediante un estímulo externo, se puede producir apoptosis y eliminar las células mutadas. Actualmente se están siguiendo numerosos enfoques para lograr esto, incluidas biomoléculas recombinantes, estrategias antisentido, terapia génica y química combinatoria orgánica clásica para apuntar a reguladores apoptóticos específicos en el enfoque para corregir la muerte celular excesiva o deficiente en enfermedades humanas.
En general, la regulación positiva de las proteínas antiapoptóticas conduce a la prevención de la apoptosis, que puede resolverse mediante inhibidores, y la regulación negativa de las proteínas antiapoptóticas conduce a la inducción de la apoptosis, que se revierte mediante activadores que pueden unirse y modificar su actividad. Una molécula diana importante en las terapias basadas en apoptosis es Bcl-2 para el diseño de fármacos. Bcl-2 fue el primer oncogén que causa apoptosis inhibidora del cáncer. Se sobreexpresa en tumores y es resistente a la quimioterapia. Los científicos han descubierto que la unión de los depresores a las proteínas antiapoptóticas Bcl-2 las inhibe y deja a los activadores directos libres para interactuar con Bax y Bak.
Otra molécula específica para la terapia contra el cáncer involucra a la familia de las caspasas y sus reguladores. La inhibición de la actividad de la caspasa bloquea la muerte celular en enfermedades humanas, incluidos trastornos neurodegenerativos, accidentes cerebrovasculares, ataques cardíacos y lesiones hepáticas. Por lo tanto, los inhibidores de caspasa son una herramienta farmacológica prometedora que proporciona tratamientos para el accidente cerebrovascular y otras enfermedades humanas. Hay varios inhibidores de caspasa que se encuentran actualmente en etapa preclínica y que han mostrado evidencia prometedora de efectos reversos de algunas enfermedades neurodegenerativas. En un estudio reciente, los investigadores desarrollaron un inhibidor reversible de caspasa-3 llamado M-826 y lo probaron en un modelo de ratón donde bloqueó el daño al tejido cerebral. Además, se probó en un ratón con la enfermedad de Huntington y el inhibidor evitó la muerte de las neuronas estriadas, lo que reveló efectos prometedores para estudios posteriores de este inhibidor de caspasa.
El complejo de apoptosoma ha revelado nuevos objetivos potenciales para la terapia molecular
La formación del apoptosoma Apaf1/caspasa-9 es un evento crucial en la cascada apoptótica. La identificación de nuevos fármacos potenciales que prevengan o estabilicen la formación de complejos apoptosómicos activos es la estrategia ideal para el tratamiento de enfermedades caracterizadas por una apoptosis excesiva o insuficiente. Recientemente se ha descubierto que la taurina previene la apoptosis inducida por isquemia en cardiomiocitos a través de su capacidad para inhibir la formación de apoptosoma Apaf1/caspasa-9 sin prevenir la disfunción mitocondrial. Se identificó que el posible mecanismo por el cual la taurina inhibe la formación del apoptosoma es capaz de reducir la expresión de caspasa-9, un componente fundamental del apoptosoma. Sin embargo, hay estudios que muestran que Apaf1 y caspasa-9 tienen funciones independientes además del apoptosoma, por lo que alterar sus niveles también podría alterar la función celular. Así, a pesar de los datos experimentales alentadores, varios problemas siguen sin resolverse y limitan el uso de fármacos experimentales en la práctica clínica.
El descubrimiento de inhibidores de apoptosoma proporcionará una nueva herramienta terapéutica para el tratamiento de la enfermedad mediada por apoptosis. De particular importancia son aquellos nuevos compuestos capaces de inhibir la estabilidad y actividad del apoptosoma, actuando sobre las interacciones proteína-proteína intracelular sin alterar los niveles transcripcionales de los componentes del apoptosoma. Los estudios estructurales recientes del apoptosoma pueden proporcionar herramientas valiosas para diseñar terapias basadas en apoptosomas.