Antagonista 5-HT3
Los antagonistas de los receptores 5-HT3, conocidos informalmente como "setrones", son una clase de fármacos que actúan como antagonistas de los receptores 5-HT3, un subtipo de receptor de serotonina que se encuentra en las terminales del nervio vago y en ciertas áreas del cerebro. Con las notables excepciones del alosetrón y el cilansetrón, que se utilizan en el tratamiento del síndrome del intestino irritable, todos los antagonistas de los receptores 5-HT3 son antieméticos, que se utilizan en la prevención y el tratamiento de las náuseas y los vómitos. Son particularmente eficaces para controlar las náuseas y los vómitos producidos por la quimioterapia contra el cáncer y se consideran el estándar de oro para este propósito.
Los antagonistas de 5-HT3 pueden identificarse por el sufijo -setrón y están clasificados bajo el código A04AA del Sistema de Clasificación Anatómica Terapéutica Química de la OMS.
Usos médicos
Los antagonistas de 5-HT3 también están indicados en la prevención y el tratamiento de las náuseas y vómitos inducidos por radiación (NVI), cuando sea necesario, y de las náuseas y vómitos posoperatorios (NVPO). Aunque son más eficaces para controlar las NVIQ (en las que detienen los síntomas por completo en hasta el 70% de las personas y los reducen en el 30% restante), son igual de eficaces que otros agentes para las NVIPO.
La evidencia actual sugiere que los antagonistas de 5-HT3 son ineficaces para controlar el mareo por movimiento. Un ensayo aleatorizado y controlado con placebo de ondansetrón para tratar el mareo por movimiento en el personal de ambulancias aéreas mostró una mejoría subjetiva, pero no fue estadísticamente significativa.
Agentes disponibles
- Ondansetron fue el primer 5-HT3 antagonista, desarrollado por Glaxo alrededor de 1984. Su eficacia se estableció por primera vez en 1987, en modelos animales, y fue ampliamente estudiado durante los años siguientes. Ondansetron fue aprobado por la Administración de Alimentos y Medicamentos de Estados Unidos en 1991, y desde entonces está disponible en varios otros países, incluyendo el Reino Unido, Irlanda, Australia, Canadá, Francia y Brasil. A partir de 2008, el ondansetrón y el granisetrón son los únicos 5-HT3 antagonistas disponibles como una droga genérica en los Estados Unidos. El ondansetrón se puede administrar varias veces al día, dependiendo de la gravedad de los síntomas.
- Tropisetron también se describió por primera vez en 1984. Está disponible en varios países, como el Reino Unido, Australia y Francia, pero no en los Estados Unidos. Los efectos del tropisetrón duran hasta 24 horas, por lo que sólo requiere administración una vez por día.
- Granisetron fue desarrollado alrededor de 1988. Está disponible en Estados Unidos, Reino Unido, Australia y otros países. Los ensayos clínicos sugieren que es más eficaz que otros 5-HT3 antagonistas en la prevención demora CINV (nausea y vómitos que ocurren más de 24 horas después de la primera dosis de quimioterapia). Se toma una vez al día.
- Dolasetron fue mencionado por primera vez en la literatura en 1989. Es un medicamento, y la mayoría de sus efectos se deben a su metabolito activo, hydrodolasetron, que se forma en el hígado por la enzima carbonil reductase. Dolasetron fue aprobado por la FDA en 1997, y también se administra una vez al día.
- Palonosetron es el más nuevo 5-HT3 antagonista para estar disponible en el mercado estadounidense. Es un derivado isoquinolina, y es eficaz para prevenir retrasos en CINV. Palonosetron fue aprobado por la FDA en 2003, inicialmente para uso intravenoso. El 22 de agosto de 2008 se aprobó una formulación oral para la prevención del CINV agudo, ya que un ensayo clínico amplio no mostró que la administración oral fuera tan eficaz como el uso IV contra el CINV retrasado.
- Ramosetron sólo está disponible en Japón y en algunos países de Asia sudoriental a partir de 2008. Tiene mayor afinidad para el 5-HT3 que el receptor más antiguo de 5-HT3 antagonistas, y mantiene sus efectos durante dos días; por lo tanto, es significativamente más eficaz para el CINV retrasado. En estudios de animales, ramosetron también fue eficaz contra síntomas similares al síndrome de intestino irritable.
El alosetrón y el cilansetrón (este último fue desarrollado por Solvay pero nunca fue aprobado por la FDA) no son antieméticos; en cambio, están indicados en el tratamiento de un subconjunto del síndrome del intestino irritable en el que la diarrea es el síntoma dominante. El alosetrón fue retirado del mercado estadounidense en 2000 debido a efectos secundarios graves inaceptablemente frecuentes, incluida la colitis isquémica, y solo está disponible a través de un programa restrictivo para pacientes que cumplen ciertos requisitos.
Ciertos fármacos procinéticos como la cisaprida, la renzaprida y la metoclopramida, aunque no son antagonistas de 5-HT3 propiamente dichos, poseen un efecto antagonista débil en el receptor 5-HT3. La galanolactona, un diterpenoide que se encuentra en el jengibre, es un antagonista de 5-HT3 y se cree que media al menos parcialmente la actividad antiemética de esta planta. La mirtazapina es un antidepresivo tetracíclico con efectos antagonistas de 5-HT2 y 5-HT3 que también posee fuertes propiedades antieméticas, aunque también es muy sedante. Los estudios muestran que la mirtazapina es tan eficaz en el tratamiento de las náuseas y los vómitos relacionados con la quimioterapia como los tratamientos estándar; también es más barata y tiene menos efectos secundarios que los antieméticos típicos, y sus cualidades antidepresivas pueden ser un beneficio adicional para las poblaciones con cáncer. La mirtazapina también se ha utilizado en el tratamiento de la gastroparesia, un trastorno de la motilidad, debido a sus efectos antieméticos. La olanzapina, un antipsicótico atípico con propiedades antieméticas similares a las de la mirtazapina, también es prometedora en el tratamiento de las náuseas y los vómitos inducidos por la quimioterapia.
Efectos adversos
Existen pocos efectos secundarios relacionados con el uso de antagonistas 5-HT3; los más comunes son estreñimiento o diarrea, dolor de cabeza y mareos. A diferencia de los antihistamínicos con propiedades antieméticas como la ciclizina, los antagonistas 5-HT3 no producen sedación, ni causan efectos extrapiramidales, como a veces lo hacen las fenotiazinas (como la proclorperazina).
Todos los antagonistas de 5-HT3 se han asociado con cambios asintomáticos en el electrocardiograma, como prolongación de los intervalos TP y QTc y ciertas arritmias. Se desconoce la importancia clínica de estos efectos secundarios.
Farmacología
Mecanismo de acción
Los receptores 5-HT3 están presentes en varios sitios críticos involucrados en la emesis, incluyendo las aferencias vagales, el núcleo del tracto solitario (STN) y el área postrema misma. La serotonina es liberada por las células enterocromafines del intestino delgado en respuesta a agentes quimioterapéuticos y puede estimular las aferencias vagales (a través de los receptores 5-HT3) para iniciar el reflejo del vómito. Los antagonistas del receptor 5-HT3 suprimen los vómitos y las náuseas al inhibir la unión de serotonina a los receptores 5-HT3. La concentración más alta de receptores 5-HT3 en el sistema nervioso central (SNC) se encuentra en el STN y la zona gatillo de los quimiorreceptores (CTZ), y los antagonistas 5-HT3 también pueden suprimir los vómitos y las náuseas al actuar en estos sitios. Los antagonistas 5-HT3 son muy selectivos y tienen poca afinidad por otros receptores, como los receptores de dopamina, histamina y acetilcolina muscarínicos.
Farmacocinética
Todos los antagonistas de 5-HT3 se absorben bien y son eficaces después de la administración oral, y todos son metabolizados en el hígado por diversas isoenzimas del sistema del citocromo P450. Sin embargo, no inhiben ni inducen estas enzimas.
Farmacia comparada
A pesar de que los antagonistas del receptor 5-HT3 comparten su mecanismo de acción, tienen diferentes estructuras químicas y presentan diferencias en la afinidad por el receptor, la respuesta a la dosis y la duración del efecto. También se metabolizan de diferentes maneras, es decir, en el metabolismo de los antagonistas predominan diferentes componentes del sistema del citocromo P450 (CYP).
Por este motivo, los pacientes resistentes a un antagonista pueden beneficiarse de otro. Existe una correlación entre el número de alelos activos del CYP 2D6 y el número de episodios de vómitos en pacientes que reciben tratamiento con cisplatino y ondansetrón o tropisetrón. Los pacientes con múltiples alelos tienden a no responder al fármaco antiemético y viceversa.
| Drogas | Productos químicos naturaleza | Receptor antagonistas | T1/2 h) | Metabolismo | Dose |
|---|---|---|---|---|---|
| Ondansetron | Carbazole derivativo | 5-HT3 antagonista del receptor y débil 5-HT4 antagonista | 3,9 horas | CYP1A1/2, CYP2D6, CYP 3A3/4/5 | 150 μg/kg |
| Granisetron | Indazole | 5-HT3 receptor antagonista | 9 a 11,6 horas | CYP3A3/4/5 | 10 μg/kg |
| Dolasetron | Indole | 5-HT3 receptor antagonista | 7 a 9 horas | CYP 3A3/4/5, CYP2D6 | 600 – 3000 μg/kg |
| Palonosetron | Isoquinoline | 5-HT3 antagonista del receptor; afinidad más alta para 5-HT3 receptor en esta clase | 40 horas | CYP1A2, CYP2D6, CYP3A3/4/5 | Dosis de 0,25 mg |
| Ramosetron | Benzimidazole derivative | 5-HT3 receptor antagonista | 5,8 horas | 300 μg/kg | |
| Tropisetron | Indole | 5-HT3 receptor antagonista | 5,6 horas | CYP 3A3/4/5, CYP2D6 | 200 μg/kg |
| Vortioxetina | Phenylpiperazine | 5-HT3 receptor antagonista Antidepresivo | 66h | CYP 2D6/ 2A6/CYP2B6/CYP2C8/9, CYP2C19 | 5 mg, 10 mg, dosis de 20 mg |
Historia
La historia de los antagonistas del receptor 5-HT3 comenzó en 1957, cuando John Gaddum y Zuleika P. Picarelli, de la Universidad de Edimburgo, propusieron la existencia de dos subtipos de receptores de serotonina, los receptores M y D (denominados así porque su función podía ser bloqueada por la morfina y la dibencilina, respectivamente). Más tarde se descubrió que el receptor 5-HT3 se correspondía con el receptor M. En la década de 1970, John Fozard descubrió que la metoclopramida y la cocaína eran antagonistas débiles del receptor 5-HT3 (5-HT-M). Fozard y Maurice Gittos sintetizaron más tarde MDL 72222, el primer antagonista potente y verdaderamente selectivo del receptor 5-HT3. Se descubrió que los efectos antieméticos de la metoclopramida se debían en parte a su antagonismo de la serotonina.
Mientras Fozard investigaba los análogos de la cocaína, los investigadores de Sandoz identificaron el potente antagonista selectivo del receptor 5-HT3 ICS 205-930, a partir del cual se desarrollaron los primeros antagonistas selectivos del receptor 5-HT3 comercializados, ondansetrón y granisetrón, que se aprobaron en 1991 y 1993 respectivamente. Se sintetizaron varios compuestos relacionados con MDL 72222, lo que finalmente dio como resultado la aprobación del tropisetrón en 1994 y del dolasetrón en 1997. En 2003 se aprobó un nuevo y mejorado antagonista del receptor 5-HT3, llamado palonosetrón. El desarrollo de antagonistas selectivos del receptor 5-HT3 supuso una mejora espectacular en el tratamiento de las náuseas y los vómitos. Ondansetrón, granisetrón, dolasetrón y palonosetrón están aprobados actualmente en los Estados Unidos y constituyen la piedra angular de la terapia para el control de la emesis aguda con agentes de quimioterapia con potencial emetogénico de moderado a alto.
Desarrollo
Diseño de drogas
Los experimentos han demostrado evidencia de que el sitio de unión del ligando se encuentra en la interfaz de dos subunidades adyacentes. El sitio de unión del ligando está formado por tres bucles (A-C) de la subunidad principal de unión del ligando (cara principal) y tres cadenas β (D-F) de la subunidad adyacente (cara complementaria). El residuo de aminoácido E129 en el bucle A está orientado hacia el bolsillo de unión y forma un enlace de hidrógeno crítico con el grupo hidroxilo de 5-HT. El bucle B contiene W183, un residuo crítico de unión del ligando de triptófano que contribuye a una interacción catión-π entre la densidad electrónica pi del triptófano y la amina primaria de 5-HT. Los residuos del bucle C se han considerado como candidatos para la farmacología diferente de los receptores 5-HT3 de roedores y humanos debido a su divergencia entre especies. El residuo aromático más importante dentro del bucle C es probablemente Y234, que se encuentra opuesto al triptófano del bucle B en el bolsillo de unión del ligando y está involucrado en la unión del ligando. Los bucles D y F son, de hecho, cadenas β, no bucles. W90 en el bucle D es crítico para la unión del ligando y los antagonistas pueden entrar en contacto directamente con R92. El anillo azabicíclico del antagonista competitivo granisetrón se encuentra cerca de W183, formando una interacción catión-pi. Los residuos Y143, G148, E149, V150, Q151, N152, Y153 y K154 del bucle E pueden ser importantes para la unión del granisetrón. La estructura del bucle F aún debe aclararse, pero W195 y D204 parecen ser críticos para la unión del ligando.
| 5-HT3 antagonistas receptores | Afinidad vinculante (Kd, Ki, K50) | Especies |
|---|---|---|
| Tropisetron | 11 nM | Human |
| Granisetron | 1.44 nM | Human |
| Ondansetron | 4,9 nM | Human |
| Palonosetron | 31.6 NM | Córtex cerebral de rata, conejo lédenrico mienterico plexo, guinea-pig plexo ileal |
| Dolasetron | 20.03 nM | NG 108-15 |
| Metoclopramida (no selectiva) | 355 nM | Human |
| Cocaine | 2.45-83 nM | Rabbit |
Camiseta farmacéutica
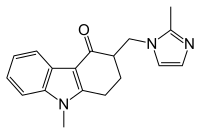

Las estructuras químicas del antagonista del receptor 5-HT3 de primera generación se pueden clasificar en tres clases principales
- Carbazole derivatives (ondansetron)
- Indazoles (Granisetron)
- Indoles (Tropisetron y Dolasetron)
Los antagonistas de los receptores 5-HT3 de primera generación (ondansetrón, dolasetrón, granisetrón y tropisetrón) han sido los fármacos más importantes en la terapia antiemética para la quimioterapia emetógena. Son especialmente eficaces en el tratamiento de la emesis aguda, que se produce en las primeras 24 horas posteriores a la quimioterapia. Un fármaco más nuevo, el palonosetrón, es un antagonista de los receptores 5-HT3 de segunda generación, farmacológicamente distinto y altamente selectivo. El palonosetrón tiene dos centros estereogénicos y existe como cuatro estereoisómeros. El palonosetrón tiene una vida media más larga (40 h) y una mayor afinidad de unión al receptor (>30 veces; en comparación con los antagonistas de primera generación).
Pharmacophore

Relación estructura-actividad


Los estudios de la relación estructura-actividad (SAR) de los ligandos del receptor LGIC son valiosos para investigar su estructura y función. Una molécula similar a un antagonista con baja actividad intrínseca (ia) disminuye la frecuencia de apertura del canal y la permeabilidad de los iones. Los sustituyentes C5 lipofílicos pequeños (R1) (ver figura 5) proporcionan compuestos con un potente antagonismo, lo que indica que el sustituyente C5 puede encajar en un surco angosto e hidrofóbico de la región de unión en el receptor. Parece que los residuos de aminoácidos que interactúan con los sustituyentes C7 (R2) tienen poco que ver con la unión del ligando, pero desempeñan un papel importante en la activación del canal iónico. Los sustituyentes estéricamente voluminosos muestran una mayor interacción con los residuos de aminoácidos que activan el canal iónico y favorecen la conformación abierta del canal iónico debido a la repulsión estérica.

El ondansetrón es un racemato, pero la estereoquímica del átomo de carbono asimétrico no es un factor importante en la interacción con el receptor 5-HT3. La anexión de las posiciones 1,7 del núcleo indólico del ondansetrón produce una mayor afinidad por el receptor.
Un grupo metilo parece ser tan eficaz funcionalmente como un cloro en la posición R (ver figura 6). El grupo carbonilo es responsable de una fuerte interacción con el receptor y contribuye significativamente al proceso de unión. Este grupo carbonilo es completamente coplanar con el anillo aromático adyacente, lo que indica que la conformación unida al receptor corresponde a una de las conformaciones más estables de este grupo en los compuestos flexibles.
Research
Un pequeño ensayo abierto realizado en 2000 concluyó que el ondansetrón era útil para tratar la discinesia tardía inducida por antipsicóticos en personas con esquizofrenia. Los pacientes del estudio también mostraron una mejora significativa de los síntomas de la enfermedad; un ensayo controlado aleatorio, doble ciego posterior también concluyó que el ondansetrón mejoraba significativamente los síntomas de la esquizofrenia cuando se utilizaba como complemento del haloperidol, y las personas que tomaban ambos fármacos experimentaban menos efectos adversos que los que se asocian comúnmente con el haloperidol.
Véase también
- Transporte de serotonina
Referencias
- ^ de Wit R, Aapro M, Blower PR (2005). "¿Hay una base farmacológica para las diferencias en la eficacia antagonista del receptor 5-HT3 en pacientes refractarios?". Cáncer Chemother Pharmacol. 56 3): 231 –8. doi:10.1007/s00280-005-1033-0. PMID 15838653. S2CID 27576150.
- ^ Organización Mundial de la Salud (2006). "El uso de tallos en la selección de Nombres No Propietarios Internacionales (INN) para sustancias farmacéuticas" (PDF). (703 KiB). Ginebra: OMS Prensa. Consultado el 2007-05-15.
- ^ Herrstedt, J.; Aapro, M. S.; Roila, F.; Kataja, V. V.; ESMO Guidelines Task Force (2005). ""ESMO Recomendaciones clínicas mínimas para la profilaxis de náuseas y vómitos inducidos por el quimio (NV)"". Annals of Oncology. 16: i77 – i79. doi:10.1093/annonc/mdi805. PMID 15888767.
- ^ a b Lindley C, Blower P (2000). "Antagonistas orales de serotonina tipo 3 receptores para la prevención de la emesis inducida por quimioterapia". Am J Health-Syst Pharm. 57 (18): 1685–97. doi:10.1093/ajhp/57.18.1685. PMID 11006796. Texto completo gratuito con registro en Medscape
- ^ Roila F, Fatigoni S (2006). "Nuevos medicamentos antieméticos". Ann Oncol. 17 (Supl 2): ii96–100. doi:10.1093/annonc/mdj936. PMID 16608997.
- ^ Stott JR, Barnes GR, Wright RJ, Ruddock CJ (1989). "El efecto sobre la enfermedad de movimiento y la función oculomotor de GR 38032F, un antagonista receptor 5-HT3 con propiedades antieméticas". British Journal of Clinical Pharmacology. 27 2): 147–57. doi:10.1111/j.1365-2125.1989.tb05345.x. PMC 1379774. PMID 2523720.
- ^ Levine ME, Chillas JC, Stern RM, Knox GW (2000). "Los efectos de la serotonina (5-HT3) antagonistas del receptor en la tachyarritmia gástrica y los síntomas de la enfermedad del movimiento". Aviat Space Environ Med. 71 (11): 1111–4. PMID 11086664.
- ^ Muth ER, Elkins AN (Julio 2007). "High dosis ondansetron para reducir la enfermedad de movimiento en sujetos altamente susceptibles". Aviat Space Environ Med. 78 (7): 686 –92. PMID 17679566.
- ^ Dula D, Rosenbach S (2006). "Un ensayo clínico aleatorizado que compara ondansetron con placebo en persona aeromédica con enfermedad de movimiento". Paper presented at the annual meeting of the National Association of EMS Physicians, Registry Resort, Naples, FL, January 19–21, 2006. Consultado el 25 de abril de 2009.
- ^ Hagan RM, Butler A, Hill JM, Jordan CC, Ireland SJ, Tyers MB (1987). "Efecto del antagonista del receptor 5-HT3, GR38032F, en las respuestas a la inyección de un agonista de neurokinina en el área tegmental ventral del cerebro de la rata". Eur. J. Pharmacol. 138 2): 303 –5. doi:10.1016/0014-2999(87)90450-X. PMID 2442006.
- ^ Costall B, Gunning SJ, Naylor RJ, Tyers MB (1987). "El efecto de GR38032F, novedoso antagonista de receptor 5-HT3 sobre vaciado gástrico en la grieta". Br. J. Pharmacol. 91 2): 263 –4. doi:10.1111/j.1476-5381.1987.tb10280.x. PMC 1853517. PMID 2955843.
- ^ See Cáncer de Eur J Clin Oncol 1989; 25 Suppl 1.
- ^ Donatsch P, Engel G, Richardson BP, Stadler PA (1984). "Un antagonista altamente selectivo y potente receptores de triptamina neuronal periferal 5-hidroxi". Br J Pharmacol 81: 34P.
- ^ Zussman BD, Clarkeson A, Coates PE, Rapeport WG (1988). "La farmacocinética perfil de BRL 43694, un nuevo antagonista receptor 5-HT3, en macho sano voluntarios". Br J Clin Pharmacol 25: 107P.
- ^ Aapro M (2004). "Granisetron: una actualización sobre su uso clínico en la gestión de náuseas y vómitos". Oncologist. 9 (6): 673 –86. doi:10.1634/theoncologist.9-6-673. PMID 15561811. Texto completo gratuito
- ^ Sorensen SM, Humphreys TM, Palfreyman MG (1989). "Efecto de las neuronas agudas y crónicas de MDL 73.147EF, un antagonista receptor 5-HT3, en las neuronas de dopamina A9 y A10". Eur. J. Pharmacol. 163 1): 115 –8. doi:10.1016/0014-2999(89)90402-0. PMID 2744086.
- ^ De Leon A (2006). "Palonosetron (Aloxi): antagonista del receptor 5-HT3 de segunda generación para las náuseas y vómitos inducidos por quimioterapia". Proceedings (Baylor University. Medical Center). 19 4): 413 –6. doi:10.1080/08998280.2006.118210. PMC 1618755. PMID 17106506.
- ^ "FDA aprueba Aloxi (Palonosetron) Para Tratamiento de la Nausea y el Vomiting Relacionados con Quimioterapia" (publicación de prensa). Guía del Doctor Publishing Limited. 28 de julio de 2003. Retrieved 2007-05-15.
- ^ Waknine, Yael (4 de septiembre de 2008). "FDA Aprobaciones: Nplate, Aloxi, Vidaza". Medscape. Archivado desde el original el 2 de diciembre de 2008. Retrieved 2008-09-04. Libremente disponible con registro.
- ^ Abridged prescribing information - Nasea (MIMS Philippines). Consultado el 13 de junio de 2008.
- ^ Rabasseda X (febrero de 2002). "Ramosetron, un antagonista receptor 5-HT3 para el control de las náuseas y los vómitos". Drogas de hoy. 38 2): 75–89. doi:10.1358/dot.2002.38.2.820104. PMID 12532186.
- ^ Hirata T, Funatsu T, Keto Y, Nakata M, Sasamata M (febrero de 2007). "Pharmacological profile of ramosetron, un nuevo agente terapéutico para IBS". Inflammopharmacology. 15 1): 5 –9. doi:10.1007/s10787-006-1537-1. PMID 17323187. S2CID 29179265.
- ^ GlaxoSmithKline (2005). "Lotronex Prescribing Information" (PDF). (203 KiB). U.S. Food and Drug Administration. Consultado el 2009-07-30.
- ^ Ku, Valerie (2003). Ginger. University of Colorado at Denver and Health Sciences Center School of Pharmacy. Consultado el 2007-10-25.
- ^ Huang QR; Iwamoto M; Aoki S; et al. (1991). "Efecto anti-5-hidroxitryptamina3 de galanolactona, diterpenoides aislados de jengibre". Chem Pharm Bull. 39 2): 397 –9. doi:10.1248/cpb.39.397. PMID 2054863.
- ^ a b Kast R E; Foley, KF (2007). "Quimioterapia y caquexia del cáncer: mirtazapina y olanzapina son antagonistas de 5-HT3 con buenos efectos de antinausea". European Journal of Cancer Care. 16 4): 351 –354. doi:10.1111/j.1365-2354.2006.00760.x. PMID 17587360.
- ^ Kim S; Shin, IS; Kim, JM; Kang, HC; Mun, JU; Yang, SJ; Yoon, JS (2006). "Mirtazapine for Severe Gastroparesis Unresponsive to Conventional Prokinetic Treatment". Psosomatics. 47 5): 440 –442. doi:10.1176/appi.psy.47.5.440. PMID 16959934.
- ^ a b c d e "5-Hydroxytryptamine3 (5-HT3) Antagonistas del receptor" (PDF). Oregon State University College of Pharmacy. 2003. Archivado desde el original (PDF) on 2013-03-13. Retrieved 2007-05-15.
- ^ a b c Brunton, Laurence L.; Lazo, John S.; Parker, Keith L. (2006). Goddman ' Gilman The Pharmacological Basis of Therapeutics. Nueva York: McGraw-Hill. pp. 1000 –3. ISBN 978-0-07-142280-2.
- ^ a b c d e f Gan TJ (2005). "Antagonistas selectivos del receptor de serotonina 5-HT3 para náuseas postoperatorias y vómitos: ¿son todos iguales?". CNS Drogas. 19 3): 225 –38. doi:10.2165/00023210-200519030-00004. PMID 15740177. S2CID 23209789.
- ^ Sanger GJ (septiembre de 2008). "5-hidroxitryptamina y el tracto gastrointestinal: ¿dónde siguiente?". Tendencias en Ciencias Farmacológicas. 29 (9): 465 –71. doi:10.1016/j.tips.2008.06.008. PMID 19086255.
- ^ Aapro M (2005). "5-HT(3)-antagonistas receptores en la gestión de náuseas y vómitos en el tratamiento del cáncer y del cáncer". Oncología. 69 2): 97 –109. doi:10.1159/000087979. S2CID 71759860.
- ^ GADDUM JH, PICARELLI ZP (septiembre 1957). "Dos tipos de receptores de triptamina". British Journal of Pharmacology and Chemotherapy. 12 3): 323 –8. doi:10.1111/j.1476-5381.1957.tb00142.x. PMC 1509685. PMID 13460238.
- ^ a b c Barnes NM, Hales TG, Lummis SC, Peters JA (enero de 2009). "El receptor 5-HT3 - la relación entre estructura y función". Neurofarmacología. 56 1): 273 –84. doi:10.1016/j.neuropharm.2008.08.003. PMC 6485434. PMID 18761359.
- ^ a b King, Frank D.; Jones, Brian J.; Sanger, Gareth J. (1993). 5-Hydroxytryptamine-3 Antagonistas receptor. CRC Prensa. pp. 2-3. ISBN 978-0-8493-5463-2.
- ^ Galvan, M.; Gittos, M.; Fatmi, M. (octubre de 1996). "DISCOVERY OF 5-HT3 RECEPTOR ANTAGONISTS AND DOLASETRON MESILATE". EJHP Journal (6): 10 –11. Archivado desde el original el 2011-07-20. Retrieved 2010-01-06.
- ^ a b c Billio, Atto; Clarke, Mike J.; Morello, Enrico; Billio, Atto (2006). Billio, Atto (ed.). " Comparación de la eficacia clínica de los antagonistas de los receptores de serotonina en la quimioterapia altamente emetógena". Cochrane Base de Datos de Reseñas Sistemáticas (4). doi:10.1002/14651858.CD006272.
- ^ a b c Oo TH, Hesketh PJ (abril de 2005). "Prueba del medicamento: Nuevos antieméticos en la gestión de las náuseas y vómitos inducidos por quimioterapia". Naturaleza Práctica Clínica Oncología. 2 4): 196–201. doi:10.1038/ncponc0132. PMID 16264934. S2CID 20464189.
- ^ a b Kamm MA (marzo de 2002). "Artículo de revisión: la complejidad del desarrollo de drogas para el síndrome del intestino irritable". Farmacología Alimentaria. 16 3): 343 –51. doi:10.1046/j.1365-2036.2002.01185.x. PMID 11876686. S2CID 24133545.
- ^ Zhu LP, Ye DY, Tang Y (enero de 2007). "Estudios 3D-QSAR basados en la estructura sobre los tiazoles como antagonistas de receptores 5-HT3". Journal of Molecular Modeling. 13 1): 121 –31. doi:10.1007/s00894-006-0131-1. PMID 16953442. S2CID 30877434.
- ^ Reeves DC, Lummis SC (2002). "La base molecular de la estructura y función del receptor 5-HT3: un canal de ion ligando modelo (revisión)". Molecular Membrane Biology. 19 1): 11–26. doi:10.1080/09687680110110048. PMID 11989819. S2CID 36985954.
- ^ Duffy NH, Lester HA, Dougherty DA (2007). "Ondansetron y Granisetron Binding Orientation en el Receptor 5-HT3 Determinado por la Mutagenesis Aminoácidos Nonaturales". ACS Chemical Biology. 7 (10): 1738 –45. doi:10.1021/cb300246j. 3477246. PMID 22873819.
- ^ a b c d e Thompson AJ, Lummis SC (2006). "Receptores 5-HT3". Farmacéutica actual Diseño. 12 (28): 3615 –30. doi:10.2174/138161206778522029. 2664614. PMID 17073663.
- ^ a b Tian K, Chen H, Tang J, Chen X, Hu Z (noviembre de 2006). "Enantioseparation of palonosetron hydrochloride by micellar electrokinetic chromatography with sodium cholate as chiral selector". Journal of Chromatography A. 1132 ()1 –2): 333–6. doi:10.1016/j.chroma.2006.08.090. PMID 16999973.
- ^ a b Hibert MF, Hoffmann R, Miller RC, Carr AA (junio de 1990). "Estudio de relación-actividad de información de los antagonistas receptores 5-HT3 y definición de un modelo para este sitio receptor". Revista de Química Medicinal. 33 (6): 1594–600 doi:10.1021/jm00168a011. PMID 2342053.
- ^ a b c Swain CJ; Baker R; Kneen C; et al. (enero de 1991). "Antagonistas de 5-HT3 de altura. Indole oxadiazoles". Revista de Química Medicinal. 34 1): 140–51. doi:10.1021/jm00105a021. PMID 1992112.
- ^ Cappelli A; Donati A; Anzini M; et al. (agosto de 1996). "La estructura molecular y la dinámica de algunos potentes antagonistas del receptor 5-HT3. Insight into the interaction with the receive". Bioorgánico & Medicinal Química. 4 (8): 1255–69. doi:10.1016/0968-0896(96)00122-8. PMID 8879547.
- ^ Yoshida S, Watanabe T, Sato Y (mayo de 2007). "Las moléculas reguladoras para el sistema de gating de canal de iones de receptores 5-HT3". Bioorgánico & Medicinal Química. 15 (10): 3515–23. doi:10.1016/j.bmc.2007.02.054. PMID 17391967.
- ^ van Wijngaarden I; Hamminga D; van Hes R; et al. (noviembre de 1993). "Desarrollo de antagonistas receptores de alta afinidad 5-HT3. Relaciones de estructura-afinidad de los derivados de indole novedosos 1,7-analados". Revista de Química Medicinal. 36 (23): 3693 –9. doi:10.1021/jm00075a026. PMID 8246239.
- ^ Zullino DF, Eap CB, Voirol P (2001). "Ondansetron for tardive dyskinesia". Am J Psychiatry. 158 4): 657 –8. doi:10.1176/appi.ajp.158.4.657-a. PMID 11282718.
- ^ Sirota P, Mosheva T, Shabtay H, Giladi N, Korczyn AD (2000). "Uso de la ondansetron antagonista selectiva del receptor de serotonina 3 en el tratamiento de la disquinesia tardiva inducida por neuroléptica". Am J Psychiatry. 157 2): 287 –9. doi:10.1176/appi.ajp.157.287. PMID 10671405. Texto completo gratuito
- ^ Zhang ZJ, Kang WH, Li Q, Wang XY, Yao SM, Ma AQ (2006). "Efectos beneficiosos del ondansetrón como un adjunto al haloperidol para la esquizofrenia crónica resistente al tratamiento: un estudio doble ciego, aleatorizado y controlado por placebo". Esquizofrenia Research. 88 ()1 –3): 102 –10. doi:10.1016/j.schres.2006.07.010. PMID 16959472. S2CID 24911372.
- Pasricha, Pankaj J. (2006). "Treatment of Disorders of Bowel Motility and Water Flux; Antiemetics; Agents used in Biliary and Pancreatic Disease". En Laurence Brunton; John Lazo; Keith Parker (eds.). Goodman & Gilman's The Pharmacological Basis of Therapeutics (11th ed.). Nueva York: McGraw-Hill. ISBN 978-0-07-142280-2.
- Hillier, Keith; Robert J. Naylor (2006). "Drugs and the Gastrointestinal System". En Clive Page; Brian Hoffmann; Michael Curtis; Michael Walker (eds.). Farmacología Integrada (3a edición). Mosby. ISBN 978-0-323-04080-8.