Anofeles
Anopheles o Mosquitos de los pantanos() es un género de mosquito descrito y nombrado por primera vez por J. W. Meigen en 1818. Se reconocen alrededor de 460 especies.; Si bien más de 100 pueden transmitir la malaria humana, sólo entre 30 y 40 comúnmente transmiten parásitos del género Plasmodium, que causan la malaria en humanos en áreas endémicas. Anopheles gambiae es uno de los más conocidos, debido a su papel predominante en la transmisión de la especie de parásito de la malaria más peligrosa (para los humanos): Plasmodium falciparum.
El nombre proviene de la palabra griega antigua ἀνωφελής anōphelḗs 'inútil', derivado de ἀν- an-, 'no', 'no-' y ὄφελος óphelos 'beneficio'.
Mosquitos de otros géneros (Aedes, Culex, Culiseta, Haemagogus y Ochlerotatus) también pueden servir como vectores de agentes patógenos, pero no de la malaria humana.
Evolución
Los antepasados de Drosophila y los mosquitos divergieron hace hace 260 millones de años. Los clados de mosquitos culicine y Anopheles divergieron entre hace 120 millones de años y Hace 150 millones de años. Las especies Anopheles del Viejo y Nuevo Mundo divergieron posteriormente entre hace 80 millones de años y Hace 95 millones de años. Anopheles darlingi se separó de los vectores africanos y asiáticos de la malaria ~hace 100 millones de años. Los clados Anopheles gambiae y Anopheles funestus divergieron hace hace 80 millones de años y hace 36 millones de años. Un estudio molecular de varios genes en siete especies ha proporcionado apoyo adicional para una expansión de este género durante el período Cretácico.
El genoma de Anopheles, de 230 a 284 millones de pares de bases (Mbp), es comparable en tamaño al de Drosophila, pero considerablemente más pequeño que los que se encuentran en otras culicinas. genomas (528 Mbp – 1,9 Gbp). Como la mayoría de las especies de culicinas, el genoma es diploide con seis cromosomas.
Los únicos fósiles conocidos de este género son los de Anopheles (Nyssorhynchus) dominicanus Zavortink & Poinar contenido en el ámbar dominicano del Eoceno tardío (hace 40,4 millones de años a hace 33,9 millones de años) y Anopheles rottensis Statz contenidos en el ámbar alemán del Oligoceno tardío (hace 28,4 millones de años a hace 23 millones de años).
Sistemática
El género Anopheles Meigen (distribución casi mundial) pertenece a la subfamilia Anophelinae junto con otros dos géneros: Bironella Theobald (solo Australia) y Chagasia Cruz (Neotrópico). La taxonomía sigue estando incompleta. La clasificación en especies se basa en características morfológicas: manchas en las alas, anatomía de la cabeza, anatomía de las larvas y pupas, estructura cromosómica y, más recientemente, en secuencias de ADN. En la taxonomía publicada por Harbach et al en 2016, se demostró que tres especies de Bironella: confusa, gracilis y hollandi son filogenéticamente similares Anopheles kyondawensis que otras especies de Bironella. La misma filogenia también sostiene que, basándose en la similitud genética, Anopheles implexus es en realidad divergente del ancestro común del género Anopheles, lo que plantea nuevas preguntas sobre la taxonomía y la clasificación.
El género se ha subdividido en siete subgéneros basándose principalmente en el número y las posiciones de las setas especializadas en las gonocoxitas de los genitales masculinos. El sistema de subgéneros se originó con el trabajo de Christophers, quien en 1915 describió tres subgéneros: Anopheles (ampliamente distribuido), Myzomyia (posteriormente rebautizado como Cellia) (Viejo Mundo) y Nyssorhynchus (Neotropical). Nyssorhynchus fue descrito por primera vez como Lavernia por Frederick Vincent Theobald. Frederick Wallace Edwards en 1932 añadió el subgénero Stethomyia (distribución neotropical). Kerteszia también fue descrita por Edwards en 1932, pero luego reconocida como un subgrupo de Nyssorhynchus. Komp lo elevó al estado de subgénero en 1937 y también se encuentra en el Neotrópico. Desde entonces se han reconocido dos subgéneros adicionales: Baimaia (sólo en el sudeste asiático) por Harbach et al. en 2005 y Lophopodomyia (neotropical) por Antunes en 1937.
Se utilizan dos agrupaciones principales dentro del género Anopheles: una formada por los subgéneros Celia y Anopheles y una segunda por Kerteszia , Lophopodomyia y Nyssorhynchus. El subgénero Stethomyia es un caso atípico con respecto a estos dos taxones. Dentro del segundo grupo, Kerteszia y Nyssorhynchus parecen ser taxones hermanos.
El número de especies reconocidas actualmente dentro de los subgéneros se indica aquí entre paréntesis: Anopheles (206 especies), Baimaia (1), Cellia (216), Kerteszia (12), Lophopodomyia (6), Nyssorhynchus (34) y Stethomyia (5).
Las unidades taxonómicas entre subgénero y especie no están reconocidas actualmente como nombres zoológicos oficiales. En la práctica, se han introducido varios niveles taxonómicos. Los subgéneros más grandes (Anopheles, Cellia y Nyssorhynchus) se han subdividido en secciones y series que a su vez se han dividido en grupos y subgrupos. Debajo del subgrupo pero por encima del nivel de especie se encuentra el complejo de especies. Los niveles taxonómicos por encima del complejo de especies se pueden distinguir por motivos morfológicos. Las especies dentro de un complejo de especies son morfológicamente idénticas o extremadamente similares y sólo pueden separarse de manera confiable mediante un examen microscópico de los cromosomas o la secuenciación del ADN. La clasificación continúa siendo revisada.
ElSubgénero Nyssorhynchus se ha dividido en tres secciones: Albimanus (19 especies), Argyritarsis (11 especies) y Myzorhynchella (4 especies). La sección Argyritarsis se ha subdividido en los grupos Albitarsis y Argyritarsis.
Edwards dividió el grupo Anopheles en cuatro series: Anopheles (mundial), Myzorhynchus (palártico, oriental, australasiano y afrotropical)., Cycloleppteron (Neotropical) y Lophoscelomyia (Oriental); y dos grupos, Arribalzagia (Neotropical) y Christya (Afrotropical). Reid y Knight (1961) modificaron esta clasificación y en consecuencia subdividieron el subgénero Anopheles en dos secciones, Angusticorn y Laticorn y seis series. Se consideraron series los Grupos Arribalzagia y Christya. La Sección Laticorn incluye las series Arribalzagia (24 especies), Christya y Myzorhynchus. La sección Angusticorn incluye miembros de las series Anopheles, Cycloleppteron y Lophoscelomyia.
Todas las especies que se sabe que son portadoras de malaria humana se encuentran dentro de las series Myzorhynchus o Anopheles.
Etapas de la vida
Como todos los mosquitos, los anofelinos pasan por cuatro etapas en su ciclo de vida: huevo, larva, pupa e imago. Las primeras tres etapas son acuáticas y juntas duran de 5 a 14 días, según la especie y la temperatura ambiente. La etapa adulta es cuando la hembra del mosquito Anopheles actúa como vector de la malaria. Las hembras adultas pueden vivir hasta un mes (o más en cautiverio), pero lo más probable es que no vivan más de dos semanas en la naturaleza.
Huevos

Las hembras adultas ponen entre 50 y 200 huevos por oviposición. Los huevos son bastante pequeños (alrededor de 0,5 × 0,2 mm). Los huevos se ponen individualmente y directamente sobre el agua. Son únicos porque tienen flotadores a ambos lados. Los huevos no son resistentes a la desecación y eclosionan en 2 a 3 días, aunque la eclosión puede tardar hasta 2 a 3 semanas en climas más fríos.
Larvas


La larva del mosquito tiene una cabeza bien desarrollada con cepillos bucales que se utilizan para alimentarse, un tórax grande y un abdomen de nueve segmentos. No tiene piernas. A diferencia de otros mosquitos, la larva Anopheles carece de sifón respiratorio, por lo que se posiciona de manera que su cuerpo quede paralelo a la superficie del agua. Por el contrario, la larva que se alimenta de una especie de mosquito no anofelino se adhiere a la superficie del agua con su sifón posterior, con su cuerpo apuntando hacia abajo.
Las larvas respiran a través de espiráculos ubicados en el octavo segmento abdominal, por lo que deben salir a la superficie con frecuencia. Las larvas pasan la mayor parte del tiempo alimentándose de algas, bacterias y otros microorganismos en la microcapa superficial. Se sumergen bajo la superficie sólo cuando se les molesta. Las larvas nadan mediante movimientos bruscos de todo el cuerpo o mediante propulsión con los cepillos bucales.
Las larvas se desarrollan a través de cuatro etapas, o estadios, después de los cuales se metamorfosean en pupas. Al final de cada estadio, las larvas mudan y se deshacen de su exoesqueleto o piel para permitir un mayor crecimiento. Las larvas del primer estadio miden aproximadamente 1 mm de longitud; las larvas del cuarto estadio normalmente miden entre 5 y 8 mm de longitud.
El proceso desde la puesta de los huevos hasta la aparición del adulto depende de la temperatura, con un tiempo mínimo de siete días.
Las larvas se encuentran en una amplia gama de hábitats, pero la mayoría de las especies prefieren agua limpia y no contaminada. Se han encontrado larvas de mosquitos Anopheles en marismas de agua dulce o salada, manglares, arrozales, zanjas cubiertas de hierba, orillas de arroyos y ríos, y pequeños charcos de lluvia temporales. Muchas especies prefieren hábitats con vegetación. Otros prefieren hábitats sin ninguno. Algunos se reproducen en estanques abiertos e iluminados por el sol, mientras que otros se encuentran sólo en sitios de reproducción sombreados en los bosques. Algunas especies se reproducen en los huecos de los árboles o en las axilas de las hojas de algunas plantas.
Pupas
La pupa (también conocida como vaso) tiene forma de coma cuando se ve desde un lado. La cabeza y el tórax se fusionan en un cefalotórax con el abdomen curvado por debajo. Al igual que las larvas, las pupas deben salir a la superficie con frecuencia para respirar, lo que hacen a través de un par de trompetas respiratorias en el cefalotórax. Después de unos días como pupa, la superficie dorsal del cefalotórax se divide y emerge el mosquito adulto. La etapa de pupa dura entre 2 y 3 días en zonas templadas.
Adultos
La duración desde el huevo hasta el adulto varía considerablemente entre especies y está fuertemente influenciada por la temperatura ambiente. Los mosquitos pueden pasar de huevo a adulto en tan solo cinco días, pero en condiciones tropicales pueden tardar entre 10 y 14 días.
Como todos los mosquitos, las especies adultas de Anopheles tienen cuerpos delgados con tres secciones: cabeza, tórax y abdomen.
La cabeza está especializada en adquirir información sensorial y en alimentarse. Contiene los ojos y un par de antenas largas y multisegmentadas. Las antenas son importantes para detectar los olores del huésped, así como los olores de los lugares de reproducción donde las hembras ponen huevos. La cabeza también tiene una probóscide alargada que se proyecta hacia adelante y que se utiliza para alimentarse, y dos palpos maxilares. Estos palpos también transportan receptores de dióxido de carbono, un importante atrayente para la ubicación del huésped del mosquito.
El tórax está especializado para la locomoción. Al tórax se unen tres pares de patas y un par de alas.
El abdomen está especializado en la digestión de los alimentos y el desarrollo de los óvulos. Esta parte segmentada del cuerpo se expande considerablemente cuando una hembra ingiere sangre. La sangre se digiere con el tiempo, sirviendo como fuente de proteínas para la producción de óvulos, que poco a poco llenan el abdomen.
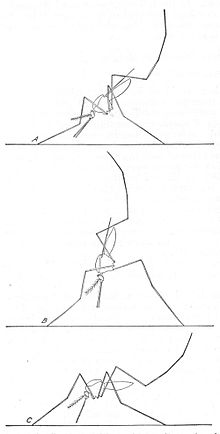
Los mosquitosAnopheles se pueden distinguir de otros mosquitos por los palpos, que son tan largos como la probóscide, y por la presencia de bloques discretos de escamas blancas y negras en las alas. Los adultos también pueden identificarse por su posición típica de descanso: machos y hembras descansan con el abdomen hacia arriba en el aire en lugar de paralelo a la superficie sobre la que descansan.
Los mosquitos adultos generalmente se aparean unos días después de salir de la etapa de pupa. En la mayoría de las especies, los machos forman grandes enjambres, generalmente al anochecer, y las hembras vuelan hacia los enjambres para aparearse.

Los machos viven aproximadamente una semana y se alimentan de néctar y otras fuentes de azúcar. Los machos no pueden alimentarse de sangre, ya que parece producir efectos tóxicos y los mata en unos pocos días, aproximadamente la misma esperanza de vida que una dieta basada únicamente en agua. Las hembras también se alimentan de fuentes de azúcar para obtener energía, pero normalmente necesitan sangre para el desarrollo de los huevos. Después de obtener una alimentación completa de sangre, la hembra descansará durante unos días mientras se digiere la sangre y se desarrollan los huevos. Este proceso depende de la temperatura, pero suele tardar entre 2 y 3 días en condiciones tropicales. Una vez que los huevos están completamente desarrollados, la hembra los pone y continúa buscando huésped.
El ciclo se repite hasta que la hembra muere. Si bien las hembras pueden vivir más de un mes en cautiverio, la mayoría no vive más de una o dos semanas en la naturaleza. Su esperanza de vida depende de la temperatura, la humedad y su capacidad para obtener sangre con éxito evitando las defensas del huésped.
En un estudio realizado por la London School of Hygiene & Los investigadores de Medicina Tropical descubrieron que los mosquitos hembra portadores de parásitos de la malaria se sienten significativamente más atraídos por el aliento y los olores humanos que los mosquitos no infectados. El equipo de investigación infectó mosquitos Anopheles gambiae criados en laboratorio con parásitos Plasmodium, dejando un grupo de control sin infectar. Luego se realizaron pruebas en los dos grupos para registrar su atracción por los olores humanos. Los mosquitos hembra se sienten particularmente atraídos por el olor de los pies, y una de las pruebas mostró que mosquitos infectados aterrizaban y picaban repetidamente a un posible huésped. El equipo especula que el parásito mejora la calidad de vida de los mosquitos. sentido del olfato. También puede reducir su aversión al riesgo.
Hábitat
Aunque hoy en día la malaria se limita a las zonas tropicales, sobre todo a las regiones del África subsahariana, muchas especies de Anopheles viven en latitudes más frías (consulte este mapa de los CDC). De hecho, en el pasado se produjeron brotes de malaria en climas más fríos, por ejemplo durante la construcción del Canal Rideau en Canadá durante la década de 1820. Desde entonces, el parásito Plasmodium (no el mosquito Anopheles) ha sido eliminado de los países del primer mundo.
Sin embargo, los CDC advierten que los Anopheles que pueden transmitir la malaria se encuentran no sólo en áreas endémicas de malaria, sino también en áreas donde la malaria ha sido eliminada. Por tanto, estas últimas zonas corren constantemente el riesgo de que la enfermedad se reintroduzca.
Susceptibilidad a convertirse en una enfermedad vectorial
Algunas especies son malos vectores de malaria, ya que los parásitos no se desarrollan bien (o no se desarrollan en absoluto) dentro de ellas. También hay variación dentro de las especies. En el laboratorio es posible seleccionar cepas de A. gambiae que son refractarias a la infección por parásitos de la malaria. Estas cepas refractarias tienen una respuesta inmune que encapsula y mata a los parásitos después de que han invadido la pared del estómago del mosquito. Los científicos están estudiando el mecanismo genético de esta respuesta. Los mosquitos genéticamente modificados refractarios a la malaria posiblemente podrían reemplazar a los mosquitos salvajes, limitando o eliminando así la transmisión de la malaria.
Transmisión y control de la malaria
Comprender la biología y el comportamiento de los mosquitos Anopheles puede ayudar a comprender cómo se transmite la malaria y puede ayudar a diseñar estrategias de control adecuadas. Los factores que afectan la capacidad de un mosquito para transmitir la malaria incluyen su susceptibilidad innata al Plasmodium, su elección de huésped y su longevidad. Los factores que deben tenerse en cuenta al diseñar un programa de control incluyen la susceptibilidad de los vectores de la malaria a los insecticidas y el lugar preferido para alimentarse y descansar de los mosquitos adultos.
El 21 de diciembre de 2007, un estudio publicado en PLoS Pathogens encontró que la lectina hemolítica de tipo C CEL-III de Cucumaria echinata, un pepino de mar encontrado en la Bahía de Bengala, alteraba el desarrollo de el parásito de la malaria cuando es producido por A transgénico. stephensi. Esto podría usarse potencialmente para controlar la malaria mediante la propagación de mosquitos genéticamente modificados refractarios a los parásitos, aunque deben superarse numerosas cuestiones científicas y éticas antes de que se pueda implementar tal estrategia de control.
Fuentes preferidas para ingerir sangre
Un factor de comportamiento importante es el grado en que una especie de Anopheles prefiere alimentarse de humanos (antropofilia) o de animales como ganado vacuno o aves (zoofilia). Los Anopheles antropofílicos tienen más probabilidades de transmitir los parásitos de la malaria de una persona a otra. La mayoría de los mosquitos Anopheles no son exclusivamente antropofílicos o zoofílicos, incluido el principal vector de la malaria en el oeste de Estados Unidos, A. freeborni. Sin embargo, los principales vectores de malaria en África, A. gambiae y A. funestus, son fuertemente antropófilos y, en consecuencia, son dos de los vectores de malaria más eficientes del mundo.
Una vez ingeridos por un mosquito, los parásitos de la malaria deben desarrollarse dentro del mosquito antes de que sean infecciosos para los humanos. El tiempo necesario para el desarrollo del mosquito (el período de incubación extrínseca) oscila entre 10 y 21 días, según la especie del parásito y la temperatura. Si un mosquito no sobrevive más tiempo que el período de incubación extrínseco, no podrá transmitir ningún parásito de la malaria.
No es posible medir directamente la esperanza de vida de los mosquitos en la naturaleza, pero se han hecho estimaciones indirectas de la supervivencia diaria de varias especies de Anopheles. Estimaciones de supervivencia diaria de A. gambiae en Tanzania osciló entre 0,77 y 0,84, lo que significa que al final de un día, entre el 77% y el 84% habrán sobrevivido.
Suponiendo que esta supervivencia sea constante durante la vida adulta de un mosquito, menos del 10% de las hembras A. gambiae sobreviviría más de un período de incubación extrínseca de 14 días. Si la supervivencia diaria aumentara a 0,9, más del 20% de los mosquitos sobrevivirían más que el mismo período. Las medidas de control que dependen de insecticidas (por ejemplo, la fumigación residual en interiores) pueden en realidad afectar la transmisión de la malaria más por su efecto en la longevidad de los adultos que por su efecto en la población de mosquitos adultos.
Patrones de alimentación y descanso
La mayoría de los mosquitos Anopheles son crepusculares (activos al anochecer o al amanecer) o nocturnos (activos durante la noche). Algunos se alimentan en el interior (endofágicos), mientras que otros se alimentan al aire libre (exofágicos). Después de alimentarse, algunos mosquitos de sangre prefieren descansar en el interior (endofílicos), mientras que otros prefieren descansar al aire libre (exofílicos), aunque esto puede diferir regionalmente según el ecotipo del vector local y la composición cromosómica del vector, así como el tipo de vivienda y las condiciones microclimáticas locales. Las picaduras de mosquitos nocturnos endófagos Anopheles se pueden reducir notablemente mediante el uso de mosquiteros tratados con insecticida o mediante la mejora de la construcción de viviendas para evitar la entrada de mosquitos (por ejemplo, mosquiteros en las ventanas). Los mosquitos endófilos se controlan fácilmente rociando interiores con insecticidas residuales. Por el contrario, los vectores exofágicos/exofílicos se controlan mejor mediante la reducción de la fuente (destrucción de los sitios de reproducción).
Flora intestinal
Debido a que la transmisión de enfermedades por parte del mosquito requiere la ingestión de sangre, la flora intestinal puede influir en el éxito de la infección del mosquito huésped. Este aspecto de la transmisión de enfermedades no se ha investigado hasta hace poco. El intestino de las larvas y pupas está colonizado en gran medida por cianobacterias fotosintéticas, mientras que en el adulto predominan Pseudomonadota y Bacteroidota. La ingesta de sangre reduce drásticamente la diversidad de organismos y favorece las bacterias entéricas.
Resistencia a insecticidas
Las medidas de control basadas en insecticidas (por ejemplo, fumigación interior con insecticidas, mosquiteros) son las principales formas de matar los mosquitos que pican en el interior. Sin embargo, después de una exposición prolongada a un insecticida durante varias generaciones, las poblaciones de mosquitos, al igual que las de otros insectos, pueden desarrollar resistencia, es decir, la capacidad de sobrevivir al contacto con un insecticida. Dado que los mosquitos pueden tener muchas generaciones por año, pueden desarrollarse muy rápidamente altos niveles de resistencia. La resistencia de los mosquitos a algunos insecticidas se ha documentado apenas unos años después de su introducción. Más de 125 especies de mosquitos tienen resistencia documentada a uno o más insecticidas. La evolución de la resistencia a los insecticidas utilizados en la fumigación residual de interiores fue un impedimento importante durante la Campaña Mundial de Erradicación de la Malaria. El uso sensato de insecticidas para el control de mosquitos puede limitar la evolución y propagación de la resistencia. Sin embargo, a menudo se ha implicado que el uso de insecticidas en la agricultura contribuye a la resistencia en las poblaciones de mosquitos. Es posible detectar la evolución de la resistencia en las poblaciones de mosquitos, por lo que es aconsejable que los programas de control realicen vigilancia para detectar este problema potencial. En Malawi y otros lugares se utiliza un arbusto conocido como mpungabwi (Ocimum americanum) para repeler los mosquitos.
Erradicación
Con un número sustancial de casos de malaria que afectan a personas de todo el mundo, en regiones tropicales y subtropicales, especialmente en el África subsahariana, donde millones de niños mueren a causa de esta enfermedad infecciosa, la erradicación vuelve a estar en la agenda sanitaria mundial.
Aunque la malaria ha existido desde la antigüedad, su erradicación fue posible en Europa, América del Norte, el Caribe y partes de Asia y el sur de América Central durante las primeras campañas regionales de eliminación a fines de la década de 1940. Sin embargo, no se lograron los mismos resultados en el África subsahariana.
Aunque la Organización Mundial de la Salud adoptó una política formal sobre el control y la erradicación del parásito de la malaria desde 1955, sólo recientemente, después del Foro Gates sobre Malaria en octubre de 2007, organizaciones clave iniciaron el debate sobre los pros y los contras de redefinir la erradicación. como objetivo para controlar la malaria.
Claramente, el costo de prevenir la malaria es mucho menor que tratar la enfermedad, a largo plazo. Sin embargo, la erradicación de los mosquitos no es una tarea fácil. Para una prevención eficaz de la malaria, se deben cumplir algunas condiciones, como condiciones propicias en el país, recopilación de datos sobre la enfermedad, enfoques técnicos específicos para el problema, liderazgo muy activo y comprometido, apoyo gubernamental total, recursos monetarios suficientes, participación de la comunidad, y técnicos capacitados en diferentes campos, así como una adecuada implementación.
Actualmente, existen propuestas para erradicar Anopheles gambiae, el principal vector de la malaria, con un sistema de impulso genético CRISPR-Cas9. Este sistema tiene como objetivo erradicar la especie mediante la introducción de un gen que provocaría esterilidad femenina, provocando así que el gen no pudiera replicarse. En un estudio realizado por Kyrou et al se ha demostrado que dicho sistema de impulso genético puede suprimir a un An enjaulado por completo. gambiae atacando y eliminando el gen dsx, que es vital para la fertilidad femenina. Al utilizar las tendencias de conservación de los genes egoístas, Kyrou et al demostraron la supresión total de la población en un plazo de 7 a 11 generaciones, normalmente menos de un año. Por supuesto, esto ha generado preocupaciones tanto con la eficiencia de un sistema de impulso genético como con el impacto ético y ecológico de tal programa de erradicación. Por lo tanto, se han realizado esfuerzos para utilizar el sistema de impulso genético para introducir de manera más eficiente genes de resistencia a Plasmodium en la especie, como apuntar y eliminar el gen FREP1 en Anopheles gambiae. Estos sistemas pueden generar menos impacto ecológico, ya que las especies no se eliminan del ecosistema, aunque aún persisten preocupaciones con respecto a la eficiencia.
Investigadores de Burkina Faso han creado una cepa del hongo metarhizium pinghaense genéticamente modificado para producir el veneno de una araña de tela en embudo australiana; La exposición al hongo provocó que las poblaciones de mosquitos Anopheles disminuyeran en un 99 % en un ensayo controlado.
Se necesita una amplia gama de estrategias para lograr la erradicación de la malaria, desde pasos simples hasta estrategias complicadas que tal vez no sean posibles de implementar con las herramientas actuales.
Aunque el control de mosquitos es un componente importante de la estrategia de control de la malaria, la eliminación de la malaria en un área no requiere la eliminación de todos los mosquitos Anopheles. Por ejemplo, en América del Norte y Europa, aunque los mosquitos vectores Anopheles todavía están presentes, el parásito ha sido eliminado. Algunas mejoras socioeconómicas (por ejemplo, casas con ventanas con malla metálica, aire acondicionado), una vez combinadas con esfuerzos de reducción de vectores y un tratamiento eficaz, conducen a la eliminación de la malaria sin la eliminación completa de los vectores. Algunas medidas importantes que se deben seguir en el control de mosquitos son: desalentar la puesta de huevos, prevenir el desarrollo de huevos en larvas y adultos, matar a los mosquitos adultos, no permitir que los mosquitos adultos entren en lugares de vivienda humana, evitar que los mosquitos piquen a los seres humanos y negarles comidas de sangre.
La investigación en este sentido continúa y un estudio ha sugerido que los mosquitos estériles podrían ser la respuesta para la eliminación de la malaria. Esta investigación sugiere que el uso de la técnica de los insectos estériles, en la que se liberan insectos macho sexualmente estériles para eliminar una población de plagas, podría ser una solución al problema de la malaria en África. Esta técnica trae esperanza, ya que las hembras de los mosquitos sólo se aparean una vez durante su vida y, al hacerlo, con mosquitos machos estériles, la población de insectos disminuiría. Esta es otra opción a considerar por las autoridades locales e internacionales que puede combinarse con otros métodos y herramientas para lograr la erradicación de la malaria en el África subsahariana.
Parásitos
Se sabe que existen varios parásitos de este género, incluidos los microsporidios de los géneros Amblyospora, Crepidulospora, Senoma y . Paratelohanía.
Los microsporidios que infectan las etapas acuáticas de los insectos, un grupo que incluye mosquitos y moscas negras, y los copépodos parecen formar un clado distinto de los que infectan a los insectos y peces terrestres. En este grupo se encuentran dos ciclos de vida distintos. En el primer tipo, el parásito se transmite por vía oral y es relativamente inespecífico de especie. En el segundo, aunque la vía oral es la vía habitual de infección, el parásito se ingiere dentro de un huésped intermediario ya infectado. La infección de la forma larvaria de insecto suele ser específica de un tejido y suele afectar al cuerpo graso. También se sabe que ocurre transmisión vertical (transovárica).
Se han realizado pocos estudios filogenéticos de estos parásitos y aún se está determinando su relación con sus mosquitos huéspedes. Un estudio sugirió que Parathelohania es un género de divergencia temprana dentro de este grupo.
La bacteria parásita
Depredadoras
(feminine)La araña saltadora Evarcha culicivora se alimenta indirectamente de sangre de vertebrados al cazar mosquitos hembra Anopheles. Curiosamente, las arañas juveniles eligen el Anopheles sobre todas las demás presas, independientemente de si realmente transporta sangre. Las arañas juveniles han adoptado un comportamiento de captura de presas específico de Anopheles, utilizando la postura de los mosquitos Anopheles como señal principal para identificarlos. Anopheles tiene una postura de descanso distintiva con el abdomen en ángulo hacia arriba. En este caso, la araña se desvía y se acerca por detrás del mosquito y por debajo de su abdomen, para luego atacar desde abajo.