Análisis retrosintético
El análisis retrosintético es una técnica para resolver problemas en la planificación de síntesis orgánicas. Esto se logra mediante la transformación de una molécula objetivo en estructuras precursoras más simples, independientemente de cualquier posible reactividad/interacción con los reactivos. Cada material precursor se examina usando el mismo método. Este procedimiento se repite hasta que se alcanzan estructuras simples o comercialmente disponibles. Estos compuestos más simples/disponibles comercialmente pueden usarse para formar una síntesis de la molécula diana. EJ Corey formalizó este concepto en su libro La lógica de la síntesis química.
El poder del análisis retrosintético se hace evidente en el diseño de una síntesis. El objetivo del análisis retrosintético es una simplificación estructural. A menudo, una síntesis tendrá más de una ruta sintética posible. La retrosíntesis es muy adecuada para descubrir diferentes rutas sintéticas y compararlas de una manera lógica y directa. Se puede consultar una base de datos en cada etapa del análisis, para determinar si un componente ya existe en la literatura. En ese caso, no se requeriría más exploración de ese compuesto. Si ese compuesto existe, puede ser un punto de partida para otros pasos desarrollados para llegar a una síntesis.
Definiciones
DesconexiónUn paso retrosintético que involucra la ruptura de un enlace para formar dos (o más) sintones.RetronUna subestructura molecular mínima que permite ciertas transformaciones.Árbol retrosintéticoUn gráfico acíclico dirigido de varias (o todas) retrosíntesis posibles de un solo objetivo.sintetizadorFragmento de un compuesto que ayuda en la formación de una síntesis, derivado de esa molécula diana. A continuación se muestra un sintón y el correspondiente equivalente sintético comercialmente disponible:
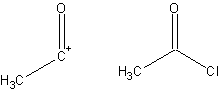
ObjetivoEl compuesto final deseado.TransformarEl reverso de una reacción sintética; la formación de materiales de partida a partir de un solo producto.
Ejemplo
Un ejemplo permitirá comprender fácilmente el concepto de análisis retrosintético.

Al planificar la síntesis de ácido fenilacético, se identifican dos sintones. Un grupo nucleófilo "-COOH" y un grupo electrofílico "PhCH 2 ". Por supuesto, ambos sintones no existen per se; los equivalentes sintéticos correspondientes a los sintones se hacen reaccionar para producir el producto deseado. En este caso, el anión cianuro es el equivalente sintético del sintón COOH, mientras que el bromuro de bencilo es el equivalente sintético del sintón bencilo.
La síntesis de ácido fenilacético determinada por análisis retrosintético es así:PhCH2Br + NaCN → PhCH2CN + NaBrPhCH 2 CN + 2 H 2 O → PhCH 2 COOH + NH 3

De hecho, el ácido fenilacético se ha sintetizado a partir de cianuro de bencilo, preparado a su vez por la reacción análoga del bromuro de bencilo con cianuro de sodio.
Estrategias
Estrategias de grupos funcionales
La manipulación de grupos funcionales puede conducir a reducciones significativas en la complejidad molecular.
Estrategias estereoquímicas
Numerosos objetivos químicos tienen demandas estereoquímicas distintas. Las transformaciones estereoquímicas (como el reordenamiento de Claisen y la reacción de Mitsunobu) pueden eliminar o transferir la quiralidad deseada, simplificando así el objetivo.
Estrategias de estructura-objetivo
Dirigir una síntesis hacia un intermedio deseable puede reducir en gran medida el enfoque del análisis. Esto permite técnicas de búsqueda bidireccional.
Estrategias basadas en transformación
La aplicación de transformaciones al análisis retrosintético puede conducir a poderosas reducciones en la complejidad molecular. Desafortunadamente, los potentes retrones basados en transformadas rara vez están presentes en moléculas complejas y, a menudo, se necesitan pasos sintéticos adicionales para establecer su presencia.
Estrategias topológicas
La identificación de una o más desconexiones de enlace clave puede conducir a la identificación de subestructuras clave o transformaciones de reordenamiento difíciles de identificar para identificar las estructuras clave.
- Se recomiendan las desconexiones que preservan las estructuras de los anillos.
- Se desaconsejan las desconexiones que crean anillos de más de 7 miembros.
- La desconexión implica creatividad.
Contenido relacionado
Aguafina
Butanol
Glóbulo fundido