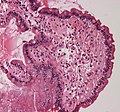
Amilosis
Amiloidosis es un grupo de enfermedades en las que proteínas anormales, conocidas como fibrillas de amiloide, se acumulan en el tejido. Existen varios signos y síntomas vagos e inespecíficos asociados con la amiloidosis. Estos incluyen fatiga, edema periférico, pérdida de peso, dificultad para respirar, palpitaciones y sensación de desmayo al estar de pie. En la amiloidosis AL, los indicadores específicos pueden incluir agrandamiento de la lengua y púrpura periorbitaria. En la amiloidosis ATTR de tipo salvaje, los síntomas no cardíacos incluyen: síndrome del túnel carpiano bilateral, estenosis espinal lumbar, rotura del tendón del bíceps, neuropatía de fibras pequeñas y disfunción autonómica.
Existen alrededor de 36 tipos diferentes de amiloidosis, cada uno de ellos debido a un plegamiento incorrecto de una proteína específica. Dentro de estas 36 proteínas, 19 se agrupan en formas localizadas, 14 se agrupan como formas sistémicas y 3 proteínas pueden identificarse como cualquiera de las dos. Estas proteínas pueden volverse irregulares debido a efectos genéticos, así como a factores ambientales adquiridos. Los cuatro tipos más comunes de amiloidosis sistémica son la cadena ligera (AL), la inflamación (AA), la relacionada con la diálisis (Aβ2M) y la hereditaria y de la vejez (ATTR y transtiretina amiloide de tipo salvaje)..
Se puede sospechar el diagnóstico cuando se encuentran proteínas en la orina, hay agrandamiento de órganos o se encuentran problemas con múltiples nervios periféricos y no está claro por qué. El diagnóstico se confirma mediante biopsia de tejido. Debido a la presentación variable, a menudo puede llevar algún tiempo llegar al diagnóstico.
El tratamiento está orientado a disminuir la cantidad de proteína involucrada. En ocasiones, esto se puede lograr determinando y tratando la causa subyacente. La amiloidosis AL ocurre en aproximadamente 3 a 13 por millón de personas por año y la amiloidosis AA en aproximadamente 2 por millón de personas por año. La edad habitual de aparición de estos dos tipos es entre los 55 y 60 años. Sin tratamiento, la esperanza de vida oscila entre seis meses y cuatro años. En el mundo desarrollado, aproximadamente 1 de cada 1.000 personas muere anualmente a causa de amiloidosis sistémica. La amiloidosis se ha descrito al menos desde 1639.
Signos y síntomas

La presentación de la amiloidosis es amplia y depende del sitio de acumulación de amiloide. El riñón y el corazón son los órganos más comúnmente afectados.
Riñones
El depósito de amiloide en el riñón a menudo afecta los capilares glomerulares y las regiones mesangiales, lo que afecta la capacidad del órgano para filtrar y excretar desechos y retener proteínas plasmáticas. Esto puede provocar niveles elevados de proteínas en la orina (proteinuria) y síndrome nefrótico. Varios tipos de amiloidosis, incluidos los tipos AL y AA, se asocian con el síndrome nefrótico. Aproximadamente el 20% y el 40-60% de las personas con amiloidosis AL y AA, respectivamente, progresan a una enfermedad renal terminal que requiere diálisis.
Corazón
El depósito de amiloide en el corazón puede causar insuficiencia cardíaca tanto diastólica como sistólica. Es posible que se presenten cambios en el ECG, que muestran bajo voltaje y anomalías de la conducción, como bloqueo auriculoventricular o disfunción del nódulo sinusal. En la ecocardiografía, el corazón muestra un patrón de llenado restrictivo, con una función sistólica normal o levemente reducida. La amiloidosis AA generalmente no afecta al corazón. La amiloidosis cardíaca puede presentarse con síntomas de insuficiencia cardíaca que incluyen dificultad para respirar, fatiga y edema. A medida que avanza la amiloidosis cardíaca, el depósito de amiloide puede afectar la capacidad del corazón para bombear y llenar sangre, así como su capacidad para mantener un ritmo normal, lo que empeora la función cardíaca y reduce la calidad de vida de las personas.
Sistema nervioso
Las personas con amiloidosis pueden tener afectación del sistema nervioso central, además de afectación periférica que causa neuropatías sensoriales y autonómicas. La neuropatía sensorial se desarrolla con un patrón simétrico y progresa de distal a proximal. La neuropatía autónoma puede presentarse como hipotensión ortostática, pero puede manifestarse más gradualmente con síntomas gastrointestinales inespecíficos como estreñimiento, náuseas o saciedad temprana. La amiloidosis del sistema nervioso central puede tener presentaciones sistémicas más graves que pueden incluir arritmias potencialmente mortales, insuficiencia cardíaca, desnutrición, infección o muerte.
La presentación neuropática puede depender de la etiología de la amiloidosis. Las personas con amiloidosis pueden experimentar disfunción en varios sistemas de órganos según la ubicación y el grado de afectación del sistema nervioso. Por ejemplo, la neuropatía periférica puede causar disfunción eréctil, incontinencia y estreñimiento, disfunción pupilar y pérdida sensorial según la distribución de la amiloidosis a lo largo de los diferentes nervios periféricos.
Órganos gastrointestinales y accesorios
La acumulación de proteínas amiloides en el sistema gastrointestinal puede ser causada por una amplia gama de trastornos amiloides y tener diferentes presentaciones según el grado de afectación del órgano. Los síntomas potenciales incluyen pérdida de peso, diarrea, dolor abdominal, acidez de estómago (reflujo gastrointestinal) y sangrado gastrointestinal. La amiloidosis también puede afectar los órganos digestivos accesorios, incluido el hígado, y puede presentarse con ictericia, heces grasas, anorexia, acumulación de líquido en el abdomen y agrandamiento del bazo.
La acumulación de proteínas amiloides en el hígado puede provocar elevaciones de las aminotransferasas séricas y la fosfatasa alcalina, dos biomarcadores de lesión hepática, que se observan en aproximadamente un tercio de las personas. El agrandamiento del hígado es común. Por el contrario, el agrandamiento del bazo es poco común y ocurre en el 5% de las personas. La disfunción esplénica, que conduce a la presencia de cuerpos de Howell-Jolly en el frotis de sangre, ocurre en el 24% de las personas con amiloidosis. La malabsorción se observa en el 8,5% de las amiloidosis AL y en el 2,4% de las amiloidosis AA. Un mecanismo sugerido para la malabsorción observada es que los depósitos de amiloide en las puntas de las vellosidades intestinales (proyecciones en forma de dedos que aumentan el área intestinal disponible para la absorción de alimentos) comienzan a erosionar la funcionalidad de las vellosidades, presentando un cuadro similar a un esprúe.
Glándulas
Se pueden infiltrar tanto la tiroides como las glándulas suprarrenales. Se estima que entre el 10% y el 20% de las personas con amiloidosis tienen hipotiroidismo. La infiltración suprarrenal puede ser más difícil de apreciar dado que sus síntomas de hipotensión ortostática y baja concentración de sodio en sangre pueden atribuirse a neuropatía autonómica e insuficiencia cardíaca.
"Los depósitos de amiloide se producen en el páncreas de personas que también tienen diabetes mellitus, aunque no se sabe si esto es funcionalmente importante. El componente principal del amiloide pancreático es un péptido de residuos de 37 aminoácidos conocido como polipéptido amiloide de los islotes o "amilina". Este se almacena con la insulina en gránulos secretores en las células β y se cosecreta con la insulina." (Farmacología de Rang y Dale, 2015.)
Sistema musculoesquelético
Las proteínas amiloides se depositan con mayor frecuencia dentro de la rodilla, seguidas de las manos, las muñecas, el codo, la cadera y el tobillo, lo que provoca dolor en las articulaciones. En hombres de edad avanzada (>80 años), existe un riesgo significativo de depósito de amiloide de transtiretina de tipo salvaje en el tejido sinovial de la articulación de la rodilla, pero predominantemente en la vejez se observa depósito de transtiretina de tipo salvaje en los ventrículos cardíacos. Se han encontrado depósitos de ATTR en el ligamento amarillo de pacientes sometidos a cirugía por estenosis espinal lumbar.
En la amiloidosis beta 2-microglobulina, los hombres tienen un alto riesgo de padecer el síndrome del túnel carpiano. La amiloidosis Aβ2MG (amiloidosis asociada a hemodiálisis) tiende a depositarse en el tejido sinovial, provocando una inflamación crónica del tejido sinovial en la rodilla, la cadera, el hombro y las articulaciones interfalángicas. El depósito de cadenas ligeras de amiloide en la articulación del hombro provoca agrandamiento de los hombros, también conocido como "signo de la hombrera". Los depósitos de cadenas ligeras de amiloide también pueden causar poliartritis simétrica bilateral.
El depósito de proteínas amiloides en la médula ósea sin causar discrasias de células plasmáticas se llama amiloidoma. Se encuentra comúnmente en las vértebras cervicales, lumbares y sacras. Los afectados pueden presentar dolor óseo debido a lisis ósea, paraparesia lumbar y una variedad de síntomas neurológicos. Las fracturas vertebrales también son comunes.
Ojos
Un desarrollo poco común es la púrpura amiloide, una susceptibilidad a sangrar con hematomas alrededor de los ojos, denominados "ojos de mapache". La púrpura amiloide es causada por el depósito de amiloide en los vasos sanguíneos y la actividad reducida de la trombina y el factor X, dos proteínas de la coagulación que pierden su función después de unirse al amiloide.
Cavidad bucal
Los depósitos de amiloide en el tejido pueden causar agrandamiento de las estructuras. El veinte por ciento de las personas con amiloidosis AL tienen la lengua agrandada, lo que puede provocar apnea obstructiva del sueño, dificultad para tragar y alteración del gusto. El agrandamiento de la lengua no ocurre en la amiloidosis ATTR o AA. El depósito de amiloide en la garganta puede provocar ronquera.
Patogenia
Las amiloidosis pueden considerarse enfermedades por plegamiento incorrecto de proteínas. La gran mayoría de las proteínas que forman depósitos de amiloide son proteínas secretadas, por lo que el plegamiento incorrecto y la formación de amiloide se producen fuera de las células, en el espacio extracelular. De las 37 proteínas identificadas hasta ahora como vulnerables a la formación de amiloide, sólo cuatro son citosólicas. La mayoría de las proteínas formadoras de amiloide son relativamente pequeñas, pero por lo demás no hay evidencia de similitudes estructurales o funcionales entre las proteínas que se sabe que forman amiloides asociados a enfermedades. Un tercio de la enfermedad amiloide es hereditaria, en cuyo caso normalmente aparece a una edad temprana. La mitad de las enfermedades relacionadas con el amiloide son esporádicas y tienen una edad de aparición tardía; en estos casos, la agregación de proteínas puede estar asociada con una disminución de la regulación de las proteínas relacionada con el envejecimiento. Algunos tratamientos médicos están asociados con la enfermedad amiloide, pero esto es poco común.
Las proteínas formadoras de amiloide se agregan en formas fibrilares distintivas con una estructura de lámina beta. La forma de lámina beta del amiloide es resistente a la proteólisis, lo que significa que no se puede degradar ni descomponer. Como resultado, el amiloide se deposita en el espacio extracelular del cuerpo. Se cree que el proceso de formación de fibrillas de amiloide tiene formas oligoméricas intermedias. Tanto los oligómeros como las fibrillas de amiloide pueden ser tóxicos para las células y pueden interferir con el funcionamiento adecuado de los órganos. La importancia relativa de las diferentes especies de agregación puede depender de la proteína involucrada y del sistema de órganos afectado.
Diagnóstico
El diagnóstico de amiloidosis generalmente requiere una biopsia de tejido. La biopsia se evalúa en busca de evidencia de depósitos de amiloide característicos. La tela se trata con varios tintes. La tinción más útil en el diagnóstico de amiloide es el rojo Congo, que, combinado con luz polarizada, hace que las proteínas amiloides aparezcan de color verde manzana en el microscopio. Además, se puede utilizar la tinción con tioflavina T. También se utilizan varias técnicas de imágenes, como una exploración PYP, una exploración DPD o una exploración SAP.
Se puede realizar una biopsia de una muestra de tejido u obtenerla directamente del órgano interno afectado, pero el sitio de primera línea de la biopsia es la grasa abdominal subcutánea, conocida como "biopsia de almohadilla grasa", debido a su facilidad. de adquisición. Una biopsia de grasa abdominal no es completamente sensible y puede dar resultados falsos negativos, lo que significa que un resultado negativo no excluye el diagnóstico de amiloidosis. Sin embargo, la biopsia directa del órgano afectado puede seguir siendo innecesaria, ya que también se pueden utilizar otros métodos de biopsia menos invasivos, como la biopsia de la mucosa rectal, las glándulas salivales, los labios o la médula ósea, con la que se puede lograr un diagnóstico hasta en el 85% de las personas.
En el depósito de amiloide de las articulaciones, habrá una señal disminuida en las imágenes de resonancia magnética ponderadas en T1 y T2. En el amiloidoma, habrá señal T1 baja con la inyección de gadolinio y señal T2 baja.
El tipo de proteína amiloide se puede determinar de varias maneras: la detección de proteínas anormales en el torrente sanguíneo (mediante electroforesis de proteínas o determinación de cadenas ligeras); unión de anticuerpos particulares al amiloide que se encuentra en el tejido (inmunohistoquímica); o extracción de la proteína e identificación de sus aminoácidos individuales. La inmunohistoquímica puede identificar la amiloidosis AA la mayor parte del tiempo, pero puede pasar por alto muchos casos de amiloidosis AL. La microdisección láser con espectrometría de masas es el método más fiable para identificar las diferentes formas de amiloidosis.
Anteriormente, la AL se consideraba la forma más común de amiloidosis y el diagnóstico a menudo comienza con la búsqueda de discrasia de células plasmáticas, células B de memoria que producen inmunoglobulinas o porciones de inmunoglobulinas aberrantes. La electroforesis por inmunofijación de orina o suero es positiva en el 90% de las personas con amiloidosis AL. La electroforesis por inmunofijación es más sensible que la electroforesis regular, pero es posible que no esté disponible en todos los centros. Alternativamente, se puede buscar la tinción inmunohistoquímica de una biopsia de médula ósea en busca de células plasmáticas dominantes en personas con una alta sospecha clínica de amiloidosis AL pero con electroforesis negativa.
Actualmente se considera que la ATTR es la forma más común de amiloidosis. Puede estar relacionada con la edad en ATTR de tipo salvaje (ATTRv) o amiloidosis familiar asociada a transtiretina; se sospecha en personas con antecedentes familiares de neuropatías idiopáticas o insuficiencia cardíaca que carecen de evidencia de discrasias de células plasmáticas. ATTR se puede identificar mediante enfoque isoeléctrico que separa formas mutadas de transtiretina. Los hallazgos pueden corroborarse mediante pruebas genéticas para buscar mutaciones específicas conocidas en la transtiretina que predispongan a la amiloidosis.
Se sospecha AA por motivos clínicos en personas con infecciones prolongadas o enfermedades inflamatorias. AA se puede identificar mediante tinción inmunohistoquímica.
Pequeño dúodeno intestinal con deposición amiloidea Congo rojo 10X
Amyloidosis, calcificación distrófica
Pequeño dúodeno intestinal con deposición amiloidea 20X
Amyloidosis, Nodo, Congo Rojo
Amyloidosis, vasos sanguíneos, H
Amyloidosis, ganglio linfático, H
Amyloidosis, ganglio linfático, polarizador
Amyloidosis cardiaca. Mancha de H.E.
Micrografo mostrando deposición amiloidea (material de flujo rojo) en el corazón (amiloidosis cardiaca). Mancha roja Congo.
Clasificación
Los sistemas de clasificación histórica se basaron en factores clínicos. Hasta principios de la década de 1970 predominó la idea de una única sustancia amiloide. Se propusieron varios sistemas de clasificación descriptivos basados en la distribución orgánica de los depósitos de amiloide y los hallazgos clínicos. La mayoría de los sistemas de clasificación incluían amiloidosis primaria (es decir, idiopática), en la que no se identificó ninguna afección clínica asociada, y amiloidosis secundaria (es decir, secundaria a afecciones inflamatorias crónicas). Algunos sistemas de clasificación incluían amiloidosis asociada a mieloma, familiar y localizada.
La era moderna de la clasificación de la amiloidosis comenzó a finales de la década de 1960 con el desarrollo de métodos para hacer solubles las fibrillas de amiloide. Estos métodos permitieron a los científicos estudiar las propiedades químicas de los amiloides. Los términos descriptivos como amiloidosis primaria, amiloidosis secundaria y otros (p. ej., amiloidosis senil), que no se basan en la causa, proporcionan poca información útil y ya no se recomiendan.
La clasificación moderna de la enfermedad amiloide tiende a utilizar una abreviatura de la proteína que produce la mayoría de los depósitos, precedida por la letra A. Por ejemplo, la amiloidosis causada por la transtiretina se denomina "ATTR". Los patrones de deposición varían entre personas, pero casi siempre están compuestos por una sola proteína amiloidogénica. La deposición puede ser sistémica (que afecta a muchos sistemas de órganos diferentes) o específica de un órgano. Muchas amiloidosis se heredan debido a mutaciones en la proteína precursora.
Otras formas se deben a diferentes enfermedades que causan una producción excesiva o anormal de proteínas, como la sobreproducción de cadenas ligeras de inmunoglobulinas (denominada amiloidosis AL) o la sobreproducción continua de proteínas de fase aguda en la inflamación crónica (que puede provocar amiloidosis AA)..
Hasta ahora se han identificado alrededor de 60 proteínas amiloides. De ellos, al menos 36 se han asociado con una enfermedad humana.
Todas las proteínas de fibrillas de amiloide comienzan con la letra "A" seguido del sufijo de proteína (y cualquier especificación aplicable). Consulte a continuación una lista de proteínas de fibrillas de amiloide que se han encontrado en humanos:
| Proteína fibril | Proteína precursora | Órganos de destino | Sistémica o localizada | Adquirido o hereditario |
|---|---|---|---|---|
| AL | Cadena ligera de inmunoglobulina | Todos los órganos, normalmente excepto el SNC | S, L | A, H |
| AH | Cadena pesada inmunoglobulina | Todos los órganos excepto el SNC | S, L | A |
| AA | (Apo) srum amyloid A | Todos los órganos excepto el SNC | S | A |
| ATTR | Transtirretina, tipo salvaje
Transtirretina, variantes | Corazón principalmente en machos, pulmón, ligamentos, tenosinonovio
PNS, ANS, corazón, ojo, leptomeninges | S
S | A
H |
| Aβ2M | β2-microglobulina, tipo salvaje
β2-microglobulina, variantes | Sistema musculoesquelético
ANS | S
S | A
H |
| AApoAI | Apolipoproteína A I, variantes | Corazón, hígado, riñón, PNS, testis, laringe (C
variantes terminales), piel (Varias terminales C) | S | H |
| AApoAII | Apolipoproteína A II, variantes | Kidney | S | H |
| AApoAIV | Apolipoproteína A IV, tipo salvaje | Medulla renal y sistémica | S | A |
| AApoCII | Apolipoproteína C II, variantes | Kidney | S | H |
| AApoCIII | Apolipoproteína C III, variantes | Kidney | S | H |
| AGel | Gelsolin, variantes | Riñón, PNS, córnea | S | H |
| ALys | Lysozyme, variantes | Kidney | S | H |
| ALECT2 | Leukocyte chemotactic factor-2 | Riñón, principalmente | S | A |
| AFib | Fibrinogen a, variantes | Riñón, principalmente | S | H |
| ACys | Cistatina C, variantes | CNS, PNS, piel | S | H |
| ABri | ABriPP, variantes | CNS | S | H |
| ADanb | ADanPP, variantes | CNS | L | H |
| Aβ | Aβ proteína precursor, tipo salvaje
Aβ proteína precursor, variante | CNS
CNS | L
L | A
H |
| AαSyn | α-Synuclein | CNS | L | A |
| ATau | Tau | CNS | L | A |
| APrP | Proteína de prión, tipo salvaje
Variantes de proteína prión Variante de proteína de prión | CJD, fatal insomnio
CJD, síndrome de GSS, insomnio fatal PNS | L
L S | A
H H |
| ACal | (Pro)calcitonin | tumores tiroideos de células C
Kidney | L
S | A
A |
| AIAPP | Polipéptido de amiloidec | Islets de Langerhans, insulinomas | L | A |
| AANF | Factor natriurético auricular | Cardiac atria | L | A |
| APro | Prolactin | Pituitary prolactinomas, aging pituitary | L | A |
| AIns | Insulina | Inyección hematogénica, local | L | A |
| SsPCd | Proteína de surfactante pulmonar | Lung | L | A |
| ACor | Corneodesmosin | Epitelia Cornificada, folículos capilares | L | A |
| AMed | Lactadherin | Senile aortic, media | L | A |
| AKer | Kerato-epithelin | Cornea, hereditario | L | A |
| ALac | Lactoferrin | Cornea | L | A |
| AOAAP | Proteína asociada con ameloblasto odontogénico | Tumores odontogénicos | L | A |
| Ssem1 | Semenogelin 1 | Vesicula seminalis | L | A |
| AEnf | Enfurvitide | Iatrogénico | L | A |
| ACatKe | Cathepsin K | tumor asociado | L | A |
| AEFEMP1e | Extracelular que contiene fibulina
proteína de matriz 1 (EFEMP1) | Venas de portal, Envejecimiento asociado | L | A |
Alternativa
Un método clínico de clasificación más antiguo se refiere a las amiloidosis como sistémicas o localizadas:
- Las amiloidosis sistémicas afectan más de un órgano o sistema corporal. Ejemplos son AL, AA y Aβ2m.
- Las amiloidosas localizadas afectan sólo a un órgano o tipo de tejido corporal. Ejemplos son Aβ, IAPP, factor natriurético auricular (en amyloidosis auricular aislada), y Calcitonina (en carcinoma medular de la tiroides)
Otra clasificación es primaria o secundaria.
- Las amiloidosas primarias surgen de una enfermedad con función celular inmune desordenada, como el mieloma múltiple u otras discrasias inmunocitarias.
- La amiloidosa secundaria (reactiva) ocurre como una complicación de alguna otra enfermedad inflamatoria crónica o destructora de tejido. Ejemplos son la amiloidosis sistémica reactiva y la amiloidosis cutánea secundaria.
Además, según los tejidos en los que se deposita, se divide en mesenquimatoso (órganos derivados del mesodermo) o parenquimatoso (órganos derivados del ectodermo o endodermo).
Tratamiento
El tratamiento depende del tipo de amiloidosis presente. El tratamiento con dosis altas de melfalán, un agente quimioterapéutico, seguido de un trasplante de células madre se ha mostrado prometedor en los primeros estudios y se recomienda para la amiloidosis AL en estadios I y II. Sin embargo, sólo entre el 20% y el 25% de las personas son elegibles para un trasplante de células madre. El tratamiento de quimioterapia que incluye ciclofosfamida-bortezomib-dexametasona es actualmente la opción de tratamiento recomendada para personas con amiloidosis AL que no son elegibles para trasplante.
En AA, los síntomas pueden mejorar si se trata la afección subyacente. En personas que tienen inflamación causada por amiloidosis AA, los inhibidores del factor de necrosis tumoral (TNF) alfa, como infliximab y etanercept, se utilizan durante una duración promedio de 20 meses. Si los inhibidores del TNF-alfa no son eficaces, se pueden considerar los inhibidores de la interleucina-1 (p. ej., anakinra, canakinumab, rilonacept) y los inhibidores de la interleucina-6 (p. ej., tocilizumab).
El tratamiento de la amiloidosis ATTR dependerá de su clasificación como tipo salvaje o variante. Ambos pueden tratarse con tafamidis, un agente oral de baja toxicidad que previene la desestabilización de las proteínas correctamente plegadas. Los estudios demostraron que tafamidis redujo la mortalidad y la hospitalización por insuficiencia cardíaca. Anteriormente, para la amiloidosis variante ATTR, el trasplante de hígado era el único tratamiento eficaz. Las nuevas terapias incluyen diflunisal, inotersen y patisiran.
El diflunisal se une a la proteína TTR mutante mal plegada para evitar su acumulación, de la misma manera que funciona el tafamidis. La evidencia de certeza baja indica que mitiga el empeoramiento de la neuropatía periférica y la discapacidad debido a la progresión de la enfermedad.
Inotersen bloquea la expresión genética de la TTR tanto de tipo salvaje como mutante, reduciendo el precursor amiloide. La evidencia de certeza moderada sugiere que mitiga el empeoramiento de la neuropatía periférica. La eficacia y seguridad a largo plazo del uso de inotersen en personas con amiloidosis relacionada con TTR mutante aún se están evaluando en un ensayo clínico de fase III a partir de 2021. Tanto el diflunisal como el inotersen también pueden mitigar la disminución de la calidad de vida, aunque la evidencia porque este efecto no está claro. Para las personas con ATTR cardíaca, el efecto del uso de inotersen no es concluyente y requiere más investigación. En 2018, la Agencia Europea de Medicamentos aprobó el inotersen para tratar la polineuropatía en adultos con amiloidosis hereditaria por transtiretina. Desde entonces ha sido aprobado para su uso en Canadá, la Unión Europea y Estados Unidos.
Patisiran funciona de manera similar a inotersen. La evidencia de certeza moderada sugiere que el patisirán mitiga el empeoramiento de la neuropatía periférica y la discapacidad debido a la progresión de la enfermedad. Además, la evidencia de certeza baja sugiere que el patisirán mitiga la disminución de la calidad de vida y reduce ligeramente la tasa de eventos adversos versus placebo. No hay evidencia de un efecto sobre la tasa de mortalidad. Una revisión de los primeros datos sobre el uso de patisirán en personas con ATTR cardíaca variante sugiere que puede reducir la mortalidad y la hospitalización; sin embargo, esto aún se está investigando y requiere más investigación. En 2018, el NICE en el Reino Unido no recomendó patisirán para la amiloidosis hereditaria relacionada con la transtiretina. Sin embargo, a partir de julio de 2019 se está llevando a cabo una revisión adicional. Sin embargo, fue aprobado para este uso en los Estados Unidos.
Aún se están investigando las funciones de inotersen y patisiran en la amiloidosis ATTR cardíaca.
En 2021, en un ensayo clínico que utilizó la técnica de edición de genes CRISPR, varios participantes tuvieron una caída del "80 % al 96 % en los niveles de TTR, igual o mejor que el promedio del 81 %" a quienes les dieron patisiran.
Vutrisiran fue aprobado por la Administración de Medicamentos y Alimentos de EE. UU. (FDA) en junio de 2022 para el tratamiento de la polineuropatía de la amiloidosis hereditaria mediada por transtiretina (hATTR) en adultos.
Grupos de apoyo
Las personas afectadas por amiloidosis cuentan con el apoyo de organizaciones, incluido el Amyloidosis Research Consortium, Amyloidosis Foundation, Amyloidosis Support Groups y Australian Amyloidosis Network.
Pronóstico
El pronóstico varía según el tipo de amiloidosis y el sistema de órganos afectado. El pronóstico de la amiloidosis cardíaca AL no tratada es malo, con una mediana de supervivencia de seis meses. Más específicamente, la amiloidosis AL se puede clasificar en estadio I, II o III según biomarcadores cardíacos como Nt-proBNP y troponina cardíaca. La supervivencia disminuye a medida que aumenta el estadio, pero los avances recientes en los tratamientos han mejorado las tasas de supervivencia media para los estadios I, II y III, a 91,2, 60 y 7 meses, respectivamente.
Los resultados en una persona con amiloidosis AA dependen de la enfermedad subyacente, los órganos afectados y se correlacionan con la concentración de proteína amiloide A sérica.
Las personas con ATTR, ATTR mutante y ATTR de tipo salvaje tienen un mejor pronóstico en comparación con las personas con AL y pueden sobrevivir durante más de una década. El tiempo de supervivencia no está asociado con el sexo o la edad; sin embargo, algunas medidas de función cardíaca reducida están asociadas con un tiempo de supervivencia más corto.
Se determinó que la amiloidosis sistémica senil es la causa principal de muerte en el 70 % de las personas mayores de 110 años a las que se les realizó autopsia.
Epidemiología
La amiloidosis tiene una prevalencia estimada combinada de 30 por 100 000 personas, siendo las tres formas más comunes AL, ATTR y AA. La edad promedio en el momento del diagnóstico es 64 años.
La AL tiene la incidencia más alta con aproximadamente 12 casos por millón de personas por año y una prevalencia estimada de 30 000 a 45 000 casos en los EE. UU. y la Unión Europea.
La amiloidosis AA es la forma más común en los países en desarrollo y puede complicar infecciones prolongadas con tuberculosis, osteomielitis y bronquiectasias. La amiloidosis AA es causada por un aumento en el depósito extracelular de proteína amiloide A (SAA) sérica. Los niveles de proteína SAA pueden aumentar de manera directa e indirecta, a través de infecciones, inflamación y tumores malignos. Las causas más comunes de amiloidosis AA en Occidente son la artritis reumatoide, la enfermedad inflamatoria intestinal, la psoriasis y la fiebre mediterránea familiar.
Las personas sometidas a hemodiálisis a largo plazo (14 a 15 años) pueden desarrollar amiloidosis por acumulación de cadenas ligeras del complejo HLA 1 que normalmente se filtra por los riñones.
La amiloidosis por transtiretina de tipo salvaje (ATTR) se encuentra en una cuarta parte de los ancianos en la autopsia. La ATTR se encuentra en entre el 13% y el 19% de las personas que padecen insuficiencia cardíaca con fracción de eyección conservada, lo que la convierte en una forma muy común de amiloidosis sistémica.
Investigación
Los tratamientos para la neuropatía relacionada con ATTR incluyen oligonucleótidos específicos de TTR en forma de pequeño ARN de interferencia (patisiran) o inotersen antisentido; el primero recibió recientemente la aprobación de la FDA. Las investigaciones sobre tratamientos para la amiloidosis ATTR han comparado el trasplante de hígado, los medicamentos orales que estabilizan la proteína que se plega mal (incluidos tafamidis y diflunisal) y agentes terapéuticos más nuevos que aún se están investigando (incluido el patisirán). Según las investigaciones disponibles, el trasplante de hígado sigue siendo la opción de tratamiento más eficaz para la amiloidosis ATTR avanzada, los fármacos estabilizadores de proteínas pueden retardar la progresión de la enfermedad, pero fueron insuficientes para justificar el retraso del trasplante de hígado, y los agentes más nuevos, como el patisirán, requieren estudios adicionales.