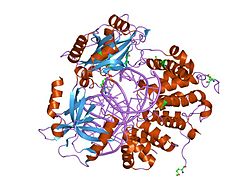
ADN ligasa 1
Discovery

Contratación y reglamentación
LIG1 codifica una enzima de 120 kDa y 919 residuos de longitud, conocida como ADN ligasa 1. El polipéptido de la ADN ligasa 1 contiene una secuencia de referencia para la fábrica de replicación (RFTS) en el extremo N-terminal, seguida de una secuencia de localización nuclear (NLS) y tres dominios funcionales. Los tres dominios consisten en un dominio de unión al ADN (DBD) en el extremo N-terminal, una nucleotidiltransferasa catalítica (NTasa) y un dominio de unión a oligonucleótidos/oligosacáridos (OB) en el extremo C-terminal. Aunque el extremo N-terminal del péptido no tiene actividad catalítica, es necesario para la actividad celular. El extremo N-terminal de la proteína contiene una secuencia de referencia para la fábrica de replicación que se utiliza para reclutarla a los sitios de replicación del ADN conocidos como fábricas de replicación.
La activación y el reclutamiento de la ADN ligasa 1 parecen estar asociados con modificaciones postraduccionales. El dominio N-terminal se completa mediante la fosforilación de cuatro residuos de serina en este dominio, Ser51, Ser76 y Ser91, por la quinasa dependiente de ciclina (CDK), y Ser66 por la caseína quinasa II (CKII). Se ha demostrado que la fosforilación de estos residuos (en particular, Ser66) regula la interacción entre los RFTS y el antígeno nuclear de células proliferantes (PCNA) cuando la ligasa 1 se recluta a las fábricas de replicación durante la fase S. Rossi et al. propusieron que, cuando Ser66 se desfosforila, los RFTS de la ligasa 1 interactúan con el PCNA, lo cual fue confirmado in vitro por Tom et al. Ambos conjuntos de datos proporcionan evidencia plausible de que la región N-terminal de la ligasa I desempeña un papel regulador en la función enzimática in vivo en el núcleo. Además, mediante análisis mutacional, se demostró que la identificación de un motivo de unión a ciclina (Cy) en el dominio catalítico C-terminal desempeña un papel en la fosforilación de las serinas 91 y 76. Juntas, las serinas N-terminales son sustratos de CDK y CKII, que parecen desempeñar un importante papel regulador en el reclutamiento de la ADN ligasa I a la fábrica de replicación durante la fase S del ciclo celular.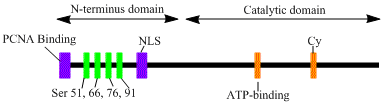
Función y mecanismo
LIG1 codifica la ADN ligasa 1, que participa en la replicación del ADN y en el proceso de reparación por escisión de bases.
La ADN ligasa 1 eucariota cataliza una reacción químicamente universal para todas las ligasas. Utiliza trifosfato de adenosina (ATP) para catalizar los eventos de ligadura energéticamente favorables, tanto en la replicación como en la reparación del ADN. Durante la fase de síntesis (fase S) del ciclo celular eucariota, se produce la replicación del ADN. La ADN ligasa 1 se encarga de unir los fragmentos de Okazaki formados durante la síntesis discontinua de ADN en la hebra rezagada, después de que la ADN polimerasa δ haya reemplazado los nucleótidos cebadores del ARN por nucleótidos de ADN. Si los fragmentos de Okazaki no se ligan correctamente, el ADN no ligado (que contiene una muesca) podría degradarse fácilmente hasta romperse en la doble hebra, un fenómeno que se sabe que causa mutaciones genéticas. Para ligar estos fragmentos, la ligasa sigue tres pasos:- Adición de un grupo monofosfato adenosino (AMP) a la enzima, denominado adenilación,
- Transferencia de monofosfato adenosina al ADN y
- Nick sellado, o formación de enlaces de fósforo.

Durante la adenililación, se produce un ataque nucleofílico al fosfato alfa del ATP de una lisina catalítica, lo que resulta en la producción de pirofosfato inorgánico (PPi) y un intermediario lisina-AMP unido covalentemente en el sitio activo de la ADN ligasa 1.
Durante la transferencia de AMP, la ADN ligasa se asocia con el ADN, localiza una muesca y cataliza una reacción en el sitio fosfato 5' de la muesca de ADN. Un oxígeno aniónico en el fosfato 5' de la muesca de ADN actúa como nucleófilo, atacando el fosfato alfa del AMP unido covalentemente, lo que provoca que el AMP se convierta en un intermediario unido covalentemente (intermediario ADN-AMP).Para que se forme el enlace fosfodiéster, es necesario escindir el intermediario ADN-AMP. Para lograrlo, se produce un ataque nucleofílico sobre el fosfato 5' desde el hidroxilo 3' aguas arriba, lo que resulta en la formación del enlace fosfodiéster. Durante este ataque nucleofílico, el grupo AMP se separa del fosfato 5' como grupo saliente, lo que permite sellar la muesca y liberar el AMP, completando así un ciclo de ligadura del ADN.En condiciones subóptimas, la ligasa puede disociarse del ADN antes de que la reacción se complete. Se ha demostrado que los niveles de magnesio pueden ralentizar el proceso de sellado de la mella, provocando que la ligasa se disocie del ADN, dejando un intermediario adenililado abortado incapaz de ser fijado sin la ayuda de una fosfodiesterasa. Se ha demostrado que la aprataxina (una fosfodiesterasa) actúa sobre los intermediarios de ADN abortados mediante la hidrólisis del enlace AMP-fosfato, restaurando el ADN a su estado inicial antes de que la ligasa reaccionara.Papel en la reparación de la base dañada

Significado clínico
Referencias
- ^ a b c GRCh38: Ensembl release 89: ENSG00000105486 – Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00056394 – Ensembl, May 2017
- ^ "Human PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Kresge N, Simoni RD, Hill RL (enero 2007). "Insights into DNA Joining: I. Robert Lehman's work on DNA Ligase". Journal of Biological Chemistry. 282 2): e1 – e3. doi:10.1016/S0021-9258(20)73504-0.
- ^ a b c Ferrari G, Rossi R, Arosio D, Vindigni A, Biamonti G, Montecucco A (septiembre de 2003). "Fosforilación dependiente del ciclo celular del ligase de ADN humano I en los sitios de cinasa dependientes de la ciclina". El Diario de Química Biológica. 278 (39): 37761 –7. doi:10.1074/jbc.M304462200. PMID 12851383.
- ^ a b Rossi R, Villa A, Negri C, Scovassi I, Ciarrocchi G, Biamonti G, Montecucco A (octubre de 1999). "La fábrica de replicación dirigida secuencia / sitio de unión PCNA se requiere en G(1) para controlar el estado de fosforilación del ligase I de ADN". El Diario EMBO. 18 (20): 5745 –54. doi:10.1093/emboj/18.20.5745. PMC 1171641. PMID 10523317.
- ^ a b c Ellenberger T, Tomkinson AE (2008). "Límites de ADN eucarísticos: ideas estructurales y funcionales". Examen anual de la bioquímica. 77: 313–38. doi:10.1146/annurev.biochem.77.061306.123941. PMC 2933818. PMID 18518823.
- ^ Prigent C, Lasko DD, Kodama K, Woodgett JR, Lindahl T (agosto de 1992). "Activación de ligasa de ADN mamífero I a través de la fosforilación por casein kinase II". El Diario EMBO. 11 (8): 2925–33. doi:10.1002/j.1460-2075.1992.tb05362.x. PMC 556774. PMID 1639065.
- ^ a b "Entrez Gene: LIG1 ligase I, ADN, ATP-dependiente".
- ^ Sriskanda V, Shuman S (enero de 1998). "Chlorella virus ADN ligase: reconocimiento de nick y análisis mutacional". Nucleic Acids Research. 26 2): 525 –31. doi:10.1093/nar/26.2.525 (inactivo 1 de noviembre de 2024). PMC 147278. PMID 9421510.
{{cite journal}}: CS1 maint: DOI inactive as of November 2024 (link) - ^ Taylor MR, Conrad JA, Wahl D, O'Brien PJ (julio de 2011). "Mecanismo Kinetic de ligasa humana de ADN revela cambios dependientes del magnesio en el paso delimitación de velocidad que compromete la eficiencia de ligación". El Diario de Química Biológica. 286 (26): 23054–62. doi:10.1074/jbc.M111.248831. PMC 3123073. PMID 21561855.
- ^ a b Rass U, Ahel I, West SC (marzo de 2007). "Actions of aprataxin in multiple DNA repair pathways". El Diario de Química Biológica. 282 (13): 9469 –74. doi:10.1074/jbc.M611489200. PMID 17276982.
- ^ a b Sattler U, Frit P, Salles B, Calsou P (abril de 2003). "Síntesis de reparación de ADN durante la reparación de la escisión base en células mamíferas". EMBO Informes. 4 4): 363 –7. doi:10.1038/sj.embor.embor796. PMC 1319152. PMID 12671676.
- ^ a b Hegde ML, Hazra TK, Mitra S (enero de 2008). "Early steps in the DNA base excision/single-strand inspection pathway in mammalian cells". Cell Research. 18 1): 27 –47. doi:10.1038/cr.2008.8. PMC 2692221. PMID 18166975.
- ^ a b Balakrishnan L, Brandt PD, Lindsey-Boltz LA, Sancar A, Bambara RA (mayo de 2009). "La reparación de la escisión base de parche largo procede mediante la estimulación coordinada del complejo de reparación de ADN multienzima". El Diario de Química Biológica. 284 (22): 15158–72. doi:10.1074/jbc.M109.000505. PMC 2685697. PMID 19329425.
- ^ Maffucci P, Chavez J, Jurkiw TJ, O'Brien PJ, Abbott JK, Reynolds PR, et al. (diciembre 2018). "Las mutaciones en los ligas de ADN 1 subyacen a un espectro de deficiencias inmunitarias". The Journal of Clinical Investigation. 128 (12): 5489–5504. doi:10.1172/JCI99629. PMC 6264644. PMID 30395541.
- ^ Sun D, Urrabaz R, Nguyen M, Marty J, Stringer S, Cruz E, et al. (diciembre de 2001). "Expresión elevada de ligasa de ADN I en cánceres humanos". Clinical Cancer Research. 7 (12): 4143 –8. PMID 11751514.
- ^ Macdonald J (noviembre de 2008). "Smart DNA: Programming the Molecule of Life for Work and Play [Preview]". científicoamericano. Retrieved 2013-02-22.
Más lectura
- Leonhardt H, Cardoso MC (1996). "Formar y asociar proteínas con dominios funcionales en el núcleo: la solución insoluble". Organización estructural y funcional de la matriz nuclear. International Review of Cytology. Vol. 162B. pp. 303 –35. doi:10.1016/S0074-7696(08)62620-0. ISBN 978-0-12-364566-1. PMID 8557490.
- Tomkinson AE, Mackey ZB (febrero de 1998). "Strutura y función de ligas de ADN mamíferos". Mutation Research. 407 1): 1 –9. doi:10.1016/s0921-8777(97)00050-5. PMID 9539976.
- Perrigot M, Pierrot-Deseilligny E, Bussel B, Held JP (abril de 1976). "[Parálisis después de la radiografía Dimer X]". La Nouvelle Presse Médicale. 5 (17): 1120–2. PMID 934827.
- Webster AD, Barnes DE, Arlett CF, Lehmann AR, Lindahl T (junio de 1992). "El retraso del crecimiento y la inmunodeficiencia en un paciente con mutaciones en el gen ligase I del ADN". Lancet. 339 (8808): 1508 –9. doi:10.1016/0140-6736(92)91266-B. PMID 1351188. S2CID 11874717.
- Barnes DE, Tomkinson AE, Lehmann AR, Webster AD, Lindahl T (mayo de 1992). "Mutations in the DNA ligase I gene of an individual with immunodeficiencies and cellular hypersensitivity to DNA-damaging agents". Celular. 69 3): 495 –503. doi:10.1016/0092-8674(92)90450-Q. PMID 1581963. S2CID 11736507.
- Barnes DE, Kodama K, Tynan K, Trask BJ, Christensen M, De Jong PJ, et al. (enero de 1992). "Asignación del ligase de ADN de codificación genética I al cromosoma humano 19q13.2-13.3". Genómica. 12 1): 164 –6. doi:10.1016/0888-7543(92)90422-O. PMID 1733856.
- Petrini JH, Huwiler KG, Weaver DT (septiembre de 1991). "Un gen de ligase I de ADN de tipo salvaje se expresa en las células del síndrome de Bloom". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 88 (17): 7615–9. Bibcode:1991PNAS...88.7615P. doi:10.1073/pnas.88.17.7615. PMC 52352. PMID 1881902.
- Lasko DD, Tomkinson AE, Lindahl T (julio de 1990). " ligas de ADN mamíferos. Biosíntesis y localización intracelular de ligas de ADN I". El Diario de Química Biológica. 265 (21): 12618–22. doi:10.1016/S0021-9258(19)38388-7. PMID 2197279.
- Barnes DE, Johnston LH, Kodama K, Tomkinson AE, Lasko DD, Lindahl T (septiembre de 1990). "Human DNA ligase I cDNA: clonación y expresión funcional en Saccharomyces cerevisiae". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 87 (17): 6679–83. Bibcode:1990PNAS...87.6679B. doi:10.1073/pnas.87.17.6679. PMC 54600. PMID 2204063.
- Montecucco A, Savini E, Weighardt F, Rossi R, Ciarrocchi G, Villa A, Biamonti G (noviembre de 1995). "El dominio N-terminal del ligase humano del ADN contiene la señal de localización nuclear y dirige la enzima a sitios de replicación del ADN". El Diario EMBO. 14 (21): 5379 –86. doi:10.1002/j.1460-2075.1995.tb00222.x. PMC 394647. PMID 7489727.
- Maruyama K, Sugano S (enero de 1994). "Oligo-capping: un método simple para reemplazar la estructura de capa de mRNAs eucariotas con oligoribonucleótidos". Gene. 138 ()1 –2): 171–4. doi:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Trask B, Fertitta A, Christensen M, Youngblom J, Bergmann A, Copeland A, et al. (enero de 1993). "Fluorescence in situ Hybridization mapping of human chromosome 19: cytogenetic band location of 540 cosmids and 70 genes or DNA markers". Genómica. 15 1): 133 –45. doi:10.1006/geno.1993.1021. PMID 8432525.
- Petrini JH, Walsh ME, DiMare C, Chen XN, Korenberg JR, Weaver DT (septiembre de 1995). "Isolación y caracterización del homólogo humano MRE11". Genómica. 29 1): 80–6. doi:10.1006/geno.1995.1217. PMID 8530104.
- Bentley D, Selfridge J, Millar JK, Samuel K, Hole N, Ansell JD, Melton DW (agosto de 1996). "DNA ligase I es requerido para la eritropoiesis hepática fetal, pero no es esencial para la viabilidad celular mamífera". Nature Genetics. 13 4): 489 –91. doi:10.1038/ng0896-489. S2CID 20264173.
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K, Suyama A, Sugano S (octubre de 1997). "Construcción y caracterización de una biblioteca de cDNA completamente rica y de 5'''''' enriquecida". Gene. 200 ()1 –2): 149–56. doi:10.1016/S0378-1119(97)00411-3. PMID 9373149.
- Rossi R, Villa A, Negri C, Scovassi I, Ciarrocchi G, Biamonti G, Montecucco A (octubre de 1999). "La fábrica de replicación dirigida secuencia / sitio de unión PCNA se requiere en G(1) para controlar el estado de fosforilación del ligase I de ADN". El Diario EMBO. 18 (20): 5745 –54. doi:10.1093/emboj/18.20.5745. PMC 1171641. PMID 10523317.
- Matsumoto Y, Kim K, Hurwitz J, Gary R, Levin DS, Tomkinson AE, Park MS (noviembre de 1999). "Reconstitución de células proliferadoras nuclear antigeno-dependiente reparación de sitios apurinicos/apyrimidinicos con proteínas humanas purificadas". El Diario de Química Biológica. 274 (47): 33703 –8. doi:10.1074/jbc.274.47.33703. PMID 10559261.
- Vispé S, Satoh MS (septiembre de 2000). "DNA repara la formación de ADN de doble cadena mediada por parche en células humanas". El Diario de Química Biológica. 275 (35): 27386 –92. doi:10.1074/jbc.M003126200 (inactivo 2 de diciembre de 2024). PMID 10827190.
{{cite journal}}: CS1 maint: DOI inactive as of December 2024 (link)
Enlaces externos
- Reseña de toda la información estructural disponible en el PDB para UniProt: P18858 (DNA ligase 1) en el PDBe-KB.