Ácido hidroxámico
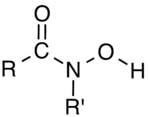
En química orgánica, los ácidos hidroxámicos son una clase de compuestos orgánicos que tienen una fórmula general R−C(=O)−N(−OH)−R' que lleva el grupo funcional −C(=O)−N(−OH)−, donde R y R' son típicamente grupos organilo (por ejemplo, alquilo o arilo) o hidrógeno. Son amidas (R−C(=O)−NH−R') en las que el átomo de nitrógeno tiene un sustituyente hidroxilo (−OH). A menudo se utilizan como quelantes de metales.
Un ejemplo común de ácido hidroxámico es el ácido aceto-N-metilhidroxámico (H3C−C(=O)−N(−OH)−CH3). Algunos ejemplos poco comunes de ácidos hidroxámicos son el ácido formo-N-clorohidroxámico (H−C(=O)−N(−OH)−Cl) y el ácido cloroformo-N-metilhidroxámico (Cl−C(=O)−N(−OH)−CH3).
Síntesis y reacciones
Los ácidos hidroxámicos se preparan generalmente a partir de ésteres o cloruros de ácido mediante una reacción con sales de hidroxilamina. Para la síntesis del ácido benzohidroxámico (C6H5−C(=O)−NH−OH o Ph−C(=O)−NH−OH, donde Ph es el grupo fenilo), la ecuación general es:
- C6H5−C(=O)−O−CH3 + NH2OH → C6H5−C(=O−NH−OH + CH3OH
Los ácidos hidroxámicos también pueden sintetizarse a partir de aldehídos y N-sulfonilhidroxilamina mediante la reacción de Angeli-Rimini. Alternativamente, el diperóxido de óxido de molibdeno oxida amidas trimetilsiladas a ácidos hidroxámicos, aunque los rendimientos son solo de alrededor del 50%. En una variación de la reacción de Nef, los compuestos nitro primarios mantenidos en una solución ácida (para minimizar el tautómero nitronato) se hidrolizan a un ácido hidroxámico.
Una reacción bien conocida de los ésteres de ácido hidroxámico es la transposición de Lossen.
Química de coordinación y bioquímica
- Galería de muestras
- Ferrichrome
- Deferoxamina
- Ácido Rhodotorulico
- Complejo Fe(III) de triacetylfusarinine
La base conjugada de los ácidos hidroxámicos se denomina hidroxamato. La desprotonación se produce en el grupo −N(−OH)−, y se elimina el átomo de hidrógeno, lo que da como resultado un anión hidroxamato R−C(=O)−N(−O−)−R'. La base conjugada resultante presenta al metal un ligando quelante aniónico conjugado O,O. Se han aislado muchos ácidos hidroxámicos y muchos hidroxamatos de hierro de fuentes naturales.
Funcionan como ligandos, generalmente para el hierro. La naturaleza ha desarrollado familias de ácidos hidroxámicos para que funcionen como compuestos que se unen al hierro (sideróforos) en las bacterias. Extraen el hierro (III) de fuentes que de otro modo serían insolubles (óxido, minerales, etc.). Los complejos resultantes se transportan a la célula, donde se extrae el hierro y se utiliza metabólicamente.
Los ligandos derivados del ácido hidroxámico y del ácido tiohidroxámico (un ácido hidroxámico en el que uno o ambos oxígenos del grupo funcional −C(=O)−N(−OH)− son reemplazados por azufre) también forman complejos fuertes con plomo(II).
Otros usos y ocurrencias
Los ácidos hidroxámicos se utilizan ampliamente en la flotación de minerales de tierras raras durante la concentración y extracción de minerales que serán sometidos a un procesamiento posterior.
Algunos ácidos hidroxámicos (por ejemplo, vorinostat, belinostat, panobinostat y tricostatina A) son inhibidores de HDAC con propiedades anticancerígenas. La fosmidomicina es un inhibidor natural del ácido hidroxámico de la 1-desoxi-D-xilulosa-5-fosfato reductoisomerasa (DXP reductoisomerasa). Los ácidos hidroxámicos también se han investigado para el reprocesamiento de combustible irradiado.
Referencias
- ^ Munson, James W. (1992). "Acidos hipodroxámicos". En S. Patai (ed.). Derivativos ácidos (1992), Volumen 2. PATAI'S Chemistry of Functional Groups. pp. 849–873. doi:10.1002/9780470772508.ch15. ISBN 9780470772508.
- ^ C. R. Hauser; W. B. Renfrow Jr (1939). "Acido benzohidroxámico". Org. Synth. 19: 15. doi:10.15227/orgsyn.019.0015.
- ^ Li, Jie Jack (2003). Reacciones de nombre: Una colección de mecanismos de reacción detallados (2a edición). Berlín, Heidelberg, Nueva York: Springer. p. 9. ISBN 978-3-662-05338-6.
- ^ Matlin, Stephen A.; Sammes, Peter G.; Upton, Roger M. (1979). "La oxidación de los ácidos trimetililillitalados a los ácidos hidroxámicos". Journal of the Chemical Society, Perkin Transactions 1: 2481–2487. doi:10.1039/p19790002481.
- ^ Smith (2020), La química orgánica de marzo, rxn. 16-3.
- ^ Wang, Zerong (2010). Reacciones y reactivos orgánicos integrales. John Wiley ' Sons, Inc. págs. 1772 a 1776. ISBN 9780471704508.
- ^ Hossain, M. B.; Eng-Wilmot, D. L.; Loghry, R. A.; an der Helm, D. (1980). "Circular Dicroismo, Estructura de Cristal y Configuración Absoluta de la Siderophore Ferric N, N', N"-Triacetylfusarinine, FeC39H57N6O15". Journal of the American Chemical Society. 102 (18): 5766–5773. doi:10.1021/ja00538a012.
- ^ Abraham Shanzer, Clifford E. Felder, Yaniv Barda (2008). "Natural and Biomimetic Hydroxamic Acid based Siderophores". En Zvi Rappoport, Joel F. Liebman (ed.). La química de hidroxilaminas, óxidos y ácidos hidroxámicos. PATAI'S Chemistry of Functional Groups. pp. 751–815. doi:10.1002/9780470741962.ch16. ISBN 9780470512616.
{{cite book}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ Agrawal, Y K (1979). "Hydroxamic Acids and Their Metal Complexes". Russian Chemical Reviews. 48 (10): 948–963. Bibcode:1979RuCRv..48..948A. doi:10.1070/RC1979v048n10ABEH002422. S2CID 250857281.
- ^ Miller, Marvin J. (noviembre de 1989). "Síntesis y Potencia Terapéutica del Ácido Hidroxámico Basado en Siderophores y Analogues". Reseñas químicas. 89 (7): 1563–1579. doi:10.1021/cr00097a011.
- ^ Farkas, Etelka; Buglyó, Péter (2017). "Capítulo 8. Líder(II) Complejos de Aminoácidos, Peptidos y Otros Ligados Relacionados de Interés Biológico". En Astrid, S.; Helmut, S.; Sigel, R. K. O. (eds.). Lead: Sus efectos sobre el medio ambiente y la salud. Hiones de metal en Ciencias de la Vida. Vol. 17. de Gruyter. pp. 201–240. doi:10.1515/97831104330-008. ISBN 9783110434330. PMID 28731301.
- ^ Marion, Christopher; Jordens, Adam; Li, Ronghao; Rudolph, Martin; Waters, Kristian E. (agosto de 2017). "Una evaluación de los coleccionistas hidroxamato para flotación malachita". Tecnología de la separación y la purificación. 183: 258–269. doi:10.1016/j.seppur.2017.02.056.
- ^ Jordens, Adam; Cheng, Ying Ping; Waters, Kristian E. (Febrero 2013). "Una revisión del beneficio de los minerales de rodamientos de elementos de tierra raras". Minerals Engineering. 41: 97–114. Código:2013MiEng..41...97J. doi:10.1016/j.mineng.2012.10.017.
Más lectura
- Fouché, K. F.; H. J. le Roux; F. Phillips (junio de 1970). "Formación compleja de Zr(IV) y Hf(IV) con ácidos hidroxámicos en soluciones ácidas". Journal of Inorganic and Nuclear Chemistry. 32 (6): 1949-1962. doi:10.1016/0022-1902(70)80604-2. ISSN 0022-1902. Archivado desde el original en 2013-01-04. Retrieved 2009-04-24.
- Barocas, A.; F. Baroncelli; G. B. Biondi; G. Grossi (diciembre de 1966). "El poder complejo de los ácidos hidroxámicos y su efecto en el comportamiento de los extractores orgánicos en el reprocesamiento de los combustibles irradiados -II: Los complejos entre el ácido benzohidroxámico y el torio, el uranio (IV) y el plutonio (IV)". Journal of Inorganic and Nuclear Chemistry. 28 (12): 2961–2967. doi:10.1016/0022-1902(66)80023-4. ISSN 0022-1902. Archivado desde el original en 2013-01-04. Retrieved 2009-04-24.
- Baroncelli, F.; G. Grossi (mayo de 1965). "El poder complejo de los ácidos hidroxámicos y su efecto sobre el comportamiento de los extractores orgánicos en el reprocesamiento de los combustibles irradiados: los complejos entre el ácido benzohidroxámico y el circonio, el hierro (III) y el uranio (VI)". Journal of Inorganic and Nuclear Chemistry. 27 (5): 1085–1092. doi:10.1016/0022-1902(65)80420-1. ISSN 0022-1902. Archivado desde el original en 2013-01-04. Retrieved 2009-04-24.
- Al-Jarrah, R. H.; A. R. Al-Karaghouli; S. A. Al-Assaf; N. H. Shamon (1981). "Extracción solvente de uranio y algunos otros iones metálicos con ácido octanohidroxámico 2-N-butyl-2-ethyl". Journal of Inorganic and Nuclear Chemistry. 43 (11): 2971–2973. doi:10.1016/0022-1902(81)80652-5. ISSN 0022-1902. Archivado desde el original en 2013-01-04. Retrieved 2009-04-24.
- Gopalan, Aravamudan S.; Vincent J. Huber; Orhan Zincircioglu; Paul H. Smith (1992). "Tetrahidroxamatos novedosos para la complejidad actinida: síntesis y estudios vinculantes". Journal of the Chemical Society, Chemical Communications (17): 1266–1268. doi:10.1039/C39920001266.
- Koshti, Nirmal; Vincent Huber; Paul Smith; Aravamudan S. Gopalan (1994-02-28). "Diseño y síntesis de los químicos específicos de actinide: Síntesis de los nuevos tetrahidroxamato de ciclón (CYTROX) y tetraacetonylacetone (CYTAC) chelators". Tetraedro. 50 (9): 2657–2664. doi:10.1016/S0040-4020(01)86981-7. ISSN 0040-4020.
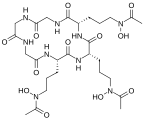

![Fe(III) complex of triacetylfusarinine[7]](https://upload.wikimedia.org/wikipedia/commons/thumb/5/5b/Fe%28hydroxamate%293.svg/125px-Fe%28hydroxamate%293.svg.png)