Ácido fluorhídrico
ácido fluorhídrico es una solución de fluoruro de hidrógeno (HF) en agua. Las soluciones de HF son incoloras, ácidas y altamente corrosivas. Se utiliza para fabricar la mayoría de los compuestos que contienen flúor; los ejemplos incluyen el medicamento antidepresivo farmacéutico de uso común fluoxetina (Prozac) y el material PTFE (teflón). A partir de él se produce flúor elemental. Se utiliza comúnmente para grabar obleas de vidrio y silicio.
Usos
Producción de compuestos organofluorados
El uso principal del ácido fluorhídrico es en la química de los organofluorados. Muchos compuestos organofluorados se preparan utilizando HF como fuente de flúor, incluidos teflón, fluoropolímeros, fluorocarbonos y refrigerantes como el freón. Muchos productos farmacéuticos contienen flúor.
Producción de fluoruros inorgánicos
La mayoría de los compuestos de fluoruro inorgánico de alto volumen se preparan a partir de ácido fluorhídrico. Los principales son Na3AlF6, criolita y AlF3, trifluoruro de aluminio. Una mezcla fundida de estos sólidos sirve como solvente de alta temperatura para la producción de aluminio metálico. Otros fluoruros inorgánicos preparados a partir de ácido fluorhídrico incluyen fluoruro de sodio y hexafluoruro de uranio.
Grabador, limpiador

Se utiliza en la industria de los semiconductores como componente principal del grabado de Wright y el grabado de óxido tamponado, que se utilizan para limpiar las obleas de silicio. De manera similar, también se usa para grabar vidrio por tratamiento con dióxido de silicio para formar fluoruros de silicio gaseosos o solubles en agua. También se puede utilizar para pulir y esmerilar vidrio.
- SiO2 + 4 HF → SiF4(g) + 2 H2O
- SiO2 + 6 HF → H2SiF6 + 2 H2O
También se usa comúnmente un gel de ácido fluorhídrico del 5 % al 9 % para grabar todas las restauraciones dentales de cerámica para mejorar la unión. Por razones similares, el ácido fluorhídrico diluido es un componente de los quitamanchas de óxido domésticos, en lavados de autos en "limpiador de ruedas" compuestos, en inhibidores de óxido de cerámica y telas, y en quitamanchas de agua. Debido a su capacidad para disolver óxidos de hierro y contaminantes a base de sílice, el ácido fluorhídrico se usa en calderas previas a la puesta en marcha que producen vapor a alta presión. El ácido fluorhídrico también es útil para disolver muestras de roca (generalmente en polvo) antes del análisis. De manera similar, este ácido se utiliza en maceraciones ácidas para extraer fósiles orgánicos de rocas de silicato. La roca fosilífera se puede sumergir directamente en el ácido, o se puede aplicar una película de nitrato de celulosa (disuelta en acetato de amilo), que se adhiere al componente orgánico y permite que la roca se disuelva a su alrededor.
Refinación de petróleo
En un proceso estándar de refinería de petróleo conocido como alquilación, el isobutano se alquila con alquenos de bajo peso molecular (principalmente una mezcla de propileno y butileno) en presencia de un catalizador ácido derivado del ácido fluorhídrico. El catalizador protona los alquenos (propileno, butileno) para producir carbocationes reactivos, que alquilan isobutano. La reacción se lleva a cabo a temperaturas suaves (0 y 30 °C) en una reacción de dos fases.
Producción
El ácido fluorhídrico fue preparado por primera vez en 1771 por Carl Wilhelm Scheele. Ahora se produce principalmente mediante el tratamiento del mineral fluorita, CaF2, con ácido sulfúrico concentrado a aproximadamente 265 °C.
- CaF2 + H2SO4 → 2 HF + CaSO4
El ácido también es un subproducto de la producción de ácido fosfórico a partir de apatito y fluoroapatito. La digestión del mineral con ácido sulfúrico a temperaturas elevadas libera una mezcla de gases, incluido el fluoruro de hidrógeno, que puede recuperarse.
Debido a su alta reactividad con el vidrio, el ácido fluorhídrico se almacena en recipientes de plástico fluorado (a menudo PTFE).
Propiedades
En solución acuosa diluida, el fluoruro de hidrógeno se comporta como un ácido débil, La espectroscopia infrarroja se ha utilizado para demostrar que, en solución, la disociación va acompañada de la formación del par de iones H3O+·F−.
- H2O + HF ⇌ H3O+⋅F−pKa = 3.17
Este par de iones se ha caracterizado en estado cristalino a muy baja temperatura. Se ha caracterizado una asociación adicional tanto en solución como en estado sólido.
- HF + F− ⇌ HF−
2log K = 0,6
Se supone que la polimerización se produce a medida que aumenta la concentración. Esta suposición está respaldada por el aislamiento de una sal de un anión tetramérico H
3F−
4 y por cristalografía de rayos X a baja temperatura. No se han caracterizado todas las especies que están presentes en soluciones acuosas concentradas de fluoruro de hidrógeno; además de HF−
2 que se conoce la formación de otras especies poliméricas, H
n−1F−
n, es muy probable.
La función de acidez de Hammett, H0, para 100 % HF se informó por primera vez como -10,2, mientras que compilaciones posteriores muestran -11, comparable a valores cercanos a -12 para ácido sulfúrico puro.
Acidez
A diferencia de otros ácidos hidrohálicos, como el ácido clorhídrico, el fluoruro de hidrógeno es solo un ácido débil en solución acuosa diluida. Esto se debe en parte a la fuerza del enlace hidrógeno-flúor, pero también a otros factores, como la tendencia de HF, H
2 O y F−
aniones para formar grupos. En altas concentraciones, las moléculas de HF se homoasocian para formar iones poliatómicos (como bifluoruro, HF−
2) y protones, por lo que en gran medida aumentando la acidez. Esto conduce a la protonación de ácidos muy fuertes como el clorhídrico, sulfúrico o nítrico cuando se utilizan soluciones concentradas de ácido fluorhídrico. Aunque el ácido fluorhídrico se considera un ácido débil, es muy corrosivo e incluso ataca al vidrio cuando está hidratado.
La acidez de las soluciones de ácido fluorhídrico varía con la concentración debido a la homoasociación, que se refiere al efecto de F- sobre HF. Las soluciones diluidas son débilmente ácidas con una constante de ionización ácida Ka = 6.6×10−4 (o pKa = 3.18), en contraste con las soluciones correspondientes de los otros haluros de hidrógeno, que son ácidos fuertes (pKa < 0). Sin embargo, las soluciones concentradas de fluoruro de hidrógeno son mucho más ácidas de lo que implica este valor, como lo demuestran las mediciones de la función de acidez de Hammett H0(o "pH efectivo& #34;). Durante la autoionización de HF líquido al 100 %, el H0 se midió primero como -10,2 y luego se compiló como -11, comparable a valores cercanos a -12 para el ácido sulfúrico.
En términos termodinámicos, las soluciones de HF son altamente no ideales, ya que la actividad del HF aumenta mucho más rápidamente que su concentración. La acidez débil en solución diluida a veces se atribuye a la alta fuerza del enlace HF, que se combina con la alta entalpía de disolución del HF para compensar la entalpía de hidratación más negativa del ion fluoruro. Paul Giguère y Sylvia Turrell han demostrado mediante espectroscopia infrarroja que la especie de soluto predominante en solución diluida es el par de iones unidos por enlaces de hidrógeno H3O+·F−.
- H2O + HF ⇌ H3O+⋅F−
Con el aumento de la concentración de HF, la concentración del ion difluoruro de hidrógeno también aumenta. La reacción
- 3 HF ⇌ HF−
2 + H2F+
es un ejemplo de homoconjugación.
Salud y seguridad
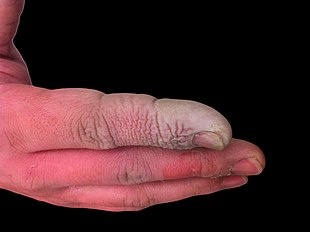
Además de ser un líquido altamente corrosivo, el ácido fluorhídrico también es un poderoso veneno de contacto. Debido a la capacidad del ácido fluorhídrico para penetrar en los tejidos, el envenenamiento puede ocurrir fácilmente por exposición de la piel o los ojos, o por inhalación o ingestión. Los síntomas de la exposición al ácido fluorhídrico pueden no ser evidentes de inmediato, y esto puede proporcionar una falsa tranquilidad a las víctimas, lo que hace que retrasen el tratamiento médico. A pesar de tener un olor irritante, el HF puede alcanzar niveles peligrosos sin un olor evidente. HF interfiere con la función nerviosa, lo que significa que las quemaduras pueden no ser dolorosas al principio. Las exposiciones accidentales pueden pasar desapercibidas, retrasando el tratamiento y aumentando el alcance y la gravedad de la lesión. Los síntomas de la exposición al HF incluyen irritación de los ojos, la piel, la nariz y la garganta, quemaduras en los ojos y la piel, rinitis, bronquitis, edema pulmonar (acumulación de líquido en los pulmones) y daño óseo.
Las quemaduras por hidrofluórico se tratan con un gel de gluconato de calcio.