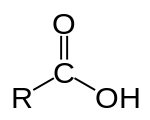
Ácido carboxílico
En química orgánica, un ácido carboxílico es un ácido orgánico que contiene un grupo carboxilo (C(=O)OH) adjunto a un grupo R. La fórmula general de un ácido carboxílico es R−COOH o R−CO2H, donde R se refiere al alquilo, alquenilo, arilo u otro grupo. Los ácidos carboxílicos se encuentran ampliamente. Los ejemplos importantes incluyen los aminoácidos y los ácidos grasos. La desprotonación de un ácido carboxílico da un anión carboxilato.
Ejemplos y nomenclatura
Los ácidos carboxílicos se identifican comúnmente por sus nombres triviales. A menudo tienen el sufijo -ic acid. También existen nombres recomendados por la IUPAC; en este sistema, los ácidos carboxílicos tienen un sufijo -ácido oico. Por ejemplo, el ácido butírico (C3H7CO2H) es ácido butanoico según las pautas de la IUPAC. Para la nomenclatura de moléculas complejas que contienen un ácido carboxílico, el carboxilo se puede considerar en la posición uno de la cadena principal incluso si hay otros sustituyentes, como el ácido 3-cloropropanoico. Alternativamente, se puede nombrar como "carboxi" o "ácido carboxílico" sustituyente en otra estructura original, como 2-carboxifurano.
El anión carboxilato (R–COO− o RCO2−) de un ácido carboxílico suele nombrarse con el sufijo -ate, de acuerdo con el patrón general de -ic acid y -ate para un ácido conjugado y su base conjugada, respectivamente. Por ejemplo, la base conjugada del ácido acético es acetato.
El ácido carbónico, que se encuentra en los sistemas tampón de bicarbonato en la naturaleza, generalmente no se clasifica como uno de los ácidos carboxílicos, a pesar de que tiene un resto que parece un grupo COOH.
| Carbon átomos | Nombre común | IUPAC Nombre | Fórmula química | Ubicación o uso común |
|---|---|---|---|---|
| 1 | Ácido formico | Ácido metanoico | HCOOH | picaduras de insectos |
| 2 | Ácido acético | Ácido etanoico | CH3COOH | Vinegar |
| 3 | Ácido propiónico | Ácido propanoico | CH3CH2COOH | Conservación de granos almacenados, olor corporal, leche, mantequilla, queso |
| 4 | Ácido butírico | Ácido butanoico | CH3(CH)2)2COOH | Butter |
| 5 | Ácido valer | Ácido pentanoico | CH3(CH)2)3COOH | Planta valeriana |
| 6 | Ácido caproico | Ácido hexanoico | CH3(CH)2)4COOH | Goat fat |
| 7 | Ácido entático | Ácido heptanoico | CH3(CH)2)5COOH | Fragancia |
| 8 | Ácido caprílico | Ácido octonoico | CH3(CH)2)6COOH | Cocos |
| 9 | Ácido pelargonico | Ácido no anoico | CH3(CH)2)7COOH | Planta de pelargonio |
| 10 | Ácido Capric | Ácido decano | CH3(CH)2)8COOH | Aceite de coco y de palma |
| 11 | Ácido no decilico | Ácido undecano | CH3(CH)2)9COOH | Anti-fungal agent |
| 12 | Ácido lauric | Ácido dodecanoico | CH3(CH)2)10COOH | Aceite de coco y jabón de lavado a mano |
| 13 | Ácido tridecílico | Ácido tridecanoico | CH3(CH)2)11COOH | metabolito vegetal |
| 14 | Ácido mirístico | Ácido tetradecanoico | CH3(CH)2)12COOH | Nutmeg |
| 15 | Ácido pentadecílico | Ácido pentadecanoico | CH3(CH)2)13COOH | Grasa de leche |
| 16 | Ácido palmítico | Ácido hexadecanoico | CH3(CH)2)14COOH | aceite de palma |
| 17 | Ácido margarí | Ácido heptadecanoico | CH3(CH)2)15COOH | Feromona en varios animales |
| 18 | Ácido estoárico | Ácido Octacano | CH3(CH)2)16COOH | Chocolate, ceras, jabones y aceites |
| 19 | Ácido noadecólico | Ácido noadecano | CH3(CH)2)17COOH | grasas, aceites vegetales, feromonas |
| 20 | Ácido araquidádico | Ácido Icosanoico | CH3(CH)2)18COOH | Aceite de cacahuete |
| Clase compuesta | Miembros |
|---|---|
| ácidos monocarboxílicos insaturados | ácido acrílico (2-ácido propenoico) – CH2=CHCOOH, utilizado en síntesis de polímeros |
| Ácidos grasos | Ácidos monocarboxílicos saturados e insaturados de cadena mediana a larga, con incluso número de carbonos; ejemplos: ácido docosahexaenoico y ácido eicosapentaenoico (suplementos nutricionales) |
| Aminoácidos | los bloques de construcción de proteínas |
| Ácidos de Keto | ácidos de significación bioquímica que contienen un grupo de ketona; ejemplos: ácido acetocético y ácido píruvico |
| Ácidos carboxílicos aromáticos | que contiene por lo menos un anillo aromático; ejemplos: ácido benzoico – la sal de sodio del ácido benzoico se utiliza como preservativo de alimentos; ácido salicílico – un tipo beta-hidroxi encontrado en muchos productos de cuidado de la piel; ácidos alcalónicos fenil – la clase de compuestos donde un grupo de fenilo se adjunta a un ácido carboxílico |
| Ácidos dicarboxílicos | conteniendo dos grupos de carboxilo; ejemplos: ácido adipico el monómero utilizado para producir nylon y ácido aldárico – una familia de ácidos azucareros |
| Ácidos tricarboxílicos | que contiene tres grupos de carboxilo; ejemplos: ácido cítrico – encontrado en frutas cítricas y ácido isocitrico |
| Ácidos hidroxiales alfa | que contiene un grupo hidroxi en la primera posición; ejemplos: ácido glicérico, ácido glicólico y ácido láctico (2-hidroxipropanoico ácido) – encontrado en leche agria, ácido tartárico – encontrado en vino |
| Acidos hidroxi beta | que contiene un grupo hidroxi en la segunda posición |
| Ácidos hidroxidos Omega | que contiene un grupo hidroxi más allá de la primera o segunda posición |
| Divinylether ácidos grasos | que contiene una cadena de carbono doblemente insaturada adjunta mediante un enlace de éter a un ácido graso, encontrado en algunas plantas |
Propiedades físicas
Solubilidad
Los ácidos carboxílicos son polares. Debido a que son aceptores de enlaces de hidrógeno (el carbonilo –C=O) y donantes de enlaces de hidrógeno (el hidroxilo –OH), también participan en los enlaces de hidrógeno. Juntos, el grupo hidroxilo y carbonilo forman el grupo funcional carboxilo. Los ácidos carboxílicos suelen existir como dímeros en medios no polares debido a su tendencia a "autoasociarse". Los ácidos carboxílicos más pequeños (de 1 a 5 carbonos) son solubles en agua, mientras que los ácidos carboxílicos más grandes tienen una solubilidad limitada debido a la creciente naturaleza hidrófoba de la cadena alquílica. Estos ácidos de cadena más larga tienden a ser solubles en solventes menos polares como éteres y alcoholes. El hidróxido de sodio acuoso y los ácidos carboxílicos, incluso los hidrófobos, reaccionan para producir sales de sodio solubles en agua. Por ejemplo, el ácido enántico tiene una baja solubilidad en agua (0,2 g/L), pero su sal de sodio es muy soluble en agua.
Puntos de ebullición
Los ácidos carboxílicos tienden a tener puntos de ebullición más altos que el agua, debido a sus mayores áreas superficiales y su tendencia a formar dímeros estabilizados a través de enlaces de hidrógeno. Para que ocurra la ebullición, los enlaces de dímero deben romperse o toda la disposición de dímero debe vaporizarse, lo que aumenta significativamente la entalpía de los requisitos de vaporización.
Acidez
Los ácidos carboxílicos son ácidos de Brønsted-Lowry porque son donantes de protones (H+). Son el tipo más común de ácido orgánico.
Los ácidos carboxílicos suelen ser ácidos débiles, lo que significa que solo se disocian parcialmente en cationes H3O+ y aniones RCOO− en una solución acuosa neutra. Por ejemplo, a temperatura ambiente, en una solución 1 molar de ácido acético, solo se disocia el 0,001 % del ácido (es decir, 10−5 moles de 1 mol). Los sustituyentes atractores de electrones, como el grupo -CF3, dan ácidos más fuertes (el pKa del ácido fórmico es 3,75 mientras que el ácido trifluoroacético, con un sustituyente trifluorometilo, tiene un pKa de 0,23). Los sustituyentes donantes de electrones dan ácidos más débiles (el pKa del ácido fórmico es 3,75 mientras que el ácido acético, con un sustituyente metilo, tiene un pKa de 4,76)
| Ácido carboxílico | pKa |
|---|---|
| Ácido acético (CH)3CO2H) | 4.76 |
| Ácido benzoico (C)6H5CO2H) | 4.2 |
| Ácido formico (HCOOH) | 3.75 |
| Ácido cloroacético (CH)2ClCO2H) | 2.86 |
| Ácido dicloroacético (CHCl)2CO2H) | 1.29 |
| Ácido oxálico (HO2CCO2H)
(primera disociación) | 1.27 |
| Ácido oxálico (HO2CCO2−)
(segunda disociación) | 4.14 |
| Ácido tricloroacético (CCl)3CO2H) | 0.65 |
| Ácido trifluoroacetico (CF)3CO2H) | 0.23 |
La desprotonación de ácidos carboxílicos da aniones carboxilato; estos están estabilizados por resonancia, porque la carga negativa se deslocaliza sobre los dos átomos de oxígeno, aumentando la estabilidad del anión. Cada uno de los enlaces carbono-oxígeno en el anión carboxilato tiene un carácter de doble enlace parcial. La carga positiva parcial del carbonilo carbonílico también se debilita por las cargas negativas -1/2 en los 2 átomos de oxígeno.
Olor
Los ácidos carboxílicos suelen tener fuertes olores agrios. Los ésteres de ácidos carboxílicos tienden a tener olores afrutados y agradables, y muchos se usan en perfumería.
Caracterización
Los ácidos carboxílicos se identifican fácilmente como tales mediante espectroscopia infrarroja. Presentan una banda marcada asociada con la vibración del enlace carbonilo C=O (νC=O) entre 1680 y 1725 cm−1. Aparece una banda νO–H característica como un pico ancho en la región de 2500 a 3000 cm−1. Por espectrometría 1H NMR, el hidrógeno hidroxilo aparece en la región de 10 a 13 ppm, aunque a menudo se ensancha o no se observa debido al intercambio con trazas de agua.
Ocurrencia y aplicaciones
Muchos ácidos carboxílicos se producen industrialmente a gran escala. También se encuentran con frecuencia en la naturaleza. Los ésteres de ácidos grasos son los principales componentes de los lípidos y las poliamidas de los ácidos aminocarboxílicos son los principales componentes de las proteínas.
Los ácidos carboxílicos se utilizan en la producción de polímeros, productos farmacéuticos, disolventes y aditivos alimentarios. Los ácidos carboxílicos de importancia industrial incluyen ácido acético (componente del vinagre, precursor de solventes y recubrimientos), ácidos acrílico y metacrílico (precursores de polímeros, adhesivos), ácido adípico (polímeros), ácido cítrico (un saborizante y conservante en alimentos y bebidas), ácido etilendiaminotetraacético (agente quelante), ácidos grasos (recubrimientos), ácido maleico (polímeros), ácido propiónico (conservante de alimentos), ácido tereftálico (polímeros). Las sales de carboxilato importantes son los jabones.
Síntesis
Rutas industriales
En general, las rutas industriales hacia los ácidos carboxílicos difieren de las que se utilizan a menor escala porque requieren equipos especializados.
- Carbonylation of alcohols as illustrated by the Cativa process for the production of acetic acid. El ácido formico está preparado por una vía de carbonilación diferente, también a partir del metanol.
- oxidación de aldehídos con aire utilizando catalizadores de cobalto y manganeso. Los aldehídos requeridos se obtienen fácilmente de las siglas por hidroformilación.
- Oxidación de hidrocarburos utilizando aire. Para los alkanes simples, este método es barato pero no lo suficientemente selectivo para ser útil. Los compuestos allílicos y benciólicos sufren oxidaciones más selectivas. Los grupos de alquil en un anillo de benceno se oxidan al ácido carboxílico, independientemente de su longitud de cadena. Ácido benzoico de tolueno, ácido tereftaico de para-xylene y ácido fálico de ortho-xylene son conversiones ilustrativas a gran escala. El ácido acrílico se genera a partir del propeno.
- Oxidación de etheno utilizando catalizador de ácido silicotungstic.
- Deshidrogenación de alcohol con base.
- Carbonilación unida a la adición de agua. Este método es eficaz y versátil para las siglas que generan carbocaciones secundarias y terciarias, por ejemplo isobutileno a ácido pivalico. En la reacción de Koch, la adición de monóxido de agua y carbono a las alkenes es catalizada por ácidos fuertes. Las hidrocarboxilaciones implican la adición simultánea de agua y CO. Tales reacciones a veces se llaman "Medicina de rescate".
- HCCH + CO + H2O → CH2= CHCO2H
- Hidrolisis de triglicéridos obtenidos de aceites vegetales o animales. Estos métodos de sintetización de algunos ácidos carboxílicos de cadena larga están relacionados con la fabricación de jabón.
- Fermentación de etanol. Este método se utiliza en la producción de vinagre.
- La reacción Kolbe-Schmitt proporciona una ruta hacia el ácido salicílico, precursor de la aspirina.
Métodos de laboratorio
Los métodos de preparación para reacciones a pequeña escala para la investigación o para la producción de productos químicos finos suelen emplear reactivos consumibles caros.
- Oxidación de alcoholes primarios o aldehídos con fuertes oxidantes como el dicromato de potasio, reactivo Jones, permanganato de potasio o clorito de sodio. El método es más adecuado para las condiciones de laboratorio que el uso industrial del aire, que es "verde" porque produce menos productos secundarios inorgánicos como el cromo o los óxidos de manganeso.
- Colavaje oxidativo de olefinas por ozonolisis, permanganato de potasio o dicromato de potasio.
- Hidrolisis de nitriles, ésteres o en medio, generalmente con ácido- o base-catalisis.
- Carbonation of a Grignard reagent and organolithium reagents:
- RLi + CO2 → RCO2Li
- RCO2Li + HCl → RCO2H + LiCl
- Halogenación seguida de hidrolisis de metil cetonas en la reacción haloforma
- Bloqueo de cetonas no perecederas, especialmente cetonas aryl:
- RC(O)Ar + H2O → RCO2H + ArH
Reacciones menos comunes
Muchas reacciones producen ácidos carboxílicos pero se usan solo en casos específicos o son principalmente de interés académico.
- Desproporción de un aldehído en la reacción Cannizzaro
- Rearme de diquetones en la reorganización de ácido benzilico
- La generación de ácidos benzoicos es la reacción de von Richter de nitrobencenos y la reacción de Kolbe-Schmitt de fenoles.
Reacciones
Las reacciones más practicadas convierten los ácidos carboxílicos en ésteres, amidas, sales de carboxilato, cloruros de ácido y alcoholes. Los ácidos carboxílicos reaccionan con las bases para formar sales de carboxilato, en las que el hidrógeno del grupo hidroxilo (-OH) se reemplaza con un catión metálico. Por ejemplo, el ácido acético que se encuentra en el vinagre reacciona con el bicarbonato de sodio (bicarbonato de sodio) para formar acetato de sodio, dióxido de carbono y agua:
- CH3COOH + NaHCO3 → CH3COO−Na+ + CO2 + H2O
Los ácidos carboxílicos también reaccionan con los alcoholes para dar ésteres. Este proceso es ampliamente utilizado, p. en la producción de poliésteres. Asimismo, los ácidos carboxílicos se convierten en amidas, pero esta conversión normalmente no se produce por reacción directa del ácido carboxílico y la amina. En cambio, los ésteres son precursores típicos de las amidas. La conversión de aminoácidos en péptidos es un proceso bioquímico significativo que requiere ATP.
El grupo hidroxilo de los ácidos carboxílicos se puede reemplazar con un átomo de cloro usando cloruro de tionilo para dar cloruros de acilo. En la naturaleza, los ácidos carboxílicos se convierten en tioésteres.
Reducción
Al igual que los ésteres, la mayoría de los ácidos carboxílicos se pueden reducir a alcoholes mediante hidrogenación o mediante el uso de agentes de transferencia de hidruros, como el hidruro de litio y aluminio. Los agentes de transferencia de alquilo fuertes, como los compuestos de organolitio pero no los reactivos de Grignard, reducirán los ácidos carboxílicos a cetonas junto con la transferencia del grupo alquilo.
Cloruro deN,N-dimetil(clorometileno)amonio (ClHC=N+(CH3) 2Cl−) es un agente altamente quimioselectivo para la reducción de ácidos carboxílicos. Activa selectivamente el ácido carboxílico para dar la sal de carboximetilenamonio, que se puede reducir con un reductor suave como el hidruro de tris(t-butoxi)aluminio de litio para producir un aldehído en un procedimiento de un solo recipiente. Se sabe que este procedimiento tolera funcionalidades carbonilo reactivas tales como cetona así como restos éster, olefina, nitrilo y haluro moderadamente reactivos.
Reacciones especializadas
- Como con todos los compuestos de carbono, los protones en el α-carbono son labile debido a la tautomerización de keto-enol. Así, el α-carbono se halogena fácilmente en la halogenación del infierno – Volhard–Zelinsky.
- La reacción Schmidt convierte los ácidos carboxílicos a las minas.
- Los ácidos carboxílicos están decarboxilados en la reacción Hunsdiecker.
- La reacción Dakin-West convierte un aminoácido al amino ketone correspondiente.
- En la degradación Barbier-Wieland, un ácido carboxílico en una cadena alifatica con un simple puente metileno en la posición alfa puede tener la cadena acortada por un carbono. El procedimiento inverso es la síntesis Arndt-Eistert, donde un ácido se convierte en halido acyl, que luego se reacciona con diazometano para dar un metileno adicional en la cadena alifatica.
- Muchos ácidos sufren de decarboxilación oxidativa. Las enzimas que catalizan estas reacciones se conocen como carboxílasas (EC 6.4.1) y decarboxílasas (EC 4.1.1).
- Los ácidos carboxílicos se reducen a aldehídos a través del ester y DIBAL, a través del cloruro ácido en la reducción de Rosenmund y a través del tioester en la reducción de Fukuyama.
- En los ácidos carboxílicos de decarboxilación ketónico se convierten en cetonas.
- Reactivos de organolito (>2 equiv) reaccionan con ácidos carboxílicos para dar un dilitio 1,1-diolato, un intermedio tetraedral estable que descompone para dar una ketona sobre el trabajo ácido.
- El electrolisis de Kolbe es una reacción electrolítica y decarboxilativa de dimerización. Se deshace de los grupos de carboxilo de dos moléculas ácidas, y se une a los fragmentos restantes juntos.
Radical carboxilo
El radical carboxilo, •COOH, solo existe brevemente. La constante de disociación ácida de •COOH se ha medido mediante espectroscopia de resonancia paramagnética de electrones. El grupo carboxilo tiende a dimerizarse para formar ácido oxálico.
Contenido relacionado
Poliuretano
Monosacárido
Henry Eyring (químico)