Regulação alostérica

Nos campos da bioquímica e farmacologia e um regulador alostérico (ou modulador alostérico ) é uma substância que se liga a um local em uma enzima ou receptor distinto do local ativo , resultando em uma mudança conformacional que altera a atividade da proteína, aumentando ou inibindo sua função. Por outro lado, as substâncias que se ligam diretamente a um local ativo de uma enzima ou o local de ligação do ligante endógeno de um receptor são chamadas de reguladores ou moduladores ortostericos .
O site ao qual o efetor liga é denominado local alostérico ou Site regulatório . Os locais alostéricos permitem que os efetores se ligam à proteína, geralmente resultando em uma mudança conformacional e/ou uma mudança na dinâmica de proteínas. Os efetores que aprimoram a atividade da proteína são chamados de ativadores alostéricos , enquanto aqueles que diminuem a atividade da proteína são chamados de inibidores alostéricos .
Os regulamentosalostéricos são um exemplo natural de loops de controle, como feedback de produtos a jusante ou alimentação de substratos a montante. A alostery de longo alcance é especialmente importante na sinalização celular. A regulação alostérica também é particularmente importante na capacidade da célula de ajustar a atividade enzimática.
O termo allestery vem do antigo grego allOS ( ἄλλος ), " outros " e estéreo ( στερεός ), " sólido (objeto) ". Isso se refere ao fato de que o local regulatório de uma proteína alostérica é fisicamente distinto de seu local ativo. A alostery contrasta com a apresentação do substrato, que não requer mudança conformacional para a ativação de uma enzima. O termo Ortostery vem dos antigos orthós gregos ( ὀρθός ) que significa "reto" , "Vertical", "certo" ou "correto".
Inibidores de Ortodoxo
Ortodoxo
- Binding Site: Os inibidores ortostericos ligam-se diretamente ao local ativo da enzima, onde o substrato normalmente se liga.
- Mecanismo de Ação: Ao ocupar o local ativo, esses inibidores impedem que o substrato seja ligado, bloqueando diretamente a atividade catalítica da enzima.
- Inibição Competitiva: A maioria dos inibidores ortotéricos compete com o substrato para o local ativo, o que significa que sua eficácia pode ser reduzida se a concentração de substrato aumenta.
Allosteric
- Binding Site: Inibidores alostericos se ligam a um local na enzima que é distinta e separada do local ativo, conhecido como o local alosterico.
- Mecanismo de Ação: Ligar ao local alosterico induz uma mudança conformacional na enzima que pode reduzir a afinidade do local ativo para o substrato ou alterar a atividade catalítica da enzima. Esta interferência indireta pode inibir a função da enzima mesmo que o substrato esteja presente.
- Não Competitivo Inibição: Inibidores alostericos muitas vezes exibem inibição não competitiva, o que significa que seu efeito inibitório não é dependente da concentração do substrato.
Modelos
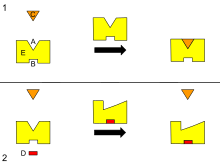
B – Site alosterico
C – Substrato
D – Inibidor
E – Enzyme
Este é um diagrama de regulação alostérica de uma enzima.
Muitos efeitos alostéricos podem ser explicados pelo modelo MWC, apresentado por Monod, Wyman e Changeux, ou pelo modelo seqüencial (também conhecido como modelo KNF) descrito por Koshland, Nemethy, e filme. Ambos postulam que as subunidades de proteínas existem em uma das duas conformações, tensas (t) ou relaxadas (R), e que as subunidades relaxadas se ligam mais facilmente do que as do estado tenso. Os dois modelos diferem mais em suas suposições sobre a interação da subunidade e a pré -existência de ambos os estados. Para proteínas nas quais existem subunidades em mais de duas conformações, o modelo de paisagem alostery descrito por CuEndet, Weinstein e Levine, pode ser usado. A regulação alostérica pode ser facilitada pela evolução de alterações conformacionais em larga escala e baixa energia, o que permite a interação alostérica de longo alcance entre os locais de ligação distantes.
Modelo concertado
O modelo concertado de Allestery, também chamado de modelo de simetria ou modelo MWC, postula que as subunidades enzimáticas são conectadas de tal maneira que uma mudança conformacional em uma subunidade seja necessariamente conferida a todas as outras subunidades. Assim, todas as subunidades devem existir na mesma conformação. O modelo sustenta ainda que, na ausência de qualquer ligante (substrato ou de outra forma), o equilíbrio favorece um dos estados conformacionais, T ou R. O equilíbrio pode ser deslocado para o estado R ou T através da ligação de um ligante (o efetor alostérico ou ligante) para um site diferente do site ativo
Modelo sequencial
O modelo seqüencial da regulação alostérica sustenta que as subunidades não estão conectadas de tal maneira que uma mudança conformacional em uma induz uma mudança semelhante nos outros. Assim, todas as subunidades enzimáticas não exigem a mesma conformação. Além disso, o modelo seqüencial determina que as moléculas de um substrato se ligam através de um protocolo de ajuste induzido. Embora esse ajuste induzido converte uma subunidade do estado tenso em estado relaxado, ele não propaga a mudança conformacional para subunidades adjacentes. Em vez disso, a ligação ao substrato em uma subunidade altera apenas ligeiramente a estrutura de outras subunidades, para que seus locais de ligação sejam mais receptivos ao substrato. Para resumir:
- subunidades não precisam existir na mesma conformação
- moléculas de substrato ligam através de protocolo induzido-fit
- alterações conformacionais não são propagadas para todas as subunidades
Modelo de Morpheein
O modelo de regulação alostérica morfeeína é um modelo concertado dissociativo.
Uma morfeeína é uma estrutura homo-oligomérica que pode existir como um conjunto de conjuntos quaternários alternativos fisiologicamente significativos e funcionalmente diferentes. As transições entre os conjuntos alternativos de morfeeína envolvem dissociação dos oligômeros, mudança conformacional no estado dissociado e remontagem a um oligômero diferente. A etapa de desmontagem do oligômero necessária diferencia o modelo de morfeeína para a regulação alostérica dos modelos clássicos de MWC e KNF.
porfobilinogênio sintase (PBGS) é o protótipo morfeeína.
Modelos semelhantes
modelos Ensemble de regulação alostérica enumeram um conjunto estatístico de um sistema alostérico "em função de sua função de energia potencial e, em seguida, relacionam medidas estatísticas específicas da alosteria a termos de energia específicos na função de energia (como uma ponte intermolecular de sal entre dois domínios). Modelos de conjunto como o modelo alostérico do conjunto e o modelo alostérico de ising assumem que cada domínio do sistema pode adotar dois estados semelhantes ao modelo MWC. O modelo de paisagem alostery introduzido por CuEndet, Weinstein e Levine permite que os domínios tenham qualquer número de estados e a contribuição de uma interação molecular específica para um determinado acoplamento alostérico pode ser estimado usando um conjunto rigoroso de regras. As simulações de dinâmica molecular podem ser usadas para estimar o conjunto estatístico de um sistema, para que possa ser analisado com o modelo de paisagem alostery.
Modulação austérica
A modulação alostérica é usada para alterar a atividade de moléculas e enzimas em bioquímica e farmacologia. Para comparação, um medicamento típico é feito para se ligar ao local ativo de uma enzima que, portanto, proíbe a ligação de um substrato àquela enzima que causa uma diminuição na atividade da enzima. A modulação alostérica ocorre quando um efetor se liga a um local alostérico (também conhecido como local regulatório) de uma enzima e altera a atividade enzimática. Os moduladores alostéricos são projetados para se ajustar ao local alostérico para causar uma mudança conformacional da enzima, em particular uma mudança na forma do local ativo, o que causa uma mudança em sua atividade. Ao contrário dos medicamentos típicos, os moduladores não são inibidores competitivos. Eles podem ser positivos (ativando), causando um aumento da atividade enzimática ou negativos (inibindo), causando uma diminuição da atividade da enzima. O uso da modulação alostérica permite o controle dos efeitos de atividades enzimáticas específicas; Como resultado, os moduladores alostéricos são muito eficazes na farmacologia. Em um sistema biológico, a modulação alostérica pode ser difícil de distinguir da modulação por apresentação do substrato.
Modelo de sensor de energia
Um exemplo desse modelo é visto com a Mycobacterium tuberculosis , uma bactéria que é perfeitamente adequada para se adaptar à vida nos macrófagos dos seres humanos. Os locais da enzima servem como uma comunicação entre diferentes substratos. Especificamente entre AMP e G6P. Sites como esses também servem como um mecanismo de detecção para o desempenho da enzima.
Modulação positiva
Modulação negativa
A modulação alostérica negativa (também conhecida como inibição alostérica ) ocorre quando a ligação de um ligante diminui a afinidade pelo substrato em outros locais ativos. Por exemplo, quando 2,3-bpg se liga a um local alostérico na hemoglobina, a afinidade pelo oxigênio de todas as subunidades diminui. É quando um regulador está ausente no local de ligação.
Os inibidores diretos de trombina fornecem um excelente exemplo de modulação alostérica negativa. Inibidores alostéricos da trombina foram descobertos que poderiam ser potencialmente usados como anticoagulantes.
Outro exemplo é a estricnina, um veneno convulsivo, que atua como um inibidor alostérico do receptor de glicina. A glicina é um dos principais neurotransmissores inibitórios pós-sinápticos na medula espinhal de mamíferos e no tronco cerebral. A estricnina atua em um local de ligação separado no receptor de glicina de maneira alostérica; isto é, sua ligação reduz a afinidade do receptor de glicina para a glicina. Assim, a estricnina inibe a ação de um transmissor inibitório, levando a convulsões.
Outra instância em que a modulação alostérica negativa pode ser vista é entre ATP e a fosfofructoquinase enzimática dentro do ciclo de feedback negativo que regula a glicólise. A fosfofructoquinase (geralmente chamada de PFK) é uma enzima que catalisa o terceiro passo da glicólise: a fosforilação do frutose-6-fosfato em frutose 1,6-bisfosfato. O PFK pode ser inibido alostericamente por altos níveis de ATP dentro da célula. Quando os níveis de ATP são altos, o ATP se ligará a um local alostérico na fosfofructoquinase, causando uma alteração na forma tridimensional enzimática. Essa mudança causa sua afinidade pelo substrato (frutose-6-fosfato e ATP) no local ativo diminuir, e a enzima é considerada inativa. Isso faz com que a glicólise cessa quando os níveis de ATP são altos, conservando a glicose do corpo e mantendo níveis equilibrados de ATP celular. Dessa forma, o ATP serve como um modulador alostérico negativo para PFK, apesar de também ser um substrato da enzima.
Tipos
Homotropic
Um modulador alostérico homotrópico é um substrato para sua proteína alvo, bem como uma molécula reguladora da atividade da proteína. É normalmente um ativador da proteína. Por exemplo, O 2 e CO são moduladores alostéricos homotrópicos da hemoglobina. Da mesma forma, no IMP/GMP específico 5 ' nucleotidase, ligação de uma molécula de GMP a uma única subunidade da enzima tetramérica leva a maior afinidade pelo GMP pelas subunidades subsequentes, conforme revelado por substrato sigmoidal versus gráficos de velocidade.
Heterotrópico
Um modulador alostérico heterotrópico é uma molécula reguladora que não é o substrato da enzima. Pode ser um ativador ou um inibidor da enzima. Por exemplo, H
Como foi amplamente destacado acima, algumas proteínas alostéricas podem ser reguladas por seus substratos e outras moléculas. Tais proteínas são capazes de interações homotrópicas e heterotrópicas.
Activadores essenciais
Alguns ativadores alostéricos são referidos como "essenciais ", ou" obrigatórios " Os ativadores, no sentido de que, na sua ausência, a atividade de sua atividade da enzima alvo é muito baixa ou insignificante, como é o caso da atividade I#39;
Alosteria não regulatória
Um local alostérico não regulatório é qualquer componente não regulador de uma enzima (ou qualquer proteína), que não é em si um aminoácido. Por exemplo, muitas enzimas requerem ligação de sódio para garantir a função adequada. No entanto, o sódio não atua necessariamente como uma subunidade regulatória; O sódio está sempre presente e não há processos biológicos conhecidos para adicionar/remover o sódio para regular a atividade da enzima. A alosteria não reguladora pode compreender outros íons além de sódio (cálcio, magnésio, zinco), bem como outros produtos químicos e possivelmente vitaminas.
Farmacologia
A modulação alostérica de um receptor resulta da ligação dos moduladores alostéricos em um local diferente (a " local regulatório ") do ligante endógeno (um site ativo ") e aprimora ou inibe os efeitos do ligante endógeno. Em circunstâncias normais, age causando uma mudança conformacional em uma molécula de receptor, o que resulta em uma mudança na afinidade de ligação do ligante. Dessa maneira, um ligante alostérico modula a ativação do receptor por seu ligante ortostérico primário e pode -se pensar em agir como um interruptor dimmer em um circuito elétrico, ajustando a intensidade da resposta.
Por exemplo, o receptor GABAA possui dois locais ativos que o neurotransmissor gama-aminobutírico (GABA) se liga, mas também possui locais de ligação regulatória de benzodiazepina e agente anestésico. Cada um dos locais regulatórios pode produzir modulação alostérica positiva, potencializando a atividade do GABA. O diazepam é um modulador alostérico positivo no local regulatório da benzodiazepina, e seu antídoto Flumazenil é um antagonista do receptor.
Exemplos mais recentes de medicamentos que modulam alostericamente seus alvos incluem o Cinacalcet que imita o cálcio e o tratamento do HIV Maraviroc.
Locais alostericos como alvos de drogas
estão envolvidas e são centrais em muitas doenças, e os locais alostéricos podem representar um novo alvo de drogas. Existem várias vantagens no uso de moduladores alostéricos como agentes terapêuticos preferidos em relação aos ligantes ortostéricos clássicos. Por exemplo, os locais de ligação alostérica do receptor acoplado à proteína G (GPCR) não enfrentaram a mesma pressão evolutiva que os locais ortostericos para acomodar um ligante endógeno, por isso são mais diversos. Portanto, uma maior seletividade do GPCR pode ser obtida pela segmentação de locais alostéricos. Isso é particularmente útil para os GPCRs onde a terapia ortosterica seletiva tem sido difícil devido à conservação da sequência do local ortostérico nos subtipos de receptores. Além disso, esses moduladores têm um potencial reduzido para efeitos tóxicos, uma vez que os moduladores com cooperatividade limitada terão um nível de teto em seu efeito, independentemente da dose administrada. Outro tipo de seletividade farmacológica exclusiva dos moduladores alostéricos é baseada na cooperatividade. Um modulador alostérico pode exibir cooperatividade neutra com um ligante ortosterico em todos os subtipos de um determinado receptor, exceto o subtipo de interesse, que é denominado seletividade absoluta de subtipo " Se um modulador alostérico não possuir eficácia apreciável, ele pode fornecer outra poderosa vantagem terapêutica sobre os ligantes ortostéricos, a saber, a capacidade de ajustar seletivamente as respostas do tecido para cima ou para baixo somente quando o agonista endógeno estiver presente. Locais de ligação a pequenas moléculas específicos para oligômeros são alvos de medicamentos para morfeeínas medicamente relevantes.
Sistemas alostericos sintéticos
Existem muitos compostos sintéticos contendo vários locais de ligação não covalentes, que exibem alterações conformacionais após a ocupação de um local. A cooperatividade entre as contribuições de ligação única nesses sistemas supramoleculares é positiva se a ocupação de um local de ligação melhorar a afinidade Δ g em um segundo local e negativo se a afinidade for maior. A maioria dos complexos alostéricos sintéticos depende da reorganização conformacional na ligação de um ligante efetor que leva a uma associação aprimorada ou enfraquecida do segundo ligante em outro local de ligação. O acoplamento conformacional entre vários locais de ligação é em sistemas artificiais geralmente muito maiores do que em proteínas com sua flexibilidade geralmente maior. O parâmetro que determina a eficiência (medido pela razão de constantes de equilíbrio krel = ka (e)/ka na presença e ausência de um efetor e) é a energia conformacional necessária para adotar uma conformação fechada ou tensa para a ligação de um ligante UM.
Em muitos sistemas supramoleculares multivalentes, podem ocorrer interação direta entre ligantes ligados, o que pode levar a grandes cooperatividades. O mais comum é uma interação tão direta entre os íons nos receptores para pares de íons. Essa cooperatividade também é frequentemente chamada de alostery, embora as mudanças conformacionais aqui não estejam necessariamente desencadeando eventos de ligação.
Recursos online
Banco de dados de alosterismo
alostery é um meio direto e eficiente para a regulação da função biológica da macromolécula, produzida pela ligação de um ligante em um local alostérico topograficamente distinto do local ortosterico. Devido à seletividade geralmente alta do receptor e à menor toxicidade baseada no alvo, a regulação alostérica também deve desempenhar um papel crescente na descoberta de medicamentos e na bioengenharia. O banco de dados alostérico (ASD) fornece um recurso central para a exibição, pesquisa e análise da estrutura, função e anotação relacionada para moléculas alostéricas. Atualmente, o ASD contém proteínas alostéricas de mais de 100 espécies e moduladores em três categorias (ativadores, inibidores e reguladores). Cada proteína é anotada com descrição detalhada da alosteria, processo biológico e doenças relacionadas, e cada modulador com afinidade de ligação, propriedades físico -químicas e área terapêutica. A integração da informação das proteínas alostéricas no TEA deve permitir que a previsão da alosteria para proteínas desconhecidas seja seguida com a validação experimental. Além disso, os moduladores com curadoria de TEA podem ser usados para investigar possíveis alvos alostéricos para um composto de consulta e podem ajudar os químicos a implementar modificações de estrutura para o novo design alostérico de medicamentos.
Resíduos alostericos e sua previsão
Nem todos os resíduos de proteínas desempenham papéis igualmente importantes na regulação alostérica. A identificação de resíduos que são essenciais para a Allestery (os chamados "resíduos alostéricos") tem sido o foco de muitos estudos, especialmente na última década. Em parte, esse interesse crescente é resultado de sua importância geral na ciência das proteínas, mas também porque os resíduos alostéricos podem ser explorados em contextos biomédicos. Proteínas farmacologicamente importantes com locais difíceis de segmentar podem ceder a abordagens nas quais um alternativamente tem como alvo os resíduos mais fáceis de alcançar que são capazes de regulamentar alostericamente o principal local de interesse. Esses resíduos podem ser amplamente classificados como aminoácidos superficiais e interiores. Os locais alostéricos na superfície geralmente desempenham papéis regulatórios que são fundamentalmente distintos daqueles dentro do interior; Os resíduos de superfície podem servir como receptores ou locais efetores na transmissão de sinal alostérico, enquanto aqueles dentro do interior podem agir para transmitir esses sinais.
Ver também
- Banco de dados ASD
- Anharmonicity
- Inibição competitiva
- Ligação cooperativa
- Enzyme cinética
- Dinâmica de proteína
- Teoria do receptor
Referências
- ^ Cooper A, Dryden DT (outubro de 1984). "Alosteria sem mudança conformacional. Um modelo plausível". Biofísica Europeia Jornal Oficial. 11 (2): 103-109. doi:10.1007/BF00276625. PMID 6544679. S2CID 12591175.
- ^ Liu J, Nussinov R (junho de 2016). «Allostery: An Overview of Its History, Concepts, Methods, and Applications» (em inglês). PLOS Biologia Computacional. 12 (6): e1004966. Bibcode:2016PLSCB..12E4966L. doi:10.1371/journal.pcbi.1004966. PMC 4890769. PMID 27253437. S2CID 3610740.
- ^ Bu Z, Callaway DJ (2011). "As proteínas se movem! Dinâmica de proteína e alosteria de longo alcance na sinalização de células". Estrutura e Doenças de Proteína. Avanços em Química Proteína e Biologia Estrutural. Vol. 83. pp. 163–221. doi:10.1016/B978-0-12-381262-9.00005-7. ISBN 9780123812629. PMID 21570668.
- ^ Monod J, Wyman J, Changeux JP (maio de 1965). «On the nature of allosteric transições:A plausible model» (em inglês). Revista de Biologia Molecular. 12: 88–118. doi:10.1016/s0022-2836(65)80285-6. PMID 14343300.
- ^ Koshland DE, Némethy G, Filmer D (janeiro de 1966). «Comparação de dados de ligação experimental e modelos teóricos em proteínas contendo subunidades». Bioquímica. 5 (1): 365–85. doi:10.1021/bi00865a047. PMID 5938952.
- ↑ a b Cuendet MA, Weinstein H, LeVine MV (dezembro de 2016). «The Allostery Landscape: Quantifying Thermodynamic Couplings in Biomolecular Systems» (em inglês). Jornal de Teoria Química e Computação. 12 (12): 5758–5767. doi:10.1021/acs.jctc.6b00841. PMC 5156960. PMID 27766843.
- ^ Eckmann JP, Rougemont J, Tlusty T (30 de julho de 2019). «Colloquium: Proteins: The Physics of amorphous evolving matter» (em inglês). Comentários de Modern Physics. 91 (3): 031001. - Sim.1907.13371. Código:2019RvMP...91c1001E. doi:10.1103/RevModPhys.91.031001. ISSN 0034-6861. S2CID 199001124.
- ^ Jaffe EK (setembro de 2005). «Morpheeins--a new Structural paradigm for allosteric Regulation» (em inglês). Tendências em Ciências Bioquímicas. 30 (9): 490–7. doi:10.1016/j.tibs.2005.07.003. PMID 16023348.
- ^ Motlagh HN, Wrabl JO, Li J, Hilser VJ (Abril 2014). «The ensemble nature of allostery» (em inglês). Natureza. 508 (7496): 331–9. Bibcode:2014Natur.508..331M. doi:10.1038/nature13001. PMC 4224315. PMID 24740064.
- ^ Hilser VJ, Wrabl JO, Motlagh HN (2012). «Structural and energetic based of allostery» (em inglês). Revisão Anual de Biofísica. 41: 585–609. doi:10.1146/annurev-biophys-050511-102319. PMC 3935618. PMID 22577828.
- ^ LeVine MV, Weinstein H (maio de 2015). «AIM for Allostery: Using the Ising Model to Understand Information Processing and Transmission in Allosteric Biomolecular Systems» (em inglês). Entropia. 17. (5): 2895–2918. Bibcode:2015Entrp..17.2895L. doi:10.3390/e17052895. PMC 4652859. PMID 26594108.
- ^ Abdel-Magid AF (fevereiro de 2015). «Allosteric modulators: a emergente concept in drug discover» (em inglês). ACS Letras de Química Medicinal. 6 (2): 104–7. doi:10.1021/ml5005365. PMC 43295. PMID 25699154.
- ^ Zhong W, Cui L, Goh BC, Cai Q, Ho P, Chionh YH, et al. (dezembro de 2017). «Allosteric pyruvate kinase-based "logic gate" synergistically senses energy and sugar level in Mycobacterium tuberculosis» (em inglês). Comunicações da Natureza. 8 (1): 1986. Bibcode:2017NatCo...8.1986Z. doi:10.1038/s41467-017-02086-y. PMC 576 milhões de ecus. PMID 29215013.
- ↑ a b d Srinivasan B, Forouhar F, Shukla A, Sampangi C, Kulkarni S, Abashidze M, et al. (março de 2014). «Allosteric Regulation and substrato enable in cytosolic nucleotidase II from Legionella pneumophila» (em inglês). O Jornal FEBS. 281 (6): 1613–1628. doi:10.1111/febs.12727. PMC 3982195. PMID 24456211.
- ^ Edelstein SJ (1975). «Cooperative interações of hemoglobin» (em inglês). Revisão Anual de Bioquímica. 44: 209–32. doi:10.1146/annurev.bi.44.070175.001233. PMID 237460.
- ^ Shi D, Allewell NM, Tuchman M (junho de 2015). «The N-Acetylglutamate Synthase Family: Structures, Function and Mechanisms» (em inglês). Jornal Internacional de Ciências Moleculares. 16. (6): 13004–22.10.3390/ijms160613004. PMC 4490483. PMID 26068232.
- ^ de Cima S, Polo LM, Díez-Fernández C, Martínez AI, Cervera J, Fita I, et al. (novembro de 2015). «Structure of human carbamoyl phosphate synthetase: deciphering the on/off switch of human ureagenesis» (em inglês). Relatórios Científicos. 5 (1): 16950. Bibcode:2015 NatSR...516950D. doi:10.1038/srep16950. PMC 46553. PMID 26592762.
- ^ Nussinov R, Tsai C (2013). «Allostery in disease and in drug discover» (em inglês). Célula. 153 (2): 293–305. doi:10.1016/j.cell.2013.03.034. PMID 23582321.
- ^ Abrusan G, Ascher DB, Inouye M (2022). «Known allosteric proteins have central roles in genetic disease» (em inglês). PLOS Biologia Computacional. 18. (2): e1009806. - Sim.2107.04318. Código: 2022PLSCB..18E9806A. - Sim.10.1371/journal.pcbi.1009806. PMID 10138267.
- ↑ a b c Christopoulos A, May LT, Avlani VA, Sexton PM (novembro de 2004). «G-protein-coupled receptor allosterism: the Promise and the problem(s)» (em inglês). Transações da Sociedade Bioquímica. 32 (Pt 5): 873–7. doi:10.1042/BST0320873. PMID 15494038.
- ↑ a b c Maio LT, Leach K, Sexton PM, Christopoulos A (2007). «Allosteric modulation of G protein-coupled receptors» (em inglês). Revisão Anual de Farmacologia e Toxicologia. 47: 1–51. doi:10.1146/annurev.pharmtox.47.120505.105159. PMID 17009927.
- ^ Jaffe EK (2010). «Morpheeins – A New Pathway for Allosteric Drug Discovery ~!2010-02-12~!2010-05-21~!2010-06-08~!». Jornal Aberta de Actividades. 1: 1–6. doi:10.2174/2210289201001010001 (inativo em 11 de março de 2024). PMC 3107518. PMID 21643557.
{{cite journal}}: Principal CS1: DOI inativo a partir de março 2024 (link) - ^ Takeuchi M, Ikeda M, Sugasaki A, Shinkai S (novembro de 2001). «Molecular design of artificial molecular and ion recognition systems with allosteric guest responses» (em inglês). Contas de Pesquisa Química. 34 (11): 865–73. doi:10.1021/ar0000410. PMID 11714258.
- ^ Kremer C, Lützen A (maio de 2013). «Artificial allosteric receptors» (em inglês). Química: Um Jornal Europeu. 19 (20): 6162–96. doi:10.1002/chem.201203814. PMID 23463705.
- ^ Kovbasyuk L, Krämer R (Junho 2004). «Allosteric supramolecular receptors and catalysts» (em inglês). Comentários de produtos químicos. 104 (6): 3161–87. doi:10.1021/cr030673a. PMID 15186190.
- ^ Schneider HJ (Setembro de 2016). «Eficiência parâmetros em sistemas alostericos artificiais». Organic & Biomolecular Química. 14 (34): 7994–8001. doi:10.1039/c6ob01303a. PMID 27431438.
- ^ Badjić JD, Nelson A, Cantrill SJ, Turnbull WB, Stoddart JF (setembro de 2005). «Multivalency and cooperativity in supramolecular Chemistry» (em inglês). Contas de Pesquisa Química. 38 (9): 723–32. doi:10.1021/ar040223k. PMID 16171315.
- ^ Kim SK, Sessler JL (outubro de 2010). «Ion pair receptors» (em inglês). Comentários da Sociedade Química. 39 (10): 3784–809. doi:10.1039/c002694h. PMC 3016456. PMID 20737073.
- ^ McConnell AJ, Beer PD (maio de 2012). «Heteroditopic receptors for ion-pair recognition» (em inglês). Angewand the Chemie. 51 (21): 5052–61. doi:10.1002/anie.201107244. PMID 22419667.
- ^ Huang Z, Zhu L, Cao Y, Wu G, Liu X, Chen Y, et al. (janeiro de 2011). «ASD: a overall database of allosteric proteins and modulators» (em inglês). Pesquisa de Ácidos Nucleicos. 39 (Database issue): D663–9. doi:10.1093/nar/gkq1022. PMC 3013650. PMID 21051350.
- ^ Panjkovich A, Daura X (outubro de 2012). «Exploiting protein flexibilidade to predict the location of allosteric sites» (em inglês). BMC Bioinformática. 13: 273.10.1186/1471-2105-13-273. PMC 3562710. PMID 23095452.
- ^ Süel GM, Lockless SW, Wall MA, Ranganathan R (janeiro de 2003). «Evolutionarily Conservad networks of Wastes mediate allosteric communication in proteins» (em inglês). Natureza Biologia estrutural. 10. (1): 59–69. doi:10.1038/nsb881. PMID 12483203. S2CID 67749580.
- ^ Mitternacht S, Berezovsky IN (setembro de 2011). «Binding alavanca as a molecular base for allosteric Regulation» (em inglês). PLOS Biologia Computacional. 7 (9): e1002148. Código:2011PLSCB...7E2148M. doi:10.1371/journal.pcbi.1002148. PMC 31741. PMID 21935347.
- ^ Gasper PM, Fuglestad B, Komives EA, Markwick PR, McCammon JA (dezembro de 2012). «Allosteric networks in tromb distingue procoagulant vs. anticoagulant activities» (em inglês). Actividades da Academia Nacional de Ciências dos Estados Unidos da América. 109 (52): 21216–22.10.1073/pnas.1218414109. PMC 3535651. PMID 23197839.
- ^ Ghosh A, Vishveshwara S (novembro de 2008). «Variações em clique e padrões comunitários em estruturas proteicas durante a comunicação alosterica: investigação de estruturas dinamicamente equilibradas de complexos metionil tRNA synthetase». Bioquímica. 47 (44): 11398–407. doi:10.1021/bi8007559. PMID 18842003.
- ^ Sethi A, Eargle J, Black AA, Luthey-Schulten Z (abril de 2009). «Dynamical networks in tRNA:protein complexes» (em inglês). Actividades da Academia Nacional de Ciências dos Estados Unidos da América. 106 (16): 6620–5. Bibcode:2009PNAS..106.6620S. doi:10.1073/pnas.0810961106. PMC 26724. PMID 19351898.
- ^ Vanwart AT, Eargle J, Luthey-Schulten Z, Amaro RE (Agosto de 2012). «Exploring residual componenttributions to dynamical network models of allostery» (em inglês). Jornal de Teoria Química e Computação. 8 (8): 2949–2961. doi:10.1021/ct300377a. PMC 34895. PMID 23139645.
- ^ Rivalta I, Sultan MM, Lee NS, Manley GA, Loria JP, Batista VS (maio de 2012). «Allosteric pathways in imidazole glycerol phosphate synthase» (em inglês). Actividades da Academia Nacional de Ciências dos Estados Unidos da América. 109 (22): E1428–36.10.1073/pnas.1120536109. PMC 3365145. PMID 22586084.
- ^ Negre CF, Morzan UN, Hendrickson HP, Pal R, Lisi GP, Loria JP, et al. (dezembro de 2018). «Eigenvector centrality for characterization of protein allosteric pathways» (em inglês). Actividades da Academia Nacional de Ciências dos Estados Unidos da América. 115 (52): E12201–E12208. - Sim.1706.02327. Código de acesso:2018PNAS..11512201N. doi:10.1073/pnas.1810452115. PMC 628 milhões de ecus. PMID 30530700.
- ^ Clarke D, Sethi A, Li S, Kumar S, Chang RW, Chen J, et al. (maio de 2016). «Identifying Allosteric Hotspots with Dynamics: Application to Inter- and Intra-species Conservation» (em inglês). Estrutura. 24. (5): 826–837. doi:10.1016/j.str.2016.03.008. PMC 48830. PMID 27066750.
- ^ Dutta S, Eckmann JP, Libchaber A, Tlusty T (maio de 2018). «Verde função de genes correlacionados em um modelo mecânico mínimo de evolução proteica». Actividades da Academia Nacional de Ciências dos Estados Unidos da América. 115 (20): E4559–E4568.1801.03681. Código:2018PNAS..115E4559D. - Sim.10.1073/pnas.1716215115. PMC 5960285. PMID 29712824.
Ligações externas
- Visão instantânea introduzindo um sistema de classificação para mecanismos de alosteria proteica da Royal Society of Chemistry