Microtúbulo
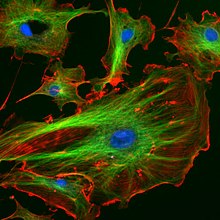
Microtúbulos são polímeros de tubulina que fazem parte do citoesqueleto e fornecem estrutura e forma às células eucarióticas. Os microtúbulos podem ter até 50 micrômetros, largura de 23 a 27 nm e diâmetro interno entre 11 e 15 nm. Eles são formados pela polimerização de um dímero de duas proteínas globulares, alfa e beta tubulina em protofilamentos que podem então se associar lateralmente para formar um tubo oco, o microtúbulo. A forma mais comum de um microtúbulo consiste em 13 protofilamentos no arranjo tubular.
Os microtúbulos desempenham um papel importante em vários processos celulares. Eles estão envolvidos na manutenção da estrutura da célula e, juntamente com microfilamentos e filamentos intermediários, formam o citoesqueleto. Eles também compõem a estrutura interna dos cílios e flagelos. Eles fornecem plataformas para o transporte intracelular e estão envolvidos em uma variedade de processos celulares, incluindo o movimento de vesículas secretoras, organelas e conjuntos macromoleculares intracelulares. Eles também estão envolvidos na divisão celular (por mitose e meiose) e são os principais constituintes dos fusos mitóticos, que são usados para separar os cromossomos eucarióticos.
Os microtúbulos são nucleados e organizados por centros organizadores de microtúbulos, como o centrossomo encontrado no centro de muitas células animais ou os corpos basais de cílios e flagelos, ou os corpos polares do fuso encontrados na maioria dos fungos.
Existem muitas proteínas que se ligam aos microtúbulos, incluindo as proteínas motoras dineína e cinesina, proteínas de separação de microtúbulos como a catanina e outras proteínas importantes para regular a dinâmica dos microtúbulos. Recentemente, uma proteína semelhante à actina foi encontrada na bactéria gram-positiva Bacillus thuringiensis, que forma uma estrutura semelhante a um microtúbulo chamada nanotúbulo, envolvida na segregação do plasmídeo. Outros microtúbulos bacterianos têm um anel de cinco protofilamentos.
História
Processos mediados por tubulina e microtúbulos, como a locomoção celular, foram observados pelos primeiros microscopistas, como Leeuwenhoek (1677). No entanto, a natureza fibrosa dos flagelos e outras estruturas foi descoberta dois séculos depois, com microscópios de luz aprimorados, e confirmada no século 20 com o microscópio eletrônico e estudos bioquímicos.
Os ensaiosIn vitro para proteínas motoras de microtúbulos, como dineína e cinesina, são pesquisados marcando fluorescentemente um microtúbulo e fixando o microtúbulo ou as proteínas motoras a uma lâmina de microscópio e, em seguida, visualizando a lâmina com vídeo aprimorado microscopia para registrar a viagem das proteínas motoras. Isso permite o movimento das proteínas motoras ao longo do microtúbulo ou o movimento do microtúbulo através das proteínas motoras. Consequentemente, alguns processos de microtúbulos podem ser determinados por quimografia.
Estrutura
Em eucariotos, os microtúbulos são cilindros longos e ocos compostos de dímeros de α- e β-tubulina polimerizados. O espaço interno dos cilindros de microtúbulos ocos é chamado de lúmen. As subunidades α e β-tubulina são aproximadamente 50% idênticas no nível de aminoácidos e ambas têm um peso molecular de aproximadamente 50 kDa.
Esses dímeros de α/β-tubulina polimerizam ponta a ponta em protofilamentos lineares que se associam lateralmente para formar um único microtúbulo, que pode então ser estendido pela adição de mais α/β-tubulina dímeros. Normalmente, os microtúbulos são formados pela associação paralela de treze protofilamentos, embora microtúbulos compostos por menos ou mais protofilamentos tenham sido observados em várias espécies, bem como in vitro.
Os microtúbulos têm uma polaridade distinta que é crítica para sua função biológica. A tubulina polimeriza ponta a ponta, com as subunidades β de um dímero de tubulina em contato com as subunidades α do dímero seguinte. Portanto, em um protofilamento, uma extremidade terá as subunidades α expostas, enquanto a outra extremidade terá as subunidades β expostas. Essas extremidades são designadas como extremidades (-) e (+), respectivamente. Os protofilamentos se agrupam paralelamente com a mesma polaridade, então, em um microtúbulo, há uma extremidade, a extremidade (+), com apenas subunidades β expostas, enquanto a outra extremidade, a extremidade (-), possui apenas α -subunidades expostas. Embora o alongamento dos microtúbulos possa ocorrer nas extremidades (+) e (-), é significativamente mais rápido na extremidade (+).
A associação lateral dos protofilamentos gera uma estrutura pseudo-helicoidal, com uma volta da hélice contendo 13 dímeros de tubulina, cada um de um protofilamento diferente. Na forma mais comum "13-3" arquitetura, o 13º dímero de tubulina interage com o próximo dímero de tubulina com um deslocamento vertical de 3 monômeros de tubulina devido à helicidade do giro. Existem outras arquiteturas alternativas, como 11-3, 12-3, 14-3, 15-4 ou 16-4, que foram detectadas em uma ocorrência muito menor. Os microtúbulos também podem se transformar em outras formas, como filamentos helicoidais, que são observados em organismos protistas como os foraminíferos. Existem dois tipos distintos de interações que podem ocorrer entre as subunidades dos protofilamentos laterais dentro do microtúbulo, chamadas redes tipo A e tipo B. Na rede do tipo A, as associações laterais de protofilamentos ocorrem entre as subunidades α e β-tubulina adjacentes (isto é, uma subunidade α-tubulina de um protofilamento interage com uma subunidade β-tubulina de um protofilamento adjacente). Na rede do tipo B, as subunidades α e β-tubulina de um protofilamento interagem com as subunidades α e β-tubulina de um protofilamento adjacente, respectivamente. Estudos experimentais mostraram que a rede do tipo B é o arranjo primário dentro dos microtúbulos. No entanto, na maioria dos microtúbulos há uma costura na qual as subunidades de tubulina interagem α-β.
A sequência e a composição exata das moléculas durante a formação dos microtúbulos podem ser resumidas da seguinte forma: Uma β-tubulina se conecta no contexto de uma ligação covalente inexistente com uma α-tubulina, que na forma conectada é um heterodímero, pois eles consistem em dois polipeptídeos diferentes (β-tubulina e α-tubulina). Então, depois que os heterodímeros são formados, eles se unem para formar longas cadeias que sobem figurativamente em uma direção (por exemplo, para cima). Esses heterodímeros, que são conectados em uma determinada direção, formam protofilamentos. Essas longas cadeias (protofilamentos) agora se acumulam gradualmente uma ao lado da outra, de modo que se forma uma estrutura tubular, que possui um lúmen típico de um tubo. Assim, principalmente 13 protofilamentos formam a parede externa dos microtúbulos. Os heterodímeros consistem em uma extremidade positiva e negativa, com a alfa-tubulina formando a extremidade negativa e a beta-tubulina a extremidade positiva. Devido ao fato de os heterodímeros serem empilhados uns sobre os outros, sempre há um final negativo e um positivo. Os microtúbulos crescem por adição de heterodímeros na extremidade positiva.
Algumas espécies de Prosthecobacter também contêm microtúbulos. A estrutura desses microtúbulos bacterianos é semelhante à dos microtúbulos eucarióticos, consistindo em um tubo oco de protofilamentos montados a partir de heterodímeros de tubulina bacteriana A (BtubA) e tubulina bacteriana B (BtubB). Ambos BtubA e BtubB compartilham características de α- e β-tubulina. Ao contrário dos microtúbulos eucarióticos, os microtúbulos bacterianos não requerem acompanhantes para se dobrar. Em contraste com os 13 protofilamentos dos microtúbulos eucarióticos, os microtúbulos bacterianos compreendem apenas cinco.
Organização intracelular
Os microtúbulos fazem parte do citoesqueleto, uma rede estrutural dentro do citoplasma da célula. As funções do citoesqueleto de microtúbulos incluem suporte mecânico, organização do citoplasma, transporte, motilidade e segregação cromossômica. Nos neurônios em desenvolvimento, os microtúbulos são conhecidos como neurotúbulos e podem modular a dinâmica da actina, outro componente do citoesqueleto. Um microtúbulo é capaz de crescer e encolher para gerar força, e existem proteínas motoras que permitem que organelas e outros componentes celulares sejam transportados ao longo de um microtúbulo. Essa combinação de papéis torna os microtúbulos importantes para organizar e mover constituintes intracelulares.
A organização dos microtúbulos na célula é específica do tipo de célula. Nos epitélios, as extremidades negativas do polímero de microtúbulos estão ancoradas perto do local de contato célula-célula e organizadas ao longo do eixo apical-basal. Após a nucleação, as extremidades negativas são liberadas e então reancoradas na periferia por fatores como Ninein e PLEKHA7. Dessa forma, podem facilitar o transporte de proteínas, vesículas e organelas ao longo do eixo apical-basal da célula. Em fibroblastos e outros tipos de células mesenquimais, os microtúbulos estão ancorados no centrossomo e irradiam com suas extremidades positivas para fora em direção à periferia da célula (como mostrado na primeira figura). Nessas células, os microtúbulos desempenham papéis importantes na migração celular. Além disso, a polaridade dos microtúbulos é influenciada por proteínas motoras, que organizam muitos componentes da célula, incluindo o retículo endoplasmático e o aparelho de Golgi.
Polimerização de microtúbulos
Nucleação
Nucleação é o evento que inicia a formação de microtúbulos a partir do dímero de tubulina. Os microtúbulos são tipicamente nucleados e organizados por organelas chamadas centros organizadores de microtúbulos (MTOCs). Contido dentro do MTOC está outro tipo de tubulina, γ-tubulina, que é distinta das subunidades α e β dos próprios microtúbulos. A γ-tubulina se combina com várias outras proteínas associadas para formar uma estrutura semelhante a uma arruela de bloqueio conhecida como "γ-tubulina anel complexo" (γ-TuRC). Este complexo atua como um molde para os dímeros de α/β-tubulina iniciarem a polimerização; ele atua como uma tampa da extremidade (-) enquanto o crescimento dos microtúbulos continua longe do MTOC na direção (+).
O centrossomo é o MTOC primário da maioria dos tipos de células. No entanto, os microtúbulos também podem ser nucleados de outros locais. Por exemplo, cílios e flagelos têm MTOCs em suas bases denominadas corpos basais. Além disso, o trabalho do grupo Kaverina em Vanderbilt, assim como outros, sugere que o aparelho de Golgi pode servir como uma plataforma importante para a nucleação de microtúbulos. Como a nucleação do centrossomo é inerentemente simétrica, a nucleação de microtúbulos associada ao Golgi pode permitir que a célula estabeleça assimetria na rede de microtúbulos. Em estudos recentes, o grupo Vale da UCSF identificou o complexo proteico augmin como um fator crítico para a geração de microtúbulos baseados em fusos dependentes do centrossoma. Foi demonstrado que ele interage com γ-TuRC e aumenta a densidade de microtúbulos ao redor da origem do fuso mitótico.
Alguns tipos de células, como células vegetais, não contêm MTOCs bem definidos. Nessas células, os microtúbulos são nucleados a partir de locais discretos no citoplasma. Outros tipos de células, como os parasitas tripanossomatídeos, têm um MTOC, mas é encontrado permanentemente na base de um flagelo. Aqui, a nucleação de microtúbulos para papéis estruturais e para a geração do fuso mitótico não é de um MTOC semelhante ao centríolo canônico.
Polimerização
Após o evento de nucleação inicial, os monômeros de tubulina devem ser adicionados ao polímero em crescimento. O processo de adição ou remoção de monômeros depende da concentração de dímeros de αβ-tubulina em solução em relação à concentração crítica, que é a concentração de estado estacionário de dímeros na qual não há mais nenhuma montagem ou desmontagem líquida no final do microtúbulo. Se a concentração do dímero for maior que a concentração crítica, o microtúbulo irá polimerizar e crescer. Se a concentração for menor que a concentração crítica, o comprimento do microtúbulo diminuirá.
Dinâmica dos microtúbulos
Instabilidade dinâmica
A instabilidade dinâmica refere-se à coexistência de montagem e desmontagem nas extremidades de um microtúbulo. O microtúbulo pode alternar dinamicamente entre as fases de crescimento e encolhimento nesta região. Os dímeros de tubulina podem se ligar a duas moléculas de GTP, uma das quais pode ser hidrolisada após a montagem. Durante a polimerização, os dímeros de tubulina estão no estado ligado a GTP. O GTP ligado à α-tubulina é estável e desempenha uma função estrutural neste estado ligado. No entanto, o GTP ligado à β-tubulina pode ser hidrolisado a GDP logo após a montagem. As propriedades de montagem da GDP-tubulina são diferentes daquelas da GTP-tubulina, pois a GDP-tubulina é mais propensa à despolimerização. Uma subunidade de tubulina ligada a GDP na ponta de um microtúbulo tenderá a cair, embora uma tubulina ligada a GDP no meio de um microtúbulo não possa sair espontaneamente do polímero. Uma vez que a tubulina se adiciona à extremidade do microtúbulo no estado ligado ao GTP, propõe-se que exista uma tampa de tubulina ligada ao GTP na ponta do microtúbulo, protegendo-o da desmontagem. Quando a hidrólise alcança a ponta do microtúbulo, ela começa uma rápida despolimerização e encolhimento. Essa mudança de crescimento para encolhimento é chamada de catástrofe. A tubulina ligada ao GTP pode começar a adicionar à ponta do microtúbulo novamente, fornecendo uma nova tampa e protegendo o microtúbulo de encolher. Isso é conhecido como "resgate".
"Pesquisar e capturar" modelo
Em 1986, Marc Kirschner e Tim Mitchison propuseram que os microtúbulos usam suas propriedades dinâmicas de crescimento e encolhimento em suas extremidades positivas para sondar o espaço tridimensional da célula. As extremidades positivas que encontram cinetocoros ou locais de polaridade são capturadas e não exibem mais crescimento ou encolhimento. Ao contrário dos microtúbulos dinâmicos normais, que têm uma meia-vida de 5 a 10 minutos, os microtúbulos capturados podem durar horas. Essa ideia é comumente conhecida como "pesquisa e captura" modelo. De fato, o trabalho desde então validou amplamente essa ideia. No cinetócoro, foi demonstrado que uma variedade de complexos capturam as extremidades (+) dos microtúbulos. Além disso, uma atividade de capping (+)-end para microtúbulos interfásicos também foi descrita. Essa atividade posterior é mediada por forminas, a proteína da polipose adenomatosa coli e EB1, uma proteína que rastreia ao longo das extremidades positivas crescentes dos microtúbulos.
Regulação da dinâmica dos microtúbulos
Modificações pós-tradução
Embora a maioria dos microtúbulos tenha uma meia-vida de 5 a 10 minutos, alguns microtúbulos podem permanecer estáveis por horas. Esses microtúbulos estabilizados acumulam modificações pós-translacionais em suas subunidades de tubulina pela ação de enzimas ligadas aos microtúbulos. No entanto, uma vez que o microtúbulo se despolimeriza, a maioria dessas modificações é rapidamente revertida por enzimas solúveis. Uma vez que a maioria das reações de modificação são lentas, enquanto suas reações reversas são rápidas, a tubulina modificada só é detectada em microtúbulos estáveis de vida longa. A maioria dessas modificações ocorre na região C-terminal da alfa-tubulina. Essa região, rica em glutamato carregado negativamente, forma caudas relativamente não estruturadas que se projetam para fora do microtúbulo e formam contatos com motores. Assim, acredita-se que as modificações da tubulina regulam a interação dos motores com os microtúbulos. Uma vez que esses microtúbulos modificados estáveis são tipicamente orientados para o local da polaridade celular nas células interfásicas, esse subconjunto de microtúbulos modificados fornece uma rota especializada que ajuda a fornecer vesículas a essas zonas polarizadas. Essas modificações incluem:
- Detyrosination: a remoção da tirosina C-terminal de alfa-tubulin. Esta reação expõe um glutamato no novo C-terminus. Como resultado, os microtúbulos que acumulam esta modificação são frequentemente referidos como Glu-microtúbulos. Embora a carboxiptidase da tubulina ainda não tenha sido identificada, a tubulina - ligase da tirosina (TTL) é conhecida.
- Delta2: a remoção dos últimos dois resíduos do termo C de alfa-tubulina. Ao contrário da destrosinação, esta reação é considerada irreversível e só foi documentada em neurônios.
- Acetilação: a adição de um grupo acetil à lisina 40 de alfa-tubulina. Esta modificação ocorre em uma lisina que é acessível apenas a partir do interior do microtúbulo, e permanece claro como as enzimas acessam o resíduo da lisina. A natureza da acetiltransferase da tubulina permanece controversa, mas foi encontrado que em mamíferos a maior acetiltransferase é ATAT1. no entanto, a reação reversa é conhecida por ser catalisada por HDAC6. O impacto real da acetilação na estrutura e função dos microtúbulos permanece elusivo.
- Poliglutamylation: a adição de um polímero glutamato (tipicamente 4-6 resíduos longos) ao grupo gamma-carboxyl de qualquer um de cinco glutamatos encontrados perto do fim da alfa-tubulin. Enzimas relacionados ao TTL adicionam o glutamato de ramificação inicial (TTL4,5 e 7), enquanto outras enzimas que pertencem à mesma família alongam a cadeia de poliglutamato (TTL6,11 e 13).
- Poliglicylation: a adição de um polímero de glicina (2-10 resíduos longos) ao grupo gamma-carboxyl de qualquer um de cinco glutamatos encontrados perto do fim da beta-tubulin. TTL3 e 8 adicionam a glicina de ramificação inicial, enquanto TTL10 alonga a cadeia de poliglicina.
A tubulina também é conhecida por ser fosforilada, ubiquitinada, sumoilada e palmitoilada.
Drogas de ligação à tubulina e efeitos químicos
Uma grande variedade de drogas é capaz de se ligar à tubulina e modificar suas propriedades de montagem. Essas drogas podem ter um efeito em concentrações intracelulares muito mais baixas do que a da tubulina. Essa interferência na dinâmica dos microtúbulos pode ter o efeito de interromper o ciclo celular de uma célula e levar à morte celular programada ou à apoptose. No entanto, existem dados que sugerem que a interferência da dinâmica dos microtúbulos é insuficiente para bloquear as células em mitose. Esses estudos demonstraram que a supressão da dinâmica ocorre em concentrações menores do que as necessárias para bloquear a mitose. Foi demonstrado que a supressão da dinâmica dos microtúbulos por mutações na tubulina ou por tratamento medicamentoso inibe a migração celular. Tanto os estabilizadores quanto os desestabilizadores de microtúbulos podem suprimir a dinâmica dos microtúbulos.
As drogas que podem alterar a dinâmica dos microtúbulos incluem:
- A classe de luta contra o câncer de drogas (paclitaxel (taxol) e docetaxel) bloqueia a instabilidade dinâmica estabilizando a tubulina do PIB no microtúbulo. Assim, mesmo quando a hidrólise do GTP atinge a ponta do microtúbulo, não há despolimerização e o microtúbulo não encolhe para trás.
Taxanos (sozinhos ou em combinação com derivados de platina (carboplatina) ou gencitabina) são usados contra neoplasias de mama e ginecológicas, carcinomas de células escamosas (câncer de cabeça e pescoço, alguns cânceres de pulmão), etc.
- Os epothilones, por exemplo, Ixabepilone, trabalham de forma semelhante aos taxanes.
- Vinorelbine, Nocodazole, vincristine e colchicine têm o efeito oposto, bloqueando a polimerização da tubulina em microtúbulos.
- Eribulin liga-se à extremidade crescente dos microtúbulos. A eribulina exerce seus efeitos de anticancer provocando a apoptose de células cancerosas após o bloqueio mitotic prolongado e irreversível.
Foi relatado que a expressão de β3-tubulina altera as respostas celulares à supressão induzida por drogas da dinâmica dos microtúbulos. Em geral, a dinâmica é normalmente suprimida por concentrações baixas e subtóxicas de fármacos microtúbulos que também inibem a migração celular. No entanto, a incorporação de β3-tubulina nos microtúbulos aumenta a concentração da droga necessária para suprimir a dinâmica e inibir a migração celular. Assim, os tumores que expressam β3-tubulina não são apenas resistentes aos efeitos citotóxicos das drogas direcionadas aos microtúbulos, mas também à sua capacidade de suprimir a metástase tumoral. Além disso, a expressão de β3-tubulina também neutraliza a capacidade dessas drogas de inibir a angiogênese, que normalmente é outra faceta importante de sua ação.
Os polímeros de microtúbulos são extremamente sensíveis a vários efeitos ambientais. Níveis muito baixos de cálcio livre podem desestabilizar os microtúbulos e isso impediu os primeiros pesquisadores de estudar o polímero in vitro. Temperaturas frias também causam rápida despolimerização dos microtúbulos. Em contraste, a água pesada promove a estabilidade do polímero de microtúbulos.
Proteínas que interagem com microtúbulos
Proteínas associadas a microtúbulos (MAPs)
Os MAPs demonstraram desempenhar um papel crucial na regulação da dinâmica dos microtúbulos in vivo. As taxas de polimerização, despolimerização e catástrofe dos microtúbulos variam dependendo de quais proteínas associadas aos microtúbulos (MAPs) estão presentes. Os MAPs originalmente identificados no tecido cerebral podem ser classificados em dois grupos com base em seu peso molecular. Esta primeira classe compreende MAPs com peso molecular abaixo de 55-62 kDa, e são chamadas de proteínas τ (tau). In vitro, foi demonstrado que as proteínas tau se ligam diretamente aos microtúbulos, promovem a nucleação e evitam a desmontagem e induzem a formação de arranjos paralelos. Além disso, as proteínas tau também demonstraram estabilizar os microtúbulos nos axônios e foram implicadas na doença de Alzheimer. A segunda classe é composta por MAPs com peso molecular de 200-1000 kDa, dos quais são conhecidos quatro tipos: MAP-1, MAP-2, MAP-3 e MAP-4. As proteínas MAP-1 consistem em um conjunto de três proteínas diferentes: A, B e C. A proteína C desempenha um papel importante no transporte retrógrado de vesículas e também é conhecida como dineína citoplasmática. As proteínas MAP-2 estão localizadas nos dendritos e no corpo dos neurônios, onde se ligam a outros filamentos do citoesqueleto. As proteínas MAP-4 são encontradas na maioria das células e estabilizam os microtúbulos. Além dos MAPs que têm um efeito estabilizador na estrutura dos microtúbulos, outros MAPs podem ter um efeito desestabilizador por clivagem ou indução da despolimerização dos microtúbulos. Observou-se que três proteínas chamadas katanina, espastina e fidgetina regulam o número e o comprimento dos microtúbulos por meio de suas atividades desestabilizadoras. Além disso, prevê-se que KIAA1211L esteja localizado nos microtúbulos.
MAPs são determinantes de diferentes formas de citoesqueleto de axônios e dendritos, com microtúbulos sendo mais distantes nos dendritos
Proteínas de rastreamento Plus-end (+TIPs)
As proteínas de rastreamento de extremidades Plus são proteínas MAP que se ligam às pontas dos microtúbulos em crescimento e desempenham um papel importante na regulação da dinâmica dos microtúbulos. Por exemplo, foi observado que os +TIPs participam das interações dos microtúbulos com os cromossomos durante a mitose. O primeiro MAP a ser identificado como +TIP foi o CLIP170 (cytoplasmic linker protein), que demonstrou desempenhar um papel nos eventos de resgate da despolimerização de microtúbulos. Exemplos adicionais de +TIPs incluem EB1, EB2, EB3, p150Glued, Dynamitin, Lis1, CLIP115, CLASP1 e CLASP2.
Proteínas motoras
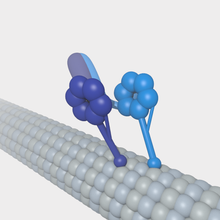
Os microtúbulos podem atuar como substratos para proteínas motoras que estão envolvidas em funções celulares importantes, como tráfego de vesículas e divisão celular. Ao contrário de outras proteínas associadas aos microtúbulos, as proteínas motoras utilizam a energia da hidrólise do ATP para gerar trabalho mecânico que move a proteína ao longo do substrato. As principais proteínas motoras que interagem com os microtúbulos são a cinesina, que geralmente se move em direção à extremidade (+) do microtúbulo, e a dineína, que se move em direção à extremidade (-).
- Adina é composta por duas cadeias pesadas idênticas, que compõem dois grandes domínios de cabeça globular, e um número variável de cadeias intermediárias e leves. O transporte mediado pordina ocorre a partir da extremidade (+) para a extremidade (-) do microtúbulo. A hidrólise ATP ocorre nos domínios da cabeça globular, que compartilham semelhanças com a família de proteínas AAA+ (ATPase associada a várias atividades celulares). A hidrólise ATP nestes domínios é acoplada ao movimento ao longo do microtúbulo através dos domínios de ligação de microtúbulos. Adina transporta vesículas e organelas em todo o citoplasma. A fim de fazer isso, as moléculas de dynein ligam membranas organelle através de um complexo proteico que contém um número de elementos incluindo a dinaactina.
- Kinesin tem uma estrutura semelhante à dynein. A quinesina está envolvida no transporte de uma variedade de cargas intracelulares, incluindo vesículas, organelas, complexos proteicos e mRNAs para a extremidade do microtúbulo (+).
Alguns vírus (incluindo retrovírus, herpesvírus, parvovírus e adenovírus) que requerem acesso ao núcleo para replicar seus genomas se ligam a proteínas motoras.
Mitose
Centossomos
O centrossomo é o principal MTOC (centro organizador de microtúbulos) da célula durante a mitose. Cada centrossoma é constituído por dois cilindros chamados centríolos, orientados em ângulos retos entre si. O centríolo é formado por 9 microtúbulos principais, cada um com dois microtúbulos parciais ligados a ele. Cada centríolo tem aproximadamente 400 nm de comprimento e cerca de 200 nm de circunferência.
O centrossomo é crítico para a mitose, pois a maioria dos microtúbulos envolvidos no processo se origina do centrossomo. As extremidades negativas de cada microtúbulo começam no centrossomo, enquanto as extremidades positivas se irradiam em todas as direções. Assim, o centrossoma também é importante na manutenção da polaridade dos microtúbulos durante a mitose.
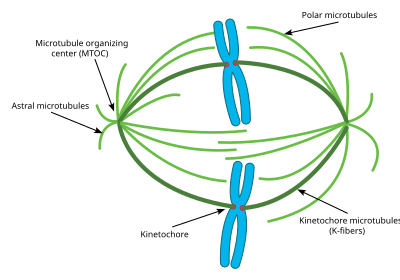
A maioria das células tem apenas um centrossomo durante a maior parte do ciclo celular, no entanto, logo antes da mitose, o centrossomo se duplica e a célula contém dois centrossomos. Alguns dos microtúbulos que se irradiam do centrossomo crescem diretamente para longe do centrossomo irmão. Esses microtúbulos são chamados de microtúbulos astrais. Com a ajuda desses microtúbulos astrais, os centrossomos se afastam um do outro em direção a lados opostos da célula. Uma vez lá, outros tipos de microtúbulos necessários para a mitose, incluindo microtúbulos interpolares e fibras K, podem começar a se formar.
Uma observação final importante sobre os centrossomos e microtúbulos durante a mitose é que, embora o centrossomo seja o MTOC para os microtúbulos necessários para a mitose, a pesquisa mostrou que uma vez que os próprios microtúbulos são formados e no local correto, os próprios centrossomos não são necessários para que ocorra a mitose.
Subclasses de microtúbulos
Microtúbulos astrais são uma subclasse de microtúbulos que só existem durante e ao redor da mitose. Eles se originam do centrossomo, mas não interagem com os cromossomos, cinetocoros ou com os microtúbulos originários do outro centrossomo. Em vez disso, seus microtúbulos irradiam em direção à membrana celular. Uma vez lá, eles interagem com proteínas motoras específicas que criam força que puxa os microtúbulos e, portanto, todo o centrossomo em direção à membrana celular. Como afirmado acima, isso ajuda os centrossomos a se orientarem um para o outro na célula. No entanto, esses microtúbulos astrais não interagem com o próprio fuso mitótico. Experimentos mostraram que sem esses microtúbulos astrais, o fuso mitótico pode se formar, mas sua orientação na célula nem sempre é correta e, portanto, a mitose não ocorre com a mesma eficácia. Outra função chave dos microtúbulos astrais é auxiliar na citocinese. Os microtúbulos astrais interagem com proteínas motoras na membrana celular para separar o fuso e toda a célula uma vez que os cromossomos tenham sido replicados.
Microtúbulos interpolares/polares são uma classe de microtúbulos que também se irradiam do centrossomo durante a mitose. Esses microtúbulos irradiam em direção ao fuso mitótico, ao contrário dos microtúbulos astrais. Os microtúbulos interpolares são a subclasse mais abundante e dinâmica de microtúbulos durante a mitose. Cerca de 95% dos microtúbulos no fuso mitótico podem ser caracterizados como interpolares. Além disso, a meia-vida desses microtúbulos é extremamente curta, pois dura menos de um minuto. Os microtúbulos interpolares que não se ligam aos cinetócoros podem ajudar na congregação cromossômica por meio da interação lateral com os cinetócoros.
Fibras K/microtúbulos do cinetócoro são a terceira subclasse importante de microtúbulos mitóticos. Esses microtúbulos formam conexões diretas com os cinetócoros no fuso mitótico. Cada fibra K é composta de 20 a 40 microtúbulos paralelos, formando um tubo forte que se liga em uma extremidade ao centrossomo e na outra ao cinetócoro, localizado no centro de cada cromossomo. Como cada centrossomo tem uma fibra K conectando-se a cada par de cromossomos, os cromossomos ficam presos no meio do fuso mitótico pelas fibras K. As fibras K têm uma meia-vida muito mais longa do que os microtúbulos interpolares, entre 4 e 8 minutos. Durante o final das mitoses, os microtúbulos que formam cada fibra K começam a se desassociar, encurtando as fibras K. À medida que as fibras K encurtam, os pares de cromossomos são separados logo antes da citocinese. Anteriormente, alguns pesquisadores acreditavam que as fibras K se formavam em sua extremidade negativa originando-se do centrossomo, assim como outros microtúbulos, no entanto, novas pesquisas apontaram para um mecanismo diferente. Nesse novo mecanismo, as fibras K são inicialmente estabilizadas em sua extremidade positiva pelos cinetócoros e crescem a partir daí. A extremidade negativa dessas fibras K eventualmente se conecta a um microtúbulo interpolar existente e, eventualmente, é conectada ao centrossomo dessa maneira.
Microtúbulo nuclear no fuso mitótico
A maioria dos microtúbulos que formam o fuso mitótico se origina do centrossomo. Originalmente, pensava-se que todos esses microtúbulos se originavam do centrossomo por meio de um método chamado busca e captura, descrito com mais detalhes na seção acima; no entanto, novas pesquisas mostraram que existem meios adicionais de nucleação de microtúbulos durante a mitose. Um dos mais importantes desses meios adicionais de nucleação de microtúbulos é a via RAN-GTP. O RAN-GTP se associa à cromatina durante a mitose para criar um gradiente que permite a nucleação local de microtúbulos próximos aos cromossomos. Além disso, uma segunda via conhecida como complexo augmin/HAUS (alguns organismos usam o complexo augmin mais estudado, enquanto outros, como os humanos, usam um complexo análogo chamado HAUS) atua como um meio adicional de nucleação de microtúbulos no fuso mitótico.
Funções
Migração celular
As extremidades dos microtúbulos geralmente estão localizadas em estruturas específicas. Nas células interfásicas polarizadas, os microtúbulos são orientados desproporcionalmente do MTOC em direção ao local de polaridade, como a borda de ataque dos fibroblastos em migração. Acredita-se que essa configuração ajude a transportar vesículas ligadas a microtúbulos do Golgi para o local de polaridade.
A instabilidade dinâmica dos microtúbulos também é necessária para a migração da maioria das células de mamíferos que rastejam. Os microtúbulos dinâmicos regulam os níveis das principais proteínas G, como RhoA e Rac1, que regulam a contratilidade celular e a disseminação celular. Os microtúbulos dinâmicos também são necessários para desencadear a desmontagem da adesão focal, necessária para a migração. Verificou-se que os microtúbulos agem como “suportes” que neutralizam as forças contráteis necessárias para a retração da borda de fuga durante o movimento celular. Quando os microtúbulos na borda posterior da célula são dinâmicos, eles são capazes de se remodelar para permitir a retração. Quando a dinâmica é suprimida, os microtúbulos não podem se remodelar e, portanto, se opõem às forças contráteis. A morfologia das células com dinâmica de microtúbulos suprimida indica que as células podem estender a borda frontal (polarizada na direção do movimento), mas têm dificuldade em retrair sua borda posterior. Por outro lado, altas concentrações de drogas ou mutações nos microtúbulos que despolimerizam os microtúbulos podem restaurar a migração celular, mas há perda de direcionalidade. Pode-se concluir que os microtúbulos agem tanto para restringir o movimento celular quanto para estabelecer a direcionalidade.
Cílios e flagelos
Os microtúbulos têm um papel estrutural importante nos cílios e flagelos eucarióticos. Cílios e flagelos sempre se estendem diretamente de um MTOC, neste caso denominado corpo basal. A ação das proteínas motoras da dineína nas várias cadeias de microtúbulos que correm ao longo de um cílio ou flagelo permite que a organela se dobre e gere força para nadar, mover material extracelular e outras funções. Os procariotos possuem proteínas semelhantes à tubulina, incluindo FtsZ. No entanto, os flagelos procarióticos são totalmente diferentes em estrutura dos flagelos eucarióticos e não contêm estruturas baseadas em microtúbulos.
Desenvolvimento
O citoesqueleto formado pelos microtúbulos é essencial para o processo morfogenético de desenvolvimento de um organismo. Por exemplo, uma rede de microtúbulos polarizados é necessária dentro do oócito de Drosophila melanogaster durante sua embriogênese para estabelecer o eixo do ovo. Sinais enviados entre as células foliculares e o oócito (como fatores semelhantes ao fator de crescimento epidérmico) provocam a reorganização dos microtúbulos de forma que suas extremidades (-) se localizem na parte inferior do oócito, polarizando a estrutura e levando ao aparecimento de um eixo ântero-posterior. Esse envolvimento na arquitetura do corpo também é visto em mamíferos.
Outra área onde os microtúbulos são essenciais é o desenvolvimento do sistema nervoso em vertebrados superiores, onde a dinâmica da tubulina e das proteínas associadas (como as proteínas associadas aos microtúbulos) são finamente controladas durante o desenvolvimento do sistema nervoso.
Regulação genética
O citoesqueleto celular é um sistema dinâmico que funciona em muitos níveis diferentes: além de dar à célula uma forma particular e apoiar o transporte de vesículas e organelas, também pode influenciar a expressão gênica. Os mecanismos de transdução de sinal envolvidos nesta comunicação são pouco compreendidos. No entanto, foi descrita a relação entre a despolimerização de microtúbulos mediada por drogas e a expressão específica de fatores de transcrição, o que forneceu informações sobre a expressão diferencial dos genes dependendo da presença desses fatores. Essa comunicação entre o citoesqueleto e a regulação da resposta celular também está relacionada à ação dos fatores de crescimento: por exemplo, essa relação existe para o fator de crescimento do tecido conjuntivo.