Leis de difusão de Fick
As leis de difusão de Fick descrevem a difusão e foram derivadas por Adolf Fick em 1855. Elas podem ser usadas para calcular o coeficiente de difusão, D. A primeira lei de Fick pode ser usada para derivar sua segunda lei, que por sua vez é idêntica à equação de difusão.
Um processo de difusão que obedece às leis de Fick é chamado de difusão normal ou Fickiana; caso contrário, é chamada de difusão anômala ou difusão não-Fickiana.
História
Em 1855, o fisiologista Adolf Fick relatou pela primeira vez suas agora conhecidas leis que regem o transporte de massa por meios difusivos. O trabalho de Fick foi inspirado pelos experimentos anteriores de Thomas Graham, que não conseguiram propor as leis fundamentais pelas quais Fick se tornaria famoso. A lei de Fick é análoga às relações descobertas na mesma época por outros cientistas eminentes: a lei de Darcy (escoamento hidráulico), a lei de Ohm (transporte de carga) e a lei de Fourier (transporte de calor).
Os experimentos de Fick (modelados nos de Graham) tratavam da medição das concentrações e fluxos de sal, difundindo-se entre dois reservatórios através de tubos de água. É notável que o trabalho de Fick envolvia principalmente a difusão em fluidos, porque na época a difusão em sólidos não era considerada geralmente possível. Hoje, as Leis de Fick formam o núcleo de nossa compreensão da difusão em sólidos, líquidos e gases (na ausência de movimento de fluido em massa nos dois últimos casos). Quando um processo de difusão não segue as leis de Fick (o que acontece nos casos de difusão através de meios porosos e difusão de penetrantes inchados, entre outros), é referido como não- Fickiano.
Primeira lei de Fick
A primeira lei de Fick relaciona o fluxo difusivo com o gradiente de concentração. Postula que o fluxo vai de regiões de alta concentração para regiões de baixa concentração, com magnitude proporcional ao gradiente de concentração (derivada espacial), ou em termos simplistas o conceito de que um soluto se moverá de uma região de alta concentração para uma região de baixa concentração através de um gradiente de concentração. Em uma dimensão (espacial), a lei pode ser escrita de várias formas, onde a forma mais comum (ver) é em base molar:
- JJ= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. DDφ φ DxNão. J=-D{frac {dvarphi }{dx}}}
onde
- JJ é o fluxo de difusão, da qual a dimensão é a quantidade de substância por área unitária por tempo unitário. JJ mede a quantidade de substância que fluirá através de uma área unitária durante um intervalo de tempo unitário.
- D é o coeficiente de difusão ou difusividade. Sua dimensão é área por unidade de tempo.
- φ (para misturas ideais) é a concentração, da qual a dimensão é a quantidade de substância por volume unitário.
- x é posição, cuja dimensão é comprimento.
D é proporcional ao quadrado da velocidade das partículas em difusão, que depende da temperatura, viscosidade do fluido e da tamanho das partículas de acordo com a relação Stokes-Einstein. Em soluções aquosas diluídas, os coeficientes de difusão da maioria dos íons são semelhantes e têm valores que, à temperatura ambiente, estão na faixa de (0.6–2)×10−9 m2/ s. Para moléculas biológicas, os coeficientes de difusão normalmente variam de 10−10 a 10−11 m2/s.
Em duas ou mais dimensões devemos usar ∇, o operador del ou gradiente, que generaliza a primeira derivada, obtendo
- JJ= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. D? ? φ φ {displaystyle mathbf {J} =-Dnabla varphi }
onde J denota o vetor de fluxo de difusão.
A força motriz para a difusão unidimensional é a quantidade −∂ φ/∂x, que para misturas ideais é o gradiente de concentração.
Variações da primeira lei
Outra forma para a primeira lei é escrevê-la com a variável primária como fração de massa (yi, dado por exemplo em kg/kg), então a equação muda para:
- JJEu...= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. ? ? DMEu...? ? Sim.Eu...{displaystyle mathbf {J_{i}} - Sim. D}{M_{i}}}nabla y_{i}}
onde
- índice Eu... denota o Eu...a espécie,
- JJEu... é o vetor de fluxo de difusão da Eu...as espécies (por exemplo, em mol/m2-
- MEu... é a massa molar do Eu...as espécies, e
- ? é a densidade da mistura (por exemplo, em kg/m3).
Note que o ? ? - Sim. está fora do operador gradiente. Isso é porque:
- Sim.Eu...= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =? ? SEu...? ? Não. y_{i}={frac {displaystyle _{si}}{rho)
onde ρsi é a densidade parcial do iésima espécie.
Além disso, em sistemas químicos diferentes de soluções ou misturas ideais, a força motriz para a difusão de cada espécie é o gradiente de potencial químico dessa espécie. Então a primeira lei de Fick (caso unidimensional) pode ser escrita
- JJEu...= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. DcEu...RT∂ ∂ μ μ Eu...∂ ∂ xNão. J_{i}=-{frac {Dc_{i}}{RT}}{frac {partial mu _{i}}{partial x}
onde
- índice Eu... denota o Eu...a espécie.
- c é a concentração (mol/m3).
- R é a constante do gás universal (J/K/mol).
- T é a temperatura absoluta (K).
- μ é o potencial químico (J/mol).
A força motriz da lei de Fick pode ser expressa como uma diferença de fugacidade:
- JJEu...= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. DRT∂ ∂ fEu...∂ ∂ xNão. J_{i}=-{frac (D){RT){frac (particular) f_{i}}{partial x}
Fugacidade fEu...Não. f_{i}} tem unidades Pa. fEu...Não. f_{i}} é uma pressão parcial do componente i em um vapor fEu...GNão. f_{i}^{G}} ou líquido fEu...LNão. f_{i}^{L}} fase. No equilíbrio líquido de vapor o fluxo de evaporação é zero porque fEu...G= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =fEu...LNão. f_{i}^{G}=f_{i}^{L}}.
Derivação da primeira lei de Fick para gases
Quatro versões da lei de Fick para misturas binárias de gases são dadas abaixo. Estes assumem: a difusão térmica é desprezível; a força corporal por unidade de massa é a mesma em ambas as espécies; e a pressão é constante ou ambas as espécies têm a mesma massa molar. Nestas condições, ref. mostra em detalhes como a equação de difusão da teoria cinética dos gases se reduz a esta versão da lei de Fick:
onde Vi é a velocidade de difusão das espécies i. Em termos de fluxo de espécies, isso é
Se, adicionalmente, ? ? ? ? = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =0{displaystyle nabla rho - Sim., isto reduz à forma mais comum da lei de Fick,
Se (em vez de ou em adição a ? ? ? ? = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =0{displaystyle nabla rho - Sim.) ambas as espécies têm a mesma massa molar, a lei de Fick torna-se
Onde? xEu...Não. x_{i}} é a fração de toupeira de espécies Eu....
Segunda lei de Fick
A segunda lei de Fick prevê como a difusão faz com que a concentração mude em relação ao tempo. É uma equação diferencial parcial que em uma dimensão lê:
- ∂ ∂ φ φ ∂ ∂ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D∂ ∂ 2φ φ ∂ ∂ x2{displaystyle varphi }{partial t}}=D,{frac ^{2}varphi ? x^{2}}
onde
- φ é a concentração em dimensões de [(montante da substância) comprimento-3], exemplo mol/m3; φ = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = φ(x,)) é uma função que depende da localização x e tempo )
- ) é tempo, exemplo s
- D é o coeficiente de difusão em dimensões de [comprimento2 Tempo- Sim.Exemplo2/
- x é a posição [comprimento], exemplo m
Em duas ou mais dimensões devemos usar o laplaciano Δ = ∇2, que generaliza a segunda derivada, obtendo a equação
- ∂ ∂ φ φ ∂ ∂ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D? ? φ φ {displaystyle varphi }{partial t}}=DDelta varphi }
A segunda lei de Fick tem a mesma forma matemática que a equação de calor e sua solução fundamental é a mesma que o kernel de calor, exceto comutação de condutividade térmica kNão. com coeficiente de difusão DNão.:
Derivação da segunda lei de Fick
A segunda lei de Fick pode ser derivada da primeira lei de Fick e da conservação de massa na ausência de quaisquer reações químicas:
- ∂ ∂ φ φ ∂ ∂ )+∂ ∂ ∂ ∂ xJJ= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =0⇒ ⇒ ∂ ∂ φ φ ∂ ∂ )- Sim. - Sim. ∂ ∂ ∂ ∂ x(D∂ ∂ ∂ ∂ xφ φ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =0{displaystyle varphi }{partial t}}+{frac {partial }{partial x}}J=0Rightarrow {frac {partial varphi }{partial t}}-{frac {partial }{partial x}}left(D{frac {partial }{partial x}}varphi right),=0}
Assumindo que o coeficiente de difusão D é uma constante, pode-se trocar as ordens de diferenciação e multiplicar pela constante:
- ∂ ∂ ∂ ∂ x(D∂ ∂ ∂ ∂ xφ φ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D∂ ∂ ∂ ∂ x∂ ∂ ∂ ∂ xφ φ = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D∂ ∂ 2φ φ ∂ ∂ x2{displaystyle {frac {partial }{partial x}}left(D{frac {partial }{partial x}}varphi right)=D{frac {partial }{partial x}}{frac {partial }{partial x}}varphi =D{frac {partial} ^{2}varphi ? x^{2}}
e, assim, receber a forma das equações de Fick como foi dito acima.
Para o caso de difusão em duas ou mais dimensões, a segunda lei de Fick torna-se
- ∂ ∂ φ φ ∂ ∂ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D? ? 2φ φ ,{displaystyle varphi }{partial t}}=D,nabla ^{2}varphi
que é análogo à equação do calor.
Se o coeficiente de difusão não é uma constante, mas depende da coordenada ou concentração, a segunda lei de Fick produz
- ∂ ∂ φ φ ∂ ∂ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =? ? )) (D? ? φ φ ).{displaystyle {frac {partial varphi }{partial t}}=nabla cdot (D,nabla varphi).}
Um exemplo importante é o caso em que φ está em estado estacionário, ou seja, a concentração não muda com o tempo, de modo que a parte esquerda da equação acima é identicamente zero. Em uma dimensão com D constante, a solução para a concentração será uma mudança linear de concentrações ao longo de x. Em duas ou mais dimensões obtemos
- ? ? 2φ φ = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =0{displaystyle nabla} ^{2}varphi - Sim.
que é a equação de Laplace, cujas soluções são referidas pelos matemáticos como funções harmônicas.
Exemplos de soluções e generalização
A segunda lei de Fick é um caso especial da equação convecção-difusão em que não há fluxo advectivo e nenhuma fonte volumétrica líquida. Pode ser derivado da equação da continuidade:
- ∂ ∂ φ φ ∂ ∂ )+? ? )) JJ= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =R,{displaystyle {frac {partial varphi }{partial t}}+nabla cdot mathbf {j} =R,}
onde j é o fluxo total e R é uma fonte volumétrica líquida para φ. A única fonte de fluxo nesta situação é assumida como fluxo difusivo:
- JJdifusão= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. D? ? φ φ {displaystyle mathbf {j} _{text{diffusion}}=-Dnabla varphi }
Integrando a definição de fluxo difusivo à equação de continuidade e assumindo que não há fonte (R = 0), chegamos a Fick's segunda lei:
- ∂ ∂ φ φ ∂ ∂ )= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =D∂ ∂ 2φ φ ∂ ∂ x2{displaystyle {displaystyle varphi} ? t}}=D{frac {partial ^{2}varphi }{partial x^{2}}
Se o fluxo for o resultado tanto do fluxo difusivo quanto do fluxo advectivo, a equação convecção-difusão é o resultado.
Exemplo de solução 1: fonte de concentração constante e comprimento de difusão
Um caso simples de difusão com o tempo t em uma dimensão (tomado como o estilo x-eixo) de um limite localizado na posição x = 0, onde a concentração é mantido em um valor n0 é
- n(x,))= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =n0Erro (x2D)).{displaystyle nleft(x,tright)=n_{0}operatorname {erfc} left({frac {x}{2{sqrt {Dt}}}}right).}
onde erfc é a função de erro complementar. Este é o caso quando gases corrosivos se difundem através da camada oxidativa em direção à superfície do metal (se assumirmos que a concentração de gases no ambiente é constante e o espaço de difusão – isto é, a camada de produtos de corrosão – é semi-infinito, começando em 0 na superfície e se espalhando infinitamente no fundo do material). Se, por sua vez, o espaço de difusão for infinito (durando ambos através da camada com n(x, 0) = 0, x > 0 e com n(x, 0) = n0, x ≤ 0), então a solução é corrigida apenas com o coeficiente 1/2 na frente de n0 (como a difusão agora ocorre em ambas as direções). Este caso é válido quando alguma solução com concentração n0 é colocada em contato com uma camada de solvente puro. (Bokstein, 2005) O comprimento 2√Dt é chamado de comprimento de difusão e fornece uma medida de até onde a concentração se propagou no estilo x-direção por difusão no tempo t (Bird, 1976).
Como uma aproximação rápida da função de erro, os dois primeiros termos da série de Taylor podem ser usados:
- n(x,))= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =n0Não.1- Sim. - Sim. 2(x2D)D D )]{displaystyle n(x,t)=n_{0}left[1-2left({frac {x}{2{sqrt {Dtpi }}right)right]}
Se D for dependente do tempo, o comprimento da difusão torna-se
- 2∫ ∫ 0)D? ? D? ? .- Sim. _{0}^{t} Dtau ,dtau }}.}
Essa ideia é útil para estimar um comprimento de difusão em um ciclo de aquecimento e resfriamento, onde D varia com a temperatura.
Exemplo de solução 2: partícula browniana e deslocamento médio quadrado
Outro caso simples de difusão é o movimento browniano de uma partícula. O deslocamento médio quadrado da partícula de sua posição original é:
Onde? nNão. é a dimensão do movimento browniano da partícula. Por exemplo, a difusão de uma molécula através de uma membrana celular 8 nm grossa é 1-D difusão por causa da simetria esférica; No entanto, a difusão de uma molécula da membrana para o centro de uma célula eucariótica é uma difusão 3-D. Para um cacto cilíndrico, a difusão de células fotossintéticas em sua superfície para seu centro (o eixo de sua simetria cilíndrica) é uma difusão 2-D.
A raiz quadrada de MSD, 2nD)(2nDt), é frequentemente usado como uma caracterização de quão longe a partícula se move após o tempo )Não. decorreu. O MSD é distribuído simetricamente sobre o espaço 1D, 2D e 3D. Assim, a distribuição de probabilidade da magnitude do MSD em 1D é Gaussian e 3D é uma distribuição Maxwell-Boltzmann.
Generalizações
- In non-homogeneous media, the diffusion coefficient varies in space, D = D(x). This dependence does not affect Fick's first law but the second law changes: ∂ φ ( x , t ) ∂ t = ∇ ⋅ ( D ( x ) ∇ φ ( x , t ) ) = D ( x ) Δ φ ( x , t ) + ∑ i = 1 3 ∂ D ( x ) ∂ x i ∂ φ ( x , t ) ∂ x i {displaystyle {frac {partial varphi (x,t)}{partial t}}=nabla cdot {bigl (}D(x)nabla varphi (x,t){bigr)}=D(x)Delta varphi (x,t)+sum _{i=1}^{3}{frac {partial D(x)}{partial x_{i}}}{frac {partial varphi (x,t)}{partial x_{i}}}}
- In anisotropic media, the diffusion coefficient depends on the direction. It is a symmetric tensor Dji = Dij. Fick's first law changes to it is the product of a tensor and a vector:J = − D ∇ φ , {displaystyle J=-Dnabla varphi}For the diffusion equation this formula givesJ i = − ∑ j = 1 3 D i j ∂ φ ∂ x j . {displaystyle J_{i}=-sum _{j=1}^{3}D_{ij}{frac {partial varphi }{partial x_{j}}}.}The symmetric matrix of diffusion coefficients Dij should be positive definite. It is needed to make the right hand side operator elliptic.∂ φ ( x , t ) ∂ t = ∇ ⋅ ( D ∇ φ ( x , t ) ) = ∑ i = 1 3 ∑ j = 1 3 D i j ∂ 2 φ ( x , t ) ∂ x i ∂ x j . {displaystyle {frac {partial varphi (x,t)}{partial t}}=nabla cdot {bigl (}Dnabla varphi (x,t){bigr)}=sum _{i=1}^{3}sum _{j=1}^{3}D_{ij}{frac {partial ^{2}varphi (x,t)}{partial x_{i}partial x_{j}}}.}
- For inhomogeneous anisotropic media these two forms of the diffusion equation should be combined in ∂ φ ( x , t ) ∂ t = ∇ ⋅ ( D ( x ) ∇ φ ( x , t ) ) = ∑ i , j = 1 3 ( D i j ( x ) ∂ 2 φ ( x , t ) ∂ x i ∂ x j + ∂ D i j ( x ) ∂ x i ∂ φ ( x , t ) ∂ x i ) . {displaystyle {frac {partial varphi (x,t)}{partial t}}=nabla cdot {bigl (}D(x)nabla varphi (x,t){bigr)}=sum _{i,j=1}^{3}left(D_{ij}(x){frac {partial ^{2}varphi (x,t)}{partial x_{i}partial x_{j}}}+{frac {partial D_{ij}(x)}{partial x_{i}}}{frac {partial varphi (x,t)}{partial x_{i}}}right).}
- The approach based on Einstein's mobility and Teorell formula gives the following generalization of Fick's equation for the multicomponent diffusion of the perfect components: where φi are concentrations of the components and Dij is the matrix of coefficients. Here, indices i and j are related to the various components and not to the space coordinates.∂ φ i ∂ t = ∑ j ∇ ⋅ ( D i j φ i φ j ∇ φ j ) . {displaystyle {frac {partial varphi _{i}}{partial t}}=sum _{j}nabla cdot left(D_{ij}{frac {varphi _{i}}{varphi _{j}}}nabla ,varphi _{j}right).}
As fórmulas de Chapman-Enskog para difusão em gases incluem exatamente os mesmos termos. Esses modelos físicos de difusão são diferentes dos modelos de teste ∂tφi = Σj Dij Δφj que são válidos para desvios muito pequenos do equilíbrio uniforme. Anteriormente, tais termos foram introduzidos na equação de difusão de Maxwell-Stefan.
Para coeficientes de difusão multicomponentes anisotrópicos, é necessário um tensor de posto quatro, por exemplo Dij,αβ , onde i, j referem-se aos componentes e α, β = 1, 2, 3 correspondem às coordenadas do espaço.
Aplicativos
Equações baseadas na lei de Fick têm sido comumente usadas para modelar processos de transporte em alimentos, neurônios, biopolímeros, produtos farmacêuticos, solos porosos, dinâmica populacional, materiais nucleares, física de plasma e processos de dopagem de semicondutores. A teoria dos métodos voltamétricos é baseada em soluções da equação de Fick. Por outro lado, em alguns casos, uma "Fickiana (outra aproximação comum da equação de transporte é a da teoria da difusão)" descrição é inadequada. Por exemplo, na ciência dos polímeros e na ciência dos alimentos, é necessária uma abordagem mais geral para descrever o transporte de componentes em materiais submetidos a uma transição vítrea. Mais uma estrutura geral são as equações de difusão de Maxwell-Stefan de transferência de massa multicomponente, a partir da qual a lei de Fick pode ser obtida como caso limite, quando a mistura é extremamente diluída e todas as espécies químicas estão interagindo apenas com o volume da mistura e não com outras espécies. Para explicar a presença de várias espécies em uma mistura não diluída, várias variações das equações de Maxwell-Stefan são usadas. Consulte também processos de transporte acoplados não diagonais (relação Onsager).
Escoamento de Fick em líquidos
Quando dois líquidos miscíveis são colocados em contato e ocorre a difusão, a concentração macroscópica (ou média) evolui seguindo a lei de Fick. Em uma escala mesoscópica, ou seja, entre a escala macroscópica descrita pela lei de Fick e a escala molecular, onde ocorrem os passeios aleatórios moleculares, as flutuações não podem ser negligenciadas. Tais situações podem ser modeladas com sucesso com a hidrodinâmica flutuante de Landau-Lifshitz. Nesse referencial teórico, a difusão se dá por flutuações cujas dimensões vão desde a escala molecular até a escala macroscópica.
Em particular, as equações hidrodinâmicas flutuantes incluem um termo de fluxo de Fick, com um determinado coeficiente de difusão, juntamente com equações hidrodinâmicas e termos estocásticos que descrevem as flutuações. Ao calcular as flutuações com uma abordagem perturbativa, a aproximação de ordem zero é a lei de Fick. A primeira ordem dá as flutuações, e resulta que as flutuações contribuem para a difusão. Isso representa de certa forma uma tautologia, pois o fenômeno descrito por uma aproximação de ordem inferior é resultado de uma aproximação de ordem superior: esse problema é resolvido apenas renormalizando as equações hidrodinâmicas flutuantes.
Taxa de absorção e frequência de colisão de soluto diluído
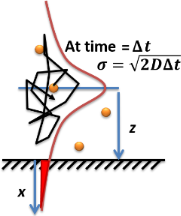
A taxa de adsorção ou absorção de um soluto diluído a uma superfície ou interface em uma solução (gás ou líquido) pode ser calculada usando as leis de difusão de Fick. O número acumulado de moléculas adsorvidas na superfície é expresso pela equação de Langmuir-Schaefer no limite de tempo curto, integrando a equação do fluxo de difusão ao longo do tempo:
- )) = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =2ACD)D D Não. Gamma = 2AC{sqrt Não. Sim.
- )) Não. "Gamma" é o número de moléculas na unidade # moléculas adsorvidas durante o tempo )Não..
- A é a área de superfície na unidade m2{displaystyle m^{2}}.
- C é a concentração de número das moléculas de adsorber na solução a granel em unidade # moléculas/m3{displaystyle m^{3}}.
- D é coeficiente de difusão do adsorber na unidade m2/SNão. m^{2}.
- ) é tempo decorrido na unidade SNão..
A equação recebeu o nome dos químicos americanos Irving Langmuir e Vincent Schaefer.
A equação de Langmuir-Schaefer pode ser estendida para a equação de Ward-Tordai para explicar a "retrodifusão" de moléculas rejeitadas da superfície:
- )) = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =2ACD)D D - Sim. - Sim. ADD D ∫ ∫ 0)Cb)(? ? ))- Sim. - Sim. ? ? D? ? Não. Gamma = 2AC{sqrt Não. }}}-A{sqrt {D}{pi }}}int _{0}^{sqrt {t}}{frac {C_{b}(tau)}{sqrt {t-tau) }}},dtau }
Onde? CNão. C. é a concentração de volume, Cb)Não. C_{b}} é a concentração subsuperfície (que é uma função de tempo dependendo do modelo de reação da adsorção), e ? ? - Sim. é uma variável fictícia.
As simulações de Monte Carlo mostram que essas duas equações funcionam para prever a taxa de adsorção de sistemas que formam gradientes de concentração previsíveis perto da superfície, mas apresentam problemas para sistemas sem ou com gradientes de concentração imprevisíveis, como sistemas de biossensores típicos ou quando fluxo e convecção são significativo.
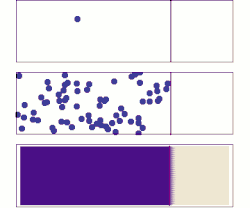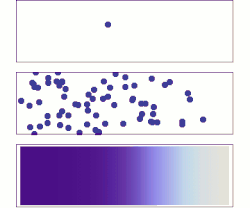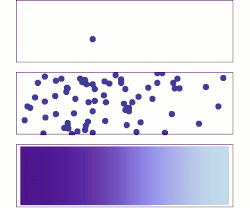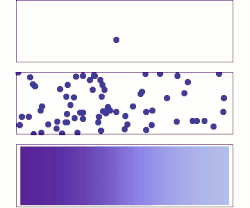
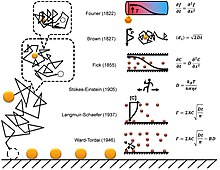
Uma breve história da adsorção difusa é mostrada na figura à direita. Um desafio notável de entender a adsorção difusiva no nível de molécula única é a natureza fractal da difusão. A maioria das simulações de computador escolhe uma etapa de tempo para difusão que ignora o fato de que existem eventos de difusão mais finos auto-semelhantes (fractal) dentro de cada etapa. A simulação da difusão fractal mostra que um fator de duas correções deve ser introduzido para o resultado de uma simulação de adsorção de passo de tempo fixo, tornando-o consistente com as duas equações acima.
No limite de tempo ultracurto, na ordem do tempo de difusão a2/D, onde a é o raio da partícula, a difusão é descrita pela equação de Langevin. Em um tempo mais longo, a equação de Langevin se funde com a equação de Stokes-Einstein. Este último é apropriado para a condição da solução diluída, onde a difusão de longo alcance é considerada. De acordo com o teorema da flutuação-dissipação baseado na equação de Langevin no limite de longo prazo e quando a partícula é significativamente mais densa que o fluido circundante, a constante de difusão dependente do tempo é:
- D())= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =μ μ kBT(1- Sim. - Sim. e- Sim. - Sim. )/(mμ μ )){displaystyle D(t)=mu ,k_{rm {B}}Tleft(1-e^{-t/(mmu)}right)}
onde (tudo em unidades SI)
- kB é a constante de Boltzmann.
- T é a temperatura absoluta.
- μ é a mobilidade da partícula no fluido ou gás, que pode ser calculada usando a relação de Einstein (teoria cinética).
- m é a massa da partícula.
- ) é tempo.
Para uma única molécula, como moléculas orgânicas ou biomoléculas (por exemplo, proteínas) em água, o termo exponencial é insignificante devido ao pequeno produto de mμ na região de picossegundos.
Quando a área de interesse é do tamanho de uma molécula (especificamente, uma molécula cilíndrica longa como o DNA), a equação da taxa de adsorção representa a frequência de colisão de duas moléculas em uma solução diluída, com uma molécula em um lado específico e a outra sem dependência estérica, ou seja, uma molécula (orientação aleatória) atinge um lado da outra. A constante de difusão precisa ser atualizada para a constante de difusão relativa entre duas moléculas em difusão. Essa estimativa é especialmente útil no estudo da interação entre uma molécula pequena e uma molécula maior, como uma proteína. A constante de difusão efetiva é dominada pela menor, cuja constante de difusão pode ser usada em seu lugar.
A equação da taxa de acerto acima também é útil para prever a cinética da automontagem molecular em uma superfície. As moléculas são orientadas aleatoriamente na solução a granel. Assumindo que 1/6 das moléculas tem a orientação correta para os locais de ligação da superfície, ou seja, 1/2 da direção z em x, y, z três dimensões, portanto, a concentração de interesse é apenas 1/6 da concentração total. Colocando esse valor na equação, será possível calcular a curva cinética de adsorção teórica usando o modelo de adsorção de Langmuir. Em uma imagem mais rígida, 1/6 pode ser substituído pelo fator estérico da geometria de encadernação.
A frequência de colisão bimolecular relacionada a muitas reações, incluindo a coagulação/agregação de proteínas, é inicialmente descrita pela equação de coagulação de Smoluchowski proposta por Marian Smoluchowski em uma publicação seminal de 1916, derivada do movimento browniano e das leis de difusão de Fick. Sob uma condição de reação idealizada para A+B->Produto em uma solução diluída, Smoluchovski sugeriu que o fluxo molecular no limite de tempo infinito pode ser calculado a partir das leis de difusão de Fick, produzindo um gradiente de concentração fixo / estável da molécula alvo, por exemplo. B é a molécula alvo segurando fixa relativamente, e A é a molécula móvel que cria um gradiente de concentração perto da molécula alvo B devido à reação de coagulação entre A e B. Smoluchowski calculou a frequência de colisão entre A e B na solução com unidade #/s/m3{displaystyle m^{3}}:
- Z.AB= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =4D D RDRCACBNão. Z_{AB=4{pi }RD_{r}C_{A}C_{B}}
onde,
- RNão. R. é o raio da colisão.
- DRNão. D_{r}} é a constante relativa difusão entre A e B, unidade m2/SNão. m^{2}.
- CANão. C_{A}} e CBNão. C_{B}} são concentrações de número de A e B respectivamente, unidade # /m3{displaystyle m^{3}}.
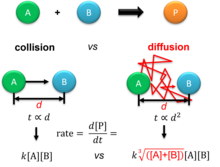
A ordem de reação desta reação bimolecular é 2, que é a analogia com o resultado da teoria da colisão, substituindo a velocidade de movimento da molécula pelo fluxo difusivo. Na teoria da colisão, o tempo de viagem entre A e B é proporcional à distância, que é uma relação semelhante para o caso de difusão se o fluxo for fixo.
No entanto, sob uma condição prática, o gradiente de concentração perto da molécula alvo está evoluindo ao longo do tempo com o fluxo molecular também evoluindo e, em média, o fluxo é muito maior do que o limite de tempo infinito do fluxo proposto por Smoluchowski. Assim, esta frequência de Smoluchowski representa o limite inferior da frequência de colisão real.
Em 2022, Chen calcula o limite superior da frequência de colisão entre A e B em uma solução assumindo que a concentração em massa da molécula em movimento é fixada após o primeiro vizinho mais próximo da molécula alvo. Assim, a evolução do gradiente de concentração pára na primeira camada vizinha mais próxima dado um tempo de parada para calcular o fluxo real. Ele nomeou este o momento crítico e deriva a frequência de colisão difusiva na unidade #/s/m3{displaystyle m^{3}}:
- Z.AB= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =8D D σ σ DRCACBCA+CB3Não. Z_{AB}={frac {8}{pi - Sim. }D_{r}C_{A}C_{B}{sqrt [{3}]{C_{A}+C_{B}}}}}}
onde,
- σ σ - Sim. é a área da seção transversal da colisão, unidade m2{displaystyle m^{2}}.
- DRNão. D_{r}} é a constante relativa difusão entre A e B, unidade m2/SNão. m^{2}.
- CANão. C_{A}} e CBNão. C_{B}} são concentrações de número de A e B respectivamente, unidade # /m3{displaystyle m^{3}}.
Esta equação assume o limite superior de uma frequência de colisão difusiva entre A e B é quando a primeira camada vizinha começa a sentir a evolução do gradiente de concentração, cuja ordem de reação é 213{displaystyle 2{frac Não. em vez de 2. Tanto a equação Smoluchowski quanto a equação JChen satisfazem verificações dimensionais com unidades SI. Mas o primeiro é dependente do raio e o último está na área da esfera de colisão. A ordem de reação real para uma reação da unidade bimolecular pode ser entre 2 e 213{displaystyle 2{frac Não., o que faz sentido porque o tempo de colisão difusivo é quadradamente dependente da distância entre as duas moléculas.
Perspectiva biológica
A primeira lei dá origem à seguinte fórmula:
- Fluxox= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. P(c2- Sim. - Sim. c1){displaystyle {text{flux}}={-Pleft (c_{2}-c_{1}right)}}
em que
- P é a permeabilidade, uma membrana experimentalmente determinada "condutância" para um determinado gás a uma determinada temperatura.
- c2 - Sim. c1 é a diferença na concentração do gás através da membrana para a direção do fluxo (de c1 para c2).
A primeira lei de Fick também é importante nas equações de transferência de radiação. No entanto, neste contexto, torna-se impreciso quando a constante de difusão é baixa e a radiação torna-se limitada pela velocidade da luz e não pela resistência do material através do qual a radiação está fluindo. Nesta situação, pode-se usar um limitador de fluxo.
A taxa de troca de um gás através de uma membrana fluida pode ser determinada usando esta lei em conjunto com a lei de Graham.
Sob a condição de uma solução diluída quando a difusão assume o controle, a permeabilidade da membrana mencionada na seção acima pode ser calculada teoricamente para o soluto usando a equação mencionada na última seção (use com cuidado especial porque a equação é derivada para densidade solutos, enquanto as moléculas biológicas não são mais densas que a água):
- P= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =2Ap? ? )mD/(D D ))Não. P=2A_{p}eta _{tm}{sqrt {D/(pi t)}}}
onde
- APNão. A_{P}} é a área total dos poros na membrana (unidade m2).
- ? ? )m{displaystyle eta _{tm}} eficiência transmembrana (unitless), que pode ser calculado a partir da teoria estocástica da cromatografia.
- D é a constante de difusão da unidade soluta m2S- Sim..
- ) é unidade de tempo s.
- c2, c1 concentração deve usar unidade mol m-3, então unidade de fluxo torna-se mol s- Sim..
O fluxo é decaído ao longo da raiz quadrada do tempo porque um gradiente de concentração se acumula perto da membrana ao longo do tempo sob condições ideais. Quando há fluxo e convecção, o fluxo pode ser significativamente diferente do que a equação prevê e mostrar um tempo efetivo t com um valor fixo, o que torna o fluxo estável em vez de decair com o tempo. Essa estratégia é adotada em biologia, como a circulação sanguínea.
Aplicações de fabricação de semicondutores
O semicondutor é um termo coletivo para uma série de dispositivos. Inclui principalmente três categorias: dispositivos de dois terminais, dispositivos de três terminais e dispositivos de quatro terminais. A combinação dos semicondutores é chamada de circuito integrado.
A relação entre a lei de Fick e os semicondutores: o princípio do semicondutor é transferir produtos químicos ou dopantes de uma camada para outra. A lei de Fick pode ser usada para controlar e prever a difusão, sabendo quanto a concentração dos dopantes ou produtos químicos se move por metro e segundo por meio da matemática.
Portanto, diferentes tipos e níveis de semicondutores podem ser fabricados.
Tecnologias de fabricação de circuitos integrados, processos modelo como CVD, oxidação térmica, oxidação úmida, dopagem, etc. usam equações de difusão obtidas da lei de Fick.
Método CVD para fabricar semicondutores
O wafer é um tipo de semicondutor cujo substrato de silício é revestido com uma camada de cadeia polimérica e filmes criados por CVD. Este filme contém dopantes tipo n e tipo p e assume a responsabilidade pela condução dos dopantes. O princípio do CVD depende da fase gasosa e da reação química gás-sólido para criar filmes finos.
O regime de fluxo viscoso de CVD é conduzido por um gradiente de pressão. CVD também inclui um componente de difusão distinto da difusão de superfície de adatoms. Na CVD, os reagentes e produtos também devem se difundir através de uma camada limite de gás estagnado que existe próximo ao substrato. O número total de etapas necessárias para o crescimento do filme CVD são difusão em fase gasosa de reagentes através da camada limite, adsorção e difusão superficial de átomos, reações no substrato e difusão em fase gasosa de produtos através da camada limite.
O perfil de velocidade para o fluxo de gás é:
- δ δ - Sim. é a espessura
- Re{displaystyle mathrm {Re} } } é o número de Reynolds
- x é o comprimento do subtrato.
- v = 0 em qualquer superfície
- ? ? - Sim. é viscosidade
- ? ? - Sim. é densidade.
Integrado o x de 0 para L, dá a espessura média:
Para manter a reação equilibrada, os reagentes devem se difundir através da camada limite estagnada para alcançar o substrato. Portanto, uma camada limite fina é desejável. De acordo com as equações, aumentar vo resultaria em mais reagentes desperdiçados. Os reagentes não alcançarão o substrato uniformemente se o fluxo se tornar turbulento. Outra opção é mudar para um novo gás de arraste com menor viscosidade ou densidade.
A primeira lei de Fick descreve a difusão através da camada limite. Em função da pressão (P) e da temperatura (T) em um gás, a difusão é determinada.
- P0Não. P_{0}} é a pressão padrão.
- T0Não. T_{0}} é a temperatura padrão.
- D0Não. D_{0}} é a difusibilidade padrão.
A equação diz que aumentar a temperatura ou diminuir a pressão pode aumentar a difusividade.
A primeira lei de Fick prevê o fluxo dos reagentes para o substrato e o produto longe do substrato:
- xNão. é a espessura δ δ - Sim.
- DcEu...Não. Dc_{i}} é a primeira concentração do reagente.
Em direito de gás ideal PV= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =nRTNão. PV=nRT, a concentração do gás é expressa por pressão parcial.
- RNão. R. é a constante do gás.
- PEu...- Sim. - Sim. P0δ δ {displaystyle {frac {P_{i}-P_{0}}{delta) é o gradiente de pressão parcial.
Como resultado, a primeira lei de Fick nos diz que podemos usar um gradiente de pressão parcial para controlar a difusividade e controlar o crescimento de filmes finos de semicondutores.
Em muitas situações realistas, a simples lei de Fick não é uma formulação adequada para o problema de semicondutores. Aplica-se apenas a certas condições, por exemplo, dadas as condições de limite do semicondutor: difusão de concentração de fonte constante, concentração de fonte limitada ou difusão de limite móvel (onde a profundidade da junção continua se movendo no substrato).
Produção de alimentos e culinária
A formulação da primeira lei de Fick pode explicar uma variedade de fenômenos complexos no contexto da alimentação e da culinária: a difusão de moléculas como o etileno promove o crescimento e o amadurecimento das plantas, as moléculas de sal e açúcar promovem a salga e a marinada da carne, e as moléculas de água promovem a desidratação. A primeira lei de Fick também pode ser usada para prever as mudanças nos perfis de umidade em um macarrão espaguete à medida que ele se hidrata durante o cozimento. Esses fenômenos são todos sobre o movimento espontâneo de partículas de solutos impulsionados pelo gradiente de concentração. Em diferentes situações, há diferente difusividade que é uma constante.
Ao controlar o gradiente de concentração, o tempo de cozimento, a forma dos alimentos e a salga podem ser controlados.
Contenido relacionado
Transformação de Lorentz
Calorimetria
Radiômetro Crookes































![{displaystyle n(x,t)=n_{0}left[1-2left({frac {x}{2{sqrt {Dtpi }}}}right)right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2cb41fde1bd0ade9d556ce64b8e96299081ce07b)



























![{displaystyle Z_{AB}={frac {8}{pi }}{sigma }D_{r}C_{A}C_{B}{sqrt[{3}]{C_{A}+C_{B}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b044fd26a0d82336e908b78db1d64acb8b558fab)




















