HIV
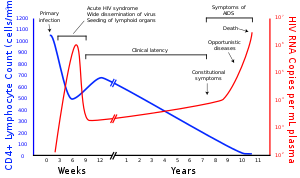
Os vírus da imunodeficiência humana (HIV) são duas espécies de Lentivírus (um subgrupo de retrovírus) que infectam humanos. Com o tempo, eles causam a síndrome da imunodeficiência adquirida (AIDS), uma condição na qual a falha progressiva do sistema imunológico permite que infecções oportunistas e cânceres com risco de vida se desenvolvam. Sem tratamento, estima-se que o tempo médio de sobrevida após a infecção pelo HIV seja de 9 a 11 anos, dependendo do subtipo do HIV.
Na maioria dos casos, o HIV é uma infecção sexualmente transmissível e ocorre por contato ou transferência de sangue, pré-ejaculação, sêmen e fluidos vaginais. A transmissão não sexual pode ocorrer de uma mãe infectada para seu filho durante a gravidez, durante o parto por exposição ao sangue ou fluido vaginal e através do leite materno. Dentro desses fluidos corporais, o HIV está presente tanto como partículas virais livres quanto como vírus dentro das células imunes infectadas. A pesquisa mostrou (tanto para casais do mesmo sexo quanto para casais do sexo oposto) que o HIV é intransmissível através de relações sexuais sem preservativo se o parceiro HIV positivo tiver uma carga viral consistentemente indetectável.
O HIV infecta células vitais no sistema imunológico humano, como células T auxiliares (especificamente células T CD4+), macrófagos e células dendríticas. A infecção pelo HIV leva a baixos níveis de células T CD4+ por meio de vários mecanismos, incluindo piroptose de células T infectadas abortivamente, apoptose de células não infectadas, morte viral direta de células infectadas e morte de CD4 infectado Células T + por linfócitos citotóxicos CD8+ que reconhecem células infectadas. Quando o número de células T CD4+ diminui abaixo de um nível crítico, a imunidade mediada por células é perdida e o corpo se torna progressivamente mais suscetível a infecções oportunistas, levando ao desenvolvimento da AIDS.
Virologia
Classificação
| Espécies | Virulência | Infecção | Prevalência | Origem diferida |
|---|---|---|---|---|
| HIV-1 | Alto. | Alto. | Global | Chimpanzé comum |
| HIV-2 | Mais baixo | Baixa | África do Sul | Mangás de soja |
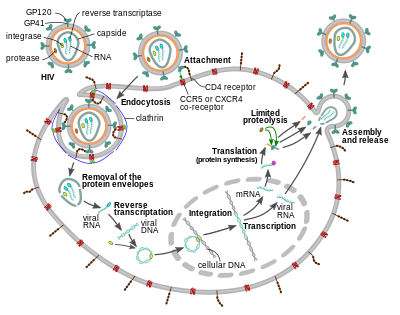
O HIV é um membro do gênero Lentivirus, pertencente à família Retroviridae. Os lentivírus têm muitas morfologias e propriedades biológicas em comum. Muitas espécies são infectadas por lentivírus, que são caracteristicamente responsáveis por doenças de longa duração com longo período de incubação. Os lentivírus são transmitidos como vírus de RNA envelopados de sentido positivo e fita simples. Ao entrar na célula-alvo, o genoma do RNA viral é convertido (transcrito reversamente) em DNA de fita dupla por uma enzima codificada pelo vírus, a transcriptase reversa, que é transportada junto com o genoma viral na partícula do vírus. O DNA viral resultante é então importado para o núcleo da célula e integrado ao DNA celular por uma enzima codificada pelo vírus, integrase e cofatores do hospedeiro. Uma vez integrado, o vírus pode ficar latente, permitindo que o vírus e sua célula hospedeira evitem a detecção pelo sistema imunológico, por tempo indeterminado. O vírus HIV pode permanecer inativo no corpo humano por até dez anos após a infecção primária; durante este período o vírus não causa sintomas. Alternativamente, o DNA viral integrado pode ser transcrito, produzindo novos genomas de RNA e proteínas virais, usando recursos da célula hospedeira, que são empacotados e liberados da célula como novas partículas virais que iniciarão novamente o ciclo de replicação.
Foram caracterizados dois tipos de HIV: HIV-1 e HIV-2. O HIV-1 é o vírus que foi inicialmente descoberto e denominado vírus associado à linfadenopatia (LAV) e vírus linfotrópico T humano 3 (HTLV-III). O HIV-1 é mais virulento e mais infeccioso do que o HIV-2 e é a causa da maioria das infecções por HIV em todo o mundo. A menor infecciosidade do HIV-2, em comparação com o HIV-1, implica que menos pessoas expostas ao HIV-2 serão infectadas por exposição. Devido à sua capacidade de transmissão relativamente fraca, o HIV-2 está amplamente confinado à África Ocidental.
Estrutura e genoma
O HIV é semelhante em estrutura a outros retrovírus. É aproximadamente esférico com um diâmetro de cerca de 120 nm, cerca de 100.000 vezes menor em volume do que um glóbulo vermelho. Ele é composto por duas cópias de RNA de fita simples de sentido positivo que codifica os nove genes do vírus envoltos por um capsídeo cônico composto por 2.000 cópias da proteína viral p24. O RNA de fita simples está fortemente ligado às proteínas do nucleocapsídeo, p7, e às enzimas necessárias para o desenvolvimento do virion, como transcriptase reversa, proteases, ribonuclease e integrase. Uma matriz composta pela proteína viral p17 envolve o capsídeo garantindo a integridade da partícula do virion.
Este é, por sua vez, circundado pelo envelope viral, que é composto pela bicamada lipídica retirada da membrana de uma célula hospedeira humana quando a partícula viral recém-formada brota da célula. O envelope viral contém proteínas da célula hospedeira e relativamente poucas cópias da proteína do envelope do HIV, que consiste em uma tampa feita de três moléculas conhecidas como glicoproteína (gp) 120, e uma haste composta por três moléculas gp41 que ancoram a estrutura no envelope viral. A proteína do envelope, codificada pelo gene env do HIV, permite que o vírus se prenda às células-alvo e funda o envelope viral com a membrana da célula-alvo, liberando o conteúdo viral na célula e iniciando o ciclo infeccioso.
Como a única proteína viral na superfície do vírus, a proteína do envelope é um alvo importante para os esforços da vacina contra o HIV. Mais da metade da massa do pico do envelope trimérico são glicanos ligados a N. A densidade é alta, pois os glicanos protegem a proteína viral subjacente da neutralização por anticorpos. Esta é uma das moléculas mais densamente glicosiladas conhecidas e a densidade é suficientemente alta para impedir o processo normal de maturação dos glicanos durante a biogênese no aparelho endoplasmático e de Golgi. A maioria dos glicanos são, portanto, estagnados como imaturos 'alto teor de manose' glicanos normalmente não presentes em glicoproteínas humanas que são secretadas ou presentes em uma superfície celular. O processamento incomum e a alta densidade significam que quase todos os anticorpos amplamente neutralizantes que foram identificados até agora (de um subconjunto de pacientes que foram infectados por muitos meses a anos) se ligam ou são adaptados para lidar com esses glicanos do envelope.
A estrutura molecular do pico viral foi agora determinada por cristalografia de raios-X e microscopia eletrônica criogênica. Esses avanços na biologia estrutural foram possíveis devido ao desenvolvimento de formas recombinantes estáveis do pico viral pela introdução de uma ligação dissulfeto intersubunidade e uma mutação de isoleucina para prolina (substituição radical de um aminoácido) na gp41. Os chamados trímeros SOSIP não apenas reproduzem as propriedades antigênicas do pico viral nativo, mas também exibem o mesmo grau de glicanos imaturos apresentados no vírus nativo. Os picos virais triméricos recombinantes são candidatos promissores a vacinas, pois exibem menos epítopos não neutralizantes do que a gp120 monomérica recombinante, que atua para suprimir a resposta imune aos epítopos alvo.
O genoma de RNA consiste em pelo menos sete marcos estruturais (LTR, TAR, RRE, PE, SLIP, CRS e INS) e nove genes (gag, pol, e env, tat, rev, nef, vif, vpr, vpu, e às vezes um décimo tev, que é uma fusão de tat, env e rev), codificando 19 proteínas. Três desses genes, gag, pol e env, contêm as informações necessárias para produzir as proteínas estruturais das novas partículas virais. Por exemplo, env codifica uma proteína chamada gp160 que é cortada em duas por uma protease celular para formar gp120 e gp41. Os seis genes restantes, tat, rev, nef, vif, vpr, e vpu (ou vpx no caso do HIV-2), são genes reguladores de proteínas que controlam a capacidade do HIV de infectar células, produzir novas cópias do vírus (replicar) ou causar doenças.
As duas proteínas tat (p16 e p14) são transativadores transcricionais para o promotor LTR que atua ligando o elemento TAR RNA. O TAR também pode ser processado em microRNAs que regulam os genes de apoptose ERCC1 e IER3. A proteína rev (p19) está envolvida no transporte de RNAs do núcleo e do citoplasma por ligação ao elemento RRE RNA. A proteína vif (p23) impede a ação da APOBEC3G (proteína celular que desamina a citidina em uridina no DNA viral de fita simples e/ou interfere na transcrição reversa). A proteína vpr (p14) interrompe a divisão celular em G2/M. A proteína nef (p27) regula negativamente o CD4 (o principal receptor viral), assim como as moléculas do MHC classe I e classe II.
Nef também interage com domínios SH3. A proteína vpu (p16) influencia a liberação de novas partículas virais das células infectadas. As extremidades de cada fita de RNA do HIV contêm uma sequência de RNA chamada de repetição terminal longa (LTR). As regiões do LTR atuam como interruptores para controlar a produção de novos vírus e podem ser acionadas por proteínas do HIV ou da célula hospedeira. O elemento Psi está envolvido no empacotamento do genoma viral e reconhecido pelas proteínas gag e rev. O elemento SLIP (TTTTTT) está envolvido no frameshift no gag-pol é necessário para tornar pol funcional.
Tropismo
O termo tropismo viral refere-se aos tipos de células que um vírus infecta. O HIV pode infectar uma variedade de células imunes, como células T CD4+, macrófagos e células microgliais. A entrada do HIV-1 nos macrófagos e nas células T CD4+ é mediada pela interação das glicoproteínas do envelope do vírion (gp120) com a molécula CD4 nas células-alvo' membrana e também com co-receptores de quimiocinas.
Estirpes macrófagos-trópicas (M-trópicas) de HIV-1, ou cepas não indutoras de sincícios (NSI; agora chamadas de vírus R5) usam o receptor de β-quimiocina, CCR5, para entrada e, portanto, são capazes de se replicar tanto em macrófagos quanto em células T CD4+. Este co-receptor CCR5 é usado por quase todos os isolados primários de HIV-1, independentemente do subtipo genético viral. De fato, os macrófagos desempenham um papel fundamental em vários aspectos críticos da infecção pelo HIV. Eles parecem ser as primeiras células infectadas pelo HIV e talvez a fonte de produção do HIV quando as células CD4+ se esgotam no paciente. Macrófagos e células microgliais são as células infectadas pelo HIV no sistema nervoso central. Nas amígdalas e adenóides de pacientes infectados pelo HIV, os macrófagos se fundem em células gigantes multinucleadas que produzem grandes quantidades de vírus.
Estirpes T-trópicas de HIV-1, ou estirpes indutoras de sincícios (SI; agora denominadas vírus X4) replicam-se em células T CD4+ primárias, bem como em macrófagos e usam o receptor de α-quimiocina, CXCR4, para entrada.
Acredita-se que cepas de HIV-1 dual-trópicas sejam cepas de transição de HIV-1 e, portanto, são capazes de usar CCR5 e CXCR4 como co-receptores para entrada viral.
A α-quimiocina SDF-1, um ligante para CXCR4, suprime a replicação de isolados T-trópicos de HIV-1. Ele faz isso regulando negativamente a expressão de CXCR4 na superfície das células-alvo do HIV. Os isolados de HIV-1 M-trópico que usam apenas o receptor CCR5 são denominados R5; aqueles que usam apenas CXCR4 são denominados X4 e aqueles que usam ambos, X4R5. No entanto, o uso de co-receptores isoladamente não explica o tropismo viral, pois nem todos os vírus R5 são capazes de utilizar CCR5 em macrófagos para uma infecção produtiva e o HIV também pode infectar um subtipo de células dendríticas mielóides, que provavelmente constituem um reservatório que mantém infecção quando os números de células T CD4+ diminuíram para níveis extremamente baixos.
Algumas pessoas são resistentes a certas cepas de HIV. Por exemplo, pessoas com a mutação CCR5-Δ32 são resistentes à infecção pelo vírus R5, pois a mutação deixa o HIV incapaz de se ligar a esse co-receptor, reduzindo sua capacidade de infectar as células-alvo.
A relação sexual é a principal forma de transmissão do HIV. Tanto o HIV X4 quanto o R5 estão presentes no fluido seminal, o que permite que o vírus seja transmitido de um homem para sua parceira sexual. Os virions podem então infectar vários alvos celulares e se disseminar por todo o organismo. No entanto, um processo de seleção leva a uma transmissão predominante do vírus R5 por essa via. Em pacientes infectados com o subtipo B do HIV-1, muitas vezes há uma troca de co-receptores na doença em estágio avançado e variantes T-trópicas que podem infectar uma variedade de células T por meio do CXCR4. Essas variantes então se replicam de forma mais agressiva com virulência elevada que causa rápida depleção de células T, colapso do sistema imunológico e infecções oportunistas que marcam o advento da AIDS. Os pacientes HIV-positivos adquirem um amplo espectro de infecções oportunistas, o que era particularmente problemático antes do início das terapias HAART; no entanto, as mesmas infecções são relatadas entre pacientes infectados pelo HIV examinados post-mortem após o início das terapias antirretrovirais. Assim, durante o curso da infecção, a adaptação viral ao uso de CXCR4 em vez de CCR5 pode ser uma etapa fundamental na progressão para AIDS. Vários estudos com indivíduos infectados pelo subtipo B determinaram que entre 40 e 50 por cento dos pacientes com AIDS podem abrigar vírus do SI e, presume-se, os fenótipos X4.
O HIV-2 é muito menos patogênico que o HIV-1 e sua distribuição mundial é restrita à África Ocidental. A adoção de "genes acessórios" pelo HIV-2 e seu padrão mais promíscuo de uso de co-receptores (incluindo a independência de CD4) pode ajudar o vírus em sua adaptação para evitar fatores de restrição inatos presentes nas células hospedeiras. A adaptação para usar a maquinaria celular normal para permitir a transmissão e infecção produtiva também ajudou no estabelecimento da replicação do HIV-2 em humanos. Uma estratégia de sobrevivência para qualquer agente infeccioso não é matar seu hospedeiro, mas, em última análise, tornar-se um organismo comensal. Tendo alcançado uma baixa patogenicidade, ao longo do tempo, as variantes que são mais bem sucedidas na transmissão serão selecionadas.
Ciclo de replicação
Entrada na célula

O vírion do HIV entra nos macrófagos e nas células T CD4+ pela adsorção de glicoproteínas em sua superfície aos receptores na célula-alvo, seguida pela fusão do envelope viral com a membrana da célula-alvo e a liberação de o capsídeo do HIV na célula.
A entrada na célula começa pela interação do complexo do envelope trimérico (pico gp160) no envelope viral do HIV e CD4 e um co-receptor de quimiocina (geralmente CCR5 ou CXCR4, mas outros são conhecidos por interagir) no alvo Superfície celular. A Gp120 liga-se à integrina α4β7 ativando LFA-1, a integrina central envolvida no estabelecimento de sinapses virológicas, que facilitam a disseminação eficiente de célula a célula do HIV- 1. O pico gp160 contém domínios de ligação para receptores CD4 e quimiocinas.
O primeiro passo na fusão envolve a ligação de alta afinidade dos domínios de ligação CD4 de gp120 a CD4. Uma vez que a gp120 se liga à proteína CD4, o complexo do envelope sofre uma alteração estrutural, expondo os domínios de ligação do receptor de quimiocina da gp120 e permitindo que eles interajam com o receptor de quimiocina alvo. Isso permite uma ligação dupla mais estável, que permite que o peptídeo de fusão N-terminal gp41 penetre na membrana celular. Sequências repetidas em gp41, HR1 e HR2 então interagem, causando o colapso da porção extracelular de gp41 em forma de grampo de cabelo. Essa estrutura de loop aproxima o vírus e as membranas celulares, permitindo a fusão das membranas e a subsequente entrada do capsídeo viral.
Depois que o HIV se liga à célula-alvo, o RNA do HIV e várias enzimas, incluindo transcriptase reversa, integrase, ribonuclease e protease, são injetados na célula. Durante o transporte baseado em microtúbulos para o núcleo, o genoma viral de RNA de fita simples é transcrito em DNA de fita dupla, que é então integrado a um cromossomo hospedeiro.
O HIV pode infectar células dendríticas (DCs) por esta rota CD4-CCR5, mas também pode ser usada outra rota usando receptores de lectina tipo C específicos de manose, como DC-SIGN. As DCs são uma das primeiras células encontradas pelo vírus durante a transmissão sexual. Atualmente, acredita-se que eles desempenhem um papel importante na transmissão do HIV para as células T quando o vírus é capturado na mucosa por DCs. Acredita-se que a presença do FEZ-1, que ocorre naturalmente nos neurônios, impeça a infecção das células pelo HIV.
A entrada do HIV-1, bem como a entrada de muitos outros retrovírus, há muito se acredita ocorrer exclusivamente na membrana plasmática. Mais recentemente, no entanto, a infecção produtiva por endocitose do HIV-1 independente do pH e mediada por clatrina também foi relatada e foi recentemente sugerida como constituindo a única via de entrada produtiva.
Replicação e transcrição
Logo após o capsídeo viral entrar na célula, uma enzima chamada transcriptase reversa libera o genoma de RNA de fita simples de sentido positivo das proteínas virais anexadas e o copia em uma molécula de DNA complementar (cDNA). O processo de transcrição reversa é extremamente sujeito a erros, e as mutações resultantes podem causar resistência a medicamentos ou permitir que o vírus escape do sistema imunológico do corpo. A transcriptase reversa também possui atividade de ribonuclease que degrada o RNA viral durante a síntese de cDNA, bem como atividade de polimerase de DNA dependente de DNA que cria um DNA sentido a partir do cDNA antisense. Juntos, o cDNA e seu complemento formam um DNA viral de fita dupla que é então transportado para o núcleo da célula. A integração do DNA viral no genoma da célula hospedeira é realizada por outra enzima viral chamada integrase.
O DNA viral integrado pode então permanecer dormente, no estágio latente da infecção pelo HIV. Para produzir ativamente o vírus, certos fatores de transcrição celular precisam estar presentes, o mais importante deles é o NF-κB (fator nuclear kappa B), que é regulado positivamente quando as células T são ativadas. Isso significa que as células com maior probabilidade de serem atacadas, penetradas e posteriormente mortas pelo HIV são aquelas que lutam ativamente contra a infecção.
Durante a replicação viral, o pró-vírus de DNA integrado é transcrito em RNA. Os RNAs genômicos completos (gRNA) podem ser empacotados em novas partículas virais em uma forma pseudodiploide. A seletividade no empacotamento é explicada pelas propriedades estruturais do confôrmero dimérico do gRNA. O dímero de gRNA é caracterizado por uma junção de três vias em tandem dentro do monômero de gRNA, na qual os hairpins SD e AUG, responsáveis pelo splicing e tradução, respectivamente, são sequestrados e o hairpin DIS (sinal de iniciação de dimerização) é exposto. A formação do dímero O dímero de gRNA é mediado por um 'beijo' interação entre os loops DIS hairpin dos monômeros de gRNA. Ao mesmo tempo, certos resíduos de guanosina no gRNA são disponibilizados para a ligação da proteína do nucleocapsídeo (NC) levando à subsequente montagem do virion. O dímero de gRNA lábil também foi relatado para alcançar uma conformação mais estável após a ligação NC, na qual ambas as regiões DIS e U5:AUG do gRNA participam de extenso pareamento de bases.
O RNA também pode ser processado para produzir RNAs mensageiros maduros (mRNAs). Na maioria dos casos, esse processamento envolve splicing de RNA para produzir mRNAs que são mais curtos do que o genoma completo. Qual parte do RNA é removida durante o splicing do RNA determina qual das sequências de codificação da proteína do HIV é traduzida.
MRNAs maduros do HIV são exportados do núcleo para o citoplasma, onde são traduzidos para produzir proteínas do HIV, incluindo Rev. cópias de RNAs do vírus e permite que eles saiam do núcleo. Alguns desses RNAs completos funcionam como mRNAs que são traduzidos para produzir as proteínas estruturais Gag e Env. As proteínas gag se ligam a cópias do genoma do RNA do vírus para empacotá-las em novas partículas virais. O HIV-1 e o HIV-2 parecem empacotar seu RNA de maneira diferente. O HIV-1 se ligará a qualquer RNA apropriado. O HIV-2 se ligará preferencialmente ao mRNA que foi usado para criar a própria proteína Gag.
Recombinação
Dois genomas de RNA são encapsidados em cada partícula do HIV-1 (consulte Estrutura e genoma do HIV). Após infecção e replicação catalisada pela transcriptase reversa, pode ocorrer recombinação entre os dois genomas. A recombinação ocorre quando os genomas de RNA de sentido positivo de fita simples são transcritos reversamente para formar o DNA. Durante a transcrição reversa, o DNA nascente pode alternar várias vezes entre as duas cópias do RNA viral. Essa forma de recombinação é conhecida como copy-choice. Eventos de recombinação podem ocorrer em todo o genoma. De dois a 20 eventos de recombinação por genoma podem ocorrer em cada ciclo de replicação, e esses eventos podem embaralhar rapidamente a informação genética que é transmitida dos genomas parentais para os descendentes.
A recombinação viral produz variação genética que provavelmente contribui para a evolução da resistência à terapia anti-retroviral. A recombinação também pode contribuir, em princípio, para superar as defesas imunológicas do hospedeiro. No entanto, para que as vantagens adaptativas da variação genética sejam realizadas, os dois genomas virais empacotados em partículas virais infectantes individuais precisam ter surgido de vírus parentais progenitores separados de constituição genética diferente. Não se sabe com que frequência essas embalagens mistas ocorrem em condições naturais.
Bonhoeffer et al. sugeriu que a troca de modelo pela transcriptase reversa atua como um processo de reparo para lidar com quebras no genoma de RNA de fita simples. Além disso, Hu e Temin sugeriram que a recombinação é uma adaptação para reparar danos nos genomas de RNA. A troca de fita (recombinação de escolha de cópia) pela transcriptase reversa pode gerar uma cópia não danificada do DNA genômico a partir de duas cópias danificadas do genoma do RNA de fita simples. Essa visão do benefício adaptativo da recombinação no HIV poderia explicar por que cada partícula do HIV contém dois genomas completos, em vez de um. Além disso, a visão de que a recombinação é um processo de reparo implica que o benefício do reparo pode ocorrer em cada ciclo de replicação, e que esse benefício pode ser obtido quer os dois genomas difiram ou não geneticamente. Na visão de que a recombinação no HIV é um processo de reparo, a geração de variação recombinacional seria uma consequência, mas não a causa, da evolução da troca de modelo.
A infecção pelo HIV-1 causa inflamação crônica e produção de espécies reativas de oxigênio. Assim, o genoma do HIV pode ser vulnerável a danos oxidativos, incluindo quebras no RNA de fita simples. Para o HIV, bem como para os vírus em geral, a infecção bem-sucedida depende da superação das estratégias de defesa do hospedeiro, que geralmente incluem a produção de espécies reativas de oxigênio que danificam o genoma. Assim, Michod et al. sugeriu que a recombinação por vírus é uma adaptação para reparar o dano do genoma e que a variação recombinatória é um subproduto que pode fornecer um benefício separado.
Montagem e liberação
A etapa final do ciclo viral, montagem de novos virions HIV-1, começa na membrana plasmática da célula hospedeira. A poliproteína Env (gp160) passa pelo retículo endoplasmático e é transportada para o aparelho de Golgi onde é clivada pela furina resultando nas duas glicoproteínas do envelope do HIV, gp41 e gp120. Estes são transportados para a membrana plasmática da célula hospedeira onde a gp41 ancora a gp120 à membrana da célula infectada. As poliproteínas Gag (p55) e Gag-Pol (p160) também se associam à superfície interna da membrana plasmática juntamente com o RNA genômico do HIV quando o vírion em formação começa a brotar da célula hospedeira. O vírion brotado ainda é imaturo, pois as poliproteínas gag ainda precisam ser clivadas na matriz real, capsídeo e proteínas do nucleocapsídeo. Essa clivagem é mediada pela protease viral empacotada e pode ser inibida por drogas antirretrovirais da classe dos inibidores de protease. Os vários componentes estruturais então se juntam para produzir um vírion HIV maduro. Somente virions maduros são então capazes de infectar outra célula.
Espalhe dentro do corpo
O processo clássico de infecção de uma célula por um vírion pode ser chamado de "disseminação livre de células" para distingui-lo de um processo reconhecido mais recentemente chamado "propagação célula a célula". Na disseminação livre de células (veja a figura), as partículas virais brotam de uma célula T infectada, entram no sangue ou fluido extracelular e depois infectam outra célula T após um encontro casual. O HIV também pode se disseminar por transmissão direta de uma célula para outra por um processo de disseminação célula a célula, para o qual foram descritas duas vias. Em primeiro lugar, uma célula T infectada pode transmitir o vírus diretamente para uma célula T alvo por meio de uma sinapse virológica. Em segundo lugar, uma célula apresentadora de antígeno (APC), como um macrófago ou célula dendrítica, pode transmitir o HIV para células T por um processo que envolve infecção produtiva (no caso de macrófagos) ou captura e transferência de virions em trans (no caso de células dendríticas). Qualquer que seja a via usada, a infecção por transferência de célula a célula é relatada como muito mais eficiente do que a propagação do vírus livre de células. Vários fatores contribuem para essa maior eficiência, incluindo o brotamento do vírus polarizado em direção ao local de contato célula a célula, aposição próxima de células, o que minimiza a difusão em fase fluida de vírions e o agrupamento de receptores de entrada do HIV na célula-alvo em direção à célula-alvo. a zona de contato. Acredita-se que a disseminação célula a célula seja particularmente importante nos tecidos linfóides, onde as células T CD4+ são densamente compactadas e provavelmente interagem com frequência. Os estudos de imagem intravital apoiaram o conceito da sinapse virológica do HIV in vivo. Os muitos mecanismos de disseminação disponíveis para o HIV contribuem para a replicação contínua do vírus, apesar das terapias anti-retrovirais.
Variabilidade genética
O HIV difere de muitos vírus porque tem uma variabilidade genética muito alta. Essa diversidade é resultado de seu rápido ciclo de replicação, com a geração de cerca de 1010 virions todos os dias, juntamente com uma alta taxa de mutação de aproximadamente 3 x 10−5 por base nucleotídica por ciclo de replicação e propriedades recombinogênicas da transcriptase reversa.
Esse cenário complexo leva à geração de muitas variantes do HIV em um único paciente infectado no decorrer de um dia. Essa variabilidade é agravada quando uma única célula é simultaneamente infectada por duas ou mais cepas diferentes de HIV. Quando ocorre infecção simultânea, o genoma dos vírions descendentes pode ser composto de cadeias de RNA de duas cepas diferentes. Este vírion híbrido então infecta uma nova célula onde sofre replicação. À medida que isso acontece, a transcriptase reversa, saltando para frente e para trás entre os dois modelos diferentes de RNA, gerará uma sequência de DNA retroviral recém-sintetizada que é um recombinante entre os dois genomas parentais. Essa recombinação é mais óbvia quando ocorre entre subtipos.
O intimamente relacionado vírus da imunodeficiência símia (SIV) evoluiu em muitas cepas, classificadas pelas espécies hospedeiras naturais. Acredita-se que as cepas de SIV do macaco verde africano (SIVagm) e do mangabey sooty (SIVsmm) tenham uma longa história evolutiva com seus hospedeiros. Esses hospedeiros se adaptaram à presença do vírus, que está presente em níveis elevados no sangue do hospedeiro, mas evoca apenas uma resposta imune leve, não causa o desenvolvimento da AIDS símia e não sofre a extensa mutação e recombinação típica da infecção pelo HIV em humanos.
Por outro lado, quando essas cepas infectam espécies que não se adaptaram ao SIV ('heterólogos' ou hospedeiros semelhantes, como os macacos rhesus ou cynomologus), os animais desenvolvem AIDS e o vírus gera uma diversidade genética semelhante à que é observada na infecção humana pelo HIV. O SIV do chimpanzé (SIVcpz), o parente genético mais próximo do HIV-1, está associado ao aumento da mortalidade e sintomas semelhantes aos da AIDS em seu hospedeiro natural. O SIVcpz parece ter sido transmitido há relativamente pouco tempo às populações de chimpanzés e humanos, de modo que seus hospedeiros ainda não se adaptaram ao vírus. Este vírus também perdeu uma função do gene nef que está presente na maioria dos SIVs. Para variantes SIV não patogênicas, nef suprime a ativação de células T através do marcador CD3. A função de Nef's em formas não patogênicas de SIV é diminuir a expressão de citocinas, MHC-1 e sinais que afetam o tráfego de células T. No HIV-1 e SIVcpz, o nef não inibe a ativação das células T e perdeu essa função. Sem essa função, a depleção de células T é mais provável, levando à imunodeficiência.
Três grupos de HIV-1 foram identificados com base nas diferenças na região do envelope (env): M, N e O. O grupo M é o mais prevalente e é subdividido em oito subtipos (ou clados), baseados em todo o genoma, que são geograficamente distintos. Os mais prevalentes são os subtipos B (encontrados principalmente na América do Norte e Europa), A e D (encontrados principalmente na África) e C (encontrados principalmente na África e na Ásia); esses subtipos formam ramificações na árvore filogenética representando a linhagem do grupo M do HIV-1. A co-infecção com subtipos distintos dá origem a formas recombinantes circulantes (CRFs). Em 2000, último ano em que foi feita uma análise da prevalência global do subtipo, 47,2% das infecções no mundo eram do subtipo C, 26,7% eram do subtipo A/CRF02_AG, 12,3% eram do subtipo B, 5,3% eram do subtipo D, 3,2% eram de CRF_AE, e os 5,3% restantes eram compostos por outros subtipos e CRFs. A maioria das pesquisas sobre HIV-1 concentra-se no subtipo B; poucos laboratórios se concentram nos outros subtipos. A existência de um quarto grupo, "P", foi hipotetizada com base em um vírus isolado em 2009. A cepa é aparentemente derivada do gorila SIV (SIVgor), isolado pela primeira vez de gorilas das planícies ocidentais em 2006.
O parente mais próximo do HIV-2 é o SIVsm, uma cepa do SIV encontrada em mangabees fuliginosos. Como o HIV-1 é derivado do SIVcpz e o HIV-2 do SIVsm, a sequência genética do HIV-2 é apenas parcialmente homóloga ao HIV-1 e mais parecida com a do SIVsm.
Diagnóstico
Muitas pessoas seropositivas não sabem que estão infectadas com o vírus. Por exemplo, em 2001, menos de 1% da população urbana sexualmente ativa na África havia sido testada, e essa proporção é ainda menor nas populações rurais. Além disso, em 2001, apenas 0,5% das mulheres grávidas atendidas nas unidades de saúde urbanas foram aconselhadas, testadas ou receberam os resultados dos testes. Mais uma vez, esta proporção é ainda menor nas unidades de saúde rurais. Como os doadores podem, portanto, não estar cientes de sua infecção, o sangue de doadores e os produtos sanguíneos usados na medicina e na pesquisa médica são rotineiramente testados para HIV.
O teste de HIV-1 é feito inicialmente usando um ensaio imunoenzimático (ELISA) para detectar anticorpos para HIV-1. Amostras com um resultado não reativo do ELISA inicial são consideradas HIV-negativas, a menos que tenha ocorrido nova exposição a um parceiro infectado ou parceiro com status de HIV desconhecido. As amostras com um resultado de ELISA reativo são testadas novamente em duplicata. Se o resultado de qualquer um dos testes duplicados for reativo, a amostra é relatada como repetidamente reativa e submetida a testes de confirmação com um teste suplementar mais específico (por exemplo, reação em cadeia da polimerase (PCR), western blot ou, menos comumente, um ensaio de imunofluorescência (IFA)). Apenas as amostras que são repetidamente reativas por ELISA e positivas por IFA ou PCR ou reativas por western blot são consideradas HIV-positivas e indicativas de infecção por HIV. Amostras que são repetidamente reativas ao ELISA ocasionalmente fornecem um resultado de western blot indeterminado, que pode ser uma resposta incompleta de anticorpos ao HIV em uma pessoa infectada ou reações inespecíficas em uma pessoa não infectada.
Mortes por HIV em 2014, excluindo os EUA.
Embora a IFA possa ser usada para confirmar a infecção nesses casos ambíguos, esse ensaio não é amplamente utilizado. Em geral, uma segunda amostra deve ser coletada mais de um mês depois e retestada para pessoas com resultados indeterminados de western blot. Embora muito menos comumente disponível, o teste de ácido nucleico (por exemplo, RNA viral ou método de amplificação de DNA proviral) também pode ajudar no diagnóstico em certas situações. Além disso, algumas amostras testadas podem fornecer resultados inconclusivos devido a uma quantidade baixa de amostras. Nessas situações, uma segunda amostra é coletada e testada para infecção pelo HIV.
Os testes de HIV modernos são extremamente precisos, quando o período de janela é levado em consideração. Um único teste de triagem está correto em mais de 99% das vezes. A chance de um resultado falso-positivo em um protocolo de teste padrão de duas etapas é estimada em cerca de 1 em 250.000 em uma população de baixo risco. O teste pós-exposição é recomendado imediatamente e depois em seis semanas, três meses e seis meses.
As recomendações mais recentes dos Centros de Controle e Prevenção de Doenças (CDC) dos EUA mostram que o teste de HIV deve começar com um teste combinado de imunoensaio para anticorpos HIV-1 e HIV-2 e antígeno p24. Um resultado negativo descarta a exposição ao HIV, enquanto um resultado positivo deve ser seguido por um imunoensaio de diferenciação de anticorpos HIV-1/2 para detectar quais anticorpos estão presentes. Isso dá origem a quatro cenários possíveis:
- 1. HIV-1 (+) & HIV-2 (−): anticorpos HIV-1 detectados
- 2. HIV-1 (−) & HIV-2 (+): Anticorpos HIV-2 detectados
- 3. HIV-1 (+) & HIV-2 (+): ambos anticorpos HIV-1 e HIV-2 detectados
- 4. HIV-1 (−) ou indeterminado & HIV-2 (−): O teste de ácido núcleo deve ser realizado para detectar a infecção aguda do HIV-1 ou sua ausência.
Pesquisa
A pesquisa sobre HIV/AIDS inclui todas as pesquisas médicas que tentam prevenir, tratar ou curar o HIV/AIDS, bem como pesquisas fundamentais sobre a natureza do HIV como agente infeccioso e sobre a AIDS como a doença causada pelo HIV.
Muitos governos e instituições de pesquisa participam de pesquisas sobre HIV/AIDS. Esta pesquisa inclui intervenções de saúde comportamental, como pesquisas sobre educação sexual e desenvolvimento de medicamentos, como pesquisas sobre microbicidas para doenças sexualmente transmissíveis, vacinas contra o HIV e medicamentos antirretrovirais. Outras áreas de pesquisa médica incluem os tópicos de profilaxia pré-exposição, profilaxia pós-exposição, circuncisão e efeitos do envelhecimento acelerado.
Tratamento e transmissão
O tratamento do HIV/AIDS normalmente inclui o uso de vários medicamentos antirretrovirais. Em muitas partes do mundo, o HIV tornou-se uma condição crônica na qual a progressão para AIDS é cada vez mais rara.
A latência do HIV e o conseqüente reservatório viral em células T CD4+, células dendríticas, bem como macrófagos, é a principal barreira para a erradicação do vírus.
Embora o HIV seja altamente virulento, a transmissão não ocorre através do sexo quando uma pessoa HIV-positiva tem uma carga viral consistentemente indetectável (<50 cópias/ml) devido ao tratamento anti-retroviral. Isso foi discutido pela primeira vez pela Comissão Federal Suíça para AIDS/HIV em 2008 na Declaração Suíça, embora a declaração fosse controversa na época. No entanto, após vários estudos, ficou claro que a chance de transmitir o HIV através do sexo é efetivamente zero quando a pessoa HIV positiva tem uma carga viral consistentemente indetectável; isso é conhecido como U=U, "Indetectável=Intransmissível", também expresso como "não pode transmiti-lo". Os estudos que demonstram U=U são: Os opostos se atraem, PARCEIRO 1, PARCEIRO 2, (para casais homem-homem) e HPTN052 (para casais heterossexuais) quando "o parceiro vivendo com HIV tinha uma carga viral suprimida de forma duradoura.' 34; Nesses estudos, casais em que um parceiro era HIV positivo e um parceiro era HIV negativo foram incluídos e os testes regulares de HIV foram concluídos. No total dos quatro estudos, 4.097 casais foram inscritos em quatro continentes e 151.880 atos de sexo sem preservativo foram relatados; houve zero transmissões filogeneticamente ligadas do HIV onde o parceiro positivo tinha uma carga viral indetectável. Em seguida, a declaração de consenso U=U defendendo o uso de "risco zero" foi assinado por centenas de indivíduos e organizações, incluindo o US CDC, a British HIV Association e a revista médica The Lancet. A importância dos resultados finais do estudo PARTNER 2 foi descrita pelo diretor médico do Terrence Higgins Trust como "impossível exagerar", enquanto a principal autora Alison Rodger declarou que a mensagem de que "vírus indetectável carga torna o HIV intransmissível... pode ajudar a acabar com a pandemia do HIV, impedindo a transmissão do HIV. Os autores resumiram suas descobertas no The Lancet da seguinte forma:
Nossos resultados fornecem um nível semelhante de evidências sobre a supressão viral e o risco de transmissão do HIV para homens gays que anteriormente geraram para casais heterossexuais e sugerem que o risco de transmissão do HIV em casais gays através do sexo sem preservativo quando a carga viral do HIV é suprimida é efetivamente zero. Nossos achados apoiam a mensagem da campanha U=U (indetectável é igual à intransmitável) e os benefícios do teste e tratamento precoces para o HIV.
Este resultado é consistente com a conclusão apresentada por Anthony S. Fauci, Diretor do Instituto Nacional de Alergia e Doenças Infecciosas dos Institutos Nacionais de Saúde dos EUA, e sua equipe em um ponto de vista publicado no Journal of a American Medical Association, que U=U é um método eficaz de prevenção do HIV quando uma carga viral indetectável é mantida.
A reativação do herpes genital (HSV-2) em pessoas infectadas com o vírus tem um aumento associado de células T CD4+ enriquecidas com CCR-5, bem como células dendríticas inflamatórias na submucosa da pele genital. O tropismo do HIV para células CCR-5 positivas explica o aumento de duas a três vezes na aquisição do HIV entre pessoas com herpes genital. A medicação antiviral diária (por exemplo, aciclovir) não reduz a inflamação subclínica pós-reativação e, portanto, não reduz o risco de aquisição do HIV.
História
Descoberta
A primeira notícia sobre "uma nova doença exótica" apareceu em 18 de maio de 1981, no jornal gay New York Native.
A AIDS foi observada clinicamente pela primeira vez em 1981 nos Estados Unidos. Os casos iniciais eram um grupo de usuários de drogas injetáveis e homens gays sem causa conhecida de comprometimento da imunidade que apresentavam sintomas de pneumonia Pneumocystis (PCP ou PJP, o último termo reconhecendo que o agente causador agora é chamado Pneumocystis jirovecii), uma infecção oportunista rara que se sabia ocorrer em pessoas com sistemas imunológicos muito comprometidos. Logo depois disso, pesquisadores da NYU School of Medicine estudaram homens gays desenvolvendo um câncer de pele anteriormente raro chamado sarcoma de Kaposi (KS). Muitos outros casos de PJP e KS surgiram, alertando os Centros de Controle e Prevenção de Doenças (CDC) dos EUA e uma força-tarefa do CDC foi formada para monitorar o surto. Acredita-se que o primeiro caso retrospectivamente descrito de AIDS tenha ocorrido na Noruega, a partir de 1966.
No início, o CDC não tinha um nome oficial para a doença, muitas vezes referindo-se a ela por meio de doenças associadas a ela, por exemplo, linfadenopatia, a doença que os descobridores do HIV originalmente batizaram vírus. Eles também usaram Sarcoma de Kaposi e Infecções Oportunistas, nome pelo qual uma força-tarefa foi criada em 1981. Na imprensa geral, o termo GRID, que significava deficiência imunológica relacionada a gays, havia sido cunhado. O CDC, em busca de um nome e olhando para as comunidades infectadas, cunhou "a doença 4H", pois parecia destacar homossexuais, usuários de heroína, hemofílicos e haitianos. No entanto, depois de determinar que a AIDS não era exclusiva da comunidade gay, percebeu-se que o termo GRID era enganoso e AIDS foi apresentado em uma reunião em julho de 1982. Em setembro de 1982, o CDC começou a usar o nome AIDS.
Em 1983, dois grupos de pesquisa separados liderados pelo americano Robert Gallo e investigadores franceses Françoise Barré- Sinoussi e Luc Montagnier declararam independentemente que um novo retrovírus pode ter infectado pacientes com AIDS e publicaram suas descobertas na mesma edição da revista Science. Gallo afirmou que um vírus que seu grupo havia isolado de uma pessoa com AIDS era surpreendentemente semelhante em forma a outros vírus T-linfotrópicos humanos (HTLVs) que seu grupo havia sido o primeiro a isolar. Gallo admitiu em 1987 que o vírus que alegou ter descoberto em 1984 era na verdade um vírus enviado a ele da França no ano anterior. O grupo de Gallo chamou seu vírus recém-isolado de HTLV-III. O grupo de Montagnier isolou um vírus de um paciente que apresentava inchaço dos gânglios linfáticos do pescoço e fraqueza física, dois sintomas clássicos da infecção primária pelo HIV. Contrariando o relato do grupo de Gallo, Montagnier e seus colegas mostraram que as proteínas centrais desse vírus eram imunologicamente diferentes das do HTLV-I. O grupo de Montagnier nomeou seu vírus isolado de vírus associado à linfadenopatia (LAV). Como esses dois vírus eram os mesmos, em 1986 LAV e HTLV-III foram renomeados para HIV.
Outro grupo trabalhando simultaneamente com os grupos Montagnier e Gallo foi o de Jay A. Levy na Universidade da Califórnia, San Francisco. Ele descobriu independentemente o vírus da AIDS em 1983 e o chamou de retrovírus associado à AIDS (ARV). Este vírus era muito diferente do vírus relatado pelos grupos Montagnier e Gallo. As cepas de ARV indicaram, pela primeira vez, a heterogeneidade dos isolados de HIV e vários deles permanecem como exemplos clássicos do vírus da AIDS encontrados nos Estados Unidos.
Origens
Acredita-se que tanto o HIV-1 quanto o HIV-2 tenham se originado em primatas não humanos na África Centro-Ocidental e acredita-se que tenham sido transferidos para humanos (um processo conhecido como zoonose) no início do século XX.
O HIV-1 parece ter se originado no sul de Camarões através da evolução do SIVcpz, um vírus da imunodeficiência símia (SIV) que infecta chimpanzés selvagens (HIV-1 descende do SIVcpz endêmico na subespécie de chimpanzé Pan troglodytes troglodytes). O parente mais próximo do HIV-2 é o SIVsmm, um vírus do fuliginoso mangabey (Cercocebus atys atys), um macaco do Velho Mundo que vive no litoral da África Ocidental (do sul do Senegal ao oeste da Costa do Marfim). Os macacos do Novo Mundo, como o macaco-coruja, são resistentes à infecção pelo HIV-1, possivelmente devido a uma fusão genômica de dois genes de resistência viral.
Acredita-se que o HIV-1 ultrapassou a barreira das espécies em pelo menos três ocasiões distintas, dando origem aos três grupos do vírus, M, N e O.
Há evidências de que humanos que participam de atividades de caça, seja como caçadores ou como vendedores de carne de caça, comumente adquirem SIV. No entanto, o SIV é um vírus fraco e normalmente é suprimido pelo sistema imunológico humano semanas após a infecção. Pensa-se que várias transmissões do vírus de indivíduo para indivíduo em rápida sucessão são necessárias para permitir tempo suficiente para se transformar em HIV. Além disso, devido à sua taxa de transmissão relativamente baixa de pessoa para pessoa, ela só pode se espalhar pela população na presença de um ou mais canais de transmissão de alto risco, que se acredita estarem ausentes na África antes do século XX.
Os canais específicos de transmissão de alto risco propostos, permitindo que o vírus se adapte aos humanos e se espalhem por toda a sociedade, dependem do momento proposto para o cruzamento entre animais e humanos. Estudos genéticos do vírus sugerem que o ancestral comum mais recente do grupo HIV-1M remonta a cerca de 1910. Os defensores dessa datação relacionam a epidemia de HIV com o surgimento do colonialismo e o crescimento de grandes cidades africanas coloniais, levando a mudanças sociais, incluindo diferentes padrões de contato sexual (especialmente parcerias múltiplas e simultâneas), a disseminação da prostituição e a alta frequência concomitante de úlceras genitais (como a sífilis) nas cidades coloniais nascentes. Embora as taxas de transmissão do HIV durante a relação sexual sejam geralmente baixas, elas aumentam muito se um dos parceiros tiver uma infecção sexualmente transmissível que resulte em úlceras genitais. As cidades coloniais do início dos anos 1900 eram notáveis por sua alta prevalência de prostituição e úlceras genitais a ponto de, em 1928, 45% das mulheres residentes do leste de Leopoldville (atualmente Kinshasa) serem prostitutas e, a partir de 1933, cerca de 15%. de todos os moradores de uma mesma cidade foram infectados por uma das formas de sífilis.
O caso mais antigo e bem documentado de HIV em humanos data de 1959 no Congo Belga. O vírus pode ter estado presente nos Estados Unidos desde meados da década de 1960, quando um homem de dezesseis anos chamado Robert Rayford apresentou sintomas em 1966 e morreu em 1969.
Uma hipótese alternativa e provavelmente complementar aponta para o uso generalizado de práticas médicas inseguras na África durante os anos após a Segunda Guerra Mundial, como a reutilização não estéril de seringas descartáveis durante campanhas de vacinação em massa, antibióticos e antimalária. A pesquisa sobre o tempo do ancestral comum mais recente para os grupos M e O do HIV-1, bem como sobre os grupos A e B do HIV-2, indica que o SIV deu origem a linhagens de HIV transmissíveis ao longo do século XX. O tempo disperso dessas transmissões para humanos implica que nenhum fator externo é necessário para explicar a transmissão entre espécies do HIV. Esta observação é consistente com as duas visões predominantes da origem da epidemia de HIV, ou seja, a transmissão do SIV para humanos durante o abate ou abate de primatas infectados e a expansão colonial das cidades da África subsaariana.
Contenido relacionado
Hidrocodona
Martim-pescador
Konrad Lorenz