Hidróxido
Hidroxido é um ânion diatômico com fórmula química OH−. Consiste em um átomo de oxigênio e hidrogênio mantidos juntos por uma única ligação covalente e carrega uma carga elétrica negativa. É um constituinte importante, mas geralmente menor da água. Ele funciona como uma base, um ligante, um nucleófilo e um catalisador. O íon hidróxido forma sais, alguns dos quais se dissociam em solução aquosa, liberando íons hidróxido solvatados. O hidróxido de sódio é uma commodity química de vários milhões de toneladas por ano. O composto eletricamente neutro correspondente HO• é o radical hidroxila. O grupo de átomos ligado covalentemente correspondente -OH é o grupo hidróxi. Tanto o íon hidróxido quanto o grupo hidroxi são nucleófilos e podem atuar como catalisadores na química orgânica.
Muitas substâncias inorgânicas que levam a palavra hidróxido em seus nomes não são compostos iônicos do íon hidróxido, mas compostos covalentes que contêm grupos hidroxi.
Íon hidróxido
O íon hidróxido é uma parte natural da água por causa da reação de auto-ionização na qual seu complemento, o hidrônio, passa pelo hidrogênio:
- H3O + OH- Sim. 2H2O
A constante de equilíbrio para esta reação, definida como
- KKO quê? Não.+Não.- Sim.]
tem um valor próximo a 10−14 a 25 °C, então a concentração de íons hidróxido na água pura é próxima a 10−7 mol∙dm−3, a fim de satisfazer a restrição de carga igual. O pH de uma solução é igual ao cologaritmo decimal da concentração do cátion hidrogênio; o pH da água pura é próximo de 7 em temperatura ambiente. A concentração de íons hidróxido pode ser expressa em termos de pOH, que é próximo a (14 − pH), portanto, o pOH da água pura também é próximo a 7. A adição de uma base à água reduzirá a concentração de cátions de hidrogênio e, portanto, aumentará a concentração do íon hidróxido (aumentar o pH, diminuir o pOH) mesmo que a base não contenha hidróxido. Por exemplo, soluções de amônia têm um pH maior que 7 devido à reação NH3 + H+ ⇌ NH+
4 , que diminui a concentração de cátions de hidrogênio, o que aumenta a concentração de íons de hidróxido. O pOH pode ser mantido em um valor quase constante com várias soluções tampão.
Em solução aquosa, o íon hidróxido é uma base no sentido de Brønsted-Lowry, pois pode aceitar um próton de um ácido de Brønsted-Lowry para formar uma molécula de água. Ele também pode atuar como uma base de Lewis doando um par de elétrons para um ácido de Lewis. Em solução aquosa, os íons de hidrogênio e hidróxido são fortemente solvatados, com ligações de hidrogênio entre os átomos de oxigênio e hidrogênio. De fato, o íon bihidróxido H
3O-
2 foi caracterizado no Estado sólido. Este composto é centrossimétrico e tem uma ligação de hidrogênio muito curta (114,5 pm) que é semelhante ao comprimento do íon bifluoreto HF−
2 (114 pm). Em solução aquosa, o íon hidróxido forma fortes ligações de hidrogênio com as moléculas de água. Uma consequência disso é que as soluções concentradas de hidróxido de sódio têm alta viscosidade devido à formação de uma extensa rede de ligações de hidrogênio como nas soluções de fluoreto de hidrogênio.
Em solução, exposto ao ar, o íon hidróxido reage rapidamente com o dióxido de carbono atmosférico, agindo como um ácido, para formar, inicialmente, o íon bicarbonato.
- Oh!- Sim. + CO2 ? HCO- Sim.
3
A constante de equilíbrio para esta reação pode ser especificada como uma reação com dióxido de carbono dissolvido ou como uma reação com gás dióxido de carbono (consulte Ácido carbônico para valores e detalhes). Em pH neutro ou ácido, a reação é lenta, mas é catalisada pela enzima anidrase carbônica, que efetivamente cria íons hidróxido no sítio ativo.
Soluções contendo o vidro de ataque de íon hidróxido. Nesse caso, os silicatos do vidro atuam como ácidos. Hidróxidos básicos, sólidos ou em solução, são armazenados em recipientes de plástico hermeticamente fechados.
O íon hidróxido pode funcionar como um típico ligante doador de pares de elétrons, formando complexos como tetrahidroxoaluminato/tetrahidroxidoaluminato [Al(OH)4]−. Também é freqüentemente encontrado em complexos de ligantes mistos do tipo [MLx(OH)y]z+, onde L é um ligante. O íon hidróxido geralmente serve como um ligante em ponte, doando um par de elétrons para cada um dos átomos que estão sendo ligados. Conforme ilustrado por [Pb2(OH)]3+, os hidróxidos metálicos geralmente são escritos em um formato simplificado. Pode até atuar como um doador de 3 pares de elétrons, como no tetrâmero [PtMe3(OH)]4.
Quando ligados a um centro metálico fortemente retirador de elétrons, os ligantes de hidróxido tendem a se ionizar em ligantes de óxido. Por exemplo, o íon bicromato [HCrO4]− dissocia-se de acordo com
- Oh!3CrO-H- Sim. O que foi?4]2- + H+
com um pKa de cerca de 5,9.
Espectros vibracionais
Os espectros infravermelhos de compostos contendo o grupo funcional OH têm fortes bandas de absorção na região centradas em torno de 3500 cm−1. A alta frequência de vibração molecular é consequência da pequena massa do átomo de hidrogênio em comparação com a massa do átomo de oxigênio, o que torna a detecção de grupos hidroxila por espectroscopia de infravermelho relativamente fácil. Uma banda devido a um grupo OH tende a ser nítida. No entanto, a largura da banda aumenta quando o grupo OH está envolvido na ligação de hidrogênio. Uma molécula de água tem um modo de curvatura HOH em cerca de 1600 cm−1, então a ausência dessa banda pode ser usada para distinguir um grupo OH de uma molécula de água.
Quando o grupo OH está ligado a um íon metálico em um complexo de coordenação, um modo de flexão M-OH pode ser observado. Por exemplo, em [Sn(OH)6]2− ocorre em 1065 cm−1. O modo de flexão para um hidróxido de ponte tende a ter uma frequência mais baixa como em [(bipiridina)Cu(OH)2Cu(bipiridina)]2+ (955 cm−1). As vibrações de alongamento M-OH ocorrem abaixo de cerca de 600 cm-1. Por exemplo, o íon tetraédrico [Zn(OH)4]2− tem bandas a 470 cm−1 (Raman-ativo, polarizado) e 420 cm−1 (infravermelho). O mesmo íon tem uma vibração de flexão (HO)–Zn–(OH) a 300 cm−1.
Aplicativos
As soluções de hidróxido de sódio, também conhecidas como lixívia e soda cáustica, são utilizadas no fabrico de pasta e papel, têxteis, água potável, sabões e detergentes e como desentupidor de esgotos. A produção mundial em 2004 foi de aproximadamente 60 milhões de toneladas. O principal método de fabricação é o processo cloralcalino.
Soluções contendo o íon hidróxido são geradas quando um sal de um ácido fraco é dissolvido em água. O carbonato de sódio é usado como um álcali, por exemplo, em virtude da reação de hidrólise
- CO2-
3 + H2O HCO- Sim.
3 + OH- Sim. (pKa2= 10.33 a 25 °C e zero força iônica)
Embora a força básica das soluções de carbonato de sódio seja menor do que uma solução concentrada de hidróxido de sódio, ela tem a vantagem de ser um sólido. Também é fabricado em grande escala (42 milhões de toneladas em 2005) pelo processo Solvay. Um exemplo do uso de carbonato de sódio como álcali é quando a carbonato de sódio (outro nome para carbonato de sódio) age sobre ésteres insolúveis, como triglicerídeos, comumente conhecidos como gorduras, para hidrolizá-los e torná-los solúveis.
A bauxita, um hidróxido básico de alumínio, é o principal minério a partir do qual o metal é fabricado. Da mesma forma, a goethita (α-FeO(OH)) e a lepidocrocita (γ-FeO(OH)), hidróxidos básicos de ferro, estão entre os principais minérios utilizados para a fabricação de ferro metálico.
Hidróxidos inorgânicos
Metais alcalinos
Além de NaOH e KOH, que desfrutam de aplicações em grande escala, os hidróxidos de outros metais alcalinos também são úteis. O hidróxido de lítio é uma base forte, com um pKb de -0,36. O hidróxido de lítio é usado em sistemas de purificação de gás respiratório para naves espaciais, submarinos e rebreathers para remover o dióxido de carbono do gás exalado.
- 2 LiOH + CO2 → Li2CO3 + H2O
O hidróxido de lítio é preferido ao de sódio por causa de sua massa menor. Hidróxido de sódio, hidróxido de potássio e os hidróxidos de outros metais alcalinos também são bases fortes.
Metais alcalinos terrosos
O hidróxido de berílio Be(OH)2 é anfótero. O próprio hidróxido é insolúvel em água, com um produto de solubilidade log K*sp de -11,7. A adição de ácido fornece produtos de hidrólise solúveis, incluindo o íon trimérico [Be3(OH)3(H2O)6]3+, que possui grupos OH fazendo ponte entre pares de íons de berílio formando um anel de 6 membros. Em pH muito baixo, o íon aqua [Be(H2O)4]2+ é formado. A adição de hidróxido a Be(OH)2 fornece o tetraidroxoberilato solúvel ou ânion tetraidroxidoberilato, [Be(OH)4]2−.
A solubilidade em água dos outros hidróxidos neste grupo aumenta com o aumento do número atômico. Hidróxido de magnésio Mg(OH)2 é uma base forte (até o limite de sua solubilidade, que é muito baixa em água pura), assim como os hidróxidos dos alcalino-terrosos mais pesados: hidróxido de cálcio, estrôncio hidróxido e hidróxido de bário. Uma solução ou suspensão de hidróxido de cálcio é conhecida como água de cal e pode ser usada para testar o dióxido de carbono ácido fraco. A reação Ca(OH)2 + CO2 ⇌ Ca2+ + HCO-
3 + OH- ilustra a basicidade do hidróxido de cálcio. A cal sodada, que é uma mistura das bases fortes NaOH e KOH com Ca(OH)2, é utilizada como absorvente de CO2.
Elementos do grupo boro
O hidróxido de boro mais simples B(OH)3, conhecido como ácido bórico, é um ácido. Ao contrário dos hidróxidos dos hidróxidos alcalinos e alcalino-terrosos, não se dissocia em solução aquosa. Em vez disso, reage com as moléculas de água agindo como um ácido de Lewis, liberando prótons.
- B (OH)3 + H2O ponto B (OH)−4 + H+
Uma variedade de oxiânions de boro são conhecidos, os quais, na forma protonada, contêm grupos hidróxido.
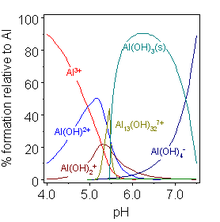
O hidróxido de alumínio Al(OH)3 é anfotérico e se dissolve em solução alcalina.
- Al(OH)3 (sólido) + OH- Sim.(aq) Servidor Al(OH)−4 (aq)
No processo Bayer para a produção de óxido de alumínio puro a partir de minerais de bauxita, esse equilíbrio é manipulado pelo controle cuidadoso da temperatura e da concentração de álcalis. Na primeira fase, o alumínio se dissolve em solução alcalina quente como Al(OH)-
4, mas outros hidróxidos geralmente presentes no mineral, como hidróxidos de ferro, não se dissolvem porque não são anfóteros. Após a retirada dos insolúveis, a chamada lama vermelha, faz-se precipitar o hidróxido de alumínio puro, reduzindo-se a temperatura e acrescentando-se água ao extrato que, ao diluir o álcali, baixa o pH da solução. O hidróxido de alumínio básico AlO(OH), que pode estar presente na bauxita, também é anfotérico.
Em soluções levemente ácidas, os complexos hidroxi/hidróxido formados pelo alumínio são um pouco diferentes dos do boro, refletindo o tamanho maior de Al(III) vs. B(III). A concentração da espécie [Al13(OH)32]7+ é muito dependente da concentração total de alumínio. Vários outros complexos hidroxo são encontrados em compostos cristalinos. Talvez o mais importante seja o hidróxido básico AlO(OH), um material polimérico conhecido pelos nomes das formas minerais boemita ou diásporo, dependendo da estrutura do cristal. Hidróxido de gálio, hidróxido de índio e hidróxido de tálio (III) também são anfotéricos. O hidróxido de tálio(I) é uma base forte.
Elementos do grupo de carbono
O carbono não forma hidróxidos simples. O composto hipotético C(OH)4 (ácido ortocarbônico ou metanotetrol) é instável em solução aquosa:
- C(OH)4 → HCO- Sim.
3 + H3O+ - HCO- Sim.
3 + H+ ?2CO3
O dióxido de carbono também é conhecido como anidrido carbônico, o que significa que se forma pela desidratação do ácido carbônico H2CO3 (OC(OH)2).
Ácido silícico é o nome dado a uma variedade de compostos com uma fórmula genérica [SiOx(OH)4−2x]n. Ácido ortosilícico foi identificado em solução aquosa muito diluída. É um ácido fraco com pKa1 = 9,84, pKa2 = 13,2 a 25 °C. Geralmente é escrito como H4SiO4, mas a fórmula Si(OH)4 é geralmente aceita. Outros ácidos silícicos, como ácido metassilícico (H2SiO3), ácido dissilícico (H2 Si2O5) e ácido pirosilícico (H6Si2O7) foram caracterizados. Esses ácidos também possuem grupos hidróxido ligados ao silício; as fórmulas sugerem que esses ácidos são formas protonadas de polioxiânions.
Poucos complexos hidroxo de germânio foram caracterizados. Hidróxido de estanho(II) Sn(OH)2 foi preparado em meio anidro. Quando o óxido de estanho(II) é tratado com álcali, o complexo hidroxo piramidal Sn(OH)-
3 é formado. Quando soluções contendo este íon são acidificadas, o íon [Sn3(OH)4]2+ é formado junto com alguns complexos hidroxo básicos. A estrutura de [Sn3(OH)4]2+ tem um triângulo de átomos de estanho conectados por grupos de hidróxido em ponte. O hidróxido de estanho(IV) é desconhecido, mas pode ser considerado como o ácido hipotético do qual os estanatos, com uma fórmula [Sn(OH)6]2−, são derivados por reação com o íon hidróxido básico (Lewis).
A hidrólise de Pb2+ em solução aquosa é acompanhada pela formação de vários complexos contendo hidroxo, alguns dos quais são insolúveis. O complexo hidroxo básico [Pb6O(OH)6]4+ é um aglomerado de seis centros de chumbo com ligações metal-metal envolvendo um íon óxido central. Os seis grupos hidróxidos estão nas faces dos dois tetraedros externos de Pb4. Em soluções fortemente alcalinas, íons de plumbato solúveis são formados, incluindo [Pb(OH)6]2−.
Outros elementos do grupo principal
| Ácido fosforoso | Ácido fosfórico | Ácido sulfúrico | Ácido Tellurístico | Ortho.- ácido periódico | Ácido Xenic |
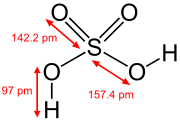
Nos estados de oxidação mais elevados dos pnictogênios, calcogênios, halogênios e gases nobres, existem oxoácidos nos quais o átomo central está ligado a íons óxidos e íons hidróxidos. Exemplos incluem ácido fosfórico H3PO4 e ácido sulfúrico H2SO4. Nesses compostos, um ou mais grupos hidróxidos podem se dissociar com a liberação de cátions de hidrogênio como em um ácido de Brønsted-Lowry padrão. Muitos oxoácidos de enxofre são conhecidos e todos apresentam grupos OH que podem se dissociar.
O ácido telúrico geralmente é escrito com a fórmula H2TeO4·2H2O, mas é melhor descrito estruturalmente como Te(OH) 6.
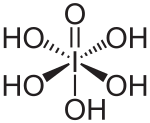
O ácidoorto-periódico pode perder todos os seus prótons, eventualmente formando o íon periodato [IO4]−. Também pode ser protonado em condições fortemente ácidas para dar o íon octaédrico [I(OH)6]+, completando a série isoeletrônica, [E(OH) 6]z, E = Sn, Sb, Te, I; z = −2, −1, 0, +1. Outros ácidos de iodo(VII) que contêm grupos hidróxido são conhecidos, em particular em sais como o íon mesoperiodato que ocorre em K4[I2O8(OH)2]·8H2O.
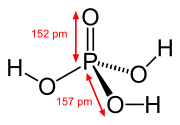
Como é comum fora dos metais alcalinos, os hidróxidos dos elementos em estados de oxidação mais baixos são complicados. Por exemplo, o ácido fosforoso H3PO3 tem predominantemente a estrutura OP(H)(OH)2, em equilíbrio com uma pequena quantidade de P(OH)3.
Os oxoácidos de cloro, bromo e iodo têm a fórmula On− 1/2A(OH), onde n é o número de oxidação: +1, +3, +5 ou +7, e A = Cl, Br ou I. O único oxoácido do flúor é F(OH), ácido hipofluorado. Quando esses ácidos são neutralizados, o átomo de hidrogênio é removido do grupo hidróxido.
Metais de transição e pós-transição
Os hidróxidos dos metais de transição e pós-transição geralmente têm o metal no +2 (M = Mn, Fe, Co, Ni, Cu, Zn) ou +3 (M = Fe, Ru, Rh, Ir) Estado de oxidação. Nenhum é solúvel em água e muitos são mal definidos. Uma característica complicada dos hidróxidos é sua tendência a sofrer mais condensação nos óxidos, um processo chamado olação. Hidróxidos de metais no estado de oxidação +1 também são mal definidos ou instáveis. Por exemplo, o hidróxido de prata Ag(OH) se decompõe espontaneamente no óxido (Ag2O). Hidróxidos de cobre(I) e ouro(I) também são instáveis, embora sejam conhecidos adutos estáveis de CuOH e AuOH. Os compostos poliméricos M(OH)2 e M(OH)3 são geralmente preparados aumentando o pH de uma solução aquosa dos cátions metálicos correspondentes até que o hidróxido precipite de solução. Pelo contrário, os hidróxidos dissolvem-se em solução ácida. Hidróxido de zinco Zn(OH)2 é anfótero, formando o íon tetrahidroxidozincato Zn(OH)2−
4 em solução fortemente alcalina.
Existem numerosos complexos de ligantes mistos desses metais com o íon hidróxido. Na verdade, elas são geralmente mais bem definidas do que as derivadas mais simples. Muitos podem ser produzidos por desprotonação do correspondente metal aquo complexo.
- LnM (OH)2)nM(OH) + BH+ (L = ligante, B = base)
O ácido vanádico H3VO4 mostra semelhanças com o ácido fosfórico H3PO4 embora tenha um química muito mais complexa do oxoânion vanadato. Ácido crômico H2CrO4, tem semelhanças com ácido sulfúrico H2SO4; por exemplo, ambos formam sais ácidos A+[HMO4]−. Alguns metais, por ex. V, Cr, Nb, Ta, Mo, W tendem a existir em estados de alta oxidação. Ao invés de formar hidróxidos em solução aquosa, eles se convertem em grupos oxo pelo processo de olação, formando polioxometalatos.
Sais básicos contendo hidróxido
Em alguns casos, os produtos da hidrólise parcial do íon metálico, descritos acima, podem ser encontrados em compostos cristalinos. Um exemplo notável é encontrado com zircônio (IV). Devido ao alto estado de oxidação, os sais de Zr4+ são extensivamente hidrolisados em água mesmo em pH baixo. O composto originalmente formulado como ZrOCl2·8H2O foi encontrado para ser o sal de cloreto de um cátion tetramérico [Zr4(OH)8(H2O)16]8+ em que há um quadrado de Zr4+ íons com dois grupos de hidróxido em ponte entre átomos de Zr em cada lado do quadrado e com quatro moléculas de água ligadas a cada átomo de Zr.
O mineral malaquita é um exemplo típico de carbonato básico. A fórmula, Cu2CO3(OH)2 mostra que está a meio caminho entre o carbonato de cobre e o hidróxido de cobre. De fato, no passado a fórmula era escrita como CuCO3·Cu(OH)2. A estrutura cristalina é composta por íons de cobre, carbonato e hidróxido. O mineral atacamita é um exemplo de cloreto básico. Tem a fórmula, Cu2Cl(OH)3. Neste caso, a composição é mais próxima do hidróxido do que do cloreto CuCl2·3Cu(OH)2. O cobre forma compostos de hidroxifosfato (libetenita), arsenato (olivenita), sulfato (brocantita) e nitrato. Chumbo branco é um carbonato de chumbo básico, (PbCO3)2·Pb(OH)2, que tem sido usado como pigmento branco porque de sua qualidade opaca, embora seu uso seja agora restrito porque pode ser uma fonte de envenenamento por chumbo.
Química estrutural
O íon hidróxido parece girar livremente em cristais dos hidróxidos de metais alcalinos mais pesados em temperaturas mais altas, de modo a se apresentar como um íon esférico, com um raio iônico efetivo de cerca de 153 pm. Assim, as formas de alta temperatura de KOH e NaOH têm a estrutura de cloreto de sódio, que gradualmente congela em uma estrutura de cloreto de sódio monoclinicamente distorcida a temperaturas abaixo de cerca de 300°C. Os grupos OH ainda giram mesmo à temperatura ambiente em torno de seus eixos de simetria e, portanto, não podem ser detectados por difração de raios-X. A forma de NaOH à temperatura ambiente tem a estrutura do iodeto de tálio. LiOH, no entanto, tem uma estrutura em camadas, composta por unidades tetraédricas Li(OH)4 e (OH)Li4. Isso é consistente com o caráter fracamente básico do LiOH em solução, indicando que a ligação Li-OH tem muito caráter covalente.
O íon hidróxido exibe simetria cilíndrica em hidróxidos de metais bivalentes Ca, Cd, Mn, Fe e Co. Por exemplo, hidróxido de magnésio Mg(OH)2 (brucita) cristaliza com o iodeto de cádmio estrutura de camada, com uma espécie de compactação de íons de magnésio e hidróxido.
O hidróxido anfótero Al(OH)3 tem quatro formas cristalinas principais: gibbsita (mais estável), bayerita, nordstrandita e doileíta. Todos esses polimorfos são constituídos por camadas duplas de íons de hidróxido - os átomos de alumínio em dois terços dos orifícios octaédricos entre as duas camadas - e diferem apenas na sequência de empilhamento das camadas. As estruturas são semelhantes à estrutura brucite. No entanto, enquanto a estrutura da brucita pode ser descrita como uma estrutura compactada na gibbsita, os grupos OH na parte inferior de uma camada repousam nos grupos da camada abaixo. Esse arranjo levou à sugestão de que existem ligações direcionais entre grupos OH em camadas adjacentes. Esta é uma forma incomum de ligação de hidrogênio, uma vez que se espera que os dois íons hidróxido envolvidos apontem para longe um do outro. Os átomos de hidrogênio foram localizados por experimentos de difração de nêutrons em α-AlO(OH) (diásporo). A distância O–H–O é muito curta, às 265 pm; o hidrogênio não é equidistante entre os átomos de oxigênio e a ligação OH curta faz um ângulo de 12° com a linha O–O. Um tipo semelhante de ligação de hidrogênio foi proposto para outros hidróxidos anfotéricos, incluindo Be(OH)2, Zn(OH)2 e Fe(OH)3 .
Vários hidróxidos mistos são conhecidos com estequiometria A3MIII(OH)6, A2MIV(OH)6 e AMV(OH)6. Como a fórmula sugere, essas substâncias contêm M(OH)6 unidades estruturais octaédricas. Hidróxidos duplos em camadas podem ser representados pela fórmula [Mz+
1−x M3+
x(OH)
2]q+ (Xn−)
q⁄n·yH
2O. Mais comumente, z = 2 e M2+ = Ca2+, Mg2+, Mn2+, Fe2+, Co2+, Ni2+, Cu2+ ou Zn2+; portanto, q = x.
Em reações orgânicas
O hidróxido de potássio e o hidróxido de sódio são dois reagentes bem conhecidos em química orgânica.
Catálise de base
O íon hidróxido pode atuar como um catalisador básico. A base abstrai um próton de um ácido fraco para dar um intermediário que passa a reagir com outro reagente. Substratos comuns para abstração de prótons são álcoois, fenóis, aminas e ácidos de carbono. O valor de pKa para a dissociação de uma ligação C-H é extremamente alto, mas o pKa hidrogênios alfa de um composto carbonílico é cerca de 3 unidades logarítmicas menor. Os valores pKa típicos são 16,7 para acetaldeído e 19 para acetona. A dissociação pode ocorrer na presença de uma base adequada.
- RC(O)CH2R' + B RC (O)CH- Sim.R' + BH+
A base deve ter um valor de pKa não inferior a cerca de 4 unidades logarítmicas menor, ou o equilíbrio ficará quase completamente à esquerda.
O íon hidróxido por si só não é uma base forte o suficiente, mas pode ser convertido em uma adicionando hidróxido de sódio ao etanol
- Oh!- Sim. + EtOH- Sim. + H2O
para produzir o íon etóxido. O pKa para a autodissociação do etanol é de cerca de 16, então o íon alcóxido é uma base suficientemente forte. A adição de um álcool a um aldeído para formar um hemiacetal é um exemplo de reação que pode ser catalisada pela presença de hidróxido. O hidróxido também pode atuar como um catalisador de base de Lewis.
Como reagente nucleofílico
O íon hidróxido é intermediário em nucleofilicidade entre o íon flúor F− e o íon amida NH-
2. Hidrólise de éster sob condições alcalinas (também conhecida como hidrólise de base)
- R1C(O)OR2 + OH- Sim. ⇌1CO(O)H + - Sim.OU2 ⇌1CO2- Sim. + HOR2
é um exemplo de uma substituição nucleofílica de acil com o íon hidróxido atuando como um nucleófilo. O grupo abandonador na ilustração é um íon alcóxido que sofre rapidamente uma reação de transferência de prótons de Brønsted-Lowry para produzir o produto álcool. O intermediário ácido carboxílico é a fonte dessa transferência de prótons, embora a reação possa ocorrer indiretamente através do solvente (isto é, o alcóxido pode desprotonar uma molécula de água para dar um íon hidróxido, que por sua vez desprotona o produto ácido carboxílico), explicando por que um ânion carboxilato é o segundo produto. Os primeiros métodos de fabricação de sabão faziam reagir triglicerídeos de gordura animal (o éster) com soda cáustica. O subproduto glicerol pode ser deixado na mistura do sabão, ou pode ser adicionado cloreto de sódio para salgar a mistura de sais de ácidos graxos (ingredientes do sabão), em uma aplicação do efeito do íon comum. Os próprios ácidos graxos podem ser reformados pela acidificação da mistura de produtos. Vários experimentos de laboratório de química orgânica de graduação envolvendo a extração do triglicerídeo trimiristina da noz-moscada em pó e sua transformação no ácido graxo ácido mirístico ou em um sabão foram descritos.
Outros casos em que o hidróxido pode atuar como reagente nucleofílico são a hidrólise de amida, a reação de Cannizzaro, a substituição nucleofílica alifática, a substituição nucleofílica aromática e em reações de eliminação. O meio de reação para KOH e NaOH é geralmente água, mas com um catalisador de transferência de fase, o ânion hidróxido também pode ser transportado para um solvente orgânico, por exemplo, na geração do intermediário reativo diclorocarbeno.
Contenido relacionado
Célula eletroquímica
Cristal
Processo endotérmico
Isomeria cis-trans
Hélio