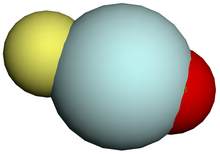
Hélio
Hélio (do grego: ἥλιος, romanizado: < i lang="el-Latn">hélios, lit. 'sol') é um elemento químico com o símbolo He e número atômico 2. É um gás incolor, inodoro, insípido, não tóxico, inerte, monoatômico e o primeiro do grupo dos gases nobres da tabela periódica. Seu ponto de ebulição é o mais baixo entre todos os elementos e não possui ponto de fusão à pressão padrão. É o segundo elemento mais leve e o segundo mais abundante no universo observável, depois do hidrogênio. Está presente em cerca de 24% da massa elementar total, que é mais de 12 vezes a massa de todos os elementos mais pesados combinados. Sua abundância é semelhante a esta no Sol e em Júpiter, devido à altíssima energia de ligação nuclear (por núcleon) do hélio-4, em relação aos próximos três elementos após o hélio. Essa energia de ligação do hélio-4 também explica por que ele é um produto tanto da fusão nuclear quanto do decaimento radioativo. O isótopo de hélio mais comum no universo é o hélio-4, cuja grande maioria foi formada durante o Big Bang. Grandes quantidades de novo hélio são criadas pela fusão nuclear do hidrogênio nas estrelas.
O hélio foi detectado pela primeira vez como uma assinatura de linha espectral amarela desconhecida na luz do sol durante um eclipse solar em 1868 por Georges Rayet, capitão C. T. Haig, Norman R. Pogson e tenente John Herschel, e foi posteriormente confirmado pelo astrônomo francês Jules Janssen. Janssen é frequentemente creditado em conjunto com a detecção do elemento, junto com Norman Lockyer. Janssen registrou a linha espectral do hélio durante o eclipse solar de 1868, enquanto Lockyer a observou da Grã-Bretanha. Lockyer foi o primeiro a propor que a linha se devia a um novo elemento, ao qual deu o nome de sol. A descoberta formal do elemento foi feita em 1895 pelos químicos Sir William Ramsay, Per Teodor Cleve e Nils Abraham Langlet, que encontraram hélio emanando do minério de urânio, cleveite, que agora não é considerado como um espécies minerais separadas, mas como uma variedade de uraninite. Em 1903, grandes reservas de hélio foram encontradas em campos de gás natural em partes dos Estados Unidos, de longe o maior fornecedor do gás hoje.
O hélio líquido é usado em criogenia (seu maior uso individual, consumindo cerca de um quarto da produção) e no resfriamento de ímãs supercondutores, com sua principal aplicação comercial em scanners de ressonância magnética. Os outros usos industriais do hélio - como gás de pressurização e purga, como atmosfera protetora para soldagem a arco e em processos como o cultivo de cristal para fazer pastilhas de silício - respondem por metade do gás produzido. Um uso pequeno, mas bem conhecido, é como gás de elevação em balões e aeronaves. Como acontece com qualquer gás cuja densidade difere da do ar, a inalação de um pequeno volume de hélio altera temporariamente o timbre e a qualidade da voz humana. Na pesquisa científica, o comportamento das duas fases fluidas do hélio-4 (hélio I e hélio II) é importante para os pesquisadores que estudam a mecânica quântica (em particular a propriedade da superfluidez) e para aqueles que observam os fenômenos, como a supercondutividade, produzidos na matéria perto do zero absoluto.
Na Terra, é relativamente raro—5,2 ppm por volume na atmosfera. A maior parte do hélio terrestre presente hoje é criada pelo decaimento radioativo natural de elementos radioativos pesados (tório e urânio, embora existam outros exemplos), já que as partículas alfa emitidas por tais decaimentos consistem em núcleos de hélio-4. Esse hélio radiogênico é aprisionado com gás natural em concentrações de até 7% em volume, do qual é extraído comercialmente por um processo de separação a baixa temperatura chamado destilação fracionada. O hélio terrestre é um recurso não renovável porque, uma vez liberado na atmosfera, escapa imediatamente para o espaço. Acredita-se que seu suprimento esteja diminuindo rapidamente. No entanto, alguns estudos sugerem que o hélio produzido nas profundezas da terra por decaimento radioativo pode se acumular nas reservas de gás natural em quantidades maiores do que o esperado, em alguns casos, tendo sido liberado pela atividade vulcânica.
História
Descobertas científicas
A primeira evidência de hélio foi observada em 18 de agosto de 1868, como uma linha amarela brilhante com um comprimento de onda de 587,49 nanômetros no espectro da cromosfera do Sol. A linha foi detectada pelo astrônomo francês Jules Janssen durante um eclipse solar total em Guntur, na Índia. Esta linha foi inicialmente considerada como sendo sódio. Em 20 de outubro do mesmo ano, o astrônomo inglês Norman Lockyer observou uma linha amarela no espectro solar, que ele denominou de D3 porque estava perto do conhecido D1 e D2 linhas Fraunhofer de sódio. Ele concluiu que foi causado por um elemento no Sol desconhecido na Terra. Lockyer e o químico inglês Edward Frankland nomearam o elemento com a palavra grega para Sol, ἥλιος (helios).
Em 1881, o físico italiano Luigi Palmieri detectou hélio na Terra pela primeira vez através de sua linha espectral D3, quando analisou um material que havia sido sublimado durante uma recente erupção do Monte Vesúvio.
Em 26 de março de 1895, o químico escocês Sir William Ramsay isolou o hélio na Terra tratando o mineral cleveita (uma variedade de uraninita com pelo menos 10% de elementos de terras raras) com ácidos minerais. Ramsay procurava o argônio mas, após separar o nitrogênio e o oxigênio do gás, liberado pelo ácido sulfúrico, notou uma linha amarela brilhante que correspondia à linha D3 observada no espectro do Sol. Essas amostras foram identificadas como hélio por Lockyer e pelo físico britânico William Crookes. Foi isolado independentemente da cleveita, no mesmo ano, pelos químicos Per Teodor Cleve e Abraham Langlet, em Uppsala, na Suécia, que coletaram gás suficiente para determinar com precisão seu peso atômico. O hélio também foi isolado pelo geoquímico americano William Francis Hillebrand, antes da descoberta de Ramsay, quando notou linhas espectrais incomuns ao testar uma amostra do mineral uraninita. Hillebrand, no entanto, atribuiu as linhas ao nitrogênio. Sua carta de felicitações a Ramsay oferece um caso interessante de descoberta e quase descoberta na ciência.
Em 1907, Ernest Rutherford e Thomas Royds demonstraram que as partículas alfa são núcleos de hélio, permitindo que as partículas penetrem na fina parede de vidro de um tubo evacuado, criando então uma descarga no tubo, para estudar o espectro do novo gás dentro. Em 1908, o hélio foi liquefeito pela primeira vez pelo físico holandês Heike Kamerlingh Onnes, resfriando o gás a menos de 5 K (−268,15 °C; −450,67 °F). Ele tentou solidificá-lo, reduzindo ainda mais a temperatura, mas falhou, porque o hélio não solidifica à pressão atmosférica. Onnes' o estudante Willem Hendrik Keesom finalmente conseguiu solidificar 1 cm3 de hélio em 1926 aplicando pressão externa adicional.
Em 1913, Niels Bohr publicou sua "trilogia" na estrutura atômica que incluiu uma reconsideração da série Pickering-Fowler como evidência central em apoio ao seu modelo do átomo. Esta série recebeu o nome de Edward Charles Pickering, que em 1896 publicou observações de linhas anteriormente desconhecidas no espectro da estrela ζ Puppis (agora se sabe que ocorrem com Wolf-Rayet e outras estrelas quentes). Pickering atribuiu a observação (linhas em 4551, 5411 e 10123 Å) a uma nova forma de hidrogênio com níveis de transição semi-inteiros. Em 1912, Alfred Fowler conseguiu produzir linhas semelhantes a partir de uma mistura de hidrogênio e hélio e apoiou a conclusão de Pickering quanto à sua origem. O modelo de Bohr não permite transições de meio inteiro (nem a mecânica quântica) e Bohr concluiu que Pickering e Fowler estavam errados e, em vez disso, atribuiu essas linhas espectrais ao hélio ionizado, He+. Fowler estava inicialmente cético, mas acabou convencido de que Bohr estava correto e, em 1915, "os espectroscopistas haviam transferido [a série Pickering-Fowler] definitivamente [do hidrogênio] para o hélio". O trabalho teórico de Bohr sobre a série Pickering demonstrou a necessidade de "um reexame de problemas que pareciam já ter sido resolvidos nas teorias clássicas". e forneceu uma confirmação importante para sua teoria atômica.
Em 1938, o físico russo Pyotr Leonidovich Kapitsa descobriu que o hélio-4 quase não tinha viscosidade em temperaturas próximas do zero absoluto, um fenômeno agora chamado de superfluidez. Este fenômeno está relacionado com a condensação de Bose-Einstein. Em 1972, o mesmo fenômeno foi observado no hélio-3, mas em temperaturas bem mais próximas do zero absoluto, pelos físicos americanos Douglas D. Osheroff, David M. Lee e Robert C. Richardson. Acredita-se que o fenômeno no hélio-3 esteja relacionado ao emparelhamento de férmions de hélio-3 para formar bósons, em analogia aos pares de elétrons de Cooper que produzem supercondutividade.
Extração e uso
Depois de uma operação de perfuração de petróleo em 1903 em Dexter, Kansas produziu um gêiser de gás que não queimava, o geólogo do estado de Kansas Erasmus Haworth coletou amostras do gás que escapava e as levou de volta para a Universidade de Kansas em Lawrence, onde, com a ajuda dos químicos Hamilton Cady e David McFarland, ele descobriu que o gás consistia, em volume, de 72% de nitrogênio, 15% de metano (uma porcentagem combustível apenas com oxigênio suficiente), 1% de hidrogênio e 12% de um gás não identificável. Com uma análise mais aprofundada, Cady e McFarland descobriram que 1,84% da amostra de gás era hélio. Isso mostrou que, apesar de sua raridade geral na Terra, o hélio estava concentrado em grandes quantidades nas Grandes Planícies americanas, disponível para extração como subproduto do gás natural.
Isso permitiu que os Estados Unidos se tornassem o principal fornecedor mundial de hélio. Seguindo uma sugestão de Sir Richard Threlfall, a Marinha dos Estados Unidos patrocinou três pequenas usinas experimentais de hélio durante a Primeira Guerra Mundial. O objetivo era abastecer balões de barragem com gás não inflamável e mais leve que o ar. Um total de 5.700 m3 (200.000 cu ft) de 92% de hélio foi produzido no programa, embora menos de um metro cúbico do gás tenha sido obtido anteriormente. Parte desse gás foi usado no primeiro dirigível cheio de hélio do mundo, o dirigível classe C C-7 da Marinha dos EUA, que fez sua viagem inaugural de Hampton Roads, Virgínia, para Bolling Field, em Washington., D.C., em 1º de dezembro de 1921, quase dois anos antes do primeiro dirigível rígido cheio de hélio da Marinha, o USS Shenandoah, construído pela Naval Aircraft Factory, voar em setembro de 1923.
Embora o processo de extração usando liquefação de gás a baixa temperatura não tenha sido desenvolvido a tempo de ser significativo durante a Primeira Guerra Mundial, a produção continuou. O hélio foi usado principalmente como gás de elevação em aeronaves mais leves que o ar. Durante a Segunda Guerra Mundial, a demanda por hélio aumentou para gás de elevação e para soldagem a arco blindado. O espectrômetro de massa de hélio também foi vital no Projeto Manhattan da bomba atômica.
O governo dos Estados Unidos criou a Reserva Nacional de Hélio em 1925 em Amarillo, Texas, com o objetivo de fornecer aeronaves militares em tempos de guerra e aeronaves comerciais em tempos de paz. Por causa da Lei do Hélio de 1925, que proibiu a exportação do escasso hélio do qual os EUA então detinham o monopólio da produção, juntamente com o custo proibitivo do gás, os zepelins alemães foram forçados a usar o hidrogênio como gás de elevação, que ganharia infâmia em o desastre de Hindenburg. O mercado de hélio após a Segunda Guerra Mundial estava deprimido, mas a reserva foi expandida na década de 1950 para garantir o fornecimento de hélio líquido como refrigerante para criar combustível de foguete de oxigênio/hidrogênio (entre outros usos) durante a Corrida Espacial e a Guerra Fria. O uso de hélio nos Estados Unidos em 1965 foi mais de oito vezes o pico de consumo durante a guerra.
Após as "Helium Acts Emendas de 1960" (Public Law 86–777), o U.S. Bureau of Mines providenciou cinco usinas privadas para recuperar hélio do gás natural. Para este programa de conservação de hélio, o Bureau construiu um oleoduto de 425 milhas (684 km) de Bushton, Kansas, para conectar essas usinas com o campo de gás parcialmente esgotado do governo em Cliffside perto de Amarillo, Texas. Esta mistura de hélio-nitrogênio foi injetada e armazenada no campo de gás de Cliffside até ser necessária, momento em que foi posteriormente purificada.
Em 1995, um bilhão de metros cúbicos do gás havia sido coletado e a reserva tinha uma dívida de US$ 1,4 bilhão, o que levou o Congresso dos Estados Unidos em 1996 a descontinuar a reserva. O resultante Helium Privatization Act de 1996 (Public Law 104–273) instruiu o Departamento do Interior dos Estados Unidos a esvaziar a reserva, com vendas começando em 2005.
O hélio produzido entre 1930 e 1945 tinha cerca de 98,3% de pureza (2% de nitrogênio), o que era adequado para aeronaves. Em 1945, uma pequena quantidade de 99,9% de hélio foi produzida para uso em soldagem. Em 1949, quantidades comerciais de grau A 99,95% de hélio estavam disponíveis.
Por muitos anos, os Estados Unidos produziram mais de 90% do hélio comercialmente utilizável no mundo, enquanto as fábricas de extração no Canadá, Polônia, Rússia e outras nações produziram o restante. Em meados da década de 1990, uma nova fábrica em Arzew, na Argélia, com produção de 17 milhões de metros cúbicos (600 milhões de pés cúbicos), entrou em operação, com produção suficiente para cobrir toda a demanda da Europa. Enquanto isso, em 2000, o consumo de hélio nos EUA aumentou para mais de 15 milhões de kg por ano. Em 2004–2006, foram construídas fábricas adicionais em Ras Laffan, no Catar, e em Skikda, na Argélia. A Argélia rapidamente se tornou o segundo maior produtor de hélio. Durante esse período, tanto o consumo de hélio quanto os custos de produção de hélio aumentaram. De 2002 a 2007, os preços do hélio dobraram.
Em 2012, a Reserva Nacional de Hélio dos Estados Unidos representava 30% do hélio mundial. Esperava-se que a reserva ficasse sem hélio em 2018. Apesar disso, um projeto de lei no Senado dos Estados Unidos permitiria que a reserva continuasse a vender o gás. Outras grandes reservas estavam em Hugoton, no Kansas, Estados Unidos, e nos campos de gás próximos do Kansas e nos panhandles do Texas e Oklahoma. Novas plantas de hélio estavam programadas para abrir em 2012 no Catar, na Rússia, e no estado americano de Wyoming, mas não se esperava que diminuíssem a escassez.
Em 2013, o Catar iniciou a maior unidade de hélio do mundo, embora a crise diplomática do Qatar em 2017 tenha afetado severamente a produção de hélio lá. 2014 foi amplamente reconhecido como um ano de excesso de oferta no negócio de hélio, após anos de escassez de renome. A Nasdaq informou (2015) que para a Air Products, uma corporação internacional que vende gases para uso industrial, os volumes de hélio permanecem sob pressão econômica devido a restrições de fornecimento de matéria-prima.
(Veja também a subseção Defensores da conservação na seção Ocorrência e produção deste artigo, abaixo.)
Características
Átomo
Na mecânica quântica
Na perspectiva da mecânica quântica, o hélio é o segundo átomo mais simples de modelar, depois do átomo de hidrogênio. O hélio é composto de dois elétrons em orbitais atômicos em torno de um núcleo contendo dois prótons e (geralmente) dois nêutrons. Como na mecânica newtoniana, nenhum sistema que consiste em mais de duas partículas pode ser resolvido com uma abordagem matemática analítica exata (consulte o problema dos 3 corpos) e o hélio não é exceção. Assim, métodos matemáticos numéricos são necessários, mesmo para resolver o sistema de um núcleo e dois elétrons. Esses métodos de química computacional têm sido usados para criar uma imagem da mecânica quântica da ligação do elétron do hélio que é precisa dentro de < 2% do valor correto, em poucos passos computacionais. Tais modelos mostram que cada elétron no hélio protege parcialmente o núcleo do outro, de modo que a carga nuclear efetiva Zeff que cada elétron vê é cerca de 1,69 unidades, não as 2 acusações de um clássico "bare" núcleo de hélio.
Estabilidade relacionada do núcleo de hélio-4 e da camada de elétrons
O núcleo do átomo de hélio-4 é idêntico a uma partícula alfa. Experimentos de dispersão de elétrons de alta energia mostram que sua carga diminui exponencialmente a partir de um máximo em um ponto central, exatamente como a densidade de carga da própria nuvem de elétrons do hélio. Essa simetria reflete uma física subjacente semelhante: o par de nêutrons e o par de prótons no núcleo do hélio obedecem às mesmas regras da mecânica quântica que o par de elétrons do hélio (embora as partículas nucleares estejam sujeitas a uma estrutura nuclear diferente). potencial de ligação), de modo que todos esses férmions ocupem totalmente os orbitais 1s em pares, nenhum deles possuindo momento angular orbital e cada um cancelando o spin intrínseco do outro. Adicionar outra dessas partículas exigiria momento angular e liberaria substancialmente menos energia (na verdade, nenhum núcleo com cinco nucleons é estável). Esse arranjo é, portanto, energeticamente extremamente estável para todas essas partículas, e essa estabilidade é responsável por muitos fatos cruciais sobre o hélio na natureza.
Por exemplo, a estabilidade e a baixa energia do estado da nuvem de elétrons no hélio são responsáveis pela inércia química do elemento e também pela falta de interação dos átomos de hélio entre si, produzindo os pontos de fusão e ebulição mais baixos do todos os elementos.
De maneira semelhante, a estabilidade energética particular do núcleo de hélio-4, produzida por efeitos semelhantes, explica a facilidade de produção de hélio-4 em reações atômicas que envolvem emissão ou fusão de partículas pesadas. Algum hélio-3 estável (dois prótons e um nêutron) é produzido em reações de fusão do hidrogênio, mas é uma fração muito pequena comparada ao hélio-4 altamente favorável.
A estabilidade incomum do núcleo de hélio-4 também é importante cosmologicamente: ela explica o fato de que nos primeiros minutos após o Big Bang, como a "sopa" de prótons e nêutrons livres que haviam sido inicialmente criados em uma proporção de cerca de 6:1 resfriados ao ponto em que a ligação nuclear era possível, quase todos os primeiros núcleos atômicos compostos a se formar eram núcleos de hélio-4. Devido à ligação relativamente forte dos núcleos de hélio-4, sua produção consumiu quase todos os nêutrons livres em poucos minutos, antes que eles pudessem decair beta e, portanto, poucos nêutrons estavam disponíveis para formar átomos mais pesados, como lítio, berílio ou boro. A ligação nuclear do hélio-4 por núcleo é mais forte do que em qualquer um desses elementos (ver nucleogênese e energia de ligação) e, portanto, uma vez que o hélio foi formado, nenhum impulso energético estava disponível para fazer os elementos 3, 4 e 5. É pouco energeticamente favorável para o hélio se fundir no próximo elemento com uma energia mais baixa por núcleon, o carbono. No entanto, devido à falta de elementos intermediários, esse processo requer que três núcleos de hélio batam um no outro quase simultaneamente (ver processo alfa triplo). Portanto, não houve tempo para a formação significativa de carbono nos poucos minutos após o Big Bang, antes que o universo em expansão inicial esfriasse até o ponto de temperatura e pressão em que a fusão do hélio ao carbono não era mais possível. Isso deixou o universo primitivo com uma proporção muito semelhante de hidrogênio/hélio como é observado hoje (3 partes de hidrogênio para 1 parte de hélio-4 em massa), com quase todos os nêutrons do universo presos em hélio-4.
Todos os elementos mais pesados (incluindo aqueles necessários para planetas rochosos como a Terra, e para a base de carbono ou outra forma de vida) foram criados desde o Big Bang em estrelas que eram quentes o suficiente para fundir o próprio hélio. Todos os elementos, exceto o hidrogênio e o hélio, representam hoje apenas 2% da massa de matéria atômica no universo. O hélio-4, por outro lado, compõe cerca de 23% da matéria comum do universo – quase toda a matéria comum que não é hidrogênio.
Fases de gás e plasma
O hélio é o segundo gás nobre menos reativo depois do néon e, portanto, o segundo menos reativo de todos os elementos. É quimicamente inerte e monoatômico em todas as condições padrão. Por causa da massa molar (atômica) relativamente baixa do hélio, sua condutividade térmica, calor específico e velocidade do som na fase gasosa são todos maiores do que qualquer outro gás, exceto o hidrogênio. Por essas razões e pelo pequeno tamanho das moléculas monoatômicas do hélio, o hélio se difunde através dos sólidos a uma taxa três vezes maior que a do ar e cerca de 65% maior que a do hidrogênio.
O hélio é o gás monoatômico menos solúvel em água e um dos menos solúveis em água de qualquer gás (CF4, SF6 e C4F8 têm solubilidades de fração molar mais baixas: 0,3802, 0,4394 e 0,2372 x2/10−5, respectivamente, contra hélio's 0,70797 x2/10−5) e hélio' s índice de refração é mais próximo da unidade do que o de qualquer outro gás. O hélio tem um coeficiente Joule-Thomson negativo em temperaturas ambientes normais, o que significa que ele aquece quando se expande livremente. Somente abaixo de sua temperatura de inversão Joule-Thomson (de cerca de 32 a 50 K a 1 atmosfera) ele esfria após a expansão livre. Uma vez pré-resfriado abaixo dessa temperatura, o hélio pode ser liquefeito por meio do resfriamento por expansão.
A maior parte do hélio extraterrestre é plasma em estrelas, com propriedades bastante diferentes das do hélio atômico. Em um plasma, os elétrons do hélio não estão ligados ao seu núcleo, resultando em uma condutividade elétrica muito alta, mesmo quando o gás está apenas parcialmente ionizado. As partículas carregadas são altamente influenciadas por campos magnéticos e elétricos. Por exemplo, no vento solar junto com o hidrogênio ionizado, as partículas interagem com a magnetosfera da Terra, dando origem às correntes de Birkeland e à aurora.
Fase líquida

Ao contrário de qualquer outro elemento, o hélio permanecerá líquido até o zero absoluto em pressões normais. Este é um efeito direto da mecânica quântica: especificamente, a energia do ponto zero do sistema é muito alta para permitir o congelamento. O hélio sólido requer uma temperatura de 1–1,5 K (cerca de −272 °C ou −457 °F) a cerca de 25 bar (2,5 MPa) de pressão. Muitas vezes é difícil distinguir o hélio sólido do líquido, pois o índice de refração das duas fases é quase o mesmo. O sólido tem um ponto de fusão agudo e uma estrutura cristalina, mas é altamente compressível; aplicar pressão em um laboratório pode diminuir seu volume em mais de 30%. Com um módulo de volume de cerca de 27 MPa, é aproximadamente 100 vezes mais compressível que a água. O hélio sólido tem uma densidade de 0,214±0,006 g/cm3 a 1,15 K e 66 atm; a densidade projetada a 0 K e 25 bar (2,5 MPa) é 0,187±0.009 g/cm3. Em temperaturas mais altas, o hélio solidificará com pressão suficiente. À temperatura ambiente, isso requer cerca de 114.000 atm.
Hélio I
Abaixo do ponto de ebulição de 4,22 K (−268,93 °C; −452,07 °F) e acima do ponto lambda de 2,1768 K (−270,9732 °C; −455,7518 °F), o isótopo hélio-4 existe em um estado normal estado líquido incolor, chamado hélio I. Como outros líquidos criogênicos, o hélio I ferve quando é aquecido e se contrai quando sua temperatura é reduzida. Abaixo do ponto lambda, no entanto, o hélio não ferve e se expande à medida que a temperatura diminui ainda mais.
O hélio I tem um índice de refração semelhante ao gás de 1,026, o que torna sua superfície tão difícil de ver que flutuadores de isopor são frequentemente usados para mostrar onde está a superfície. Este líquido incolor tem uma viscosidade muito baixa e uma densidade de 0,145–0,125 g/mL (entre cerca de 0 e 4 K), que é apenas um quarto do valor esperado da física clássica. A mecânica quântica é necessária para explicar essa propriedade e, portanto, ambos os estados do hélio líquido (hélio I e hélio II) são chamados de fluidos quânticos, o que significa que exibem propriedades atômicas em escala macroscópica. Isso pode ser um efeito de seu ponto de ebulição estar tão próximo do zero absoluto, impedindo que o movimento molecular aleatório (energia térmica) mascare as propriedades atômicas.
Hélio II
O hélio líquido abaixo de seu ponto lambda (chamado hélio II) exibe características muito incomuns. Devido à sua alta condutividade térmica, quando ferve, não borbulha, mas evapora diretamente de sua superfície. O hélio-3 também possui uma fase superfluida, mas apenas em temperaturas muito mais baixas; como resultado, menos se sabe sobre as propriedades do isótopo.

O hélio II é um superfluido, um estado mecânico quântico (ver: fenômenos quânticos macroscópicos) de matéria com propriedades estranhas. Por exemplo, quando flui através de capilares tão finos quanto 10−7 a 10−8 m, não tem viscosidade mensurável. No entanto, quando as medições foram feitas entre dois discos em movimento, observou-se uma viscosidade comparável à do hélio gasoso. A teoria atual explica isso usando o modelo de dois fluidos para o hélio II. Neste modelo, o hélio líquido abaixo do ponto lambda é visto como contendo uma proporção de átomos de hélio em um estado fundamental, que são superfluidos e fluem com viscosidade exatamente zero, e uma proporção de átomos de hélio em um estado excitado, que se comportam mais como um fluido comum.
No efeito fonte, é construída uma câmara conectada a um reservatório de hélio II por um disco sinterizado através do qual o hélio superfluido vaza facilmente, mas através do qual o hélio não superfluido não pode passar. Se o interior do recipiente for aquecido, o hélio superfluido muda para hélio não superfluido. A fim de manter a fração de equilíbrio do hélio superfluido, o hélio superfluido vaza e aumenta a pressão, fazendo com que o líquido saia do recipiente.
A condutividade térmica do hélio II é maior que a de qualquer outra substância conhecida, um milhão de vezes a do hélio I e várias centenas de vezes a do cobre. Isso ocorre porque a condução de calor ocorre por um mecanismo quântico excepcional. A maioria dos materiais que conduzem bem o calor tem uma banda de valência de elétrons livres que servem para transferir o calor. O hélio II não tem essa banda de valência, mas conduz bem o calor. O fluxo de calor é governado por equações semelhantes à equação de onda usada para caracterizar a propagação do som no ar. Quando o calor é introduzido, ele se move a 20 metros por segundo a 1,8 K através do hélio II como ondas em um fenômeno conhecido como segundo som.
O hélio II também exibe um efeito rastejante. Quando uma superfície ultrapassa o nível de hélio II, o hélio II se move ao longo da superfície, contra a força da gravidade. O hélio II escapará de um recipiente que não está selado arrastando-se pelas laterais até atingir uma região mais quente onde evapora. Ele se move em um filme de 30 nm de espessura, independentemente do material da superfície. Este filme é chamado de filme de Rollin e recebeu o nome do homem que primeiro caracterizou essa característica, Bernard V. Rollin. Como resultado desse comportamento rastejante e da capacidade do hélio II de vazar rapidamente por pequenas aberturas, é muito difícil confiná-lo. A menos que o recipiente seja cuidadosamente construído, o hélio II se arrastará pelas superfícies e pelas válvulas até chegar a algum lugar mais quente, onde evaporará. As ondas que se propagam através de um filme de Rollin são regidas pela mesma equação que as ondas de gravidade em águas rasas, mas, em vez da gravidade, a força restauradora é a força de van der Waals. Essas ondas são conhecidas como terceiro som.
Isótopos
Existem nove isótopos conhecidos de hélio, dos quais dois, hélio-3 e hélio-4, são estáveis. Na atmosfera da Terra, um átomo é 3
Ele para cada milhão que são 4
Ele. Ao contrário da maioria dos elementos, a abundância isotópica do hélio varia muito por origem, devido aos diferentes processos de formação. O isótopo mais comum, o hélio-4, é produzido na Terra pelo decaimento alfa de elementos radioativos mais pesados; as partículas alfa que emergem são núcleos de hélio-4 totalmente ionizados. O hélio-4 é um núcleo excepcionalmente estável porque seus núcleos são arranjados em conchas completas. Também foi formado em enormes quantidades durante a nucleossíntese do Big Bang.
O hélio-3 está presente na Terra apenas em quantidades vestigiais. A maior parte está presente desde a formação da Terra, embora alguns caiam na Terra presos em poeira cósmica. Traços também são produzidos pelo decaimento beta do trítio. As rochas da crosta terrestre têm proporções de isótopos variando até um fator de dez, e essas proporções podem ser usadas para investigar a origem das rochas e a composição do manto da Terra. 3
Ele é muito mais abundante nas estrelas como produto da fusão nuclear. Assim, no meio interestelar, a proporção de 3
Ele para 4
Ele é cerca de 100 vezes maior do que na Terra. O material extraplanetário, como o regolito lunar e asteróide, possui vestígios de hélio-3 por ser bombardeado por ventos solares. A superfície da Lua contém hélio-3 em concentrações da ordem de 10 ppb, muito superiores aos cerca de 5 ppt encontrados na atmosfera terrestre. Várias pessoas, começando com Gerald Kulcinski em 1986, propuseram explorar a lua, minerar regolito lunar e usar o hélio-3 para fusão.
O hélio-4 líquido pode ser resfriado a cerca de 1 K (−272,15 °C; −457,87 °F) usando resfriamento evaporativo em um pote de 1-K. O resfriamento semelhante do hélio-3, que tem um ponto de ebulição mais baixo, pode atingir cerca de 0,2 kelvin em um refrigerador de hélio-3. Misturas iguais de líquidos 3
Ele e 4
Ele abaixo de 0,8 K se separa em duas fases imiscíveis devido à sua dissimilaridade (eles seguem diferentes estatísticas quânticas: átomos de hélio-4 são bósons enquanto átomos de hélio-3 são férmions). Os refrigeradores de diluição usam essa imiscibilidade para atingir temperaturas de alguns milikelvins.
É possível produzir isótopos de hélio exóticos, que se decompõem rapidamente em outras substâncias. O isótopo de hélio pesado de vida mais curta é o hélio-10 não ligado com uma meia-vida de 2.6(4)×10−22 s. O hélio-6 decai emitindo uma partícula beta e tem uma meia-vida de 0,8 segundo. Hélio-7 e hélio-8 são criados em certas reações nucleares. Hélio-6 e hélio-8 são conhecidos por exibir um halo nuclear.
Propriedades
Tabela de propriedades térmicas e físicas do gás hélio à pressão atmosférica:
| Temperatura (K) | Densidade (kg/m^3) | Calor específico (kJ/kg °C) | Viscosidade dinâmica (kg/m s) | Viscosidade kinemática (m^2/s) | Condutividade térmica (W/m °C) | Difusividade térmica (m^2/s) | Número de Prandtl |
| 100. | 5.193 | 9.63E-06 | 1.98E-05 | 0,073 | 2.89E-05 | 0,686 | |
| 120 | 0,406 | 5.193 | 1.07E-05 | 2.64E-05 | 0,0819 | 3.88E-05 | 0,679 |
| 144 | 0,379 | 5.193 | 1.26E-05 | 3.71E-05 | 0,0928 | 5.28E-05 | 0 |
| 200 | 0,2435 | 5.193 | 1.57E-05 | 6.44E-05 | 0.1177 | 9.29E-05 | 0,69 |
| 255 | 0,1906 | 5.193 | 1.82E-05 | 9.55E-05 | 0,1357 | 1.37 milhões de ecus | 0 |
| 366 | 0,1328 | 5.193 | 2.31E-05 | 1.74 E-04 | 0,1691 | 2.45E04 | 0.71 |
| 477 | 0.10204 | 5.193 | 2.75E-05 | 2.69E04 | 0,197 | 3.72E04 | 0.72 |
| 589 | 0,082 | 5.193 | 3.11E-05 | 3.76E04 | 0,225 | 5.22. | 0.72 |
| 700 | 0,07032 | 5.193 | 3.48E-05 | 4.94E04 | 0,251 | 6.66E-04 | 0.72 |
| 800 | 0,06023 | 5.193 | 3.82E-05 | 6.34E04 | 0,275 | 8.77 E-04 | 0.72 |
| 900 | 0,05451 | 5.193 | 4.14E-05 | 7.59E-04 | 0,3 | 1.14E-03 | 0,687 |
| 1000 | 5.193 | 4.46E-05 | 9.14E-04 | 0,54 | 1.40E-03 | 0.654 |
Compostos
O hélio tem valência zero e é quimicamente não reativo em todas as condições normais. É um isolante elétrico, a menos que seja ionizado. Assim como os outros gases nobres, o hélio possui níveis de energia metaestáveis que permitem que ele permaneça ionizado em uma descarga elétrica com tensão abaixo de seu potencial de ionização. O hélio pode formar compostos instáveis, conhecidos como excímeros, com tungstênio, iodo, flúor, enxofre e fósforo quando é submetido a uma descarga incandescente, a bombardeio de elétrons ou reduzido a plasma por outros meios. Os compostos moleculares HeNe, HgHe10 e WHe2, e os íons moleculares He+
2< /span>, Ele2+
< sub style="font-size:inherit;line-height:inherit;vertical-align:baseline">2, HeH+, e HeD+
foram criados dessa maneira. HeH+ também é estável em seu estado fundamental, mas é extremamente reativo - é o ácido de Brønsted mais forte conhecido e, portanto, pode existir apenas isoladamente, pois protonará qualquer molécula ou contraânion com o qual entrar em contato. Essa técnica também produziu a molécula neutra He2, que possui um grande número de sistemas de bandas, e HgHe, que aparentemente é mantido unido apenas por forças de polarização.
Compostos de Van der Waals de hélio também podem ser formados com gás hélio criogênico e átomos de alguma outra substância, como LiHe e He2.
Teoricamente, outros compostos verdadeiros podem ser possíveis, como o fluorohidreto de hélio (HHeF), que seria análogo ao HArF, descoberto em 2000. Os cálculos mostram que dois novos compostos contendo uma ligação hélio-oxigênio podem ser estáveis. Duas novas espécies moleculares, previstas usando a teoria, CsFHeO e N(CH3)4FHeO, são derivadas de um ânion FHeO- metaestável teorizado pela primeira vez em 2005 por um grupo de Taiwan. Se confirmado por experimento, o único elemento restante sem compostos estáveis conhecidos seria o neon.
Os átomos de hélio foram inseridos nas moléculas ocas de carbono (os fulerenos) por aquecimento sob alta pressão. As moléculas de fulereno endoédricas formadas são estáveis em altas temperaturas. Quando os derivados químicos desses fulerenos são formados, o hélio fica no interior. Se o hélio-3 for usado, ele pode ser facilmente observado por espectroscopia de ressonância magnética nuclear de hélio. Muitos fulerenos contendo hélio-3 foram relatados. Embora os átomos de hélio não estejam ligados por ligações covalentes ou iônicas, essas substâncias têm propriedades distintas e uma composição definida, como todos os compostos químicos estequiométricos.
Sob altas pressões, o hélio pode formar compostos com vários outros elementos. Cristais de clatrato de hélio-nitrogênio (He(N2)11) cresceram à temperatura ambiente a pressões ca. 10 GPa em uma célula bigorna de diamante. O eletreto isolante Na2He demonstrou ser termodinamicamente estável a pressões acima de 113 GPa. Tem uma estrutura de fluorita.
Ocorrência e produção
Abundância natural
Embora seja raro na Terra, o hélio é o segundo elemento mais abundante no Universo conhecido, constituindo 23% da sua massa bariónica. Apenas o hidrogênio é mais abundante. A grande maioria do hélio foi formada pela nucleossíntese do Big Bang um a três minutos após o Big Bang. Como tal, as medições de sua abundância contribuem para os modelos cosmológicos. Nas estrelas, é formado pela fusão nuclear do hidrogênio nas reações em cadeia próton-próton e no ciclo CNO, parte da nucleossíntese estelar.
Na atmosfera da Terra, a concentração de hélio em volume é de apenas 5,2 partes por milhão. A concentração é baixa e razoavelmente constante, apesar da produção contínua de novo hélio porque a maior parte do hélio na atmosfera da Terra escapa para o espaço por vários processos. Na heterosfera da Terra, uma parte da atmosfera superior, o hélio e outros gases mais leves são os elementos mais abundantes.
A maior parte do hélio na Terra é resultado do decaimento radioativo. O hélio é encontrado em grandes quantidades em minerais de urânio e tório, incluindo uraninita e suas variedades cleveita e pechblenda, carnotita e monazita (um nome de grupo; "monazita" geralmente se refere a monazita-(Ce)), porque emitem partículas alfa (núcleos de hélio, He2+) às quais os elétrons se combinam imediatamente assim que a partícula é parada pela rocha. Desta forma, cerca de 3.000 toneladas métricas de hélio são geradas por ano em toda a litosfera. Na crosta terrestre, a concentração de hélio é de 8 partes por bilhão. Na água do mar, a concentração é de apenas 4 partes por trilhão. Há também pequenas quantidades em fontes minerais, gás vulcânico e ferro meteórico. Como o hélio fica preso no subsolo em condições que também aprisionam o gás natural, as maiores concentrações naturais de hélio no planeta são encontradas no gás natural, do qual é extraída a maior parte do hélio comercial. A concentração varia em uma ampla faixa de alguns ppm a mais de 7% em um pequeno campo de gás no condado de San Juan, Novo México.
Em 2021, as reservas mundiais de hélio foram estimadas em 31 bilhões de metros cúbicos, sendo um terço delas no Catar. Em 2015 e 2016, foram anunciadas reservas prováveis adicionais sob as Montanhas Rochosas na América do Norte e no Rift da África Oriental.
Extração e distribuição modernas
Para uso em larga escala, o hélio é extraído por destilação fracionada do gás natural, que pode conter até 7% de hélio. Como o hélio tem um ponto de ebulição mais baixo do que qualquer outro elemento, baixa temperatura e alta pressão são usadas para liquefazer quase todos os outros gases (principalmente nitrogênio e metano). O gás hélio bruto resultante é purificado por exposições sucessivas a temperaturas baixas, nas quais quase todo o nitrogênio restante e outros gases são precipitados da mistura gasosa. O carvão ativado é usado como uma etapa final de purificação, geralmente resultando em 99,995% de hélio grau A puro. A principal impureza no hélio Grau A é o neon. Em uma etapa final de produção, a maior parte do hélio produzido é liquefeito por meio de um processo criogênico. Isso é necessário para aplicações que requerem hélio líquido e também permite que os fornecedores de hélio reduzam o custo de transporte de longa distância, já que os maiores contêineres de hélio líquido têm mais de cinco vezes a capacidade dos maiores reboques de tubo de hélio gasoso.
Em 2008, aproximadamente 169 milhões de metros cúbicos padrão (SCM) de hélio foram extraídos do gás natural ou retirados das reservas de hélio com aproximadamente 78% dos Estados Unidos, 10% da Argélia e a maior parte do restante da Rússia, Polônia e Catar. Em 2013, os aumentos na produção de hélio no Catar (sob a empresa Qatargas administrada pela Air Liquide) aumentaram a fração do Catar na produção mundial de hélio para 25% e o tornaram o segundo maior exportador depois dos Estados Unidos. Um depósito estimado de 54 bilhões de pés cúbicos (1,5×109 m3) de hélio foi encontrado na Tanzânia em 2016. Uma fábrica de hélio em grande escala foi inaugurada em Ningxia, China, em 2020.
Nos Estados Unidos, a maior parte do hélio é extraída do gás natural de Hugoton e dos campos de gás próximos em Kansas, Oklahoma, e do campo Panhandle, no Texas. Grande parte desse gás já foi enviado por gasoduto para a Reserva Nacional de Hélio, mas desde 2005 essa reserva está sendo esgotada e vendida, e espera-se que seja amplamente esgotada até 2021, sob a Lei de Administração e Administração Responsável de Hélio de outubro de 2013 (H.R. 527).
A difusão de gás natural bruto através de membranas semipermeáveis especiais e outras barreiras é outro método para recuperar e purificar o hélio. Em 1996, os EUA tinham reservas de hélio comprovadas, em tais complexos de poços de gás, de cerca de 147 bilhões de pés cúbicos padrão (4,2 bilhões de SCM). Nas taxas de uso naquela época (72 milhões de SCM por ano nos EUA; veja o gráfico abaixo), isso teria sido hélio suficiente para cerca de 58 anos de uso nos EUA e menos do que isso (talvez 80% do tempo) no mundo taxas de uso, embora os fatores de economia e processamento tenham impacto nos números de reservas efetivas.
O hélio deve ser extraído do gás natural porque está presente no ar em apenas uma fração do néon, mas a demanda por ele é muito maior. Estima-se que, se toda a produção de néon fosse reequipada para economizar hélio, 0,1% da demanda mundial de hélio seria atendida. Da mesma forma, apenas 1% das demandas mundiais de hélio poderiam ser atendidas com o reequipamento de todas as plantas de destilação de ar. O hélio pode ser sintetizado pelo bombardeio de lítio ou boro com prótons de alta velocidade, ou pelo bombardeio de lítio com deutérios, mas esses processos são um método de produção completamente antieconômico.
O hélio está disponível comercialmente na forma líquida ou gasosa. Como líquido, pode ser fornecido em pequenos recipientes isolados chamados dewars, que comportam até 1.000 litros de hélio, ou em grandes recipientes ISO com capacidades nominais de até 42 m3 (cerca de 11.000 U.S. galões). Na forma gasosa, pequenas quantidades de hélio são fornecidas em cilindros de alta pressão com capacidade de até 8 m3 (aprox. 282 pés cúbicos padrão), enquanto grandes quantidades de gás de alta pressão são fornecidas em tubos reboques com capacidades de até 4.860 m3 (aprox. 172.000 pés cúbicos padrão).
Defensores da conservação
De acordo com os conservacionistas do hélio, como o físico ganhador do Prêmio Nobel Robert Coleman Richardson, escrevendo em 2010, o preço de mercado livre do hélio contribuiu para o "desperdício" uso (por exemplo, para balões de hélio). Os preços na década de 2000 foram reduzidos pela decisão do Congresso dos EUA de vender o grande estoque de hélio do país até 2015. De acordo com Richardson, o preço precisava ser multiplicado por 20 para eliminar o desperdício excessivo de hélio. No artigo Stop swandering hélio publicado em 2012, também foi proposta a criação de uma Agência Internacional de Hélio que construiria um mercado sustentável para "esta preciosa commodity".
Aplicativos
Estimativa 2014 U.S. uso de hélio fracionário por categoria. O uso total é de 34 milhões de metros cúbicos.
Embora os balões sejam talvez o uso mais conhecido de hélio, eles são uma parte menor de todo o uso de hélio. O hélio é usado para muitas finalidades que requerem algumas de suas propriedades únicas, como seu baixo ponto de ebulição, baixa densidade, baixa solubilidade, alta condutividade térmica ou inércia. Da produção total mundial de hélio em 2014 de cerca de 32 milhões de kg (180 milhões de metros cúbicos padrão) de hélio por ano, o maior uso (cerca de 32% do total em 2014) é em aplicações criogênicas, a maioria das quais envolve o resfriamento dos ímãs supercondutores em scanners MRI médicos e espectrômetros NMR. Outros usos importantes foram sistemas de pressurização e purga, soldagem, manutenção de atmosferas controladas e detecção de vazamentos. Outros usos por categoria foram frações relativamente menores.
Ambientes controlados
O hélio é usado como gás protetor no cultivo de cristais de silício e germânio, na produção de titânio e zircônio e na cromatografia gasosa, porque é inerte. Por causa de sua inércia, natureza térmica e calórica perfeita, alta velocidade do som e alto valor da taxa de capacidade de calor, também é útil em túneis de vento supersônicos e instalações de impulso.
Soldagem a arco de tungstênio a gás
O hélio é usado como gás de proteção em processos de soldagem a arco em materiais que em temperaturas de soldagem são contaminados e enfraquecidos pelo ar ou nitrogênio. Vários gases de proteção inertes são usados na soldagem a arco de tungstênio a gás, mas o hélio é usado em vez do argônio mais barato, especialmente para materiais de soldagem com maior condutividade térmica, como alumínio ou cobre.
Usos menores
Detecção de vazamento industrial
Uma aplicação industrial para o hélio é a detecção de vazamentos. Como o hélio se difunde através de sólidos três vezes mais rápido que o ar, ele é usado como gás traçador para detectar vazamentos em equipamentos de alto vácuo (como tanques criogênicos) e recipientes de alta pressão. O objeto testado é colocado em uma câmara, que é então evacuada e preenchida com hélio. O hélio que escapa pelos vazamentos é detectado por um dispositivo sensível (espectrômetro de massa de hélio), mesmo com taxas de vazamento tão pequenas quanto 10−9 mbar·L/s (10−10< /sup> Pa·m3/s). O procedimento de medição é normalmente automático e é chamado de teste integral de hélio. Um procedimento mais simples é encher o objeto testado com hélio e procurar manualmente por vazamentos com um dispositivo portátil.
Vazamentos de hélio através de rachaduras não devem ser confundidos com permeação de gás através de um material a granel. Embora o hélio tenha documentado constantes de permeação (portanto, uma taxa de permeação calculável) através de vidros, cerâmicas e materiais sintéticos, gases inertes como o hélio não irão permear a maioria dos metais a granel.
Voo
Por ser mais leve que o ar, dirigíveis e balões são inflados com hélio para sustentação. Enquanto o gás hidrogênio é mais flutuante e escapa permeando através de uma membrana a uma taxa menor, o hélio tem a vantagem de ser não inflamável e, de fato, retardador de fogo. Outro uso menor é em foguetes, onde o hélio é usado como meio de expansão para encher tanques de propelente de foguetes em vôo e para condensar hidrogênio e oxigênio para fazer combustível de foguete. Também é usado para purgar combustível e oxidante de equipamentos de apoio terrestre antes do lançamento e para pré-resfriar hidrogênio líquido em veículos espaciais. Por exemplo, o foguete Saturn V usado no programa Apollo precisou de cerca de 370.000 m3 (13 milhões de pés cúbicos) de hélio para ser lançado.
Pequenos usos comerciais e recreativos
O hélio como gás respiratório não tem propriedades narcóticas, então misturas de hélio como trimix, heliox e heliair são usadas para mergulho profundo para reduzir os efeitos da narcose, que pioram com o aumento da profundidade. À medida que a pressão aumenta com a profundidade, a densidade do gás respiratório também aumenta, e o baixo peso molecular do hélio reduz consideravelmente o esforço respiratório ao diminuir a densidade da mistura. Isso reduz o número de Reynolds do fluxo, levando a uma redução do fluxo turbulento e a um aumento do fluxo laminar, que requer menos trabalho respiratório. Em profundidades abaixo de 150 metros (490 pés), os mergulhadores que respiram misturas de hélio-oxigênio começam a sentir tremores e diminuição da função psicomotora, sintomas da síndrome nervosa de alta pressão. Esse efeito pode ser combatido até certo ponto adicionando uma quantidade de gás narcótico, como hidrogênio ou nitrogênio, a uma mistura de hélio-oxigênio.
Os lasers de hélio-neônio, um tipo de laser de gás de baixa potência que produz um feixe vermelho, tinham várias aplicações práticas que incluíam leitores de código de barras e ponteiros a laser, antes de serem quase universalmente substituídos por lasers de diodo mais baratos.
Por sua inércia e alta condutividade térmica, transparência de nêutrons e por não formar isótopos radioativos em condições de reator, o hélio é usado como meio de transferência de calor em alguns reatores nucleares refrigerados a gás.
O hélio, misturado com um gás mais pesado como o xenônio, é útil para refrigeração termoacústica devido à alta taxa de capacidade térmica resultante e ao baixo número de Prandtl. A inércia do hélio tem vantagens ambientais sobre os sistemas de refrigeração convencionais que contribuem para a destruição do ozônio ou aquecimento global.
O hélio também é usado em algumas unidades de disco rígido.
Usos científicos
O uso de hélio reduz os efeitos de distorção das variações de temperatura no espaço entre as lentes em alguns telescópios, devido ao seu baixíssimo índice de refração. Este método é especialmente usado em telescópios solares onde um tubo de telescópio apertado a vácuo seria muito pesado.
O hélio é um gás de arraste comumente usado para cromatografia gasosa.
A idade de rochas e minerais que contêm urânio e tório pode ser estimada medindo o nível de hélio com um processo conhecido como datação por hélio.
O hélio a baixas temperaturas é usado em criogenia e em certas aplicações de criogenia. Como exemplos de aplicações, o hélio líquido é usado para resfriar certos metais a temperaturas extremamente baixas necessárias para a supercondutividade, como em ímãs supercondutores para imagens de ressonância magnética. O Grande Colisor de Hádrons no CERN usa 96 toneladas métricas de hélio líquido para manter a temperatura em 1,9 K (−271,25 °C; −456,25 °F).
Usos médicos
O hélio foi aprovado para uso médico nos Estados Unidos em abril de 2020 para humanos e animais.
Como contaminante
Embora quimicamente inerte, a contaminação com hélio prejudica a operação de sistemas microeletromecânicos (MEMS) de modo que os iPhones podem falhar.
Inalação e segurança
Efeitos
O hélio neutro em condições padrão não é tóxico, não desempenha nenhum papel biológico e é encontrado em quantidades vestigiais no sangue humano.
A velocidade do som no hélio é quase três vezes a velocidade do som no ar. Como a frequência de ressonância natural de uma cavidade cheia de gás é proporcional à velocidade do som no gás, quando o hélio é inalado, ocorre um aumento correspondente nas frequências de ressonância do trato vocal, que é o amplificador do som vocal. Este aumento na frequência de ressonância do amplificador (o trato vocal) dá uma amplificação aumentada aos componentes de alta frequência da onda sonora produzida pela vibração direta das pregas vocais, em comparação com o caso quando a caixa de voz está cheia de ar. Quando uma pessoa fala após a inalação de gás hélio, os músculos que controlam a laringe ainda se movem da mesma forma que quando a laringe está cheia de ar, portanto a frequência fundamental (às vezes chamada de pitch) produzida pela vibração direta das pregas vocais não não mude. No entanto, a amplificação preferencial de alta frequência causa uma mudança no timbre do som amplificado, resultando em uma qualidade vocal esganiçada e semelhante a um pato. O efeito oposto, diminuindo as frequências de ressonância, pode ser obtido pela inalação de um gás denso, como hexafluoreto de enxofre ou xenônio.
Perigos
A inalação de hélio pode ser perigosa se for feita em excesso, uma vez que o hélio é um asfixiante simples e, portanto, desloca o oxigênio necessário para a respiração normal. Fatalidades foram registradas, incluindo um jovem que morreu sufocado em Vancouver em 2003 e dois adultos que morreram sufocados no sul da Flórida em 2006. Em 1998, uma garota australiana de Victoria ficou inconsciente e ficou temporariamente azul após inalar todo o conteúdo de um balão de festa. A inalação de hélio diretamente de cilindros pressurizados ou mesmo de válvulas de enchimento de balões é extremamente perigosa, pois altas taxas de fluxo e pressão podem resultar em barotrauma, rompendo fatalmente o tecido pulmonar.
A morte causada por hélio é rara. O primeiro caso registrado na mídia foi o de uma garota de 15 anos do Texas que morreu em 1998 por inalação de hélio na festa de um amigo; o tipo exato de morte por hélio não foi identificado.
Nos Estados Unidos, apenas duas mortes foram relatadas entre 2000 e 2004, incluindo um homem que morreu na Carolina do Norte de barotrauma em 2002. Um jovem asfixiado em Vancouver em 2003 e um homem de 27 anos na Austrália tiveram um embolia após respirar de um cilindro em 2000. Desde então, dois adultos morreram asfixiados no sul da Flórida em 2006, e houve casos em 2009 e 2010, um de um jovem californiano que foi encontrado com um saco na cabeça, preso a um tanque de hélio, e outro adolescente na Irlanda do Norte morreu por asfixia. Em Eagle Point, Oregon, uma adolescente morreu em 2012 de barotrauma em uma festa. Uma garota de Michigan morreu de hipóxia no final do ano.
Em 4 de fevereiro de 2015, foi revelado que, durante a gravação de seu principal programa de TV em 28 de janeiro, uma integrante de 12 anos (nome omitido) do grupo feminino japonês 3B Junior sofreu uma embolia aérea, perdendo a consciência e entrando em coma como resultado de bolhas de ar bloqueando o fluxo de sangue para o cérebro, após inalar grandes quantidades de hélio como parte de um jogo. O incidente só foi tornado público uma semana depois. A equipe da TV Asahi realizou uma coletiva de imprensa de emergência para comunicar que a integrante foi levada ao hospital e apresenta sinais de reabilitação, como movimentos dos olhos e membros, mas sua consciência ainda não foi suficientemente recuperada. A polícia iniciou uma investigação devido à negligência das medidas de segurança.
Os problemas de segurança do hélio criogênico são semelhantes aos do nitrogênio líquido; suas temperaturas extremamente baixas podem resultar em queimaduras de frio, e a taxa de expansão líquido-gás pode causar explosões se nenhum dispositivo de alívio de pressão for instalado. Recipientes de gás hélio de 5 a 10 K devem ser manuseados como se contivessem hélio líquido devido à rápida e significativa expansão térmica que ocorre quando o gás hélio a menos de 10 K é aquecido até a temperatura ambiente.
Em altas pressões (mais de cerca de 20 atm ou dois MPa), uma mistura de hélio e oxigênio (heliox) pode levar à síndrome nervosa de alta pressão, uma espécie de efeito anestésico reverso; adicionar uma pequena quantidade de nitrogênio à mistura pode aliviar o problema.
Contenido relacionado
Criptoanálise
Processo endotérmico
Bomba de difusão