Gelo
Gelo é água congelada em estado sólido, normalmente formando-se em temperaturas de 32 °F, 0 °C ou 273 K ou menos. Dependendo da presença de impurezas, como partículas de solo ou bolhas de ar, pode apresentar-se transparente ou de cor branco-azulada mais ou menos opaca.
No Sistema Solar, o gelo é abundante e ocorre naturalmente desde tão perto do Sol como Mercúrio até tão longe quanto os objetos da nuvem de Oort. Além do Sistema Solar, ocorre como gelo interestelar. É abundante na superfície da Terra - particularmente nas regiões polares e acima da linha de neve - e, como uma forma comum de precipitação e deposição, desempenha um papel fundamental no ciclo da água e no clima da Terra. Ele cai como flocos de neve e granizo ou ocorre como geada, pingentes de gelo ou picos de gelo e agregados de neve como geleiras e mantos de gelo.
O gelo apresenta pelo menos dezoito fases (geometrias de empacotamento), dependendo da temperatura e da pressão. Quando a água é resfriada rapidamente (têmpera), até três tipos de gelo amorfo podem se formar, dependendo de seu histórico de pressão e temperatura. Quando resfriado lentamente, o tunelamento de prótons correlacionado ocorre abaixo de -253,15 °C (20 K, −423,67 °F) dando origem a fenômenos quânticos macroscópicos. Praticamente todo o gelo na superfície da Terra e em sua atmosfera é de uma estrutura cristalina hexagonal denotada como gelo Ih (falado como "gelo um h") com traços minúsculos de gelo cúbico, denotado como gelo Ic e, mais recentemente encontrado, inclusões Ice VII em diamantes. A transição de fase mais comum para o gelo Ih ocorre quando a água líquida é resfriada abaixo de 0 ° C (273,15 K, 32 °F) à pressão atmosférica padrão. Também pode ser depositado diretamente pelo vapor d'água, como ocorre na formação da geada. A transição do gelo para a água está derretendo e do gelo diretamente para o vapor de água é a sublimação.
O gelo é usado de várias maneiras, inclusive para resfriamento, esportes de inverno e escultura em gelo.
Propriedades físicas
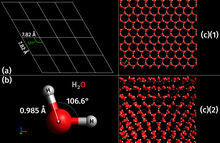
Como um sólido inorgânico cristalino de ocorrência natural com uma estrutura ordenada, o gelo é considerado um mineral. Possui uma estrutura cristalina regular baseada na molécula de água, que consiste em um único átomo de oxigênio ligado covalentemente a dois átomos de hidrogênio, ou H–O–H. No entanto, muitas das propriedades físicas da água e do gelo são controladas pela formação de pontes de hidrogênio entre os átomos adjacentes de oxigênio e hidrogênio; embora seja uma ligação fraca, é crítica no controle da estrutura da água e do gelo.
Uma propriedade incomum da água é que sua forma sólida - gelo congelado à pressão atmosférica - é aproximadamente 8,3% menos densa que sua forma líquida; isso equivale a uma expansão volumétrica de 9%. A densidade do gelo é 0,9167–0,9168 g/cm3 a 0 °C e pressão atmosférica padrão (101,325 Pa), enquanto a água tem uma densidade de 0,9998–0,999863 g/cm3 na mesma temperatura e pressão. A água líquida é mais densa, essencialmente 1,00 g/cm3, a 4 °C e começa a perder sua densidade à medida que as moléculas de água começam a formar os cristais hexagonais de gelo quando o ponto de congelamento é atingido. Isso se deve à ligação de hidrogênio que domina as forças intermoleculares, o que resulta em um empacotamento de moléculas menos compacto no sólido. A densidade do gelo aumenta ligeiramente com a diminuição da temperatura e tem um valor de 0,9340 g/cm3 a -180 °C (93 K).
Quando a água congela, aumenta de volume (cerca de 9% para água doce). O efeito da expansão durante o congelamento pode ser dramático, e a expansão do gelo é uma causa básica de intemperismo por congelamento e degelo da rocha na natureza e danos a fundações de edifícios e estradas devido ao congelamento. Também é uma causa comum de inundação de casas quando os canos de água estouram devido à pressão da expansão da água quando ela congela.
O resultado desse processo é que o gelo (em sua forma mais comum) flutua na água líquida, que é uma característica importante da biosfera da Terra. Tem sido argumentado que, sem essa propriedade, os corpos naturais de água congelariam, em alguns casos permanentemente, de baixo para cima, resultando em uma perda de vida animal e vegetal dependente do fundo na água doce e no mar. Camadas de gelo suficientemente finas permitem a passagem da luz enquanto protegem a parte inferior de condições climáticas extremas de curto prazo, como o vento frio. Isso cria um ambiente protegido para colônias de bactérias e algas. Quando a água do mar congela, o gelo é crivado de canais cheios de salmoura que sustentam organismos simpágicos como bactérias, algas, copépodes e anelídeos, que por sua vez fornecem alimento para animais como o krill e peixes especializados como o careca notothen, alimentados por sua vez por animais maiores, como pinguins imperadores e baleias minke.
Quando o gelo derrete, ele absorve tanta energia quanto seria necessário para aquecer uma massa equivalente de água em 80°C. Durante o processo de fusão, a temperatura permanece constante em 0°C. Durante a fusão, qualquer energia adicionada quebra as ligações de hidrogênio entre as moléculas de gelo (água). A energia torna-se disponível para aumentar a energia térmica (temperatura) somente depois que ligações de hidrogênio suficientes são quebradas para que o gelo possa ser considerado água líquida. A quantidade de energia consumida na quebra das pontes de hidrogênio na transição do gelo para a água é conhecida como calor de fusão.
Assim como a água, o gelo absorve luz na extremidade vermelha do espectro preferencialmente como resultado de um tom harmonioso de um trecho de ligação oxigênio-hidrogênio (O-H). Em comparação com a água, essa absorção é deslocada para energias ligeiramente mais baixas. Assim, o gelo aparece azul, com uma tonalidade ligeiramente mais esverdeada do que a água líquida. Como a absorção é cumulativa, o efeito da cor se intensifica com o aumento da espessura ou se as reflexões internas fizerem com que a luz percorra o gelo por mais tempo.
Outras cores podem aparecer na presença de impurezas que absorvem a luz, onde a impureza está ditando a cor e não o próprio gelo. Por exemplo, icebergs contendo impurezas (por exemplo, sedimentos, algas, bolhas de ar) podem aparecer marrons, cinzas ou verdes.
Como o gelo em ambientes naturais geralmente está próximo de sua temperatura de fusão, sua dureza apresenta variações de temperatura pronunciadas. Em seu ponto de fusão, o gelo tem uma dureza de Mohs de 2 ou menos, mas a dureza aumenta para cerca de 4 a uma temperatura de -44 °C (-47 °F) e para 6 a uma temperatura de -78,5 °C (-109,3 °F), o ponto de vaporização do dióxido de carbono sólido (gelo seco).
Fases
O gelo pode ser qualquer uma das 19 fases cristalinas sólidas conhecidas da água, ou em um estado sólido amorfo em várias densidades.
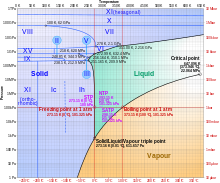
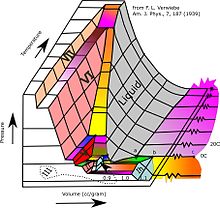
A maioria dos líquidos sob pressão elevada congela em temperaturas mais altas porque a pressão ajuda a manter as moléculas unidas. No entanto, as fortes ligações de hidrogênio na água tornam isso diferente: para algumas pressões superiores a 1 atm (0,10 MPa), a água congela a uma temperatura abaixo de 0 °C, conforme mostrado no diagrama de fases abaixo. Acredita-se que o derretimento do gelo sob altas pressões contribua para o movimento das geleiras.
Gelo, água e vapor de água podem coexistir no ponto triplo, que é exatamente 273,16 K (0,01 °C) a uma pressão de 611,657 Pa. O kelvin foi definido como 1/273,16 do diferença entre este ponto triplo e o zero absoluto, embora esta definição tenha mudado em maio de 2019. Ao contrário da maioria dos outros sólidos, o gelo é difícil de superaquecer. Em um experimento, o gelo a -3 °C foi superaquecido a cerca de 17 °C por cerca de 250 picossegundos.
Sujeito a pressões mais altas e temperaturas variáveis, o gelo pode se formar em 19 fases cristalinas conhecidas separadas. Com cuidado, pelo menos 15 dessas fases (uma das exceções conhecidas sendo o gelo X) podem ser recuperadas à pressão ambiente e baixa temperatura na forma metaestável. Os tipos são diferenciados por sua estrutura cristalina, ordenação de prótons e densidade. Existem também duas fases metaestáveis de gelo sob pressão, ambas totalmente desordenadas por hidrogênio; estes são IV e XII. Ice XII foi descoberto em 1996. Em 2006, XIII e XIV foram descobertos. Os gelos XI, XIII e XIV são formas ordenadas por hidrogênio dos gelos Ih, V e XII, respectivamente. Em 2009, o gelo XV foi encontrado em pressões extremamente altas e -143°C. Em pressões ainda mais altas, prevê-se que o gelo se torne um metal; isso foi estimado de várias maneiras para ocorrer em 1,55 TPa ou 5,62 TPa.
Assim como formas cristalinas, a água sólida pode existir em estados amorfos como água sólida amorfa (ASW) de densidades variadas. A água no meio interestelar é dominada por gelo amorfo, tornando-a provavelmente a forma mais comum de água no universo. ASW de baixa densidade (LDA), também conhecida como água vítrea hiperextinta, pode ser responsável por nuvens noctilucentes na Terra e geralmente é formada pela deposição de vapor d'água em condições de frio ou vácuo. O ASW de alta densidade (HDA) é formado pela compressão do gelo comum Ih ou LDA em pressões GPa. ASW de densidade muito alta (VHDA) é HDA ligeiramente aquecido a 160 K sob pressões de 1–2 GPa.
No espaço sideral, o gelo cristalino hexagonal (a forma predominante encontrada na Terra) é extremamente raro. Gelo amorfo é mais comum; no entanto, gelo cristalino hexagonal pode ser formado por ação vulcânica.
O gelo de uma água superiônica teorizada pode possuir duas estruturas cristalinas. Em pressões superiores a 500.000 bar (7.300.000 psi), esse gelo superiônico assumiria uma estrutura cúbica centrada no corpo. No entanto, em pressões superiores a 1.000.000 bar (15.000.000 psi), a estrutura pode mudar para uma rede cúbica de face centrada mais estável. Especula-se que o gelo superiônico poderia compor o interior de gigantes de gelo como Urano e Netuno.
| Fase | Características |
|---|---|
| Gelo amorfo | Gelo amorfo é gelo faltando estrutura de cristal. O gelo amorfo existe em quatro formas: baixa densidade (LDA) formada à pressão atmosférica, ou abaixo, média densidade (MDA), alta densidade (HDA) e muito alta densidade de gelo amorfo (VHDA), formando a pressões mais altas. LDA forma por resfriamento extremamente rápido de água líquida ("água de vidro temperado", HGW), depositando vapor de água em substratos muito frios ("água sólida amorfo", ASW) ou aquecendo formas de gelo de alta densidade na pressão ambiente ("LDA"). Recentemente, uma forma morfo de densidade média ("MDA") foi mostrada para existir, criada por gelo de moagem de bola Ih a baixas temperaturas. |
| Ih! | Gelo cristalino hexagonal normal. Praticamente todo o gelo na biosfera é gelo Ih, com excepção de uma pequena quantidade de gelo Ic. |
| IC de gelo | Uma variante cristalina cúbico metaestável de gelo. Os átomos de oxigênio são dispostos em uma estrutura de diamante. É produzido a temperaturas entre 130 e 220 K, e pode existir até 240 K, quando se transforma em gelo Ih. Pode ocasionalmente estar presente na atmosfera superior. Mais recentemente, tem sido mostrado que muitas amostras que foram descritas como gelo cúbico foram realmente empilhamento de gelo desordenado com simetria trigonal. As primeiras amostras de gelo I com simetria cúbico (ou seja, gelo cúbico) foram relatadas apenas em 2020. |
| Gelo II | Uma forma cristalina rhombohedral com estrutura altamente ordenada. Formado a partir do gelo Ih comprimindo-o à temperatura de 190-210 K. Quando aquecido, passa por transformação ao gelo III. |
| Gelo III | Um gelo cristalino tetragonal, formado por água de resfriamento até 250 K a 300 MPa. Menos densa das fases de alta pressão. Mais densa que a água. |
| Gelo IV | Uma fase rómbose metaestável. Pode ser formado por aquecimento de gelo amorfo de alta densidade lentamente a uma pressão de 810 MPa. Não se forma facilmente sem um agente nucleante. |
| Gelo V | Uma fase cristalina monoclínica. Formado por água de resfriamento a 253 K a 500 MPa. Estrutura mais complicada de todas as fases. |
| Gelo VI | Uma fase cristalina tetragonal. Formado por água de resfriamento para 270 K em 1.1 GPa. Exibe o relaxamento Debye. |
| Gelo VII | Uma fase cúbica. As posições dos átomos de hidrogénio estão desordenadas. Exibe o relaxamento Debye. As ligações de hidrogênio formam dois treliças interpenetrando. |
| Gelo VII) | Formas em cerca de 5 GPa, quando o gelo VII se torna tetragonal. |
| Gelo VIII | Uma versão mais ordenada do gelo VII, onde os átomos de hidrogênio assumem posições fixas. É formado a partir do gelo VII, refrigerando-o abaixo de 5 °C (278 K) a 2.1 GPa. |
| IX de gelo | Uma fase tetragonal. Formado gradualmente do gelo III, refrigerando-o de 208 K a 165 K, estável abaixo de 140 K e pressões entre 200 MPa e 400 MPa. Tem densidade de 1,16 g/cm3, ligeiramente superior ao gelo comum. |
| Gelo X | Gelo simétrico encomendado por prótons. Formas a pressões em torno de 70 GPa, ou talvez tão baixo quanto 30 GPa. |
| Gelo XI | Uma forma de equilíbrio ortorômbico e de baixa temperatura do gelo hexagonal. É ferroelétrico. O gelo XI é considerado a configuração mais estável do gelo Ih. |
| Gelo XII | Uma fase tetragonal, metástável, cristalina densa. É observado no espaço de fase do gelo V e gelo VI. Pode ser preparado pelo aquecimento de gelo amorfo de alta densidade de 77 K a cerca de 183 K em 810 MPa. Tem uma densidade de 1,3 g·cm-3 em 127 K (ou seja, aproximadamente 1,3 vezes mais denso do que a água). |
| Gelo XIII | Uma fase cristalina monoclínica. Formado por água de resfriamento para abaixo de 130 K a 500 MPa. A forma ordenada por prótons de gelo V. |
| Gelo XIV | Uma fase cristalina ortorômbica. Formado abaixo 118 K em 1,2 GPa. A forma ordenada por prótons de gelo XII. |
| Gelo XV | Uma forma ordenada por prótons de gelo VI formada por água de resfriamento para cerca de 80-108 K em 1.1 GPa. |
| Gelo XVI | A forma cristalina menos densa de água, topologicamente equivalente à estrutura vazia de hidratos de clatrato de sII. |
| Gelo quadrado | Os cristais de gelo quadrados formam-se à temperatura ambiente quando espremidos entre duas camadas de grafeno. O material foi uma nova fase cristalina do gelo quando foi relatado pela primeira vez em 2014. A pesquisa derivada da descoberta anterior de que o vapor de água e a água líquida poderiam passar por folhas laminadas de óxido de grafeno, ao contrário de moléculas menores, como o hélio. O efeito é pensado para ser impulsionado pela força van der Waals, que pode envolver mais de 10.000 atmosferas de pressão. |
| Gelo XVII | Uma fase cristalina hexagonal porosa com canais helicoidais, com densidade próxima à do gelo XVI. Formado colocando gelo cheio de hidrogênio em um vácuo e aumentando a temperatura até que as moléculas de hidrogênio escape. |
| Gelo XVIII | Uma forma de água também conhecida como água superiônica ou gelo superiônico em que os íons de oxigênio desenvolvem uma estrutura cristalina enquanto os íons de hidrogênio se movem livremente. |
| Gelo XIX | Outra fase relacionada ao gelo VI formado por água de resfriamento para cerca de 100 K em aproximadamente 2 GPa. |
Propriedades de atrito
O baixo coeficiente de atrito ("escorregadio") do gelo foi atribuído à pressão de um objeto que entra em contato com o gelo, derretendo uma fina camada de gelo e permitindo que o objeto deslize a superfície. Por exemplo, a lâmina de um patim de gelo, ao exercer pressão sobre o gelo, derreteria uma fina camada, proporcionando lubrificação entre o gelo e a lâmina. Essa explicação, chamada de "derretimento por pressão", teve origem no século XIX. No entanto, não leva em conta a patinação em temperaturas de gelo inferiores a -4 °C (25 °F; 269 K), que geralmente são patinadas. Além disso, o efeito da fusão sob pressão é muito pequeno para explicar o atrito reduzido comumente experimentado.
Uma segunda teoria que descreve o coeficiente de fricção do gelo sugeriu que as moléculas de gelo na interface não podem se ligar adequadamente às moléculas da massa de gelo abaixo (e, portanto, são livres para se mover como moléculas de água líquida). Essas moléculas permanecem em estado semilíquido, proporcionando lubrificação independentemente da pressão contra o gelo exercida por qualquer objeto. No entanto, o significado desta hipótese é contestado por experimentos que mostram um alto coeficiente de fricção para gelo usando microscopia de força atômica.
Uma terceira teoria é o "aquecimento por fricção", que sugere que o atrito do material é a causa do derretimento da camada de gelo. No entanto, esta teoria não explica suficientemente por que o gelo é escorregadio quando está parado, mesmo em temperaturas abaixo de zero.
Uma teoria abrangente de fricção no gelo leva em consideração todos os mecanismos de fricção mencionados acima. Este modelo permite a estimativa quantitativa do coeficiente de atrito do gelo contra vários materiais em função da temperatura e da velocidade de deslizamento. Em condições típicas relacionadas a esportes de inverno e pneus de um veículo no gelo, o derretimento de uma fina camada de gelo devido ao aquecimento por fricção é a principal razão para o escorregadio. O mecanismo que controla as propriedades friccionais do gelo ainda é uma área ativa de estudo científico.
Formação natural
O termo que descreve coletivamente todas as partes da superfície da Terra onde a água está em forma congelada é a criosfera. para o ciclo da água. Geleiras e mochilas de neve são um importante mecanismo de armazenamento para água doce; Com o tempo, eles podem sublimar ou derreter. A neve é uma fonte importante de água fresca sazonal. A organização meteorológica mundial define vários tipos de gelo, dependendo da origem, tamanho, forma, influência e assim por diante. Os hidratos de clatrato são formas de gelo que contêm moléculas de gás presas dentro de sua rede de cristal.
nos oceanos
O gelo encontrado no mar pode estar na forma de gelo flutuando na água, gelo rápido fixado a uma costa ou ancorar gelo se preso ao fundo do mar. O gelo que bezerros (quebra) de uma plataforma de gelo ou geleira pode se tornar um iceberg. O gelo do mar pode ser forçado juntos por correntes e ventos para formar cristas de pressão de até 12 metros (39 pés) de altura. A navegação através de áreas de gelo marinho ocorre em aberturas chamadas " Polynyas " OR " Leads " ou requer o uso de um navio especial chamado An " Icebreaker "
em terra e estruturas
O gelo na terra varia do tipo maior chamado de "placa de gelo" para calotas de gelo menores e campos de gelo para geleiras e correntes de gelo para a linha de neve e campos de neve.
Aufeis é um gelo em camadas que se forma nos vales árticos e subárticos. O gelo, congelado no leito do rio, bloqueia a descarga normal das águas subterrâneas e faz com que o lençol freático local suba, resultando na descarga de água no topo da camada congelada. Essa água então congela, fazendo com que o lençol freático suba ainda mais e repita o ciclo. O resultado é um depósito de gelo estratificado, geralmente com vários metros de espessura.
Chuva congelante é um tipo de tempestade de inverno chamada tempestade de gelo, onde a chuva cai e depois congela, produzindo uma camada de gelo. O gelo também pode formar pingentes de gelo, semelhantes a estalactites na aparência, ou formas semelhantes a estalagmites quando a água pinga e congela novamente.
O termo "barragem de gelo" tem três significados (outros discutidos abaixo). Em estruturas, uma barragem de gelo é o acúmulo de gelo em um telhado inclinado que impede que a água derretida seja drenada adequadamente e pode causar danos por vazamentos de água em edifícios.
Em rios e riachos
O gelo que se forma na água em movimento tende a ser menos uniforme e estável do que o gelo que se forma na água calma. Atolamentos de gelo (às vezes chamados de "represas de gelo"), quando pedaços quebrados de gelo se acumulam, são o maior perigo de gelo nos rios. Os congestionamentos de gelo podem causar inundações, danificar estruturas dentro ou perto do rio e danificar embarcações no rio. Atolamentos de gelo podem fazer com que algumas instalações industriais hidrelétricas desliguem completamente. Uma barragem de gelo é um bloqueio do movimento de uma geleira que pode produzir um lago proglacial. Fluxos pesados de gelo em rios também podem danificar embarcações e exigir o uso de um quebra-gelo para manter a navegação possível.
Os discos de gelo são formações circulares de gelo cercadas por água em um rio.
Pancake ice é uma formação de gelo geralmente criada em áreas com condições menos calmas.
Em lagos
O gelo se forma em águas calmas das margens, uma fina camada se espalhando pela superfície e depois para baixo. O gelo nos lagos é geralmente de quatro tipos: primário, secundário, sobreposto e aglomerado. O gelo primário se forma primeiro. O gelo secundário se forma abaixo do gelo primário em uma direção paralela à direção do fluxo de calor. O gelo sobreposto se forma no topo da superfície do gelo a partir da chuva ou da água que se infiltra através de rachaduras no gelo, que geralmente se depositam quando carregados com neve.
A plataforma de gelo ocorre quando pedaços flutuantes de gelo são movidos pelo vento, acumulando-se na costa de barlavento.
O gelo vela é uma forma de gelo podre que se desenvolve em colunas perpendiculares à superfície de um lago.
Um movimento de gelo ocorre quando o movimento do gelo, causado pela expansão do gelo e/ou ação do vento, ocorre na medida em que o gelo empurra as margens dos lagos, muitas vezes deslocando os sedimentos que compõem a linha costeira.
No ar
Rima
A geada é um tipo de gelo formado em objetos frios quando gotas de água cristalizam sobre eles. Isso pode ser observado em tempo de neblina, quando a temperatura cai durante a noite. A geada macia contém uma alta proporção de ar aprisionado, fazendo com que pareça branca em vez de transparente, e dando-lhe uma densidade de cerca de um quarto da do gelo puro. O tempo duro é comparativamente denso.
Películas
Os grânulos de gelo são uma forma de precipitação que consiste em pequenas e translúcidas bolas de gelo. Esta forma de precipitação também é chamada de como "granizo"; pelo Serviço Nacional de Meteorologia dos Estados Unidos. (No inglês britânico, refere -se a uma mistura de chuva e neve.) Os pellets de gelo geralmente são menores que as pedras de granizo. Eles costumam saltar quando atingem o chão e geralmente não congelam em uma massa sólida, a menos que misturados com chuva congelante. O código de metar para grânulos de gelo é pl . Os grânulos de gelo se formam quando uma camada de ar acima de zero está localizada entre 1.500 e 3.000 metros (4.900 e 9.800 pés) acima do solo, com o ar sub-congelador acima e abaixo dele. Isso causa o derretimento parcial ou completo de quaisquer flocos de neve que caem através da camada quente. À medida que voltam à camada sub-congeladora mais perto da superfície, eles congelam em pellets de gelo. No entanto, se a camada sub-congeladora sob a camada quente for muito pequena, a precipitação não terá tempo para congelar e a chuva congelante será o resultado na superfície. É provável que um perfil de temperatura que mostra uma camada quente acima do solo seja encontrado antes de uma frente quente durante a estação fria, mas ocasionalmente pode ser encontrada atrás de uma frente fria que passa.Hail
Como outra precipitação, o granizo se forma em nuvens de tempestade quando gotículas de água super -resfriadas congelam em contato com núcleos de condensação, como poeira ou sujeira. As atualizações da tempestade sopram as pedras de granizo na parte superior da nuvem. O Updraft se dissipa e as pedras de granizo caem, de volta ao ar livre e são levantadas novamente. O granizo tem um diâmetro de 5 milímetros (0,20 pol.) Ou mais. No código de metar, GR é usado para indicar granizo maior, de um diâmetro de pelo menos 6,4 milímetros (0,25 pol) e GS por menor. Pedras de 19 milímetros (0,75 pol), 25 milímetros (1,0 pol) e 44 milímetros (1,75 pol) são os tamanhos de granizo mais frequentemente relatados na América do Norte. As pedras de granizo podem crescer para 15 centímetros (6 polegadas) e pesar mais de 0,5 kg (1,1 lb). Em grandes pedras de granizo, o calor latente liberado por um congelamento adicional pode derreter a concha externa da pedra de granizo. O Hailstone pode então sofrer um crescimento úmido - onde a concha externa líquida coleta outras pedras menores. O Hailstone ganha uma camada de gelo e cresce cada vez mais a cada subida. Uma vez que uma pedra de granizo se torna muito pesada para ser suportada pela correção das tempestades, ela cai da nuvem.
O granizo se forma em nuvens de tempestade forte, particularmente aquelas com intensas atualizações, alto teor de água líquida, grande extensão vertical, gotículas de água grandes e onde uma boa parte da camada de nuvem está abaixo de zero 0 ° C (32 ° F). As nuvens produtoras de granizo geralmente são identificáveis por sua coloração verde. A taxa de crescimento é maximizada a cerca de -13 ° C (9 ° F) e torna -se desaparecida muito abaixo de -30 ° C (-22 ° F) à medida que as gotículas de água super -resfriadas se tornam raras. Por esse motivo, o granizo é mais comum nos interiores continentais das latitudes médias, pois a formação de granizo é consideravelmente mais provável quando o nível de congelamento está abaixo da altitude de 3.400 m (11.000 pés). A arrastamento do ar seco em fortes tempestades sobre os continentes pode aumentar a frequência de granizo, promovendo o resfriamento evaporacional, o que reduz o nível de congelamento de nuvens de trovoadas, dando um volume maior para crescer. De acordo, o granizo é realmente menos comum nos trópicos, apesar de um muito maior Frequência de tempestades do que nas latitudes médias, porque a atmosfera sobre os trópicos tende a ser mais quente em uma profundidade muito maior. Salve nos trópicos ocorre principalmente em elevações mais altas.
neve
Os cristais de neve se formam quando pequenas gotículas de nuvem super -resfriadas (cerca de 10 μm de diâmetro) congelam. Essas gotículas são capazes de permanecer líquido a temperaturas inferiores a -18 ° C (255 k; 0 ° F), porque para congelar, algumas moléculas na gota precisam se reunir por acaso para formar um arranjo semelhante ao de um gelo treliça; Em seguida, a gota congela em torno deste " núcleo ". Experimentos mostram que este " homogêneo " A nucleação de gotículas de nuvens ocorre apenas a temperaturas inferiores a -35 ° C (238 K; -31 ° F). Em nuvens mais quentes, uma partícula de aerossol ou#34; núcleo de gelo " deve estar presente (ou em contato com) a gota para atuar como um núcleo. Nossa compreensão do que as partículas produzem núcleos de gelo eficientes é ruim - o que sabemos é que são muito raros em comparação com os núcleos de condensação da nuvem nos quais as gotículas líquidas se formam. Argilas, poeira do deserto e partículas biológicas podem ser eficazes, embora até que ponto não esteja claro. Núcleos artificiais são usados na semeadura de nuvens. A gota cresce então pela condensação do vapor de água nas superfícies de gelo.
Diamond Dust
PODO DE DIAMAÇÃO DIAMENTO-também conhecido como agulhas de gelo ou cristais de gelo, formas em temperaturas que se aproximam de -40 ° C (-40 ° F) devido ao ar com umidade um pouco mais alta da mistura alftagem com a mistura com aloft com ar mais frio e à base de superfície. O identificador de metar para a poeira de diamantes nos relatórios climáticos internacionais de hora é IC .
ablação
Ablação de gelo refere -se ao seu derretimento e sua dissolução.
O derretimento do gelo significa que a quebra de ligações de hidrogênio entre as moléculas de água. A ordem das moléculas no sólido se decompõe a um estado menos ordenado e o sólido derrete para se tornar um líquido. Isso é conseguido aumentando a energia interna do gelo além do ponto de fusão. Quando o gelo derrete, ele absorve tanta energia quanto seria necessário para aquecer uma quantidade equivalente de água em 80 ° C. Durante a fusão, a temperatura da superfície do gelo permanece constante a 0 ° C. A taxa do processo de fusão depende da eficiência do processo de troca de energia. Uma superfície de gelo em água doce derrete apenas por convecção livre com uma taxa que depende linearmente da temperatura da água, t </sub, quando t ∞ é menor que 3,98 ° C e, super -linearmente, quando t ∞ é igual ou superior a 3,98 ° C, com a taxa sendo proporcional a (t ∞ - 3,98 ° C) α , com α = 5 / 3 para t ∞ maior que 8 ° C, e α = 4 / 3 para entre as temperaturas t ∞ .
Em condições ambientais salgadas, a dissolução, em vez de derreter, geralmente causa a ablação de gelo. Por exemplo, a temperatura do Oceano Ártico geralmente está abaixo do ponto de fusão do gelo marinho. A transição de fase do sólido para o líquido é alcançado misturando moléculas de sal e água, semelhantes à dissolução do açúcar na água, mesmo que a temperatura da água esteja muito abaixo do ponto de fusão do açúcar. Assim, a taxa de dissolução é limitada pelo transporte de sal, enquanto a fusão pode ocorrer a taxas muito mais altas que são características do transporte de calor.
Papel nas atividades humanas
Os seres humanos usaram gelo para resfriamento e preservação de alimentos há séculos, confiando na colheita de gelo natural em várias formas e depois passando para a produção mecânica do material. O ICE também apresenta um desafio ao transporte de várias formas e um cenário para esportes de inverno.resfriamento
O gelo tem sido valorizado há muito tempo como um meio de resfriamento. Em 400 aC, o Irã, os engenheiros persas já haviam dominado a técnica de armazenar gelo no meio do verão no deserto. O gelo foi trazido a partir de piscinas de gelo ou durante os invernos de montanhas próximas em quantidades a granel e armazenadas em geladeiras especialmente projetadas, naturalmente resfriadas . Este era um grande espaço subterrâneo (até 5000 m 3 ) que tinha paredes grossas (pelo menos dois metros na base) feitos de uma argamassa especial chamada Sarooj , composta por Areia, argila, claras de ovo, limão, cabelos de cabra e cinzas em proporções específicas, e que eram conhecidas por serem resistentes à transferência de calor. Pensa -se que essa mistura era completamente impenetrável na água. O espaço geralmente tinha acesso a um qanat e geralmente continha um sistema de cambacistas que poderiam facilmente trazer temperaturas dentro do espaço para níveis frígidos nos dias de verão. O gelo foi usado para relaxar para a realeza.
colheita
Houve indústrias prósperas na Inglaterra dos séculos 16 a 17, em que as áreas baixas ao longo do estuário do Tâmisa eram inundadas durante o inverno e o gelo colhido em carroças e armazenado entre as estações em casas de madeira isoladas como provisão para uma casa de gelo frequentemente localizada em grandes casas de campo e amplamente utilizado para manter o peixe fresco quando pescado em águas distantes. Isso foi supostamente copiado por um inglês que viu a mesma atividade na China. O gelo foi importado da Noruega para a Inglaterra em uma escala considerável já em 1823.
Nos Estados Unidos, a primeira carga de gelo foi enviada da cidade de Nova York para Charleston, Carolina do Sul, em 1799, e na primeira metade do século 19, a coleta de gelo havia se tornado um grande negócio. Frederic Tudor, que ficou conhecido como o "Ice King", trabalhou no desenvolvimento de melhores produtos de isolamento para remessas de gelo de longa distância, especialmente para os trópicos; isso ficou conhecido como o comércio de gelo.
Trieste enviou gelo para o Egito, Corfu e Zante; Suíça, para a França; e a Alemanha às vezes era abastecida pelos lagos da Baviera. O edifício do Parlamento Húngaro usou gelo colhido no inverno do Lago Balaton para ar condicionado.
As casas de gelo eram usadas para armazenar o gelo formado no inverno, para tornar o gelo disponível durante todo o ano, e um tipo antigo de refrigerador conhecido como caixa de gelo era resfriado usando um bloco de gelo colocado dentro dele. Em muitas cidades, não era incomum ter um serviço regular de entrega de gelo durante o verão. Desde então, o advento da tecnologia de refrigeração artificial tornou obsoleta a entrega de gelo.
O gelo ainda é colhido para eventos de escultura em gelo e neve. Por exemplo, uma serra giratória é usada para obter gelo para o Harbin International Ice and Snow Sculpture Festival todos os anos a partir da superfície congelada do rio Songhua.
Produção artificial
O mais antigo processo escrito conhecido para fazer gelo artificialmente é dos escritos do século 13 do historiador árabe Ibn Abu Usaybia em seu livro Kitab Uyun al-anba fi tabaqat-al-atibba sobre a medicina em que Ibn Abu Usaybi'a atribui o processo a um autor ainda mais antigo, Ibn Bakhtawayhi, de quem nada se sabe.
Produção mecânica
O gelo agora é produzido em escala industrial, para usos que incluem armazenamento e processamento de alimentos, fabricação de produtos químicos, mistura e cura de concreto e consumo ou gelo embalado. A maioria dos fabricantes de gelo comerciais produz três tipos básicos de gelo fragmentado: floco, tubular e placa, usando uma variedade de técnicas. Fabricantes de gelo em grandes lotes podem produzir até 75 toneladas de gelo por dia. Em 2002, havia 426 empresas comerciais de fabricação de gelo nos Estados Unidos, com um valor combinado de remessas de US$ 595.487.000. Os refrigeradores domésticos também podem fazer gelo com uma máquina de gelo embutida, que normalmente produz cubos de gelo ou gelo picado. Unidades autônomas de fabricação de gelo que produzem cubos de gelo são frequentemente chamadas de máquinas de gelo.
Transporte
O gelo pode apresentar desafios para o transporte seguro em terra, mar e ar.
Viagens terrestres
A formação de gelo nas estradas é um perigo perigoso no inverno. O gelo preto é muito difícil de ver, porque não tem a superfície gelada esperada. Sempre que há chuva ou neve congelante que ocorre a uma temperatura próxima ao ponto de fusão, é comum que o gelo se acumule nas janelas dos veículos. Dirigir requer com segurança a remoção do acúmulo de gelo. Os raspadores de gelo são ferramentas projetadas para quebrar o gelo e limpar as janelas, embora remover o gelo possa ser um processo longo e trabalhoso.
Far o suficiente abaixo do ponto de congelamento, uma fina camada de cristais de gelo pode se formar na superfície interna das janelas. Isso geralmente acontece quando um veículo é deixado sozinho depois de ser conduzido por um tempo, mas pode acontecer enquanto dirige, se a temperatura externa estiver baixa o suficiente. A umidade da respiração do motorista é a fonte de água para os cristais. É problemático remover essa forma de gelo, para que as pessoas abrem levemente suas janelas quando o veículo está estacionado para deixar a umidade se dissipar, e agora é comum que os carros tenham os desfiladeiros da janela traseira para resolver o problema. Um problema semelhante pode ocorrer nas casas, que é uma das razões pelas quais muitas regiões mais frias exigem janelas de dupla panela para isolamento.
Quando a temperatura externa permanece abaixo de zero por períodos prolongados, camadas de gelo muito grossas podem se formar em lagos e outros corpos de água, embora locais com água fluida exijam temperaturas muito mais frias. O gelo pode ficar espesso o suficiente para dirigir com automóveis e caminhões. Fazer isso requer com segurança uma espessura de pelo menos 30 cm ( 11 + 3 ⁄ 4 in).
viagens transmitidas pela água
Para os navios, o gelo apresenta dois perigos distintos. Primeiro, spray e chuva congelante podem produzir um acúmulo de gelo na superestrutura de uma embarcação suficiente para torná-la instável e exigir que ela seja cortada ou derretida com mangueiras de vapor. Em segundo lugar, os icebergs - grandes massas de gelo flutuando na água (normalmente criadas quando as geleiras atingem o mar) - podem ser perigosos se atingidos por um navio durante a navegação. Os icebergs foram responsáveis pelo naufrágio de muitos navios, sendo o mais famoso o Titanic. Para portos próximos aos pólos, estar livre de gelo, idealmente durante todo o ano, é uma vantagem importante. Exemplos são Murmansk (Rússia), Petsamo (Rússia, antiga Finlândia) e Vardø (Noruega). Os portos que não estão livres de gelo são abertos usando quebra-gelos.
Viagens aéreas
Para aeronaves, o gelo pode causar vários perigos. À medida que uma aeronave sobe, passa por camadas de ar de diferentes temperaturas e umidade, algumas das quais podem ser propícias à formação de gelo. Se o gelo formar nas asas ou nas superfícies de controle, isso pode afetar adversamente as qualidades de vôo da aeronave. Durante o primeiro voo ininterrupto do Atlântico, o capitão dos aviadores britânicos John Alcock e o tenente Arthur Whitten Brown encontraram tais condições de gelo-Brown deixou o cockpit e subiu na asa várias vezes para remover o gelo que cobria a ingestão de ar do motor do Vickers Aeronaves Vimy que estavam voando.
Uma vulnerabilidade efetuada pela glacê que está associada a motores de combustão interna alternativa é o carburador. À medida que o ar é sugado pelo carburador para o motor, a pressão do ar local é reduzida, o que causa resfriamento adiabático. Assim, em condições úmidas de quase congelamento, o carburador ficará mais frio e tendem a gelar. Isso bloqueará o suprimento de ar para o motor e fará com que ele falhe. Por esse motivo, os motores alternativos de aeronaves com carburadores recebem aquecedores de entrada de ar do carburador. O crescente uso da injeção de combustível - que não requer carburadores - fez a conclusão de carboidratos " menos um problema para os motores recíprocos.
Os motores a jato não experimentam gelo de carboidratos, mas evidências recentes indicam que elas podem ser lentas, paradas ou danificadas pela glacê interna em certos tipos de condições atmosféricas com muito mais facilidade do que se acreditava anteriormente. Na maioria dos casos, os motores podem ser reiniciados rapidamente e os vôos não estão ameaçados, mas a pesquisa continua a determinar as condições exatas que produzem esse tipo de gelo e encontram os melhores métodos para prevenir ou revertê -lo em voo.Recreação e esportes
O gelo também desempenha um papel central na recreação de inverno e em muitos esportes, como patinação no gelo, patinação de turismo, hóquei no gelo, bandy, pesca no gelo, escalada no gelo, curling, bola de vassoura e corrida de trenó em trenó, luge e esqueleto. Muitos dos diferentes esportes praticados no gelo recebem atenção internacional a cada quatro anos durante os Jogos Olímpicos de Inverno.
Uma espécie de veleiro sobre pás dá origem ao ice yachting. Outro esporte é a corrida no gelo, onde os pilotos devem acelerar no gelo do lago, enquanto também controlam a derrapagem de seu veículo (semelhante em alguns aspectos às corridas em pistas de terra). O esporte foi modificado até para pistas de gelo.
Outros usos
Como lastro térmico
- O gelo é usado para esfriar e preservar alimentos em caixas de gelo.
- Cubos de gelo ou gelo esmagado podem ser usados para refrescar bebidas. À medida que o gelo derrete, absorve calor e mantém a bebida perto de 0 °C (32 °F).
- O gelo pode ser usado como parte de um sistema de ar condicionado, usando ventiladores alimentados por bateria ou solar para soprar ar quente sobre o gelo. Isso é especialmente útil durante as ondas de calor quando a energia está fora e condicionadores de ar padrão (elétrico) não funcionam.
- O gelo pode ser usado (como outros pacotes frios) para reduzir o inchaço (por diminuição do fluxo sanguíneo) e dor pressionando-o contra uma área do corpo.
Como material estrutural
- Os engenheiros usaram a força substancial do gelo da embalagem quando construíram o primeiro cais de gelo flutuante da Antártida em 1973. Tais piers de gelo são usados durante as operações de carga para carregar e descarregar navios. O pessoal das operações da frota faz o cais flutuante durante o inverno. Eles constroem sobre a água do mar congelada naturalmente em McMurdo Som até que a doca chegue a uma profundidade de cerca de 22 pés (6,7 m). Os piers do gelo têm uma vida útil de três a cinco anos.
- Estruturas e esculturas de gelo são construídas fora de grandes pedaços de gelo ou pulverizando água As estruturas são principalmente ornamentais (como no caso de castelos de gelo), e não práticos para habitação de longo prazo. Os hotéis de gelo existem em uma base sazonal em algumas áreas frias. Igloos são outro exemplo de uma estrutura temporária, feita principalmente da neve.
- Em climas frios, as estradas são regularmente preparadas em lagos gelados e áreas de arquipélago. Temporariamente, até uma ferrovia foi construída sobre gelo.
- Durante a Segunda Guerra Mundial, o Projeto Habbakuk foi um programa aliado que investigou o uso de pikrete (fibras de madeira misturadas com gelo) como um material possível para navios de guerra, especialmente portadores de aeronaves, devido à facilidade com que um navio imune a torpedos, e um grande convés, poderia ser construído por gelo. Um protótipo de pequena escala foi construído, mas a necessidade de tal navio na guerra foi removida antes de construí-lo em grande escala.
- O gelo até foi usado como material para uma variedade de instrumentos musicais, por exemplo, pelo percussionista Terje Isungset.
Não água
As fases sólidas de várias outras substâncias voláteis também são chamadas de gelos; geralmente um volátil é classificado como gelo se seu ponto de fusão estiver acima ou em torno de 100 K. O exemplo mais conhecido é o gelo seco, a forma sólida do dióxido de carbono.
Um "análogo magnético" de gelo também é realizado em alguns materiais magnéticos isolantes nos quais os momentos magnéticos imitam a posição dos prótons no gelo de água e obedecem a restrições energéticas semelhantes às regras de gelo de Bernal-Fowler decorrentes da frustração geométrica da configuração do próton no gelo de água. Esses materiais são chamados de gelo giratório.
Contenido relacionado
Citosol
Citosina
Equídeos