Estereoquímica

A estereoquímica, uma subdisciplina da química, envolve o estudo do arranjo espacial relativo dos átomos que formam a estrutura das moléculas e sua manipulação. O estudo da estereoquímica concentra-se nas relações entre estereoisômeros, que por definição possuem a mesma fórmula molecular e sequência de átomos ligados (constituição), mas diferem no posicionamento geométrico dos átomos no espaço. Por esse motivo, também é conhecida como química 3D – o prefixo "estéreo-" significa 'tridimensionalidade'.
A estereoquímica abrange todo o espectro da química orgânica, inorgânica, biológica, física e especialmente supramolecular. A estereoquímica inclui métodos para determinar e descrever essas relações; o efeito nas propriedades físicas ou biológicas que essas relações conferem às moléculas em questão e a maneira como essas relações influenciam a reatividade das moléculas em questão (estereoquímica dinâmica).
Histórico
Foi somente depois das observações de certos fenômenos moleculares que os princípios estereoquímicos foram desenvolvidos. Em 1815, a observação da atividade óptica por Jean-Baptiste Biot marcou o início da história da estereoquímica orgânica. Ele observou que as moléculas orgânicas eram capazes de girar o plano da luz polarizada em solução ou na fase gasosa. Apesar das descobertas de Biot, Louis Pasteur é comumente descrito como o primeiro estereoquímico, tendo observado em 1842 que os sais de ácido tartárico coletados em recipientes de produção de vinho podiam girar o plano da luz polarizada, mas os sais de outras fontes não. Esta propriedade, a única propriedade física em que os dois tipos de sais tartaratos diferiam, é devida ao isomerismo óptico. Em 1874, Jacobus Henricus van 't Hoff e Joseph Le Bel explicaram a atividade óptica em termos do arranjo tetraédrico dos átomos ligados ao carbono. Kekulé usou modelos tetraédricos no início de 1862, mas nunca os publicou; Emanuele Paternò provavelmente sabia disso, mas foi o primeiro a desenhar e discutir estruturas tridimensionais, como a do 1,2-dibromoetano no Giornale di Scienze Naturali ed Economiche em 1869. O termo " quiral" foi introduzido por Lord Kelvin em 1904. Arthur Robertson Cushny, farmacologista escocês, em 1908, ofereceu pela primeira vez um exemplo definitivo de uma diferença de bioatividade entre enantiômeros de uma molécula quiral, viz. (-)-Adrenalina é duas vezes mais potente que a forma (±)- como vasoconstritor e em 1926 lançou as bases para a farmacologia quiral/estereofarmacologia (relações biológicas de substâncias opticamente isoméricas). Mais tarde, em 1966, a nomenclatura Cahn-Ingold-Prelog ou regra de sequência foi desenvolvida para atribuir configuração absoluta ao centro estereogênico/quiral (notação R e S) e estendida para ser aplicada através de ligações olefínicas (notação E e Z).
Significância
As regras de prioridade de Cahn–Ingold–Prelog fazem parte de um sistema para descrever a estereoquímica de uma molécula. Eles classificam os átomos em torno de um estereocentro de maneira padrão, permitindo que a posição relativa desses átomos na molécula seja descrita de forma inequívoca. Uma projeção de Fischer é uma maneira simplificada de representar a estereoquímica em torno de um estereocentro.
Exemplo da talidomida

A estereoquímica tem aplicações importantes no campo da medicina, particularmente na área farmacêutica. Um exemplo frequentemente citado da importância da estereoquímica refere-se ao desastre da talidomida. A talidomida é um medicamento farmacêutico, preparado pela primeira vez em 1957 na Alemanha, prescrito para o tratamento de enjôos matinais em mulheres grávidas. Descobriu-se que a droga era teratogênica, causando sérios danos genéticos ao crescimento e desenvolvimento embrionário inicial, levando à deformação dos membros dos bebês. Alguns dos vários mecanismos propostos de teratogenicidade envolvem uma função biológica diferente para os enantiômeros (R)- e (S)-talidomida. No entanto, no corpo humano, a talidomida sofre racemização: mesmo que apenas um dos dois enantiómeros seja administrado como medicamento, o outro enantiómero é produzido como resultado do metabolismo. Conseqüentemente, é incorreto afirmar que um estereoisômero é seguro enquanto o outro é teratogênico. A talidomida é actualmente utilizada para o tratamento de outras doenças, nomeadamente cancro e lepra. Regulamentações e controles rigorosos foram permitidos para evitar seu uso por mulheres grávidas e prevenir deformações no desenvolvimento. Este desastre foi a força motriz por trás da exigência de testes rigorosos de medicamentos antes de disponibilizá-los ao público.
Definições
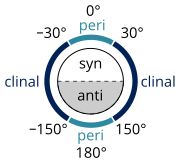
Existem muitas definições que descrevem um conformador específico (IUPAC Gold Book), desenvolvidas por William Klyne e Vladimir Prelog, constituindo seu sistema de nomenclatura Klyne-Prelog:
- um ângulo de torção de ±60° é chamado Gauche!
- um ângulo de torção entre 0° e ±90° é chamado Sincronia: (s)
- um ângulo de torção entre ±90° e 180° é chamado anti- (a)
- um ângulo de torção entre 30° e 150° ou entre –30° e –150° é chamado Clinal
- um ângulo de torção entre 0° e 30° ou 150° e 180° é chamado periplanar (p)
- um ângulo de torção entre 0° a 30° é chamado São Paulo ou Sin... ou informação (sp)
- um ângulo de torção entre 30° a 90° e –30° a –90° é chamado Sincronização ou Gauche! ou Skew (sc)
- um ângulo de torção entre 90° a 150°, e –90° a – 150° é chamado anticlinal (ac)
- um ângulo de torção entre ±150° a 180° é chamado antiperitivos ou anti- ou trans (ap).
A deformação torcional resulta da resistência à torção em torno de uma ligação.
Tipos
- Atropisomemismo
Uma forma enérgica de chirality axial. Esta forma de chirality deriva da substituição diferencial sobre uma ligação, comumente entre dois átomos de sp2-hidridized. - Cis–trans isomerismo
Também referido como isômeros geométricos, estes compostos têm configurações diferentes devido à estrutura inflexível da molécula. Dois requisitos devem ser atendidos para uma molécula apresentar isomerismo cis-trans:
1. A rotação dentro da molécula deve ser restrita.
2. Dois grupos não-identais devem estar em cada átomo de carbono duplamente ligado. - Isomerismo conformacional
Esta forma de isomerismo também é chamada de conformadores, isômeros rotativos e rotadores. O isomerismo conformacional é produzido por rotação sobre o único vínculo. - Diário de bordo
Estes estereómeros são não-imagem, não-identica. Os diastereomers ocorrem quando os estereoisomers de um composto têm configurações diferentes em estereocentros correspondentes. - Enantigo
Estereoisômeros que não são superimposable, imagens de espelho.