Cromatina
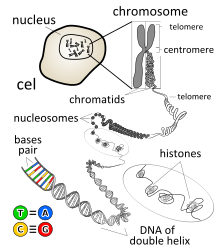
Cromatina é um complexo de DNA e proteína encontrado em células eucarióticas. A função primária é empacotar longas moléculas de DNA em estruturas mais compactas e densas. Isso evita que os fios fiquem emaranhados e também desempenha papéis importantes no reforço do DNA durante a divisão celular, evitando danos ao DNA e regulando a expressão gênica e a replicação do DNA. Durante a mitose e a meiose, a cromatina facilita a segregação adequada dos cromossomos na anáfase; as formas características dos cromossomos visíveis durante esse estágio são o resultado do DNA sendo enrolado em cromatina altamente condensada.
Os principais componentes proteicos da cromatina são as histonas. Um octâmero de dois conjuntos de quatro núcleos de histonas (Histona H2A, Histona H2B, Histona H3 e Histona H4) liga-se ao DNA e funciona como "âncoras". em torno do qual os fios são enrolados. Em geral, existem três níveis de organização da cromatina:
- O DNA envolve proteínas histone, formando nucleossomas e as chamadas contas em uma estrutura de corda (eucromatina).
- Múltiplos histones envolvem-se em uma fibra de 30 nanômetros que consiste em matrizes de nucleossomas em sua forma mais compacta (heterocromatina).
- A supercoilação de DNA de nível superior da fibra de 30 nm produz o cromossomo metafase (durante mitose e meiose).
Muitos organismos, no entanto, não seguem esse esquema de organização. Por exemplo, os espermatozóides e os glóbulos vermelhos das aves têm cromatina mais compactada do que a maioria das células eucarióticas, e os protozoários tripanossomatídeos não condensam sua cromatina em cromossomos visíveis. As células procarióticas têm estruturas totalmente diferentes para organizar seu DNA (o cromossomo procariótico equivalente é chamado de genóforo e está localizado na região nucleoide).
A estrutura geral da rede de cromatina depende ainda mais do estágio do ciclo celular. Durante a interfase, a cromatina é estruturalmente solta para permitir o acesso às polimerases de RNA e DNA que transcrevem e replicam o DNA. A estrutura local da cromatina durante a interfase depende dos genes específicos presentes no DNA. Regiões de DNA contendo genes que são ativamente transcritos ("ligados") são menos compactadas e intimamente associadas com RNA polimerases em uma estrutura conhecida como eucromatina, enquanto regiões contendo genes inativos ("desligados" 34;) são geralmente mais condensados e associados a proteínas estruturais na heterocromatina. A modificação epigenética das proteínas estruturais na cromatina via metilação e acetilação também altera a estrutura local da cromatina e, portanto, a expressão gênica. Há uma compreensão limitada da estrutura da cromatina e é uma área ativa de pesquisa em biologia molecular.
Estrutura dinâmica e hierarquia da cromatina
A cromatina sofre várias mudanças estruturais durante o ciclo celular. As proteínas histonas são os empacotadores e organizadores básicos da cromatina e podem ser modificadas por várias modificações pós-traducionais para alterar o empacotamento da cromatina (modificação das histonas). A maioria das modificações ocorre nas caudas das histonas. Os núcleos de histonas carregados positivamente neutralizam apenas parcialmente a carga negativa do esqueleto de fosfato de DNA, resultando em uma carga líquida negativa da estrutura geral. Um desequilíbrio de carga dentro do polímero causa repulsão eletrostática entre regiões vizinhas da cromatina que promovem interações com proteínas, moléculas e cátions carregados positivamente. À medida que essas modificações ocorrem, o ambiente eletrostático ao redor da cromatina fluirá e o nível de compactação da cromatina será alterado. As consequências em termos de acessibilidade e compactação da cromatina dependem tanto do aminoácido modificado quanto do tipo de modificação. Por exemplo, a acetilação de histonas resulta no afrouxamento e maior acessibilidade da cromatina para replicação e transcrição. A trimetilação da lisina pode levar ao aumento da atividade transcricional (trimetilação da histona H3 lisina 4) ou à repressão transcricional e compactação da cromatina (trimetilação da histona H3 lisina 9 ou 27). Vários estudos sugeriram que diferentes modificações poderiam ocorrer simultaneamente. Por exemplo, foi proposto que uma estrutura bivalente (com trimetilação da lisina 4 e 27 na histona H3) está envolvida no desenvolvimento inicial dos mamíferos. Outro estudo testou o papel do H4K16ac na estrutura da cromatina e descobriu que a acetilação homogênea inibiu a formação de cromatina de 30 nm e bloqueou a remodelação do trifosfato de adenosina. Esta modificação singular mudou a dinâmica da cromatina, o que mostra que a acetilação de H4 em K16 é vital para a intra e interfuncionalidade adequada da estrutura da cromatina.
As proteínas do grupo Polycomb desempenham um papel na regulação de genes através da modulação da estrutura da cromatina.
Para obter informações adicionais, consulte variante da cromatina, modificações de histonas na regulação da cromatina e controle da polimerase de RNA pela estrutura da cromatina.
Estrutura do DNA
Na natureza, o DNA pode formar três estruturas, A-, B- e Z-DNA. A- e B-DNA são muito semelhantes, formando hélices destras, enquanto o Z-DNA é uma hélice de esquerda com um esqueleto de fosfato em zig-zag. Pensa-se que o Z-DNA desempenha um papel específico na estrutura da cromatina e na transcrição devido às propriedades da junção entre B- e Z-DNA.
Na junção dos DNAs B e Z, um par de bases é desviado da ligação normal. Estes desempenham um papel duplo de um local de reconhecimento por muitas proteínas e como um sorvedouro para o estresse torcional da RNA polimerase ou da ligação do nucleossomo. As bases do DNA são armazenadas como uma estrutura de código com quatro bases químicas, como “Adenina (A), Guanina (G), Citosina (C) e Timina (T)”. A ordem e as sequências dessas estruturas químicas do DNA são refletidas como informações disponíveis para a criação e controle dos organismos humanos. "A com T e C com G" pareando para construir o par de bases de DNA. Moléculas de açúcar e fosfato também são emparelhadas com essas bases, fazendo com que os nucleotídeos do DNA organizem 2 longas fitas espirais unidas chamadas “dupla hélice”. Nos eucariotos, o DNA consiste em um núcleo celular e o DNA fornece força e direção ao mecanismo da hereditariedade. Além disso, entre as ligações nitrogenadas dos 2 DNAs, formam-se ligações homogêneas.
Nucleossomos e contas em um cordão
O elemento básico de repetição da cromatina é o nucleossomo, interconectado por seções de DNA de ligação, um arranjo muito mais curto do que o DNA puro em solução.
Além das histonas centrais, existe uma histona de ligação H1 que entra em contato com a saída/entrada da fita de DNA no nucleossomo. A partícula central do nucleossomo, juntamente com a histona H1, é conhecida como cromatossomo. Os nucleossomos, com cerca de 20 a 60 pares de bases de DNA ligante, podem formar, em condições não fisiológicas, grânulos de aproximadamente 10 nm em uma fibra de barbante.
Os nucleossomos se ligam ao DNA de forma não específica, conforme exigido por sua função no empacotamento geral do DNA. Existem, no entanto, grandes preferências de sequência de DNA que governam o posicionamento do nucleossomo. Isso se deve principalmente às propriedades físicas variadas de diferentes sequências de DNA: por exemplo, adenina (A) e timina (T) são mais favoravelmente comprimidas nos sulcos menores internos. Isso significa que os nucleossomos podem se ligar preferencialmente em uma posição aproximadamente a cada 10 pares de bases (a repetição helicoidal do DNA) - onde o DNA é girado para maximizar o número de bases A e T que ficarão no sulco menor interno. (Veja a estrutura do ácido nucleico.)
Fibra de cromatina de 30 nanômetros
Com a adição de H1, a estrutura de contas em uma corda, por sua vez, se enrola em uma estrutura helicoidal de 30 nm de diâmetro conhecida como fibra ou filamento de 30 nm. A estrutura precisa da fibra de cromatina na célula não é conhecida em detalhes.
Acredita-se que esse nível de estrutura da cromatina seja a forma de heterocromatina, que contém principalmente genes transcricionalmente silenciosos. Estudos de microscopia eletrônica demonstraram que a fibra de 30 nm é altamente dinâmica, de modo que se desdobra em uma estrutura de contas em uma corda de fibra de 10 nm quando atravessada por uma polimerase de RNA envolvida na transcrição.
Os modelos existentes geralmente aceitam que os nucleossomos ficam perpendiculares ao eixo da fibra, com histonas de ligação organizadas internamente. Uma fibra estável de 30 nm depende do posicionamento regular dos nucleossomos ao longo do DNA. O DNA do ligante é relativamente resistente à flexão e rotação. Isso torna o comprimento do DNA do ligante crítico para a estabilidade da fibra, exigindo que os nucleossomos sejam separados por comprimentos que permitam a rotação e o dobramento na orientação necessária sem estresse excessivo para o DNA. Nesta visão, diferentes comprimentos do DNA do linker devem produzir diferentes topologias de dobramento da fibra de cromatina. Trabalho teórico recente, baseado em imagens de microscopia eletrônica de fibras reconstituídas suporta esta visão.
Organização espacial da cromatina no núcleo da célula
O arranjo espacial da cromatina dentro do núcleo não é aleatório - regiões específicas da cromatina podem ser encontradas em certos territórios. Os territórios são, por exemplo, os domínios associados à lâmina (LADs) e os domínios associados topologicamente (TADs), que são unidos por complexos de proteínas. Atualmente, modelos de polímeros como o Strings & O modelo Binders Switch (SBS) e o modelo Dynamic Loop (DL) são usados para descrever o dobramento da cromatina dentro do núcleo. O arranjo da cromatina dentro do núcleo também pode desempenhar um papel no estresse nuclear e restaurar a deformação da membrana nuclear por estresse mecânico. Quando a cromatina é condensada, o núcleo torna-se mais rígido. Quando a cromatina é descondensada, o núcleo torna-se mais elástico com menos força exercida na membrana nuclear interna. Essa observação lança luz sobre outras possíveis funções celulares da organização da cromatina fora da regulação genômica.
Organização estrutural dependente do ciclo celular
- Interfase: A estrutura da cromatina durante a interfase da mitose é otimizada para permitir o acesso simples dos fatores de transcrição e reparo do DNA ao DNA ao compactar o DNA no núcleo. A estrutura varia dependendo do acesso necessário ao DNA. Os genes que exigem acesso regular pela polimerase do RNA requerem a estrutura mais solta fornecida pela euchromatin.
- Metafase: A estrutura da metafase da cromatina difere vastamente à da interfase. Ele é otimizado para força física e capacidade de gerenciamento, formando a estrutura clássica do cromossomo vista em karyotypes. Acredita-se que a estrutura da cromatina condensada seja loops de fibra de 30 nm a um andaime central de proteínas. É, no entanto, não bem-caracterizado. andaimes cromossomas desempenhar um papel importante para manter a cromatina em cromossomas compactos. Loops de 30 nm estrutura mais condense com andaime, em estruturas de ordem mais altas. Os andaimes cromossômicos são feitos de proteínas, incluindo a condensina, o tipo IIA topoisomerase e o parente da quinesina 4 (KIF4). A força física da cromatina é vital para esta fase de divisão para evitar danos de cisalhamento ao DNA como os cromossomas da filha são separados. Para maximizar a força a composição da cromatina muda à medida que se aproxima do centromere, principalmente através de alternativas histone H1 análogos. Durante a mitose, embora a maioria da cromatina seja compactada firmemente, há pequenas regiões que não são tão compactadas. Essas regiões muitas vezes correspondem a regiões promotoras de genes que estavam ativos nesse tipo de célula antes da formação de cromatina. A falta de compactação dessas regiões é chamada de bookmarking, que é um mecanismo epigenético acreditado ser importante para transmitir às células filhas a "memória" de que os genes eram ativos antes da entrada em mitose. Este mecanismo de bookmarking é necessário para ajudar a transmitir esta memória porque a transcrição cessa durante a mitose.
Cromatina e rajadas de transcrição
A cromatina e sua interação com enzimas têm sido pesquisadas, e a conclusão a que se chega é que ela é relevante e um fator importante na expressão gênica. Vincent G. Allfrey, professor da Universidade Rockefeller, afirmou que a síntese de RNA está relacionada à acetilação de histonas. O aminoácido lisina ligado ao final das histonas é carregado positivamente. A acetilação dessas caudas tornaria as extremidades da cromatina neutras, permitindo o acesso ao DNA.
Quando a cromatina se descondense, o DNA fica aberto à entrada da maquinaria molecular. As flutuações entre a cromatina aberta e fechada podem contribuir para a descontinuidade da transcrição ou ruptura transcricional. Outros fatores provavelmente estão envolvidos, como a associação e dissociação de complexos de fatores de transcrição com a cromatina. Especificamente, foi demonstrado que a polimerase de RNA e as proteínas transcricionais se reúnem em gotículas por meio de separação de fases, e estudos recentes sugeriram que a cromatina de 10 nm demonstra um comportamento semelhante ao líquido, aumentando a capacidade de direcionamento do DNA genômico. As interações entre as histonas do linker e as regiões de cauda desordenadas agem como uma cola eletrostática organizando a cromatina em larga escala em um domínio dinâmico semelhante a um líquido. A diminuição da compactação da cromatina vem com maior mobilidade da cromatina e acesso transcricional mais fácil ao DNA. O fenômeno, ao contrário de modelos probabilísticos simples de transcrição, pode explicar a alta variabilidade na expressão gênica que ocorre entre células em populações isogênicas.
Organizações alternativas de cromatina
Durante a espermiogênese dos metazoários, a cromatina da espermátide é remodelada em uma estrutura mais espaçada, alargada e quase cristalina. Este processo está associado à cessação da transcrição e envolve a troca de proteínas nucleares. As histonas são principalmente deslocadas e substituídas por protaminas (pequenas proteínas ricas em arginina). Propõe-se que em leveduras regiões desprovidas de histonas tornam-se muito frágeis após a transcrição; HMO1, uma proteína HMG-box, ajuda a estabilizar a cromatina livre de nucleossomos.
Reparo de cromatina e DNA
Vários agentes internos e externos podem causar danos ao DNA nas células. Muitos fatores influenciam como a rota de reparo é selecionada, incluindo a fase do ciclo celular e o segmento da cromatina onde ocorreu a quebra. Em termos de iniciar o reparo do DNA da extremidade 5', a proteína de ligação p53 1 (53BP1) e o BRCA 1 são componentes proteicos importantes que influenciam a seleção da via de reparo de quebra de fita dupla. O complexo 53BP1 liga-se à cromatina perto da quebra do DNA e ativa fatores a jusante, como Rap1-Interacting Factor 1 (RIF1) e Shieldin, que protege as extremidades do DNA contra a destruição nucleolítica. O processo de dano ao DNA ocorre dentro da condição da cromatina, e o ambiente em constante mudança da cromatina tem um grande efeito sobre ele. Acessando e reparando a célula danificada do DNA, o genoma se condensa em cromatina e a repara através da modificação dos resíduos de histonas. Através da alteração da estrutura da cromatina, os resíduos de histonas estão adicionando grupos químicos, nomeadamente fosfato, acetil e um ou mais de um grupo metil e estes estão controlando as expressões de construção de genes por proteínas para adquirir DNA. Além disso, ressíntese da zona encantada, o DNA será reparado processando e reestruturando as bases danificadas. A fim de manter a integridade genômica, “a recombinação homóloga e o processo clássico de junção de extremidades não homólogas” foram seguidos pelo DNA a ser reparado.
O empacotamento do DNA eucariótico na cromatina apresenta uma barreira para todos os processos baseados no DNA que requerem o recrutamento de enzimas para seus locais de ação. Para permitir o processo celular crítico de reparo do DNA, a cromatina deve ser remodelada. Em eucariotos, os complexos de remodelação da cromatina dependentes de ATP e as enzimas modificadoras de histonas são dois fatores predominantes empregados para realizar esse processo de remodelação.
O relaxamento da cromatina ocorre rapidamente no local de um dano ao DNA. Esse processo é iniciado pela proteína PARP1 que começa a aparecer no dano ao DNA em menos de um segundo, com meia acumulação máxima em 1,6 segundos após o dano. Em seguida, o remodelador de cromatina Alc1 liga-se rapidamente ao produto de PARP1 e completa a chegada ao dano do DNA em 10 segundos após o dano. Cerca de metade do relaxamento máximo da cromatina, presumivelmente devido à ação de Alc1, ocorre em 10 segundos. Isso permite o recrutamento da enzima de reparo do DNA MRE11, para iniciar o reparo do DNA, em 13 segundos.
γH2AX, a forma fosforilada de H2AX também está envolvida nas etapas iniciais que levam à descondensação da cromatina após a ocorrência de dano ao DNA. A variante de histona H2AX constitui cerca de 10% das histonas H2A na cromatina humana. γH2AX (H2AX fosforilado na serina 139) pode ser detectado em até 20 segundos após a irradiação das células (com formação de quebra de fita dupla do DNA), e metade do acúmulo máximo de γH2AX ocorre em um minuto. A extensão da cromatina com γH2AX fosforilado é de cerca de dois milhões de pares de bases no local de uma quebra de fita dupla de DNA. γH2AX não causa, por si só, descondensação da cromatina, mas dentro de 30 segundos de irradiação, a proteína RNF8 pode ser detectada em associação com γH2AX. RNF8 medeia extensa descondensação da cromatina, por meio de sua subsequente interação com CHD4, um componente da remodelação do nucleossomo e do complexo desacetilase NuRD.
Depois de sofrer relaxamento subsequente ao dano do DNA, seguido pelo reparo do DNA, a cromatina se recupera para um estado de compactação próximo ao seu nível pré-dano após cerca de 20 min.
Métodos para investigar a cromatina

- ChIP-seq (Chromatin immссяыunoprecipitation sequencing) é reconhecido como o método de identificação de cromatina amplamente utilizado tem sido usando os anticorpos que ativamente selecionados, identificar e combinar com proteínas, incluindo "histones, reestruturação histone, fatores de transação e cofactores". Isso vem fornecendo dados sobre o estado da cromatina e a transação de um gene pela guarnição de "oligonucleotides" que são unbound. O sequenciamento de imunoprecipitação de cromatina voltado para diferentes modificações de histone, pode ser usado para identificar estados de cromatina em todo o genoma. Diferentes modificações foram ligadas a vários estados de cromatina.
- DNase-seq (DNase I hypersensitive sites Sequencing) usa a sensibilidade de regiões acessíveis no genoma para a enzima DNase I para mapear regiões abertas ou acessíveis no genoma.
- FAIRECÇÃO (Formaldehyde-Assisted Isolation of Regulatory Elements sequencing) usa as propriedades químicas do DNA proteico em um método de separação de duas fases para extrair regiões depletadas do nucleosome do genoma.
- ATAC-seq (O ensaio para sequenciamento de cromatina Acessível Transpossível) usa a transposase Tn5 para integrar (sintética) transposons em regiões acessíveis do genoma, destacando conseqüentemente a localização de nucleossomas e fatores de transcrição em todo o genoma.
- Pegada de DNA é um método destinado a identificar o DNA da proteína. Ele usa rotulagem e fragmentação acoplada à eletroforese gel para identificar áreas do genoma que foram ligadas por proteínas.
- MNase-seq (sequenciamento da nuclease micrococcal) usa a enzima nuclease micrococcal para identificar o posicionamento do nucleossoma em todo o genoma.
- Captura de conformação cromossoma determina a organização espacial da cromatina no núcleo, inferindo locais genômicos que interagem fisicamente.
- Perfil MACC (Micrococcal nuclease ACCessibility profiling) usa série de titulação de digestões de cromatina com nuclease micrococal para identificar a acessibilidade da cromatina, bem como para mapear nucleossomas e proteínas não-histone DNA-binding em ambas as regiões abertas e fechadas do genoma.
Cromatina e nós
Tem sido um enigma como os cromossomos interfásicos descondensados permanecem essencialmente sem nós. A expectativa natural é que, na presença de topoisomerases de DNA tipo II, que permitem a passagem de regiões de DNA de fita dupla entre si, todos os cromossomos atinjam o estado de equilíbrio topológico. O equilíbrio topológico em cromossomos interfásicos altamente lotados formando territórios cromossômicos resultaria na formação de fibras de cromatina altamente entrelaçadas. No entanto, os métodos de Captura da Conformação Cromossômica (3C) revelaram que o decaimento dos contatos com a distância genômica nos cromossomos interfásicos é praticamente o mesmo que no estado de glóbulo amassado que se forma quando polímeros longos se condensam sem a formação de nós. Para remover os nós da cromatina altamente aglomerada, seria necessário um processo ativo que não apenas fornecesse a energia para mover o sistema do estado de equilíbrio topológico, mas também guiasse as passagens mediadas pela topoisomerase de tal forma que os nós fossem eficientemente desfeitos em vez de tornando os nós ainda mais complexos. Foi demonstrado que o processo de extrusão da alça da cromatina é ideal para desatar ativamente as fibras de cromatina nos cromossomos da interfase.
Cromatina: definições alternativas
O termo, introduzido por Walther Flemming, tem múltiplos significados:
- Definição simples e concisa: A cromatina é um complexo macromolecular de uma macromolécula de DNA e macromoléculas de proteínas (e RNA). As proteínas empacotam e organizam o DNA e controlam suas funções dentro do núcleo celular.
- Definição operacional de bioquímicos: A cromatina é o complexo DNA/proteína/RNA extraído do núcleo interfase lisado eucariótico. Apenas qual das substâncias multitudinous presentes em um núcleo constituirá uma parte do material extraído depende parcialmente da técnica que cada pesquisador usa. Além disso, a composição e as propriedades da cromatina variam de um tipo de célula para outro, durante o desenvolvimento de um tipo específico de célula e em diferentes estágios no ciclo celular.
- O DNA + histone = cromatina definição: A hélice dupla de DNA no núcleo celular é empacotada por proteínas especiais denominadas histones. O complexo de proteína/DNA formado é chamado de cromatina. A unidade estrutural básica da cromatina é o nucleossoma.
A primeira definição permite "cromatinas" a ser definido em outros domínios da vida, como bactérias e archaea, usando qualquer proteína de ligação ao DNA que condensa a molécula. Essas proteínas são geralmente referidas como proteínas associadas a nucleoides (NAPs); exemplos incluem AsnC/LrpC com HU. Além disso, algumas archaea produzem nucleossomos a partir de proteínas homólogas às histonas eucarióticas.
Remodelação da Cromatina:
A remodelação da cromatina pode resultar da modificação covalente de histonas que fisicamente remodelam, movem ou removem nucleossomos. Estudos de Sanosaka et al 2022, dizem que o remodelador de cromatina CHD7 regula a expressão gênica específica do tipo de célula em células da crista neural humana.
Prêmios Nobel
Os seguintes cientistas foram reconhecidos por suas contribuições à pesquisa da cromatina com Prêmios Nobel:
| Ano | Quem? | Prémio |
|---|---|---|
| 1910 | Albrecht Kossel (Universidade de Heidelberg) | Prêmio Nobel de Fisiologia ou Medicina por sua descoberta das cinco bases nucleares: adenina, citosina, guanina, timina e uracil. |
| 1933 | Thomas Hunt Morgan (Instituto de Tecnologia da Califórnia) | Prêmio Nobel de Fisiologia ou Medicina por suas descobertas do papel desempenhado pelo gene e cromossomo na hereditariedade, com base em seus estudos da mutação de olhos brancos na mosca da fruta Drosophila. |
| 1962 | Francis Crick, James Watson e Maurice Wilkins (MRC Laboratory of Molecular Biology, Harvard University e London University respectivamente) | Prêmio Nobel de Fisiologia ou Medicina por suas descobertas da estrutura dupla de hélice de DNA e seu significado para a transferência de informação em material vivo. |
| 1982 | Aaron Klug (Laboratório de Biologia Molecular) | Prêmio Nobel de Química "por seu desenvolvimento de microscopia de elétrons cristalográficas e sua elucidação estrutural de complexos de proteína de ácido nucleico biologicamente importantes" |
| 1993 | Richard J. Roberts e Phillip A. Sharp | Prêmio Nobel de Fisiologia "para suas descobertas independentes de genes divididos", em que seções de DNA chamadas exons expressam proteínas, e são interrompidas por seções de DNA chamadas introns, que não expressam proteínas. |
| 2006 | Roger Kornberg (Stanford University) | Prêmio Nobel de Química por sua descoberta do mecanismo pelo qual o DNA é transcrito em RNA mensageiro. |
Contenido relacionado
Diprotodonte
Raposa ártica
Alossauro
Apatossauro
Planta bienal