Conjugação bacteriana
Conjugação bacteriana é a transferência de material genético entre células bacterianas por contato direto célula a célula ou por uma conexão semelhante a uma ponte entre duas células. Isso ocorre através de um pilus. É um modo parassexual de reprodução em bactérias.
É um mecanismo de transferência horizontal de genes, assim como a transformação e a transdução, embora esses dois outros mecanismos não envolvam contato célula a célula.
Clássica E. coli conjugação bacteriana é muitas vezes considerada como o equivalente bacteriano da reprodução sexual ou acasalamento, uma vez que envolve a troca de material genético. No entanto, não é reprodução sexual, uma vez que não ocorre nenhuma troca de gametas e, de fato, nenhuma geração de um novo organismo: em vez disso, um organismo existente é transformado. Durante a clássica E. coli a célula doadora fornece um elemento genético conjugado ou mobilizável que é mais frequentemente um plasmídeo ou transposon. A maioria dos plasmídeos conjugativos possui sistemas que garantem que a célula receptora não contenha um elemento semelhante.
A informação genética transferida geralmente é benéfica para o destinatário. Os benefícios podem incluir resistência a antibióticos, tolerância a xenobióticos ou a capacidade de usar novos metabólitos. Outros elementos podem ser prejudiciais e podem ser vistos como parasitas bacterianos.
A conjugação em Escherichia coli por zigogênese espontânea e em Mycobacterium smegmatis por transferência conjugal distributiva diferem da clássica E. coli conjugação em que estes casos envolvem mistura substancial dos genomas parentais.
História
O processo foi descoberto por Joshua Lederberg e Edward Tatum em 1946.
Mecanismo
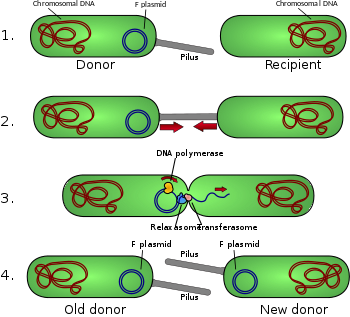
Diagrama de conjugação
- A célula doadora produz pilo.
- Pilus se liga à célula receptora e reúne as duas células.
- O plasmídeo móvel é nicked e um único fio de DNA é então transferido para a célula receptora.
- Ambas as células sintetizam uma cadeia complementar para produzir um plasmídeo circular duplo e também reproduzir pili; ambas as células são agora doador viável para o F-factor.
O fator F é um epissomo (um plasmídeo que pode se integrar ao cromossomo bacteriano por recombinação homóloga) com um comprimento de cerca de 100 kb. Ele carrega sua própria origem de replicação, o oriV, e uma origem de transferência, ou oriT. Só pode haver uma cópia do plasmídeo F em uma determinada bactéria, livre ou integrada, e as bactérias que possuem uma cópia são chamadas de F-positivas ou F-plus (denotado F+). As células que não possuem plasmídeos F são chamadas F-negativas ou F-menos (F−) e, como tal, podem funcionar como células receptoras.
Entre outras informações genéticas, o plasmídeo F carrega um locus tra e trb, que juntos têm cerca de 33 kb de comprimento e consistem em cerca de 40 genes. O locus tra inclui o gene pilina e genes reguladores, que juntos formam os pili na superfície celular. O locus também inclui os genes para as proteínas que se ligam à superfície das bactérias F- e iniciam a conjugação. Embora haja algum debate sobre o mecanismo exato de conjugação, parece que os pili não são as estruturas através das quais ocorre a troca de DNA. Isso foi demonstrado em experimentos em que os pilus podem fazer contato, mas depois são desnaturados com SDS e, ainda assim, a transformação do DNA continua. Várias proteínas codificadas no locus tra ou trb parecem abrir um canal entre as bactérias e acredita-se que a enzima traD, localizada na base do pilus, inicie fusão da membrana.
Quando a conjugação é iniciada por um sinal, a enzima relaxase cria um corte em uma das fitas do plasmídeo conjugativo no oriT. A relaxase pode funcionar sozinha ou em um complexo de mais de uma dúzia de proteínas conhecidas coletivamente como um relaxossomo. No sistema F-plasmídeo, a enzima relaxase é chamada de TraI e o relaxossomo consiste em TraI, TraY, TraM e o fator integrado do hospedeiro IHF. A fita cortada, ou T-strand, é então desenrolada da fita ininterrupta e transferida para a célula receptora na direção do terminal 5' para o terminal 3'. A cadeia restante é replicada independente da ação conjugativa (replicação vegetativa começando no oriV) ou em conjunto com a conjugação (replicação conjugativa semelhante à replicação do círculo rolante do fago lambda). A replicação conjugativa pode exigir um segundo nick antes que a transferência bem-sucedida possa ocorrer. Um relatório recente afirma ter inibido a conjugação com produtos químicos que imitam uma etapa intermediária desse segundo evento de corte.
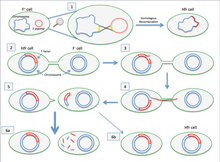
Se o plasmídeo F transferido tiver sido previamente integrado ao genoma do doador (produzindo uma cepa Hfr ["Alta Frequência de Recombinação"]), alguns dos O DNA cromossômico também pode ser transferido com o DNA plasmidial. A quantidade de DNA cromossômico que é transferida depende de quanto tempo as duas bactérias conjugadas permanecem em contato. Em cepas laboratoriais comuns de E. coli a transferência de todo o cromossomo bacteriano leva cerca de 100 minutos. O DNA transferido pode então ser integrado ao genoma receptor por meio de recombinação homóloga.
Uma cultura celular que contém em sua população células com plasmídeos F não integrados geralmente também contém algumas células que acidentalmente integraram seus plasmídeos. São essas células as responsáveis pelas transferências de genes cromossômicos de baixa frequência que ocorrem nessas culturas. Algumas cepas de bactérias com um plasmídeo F integrado podem ser isoladas e cultivadas em cultura pura. Como essas cepas transferem genes cromossômicos com muita eficiência, elas são chamadas de Hfr (high frequência de recombinação). O E. coli genoma foi originalmente mapeado por experimentos de acasalamento interrompido em que várias células Hfr no processo de conjugação foram cortadas de recipientes após menos de 100 minutos (inicialmente usando um misturador Waring). Os genes que foram transferidos foram então investigados.
Desde a integração do plasmídeo F no E. coli é uma ocorrência espontânea rara e, como os numerosos genes que promovem a transferência de DNA estão no genoma do plasmídeo, e não no genoma bacteriano, argumenta-se que a transferência conjugada de genes bacterianos, como ocorre no E. coli Hfr, não é uma adaptação evolutiva do hospedeiro bacteriano, nem é provavelmente ancestral do sexo eucariótico.
Zigogênese espontânea em E. coli
Além da conjugação bacteriana clássica descrita acima para E. coli, uma forma de conjugação referida como zigogênese espontânea (Z-mating para abreviar) é observada em certas cepas de E. coli. No acasalamento Z há mistura genética completa, e diplóides instáveis são formados que liberam células fenotipicamente haploides, das quais algumas mostram um fenótipo parental e algumas são verdadeiras recombinantes.
Transferência conjugal em micobactérias
Conjugação em Mycobacteria smegmatis, como a conjugação em E. coli, requer contato estável e prolongado entre um doador e uma cepa receptora, é resistente a DNase e o DNA transferido é incorporado ao cromossomo receptor por recombinação homóloga. No entanto, ao contrário de E. coli Hfr, a conjugação micobacteriana é cromossômica e não baseada em plasmídeo. Além disso, em contraste com E. coli conjugação Hfr, em M. smegmatis todas as regiões do cromossomo são transferidas com eficiências comparáveis. Os comprimentos dos segmentos doadores variam amplamente, mas têm um comprimento médio de 44,2 kb. Uma vez que uma média de 13 tratos são transferidos, o total médio de DNA transferido por genoma é de 575kb. Este processo é conhecido como "transferência conjugal distributiva" Gray e outros. encontrou uma mistura substancial dos genomas parentais como resultado da conjugação e considerou essa mistura como uma reminiscência daquela observada nos produtos meióticos da reprodução sexual.
Transferência de DNA semelhante à conjugação em archaea hipertermofílica
Arqueas hipertermofílicas codificam pili estruturalmente semelhantes aos pili conjugados bacterianos. No entanto, ao contrário das bactérias, onde o aparelho de conjugação normalmente medeia a transferência de elementos genéticos móveis, como plasmídeos ou transposons, a maquinaria conjugativa de archaea hipertermofílica, chamada Ced (Crenarchaeal system for exchange of DNA) e Ted (Thermoproteales system for exchange of DNA), parece ser responsável pela transferência de DNA celular entre membros da mesma espécie. Foi sugerido que nestas archaea a maquinaria de conjugação foi totalmente domesticada para promover o reparo do DNA por meio de recombinação homóloga, em vez da disseminação de elementos genéticos móveis. Além do pilus conjugativo semelhante ao VirB2, os sistemas Ced e Ted incluem componentes para o poro de acoplamento transmembrana semelhante ao VirB6 e a ATPase semelhante ao VirB4.
Transferência entre reinos
Bactérias relacionadas com os Rhizobia fixadores de nitrogênio são um caso interessante de conjugação inter-reino. Por exemplo, o plasmídeo indutor de tumor (Ti) de Agrobacterium e o plasmídeo (Ri) indutor de tumor de raiz de A. rhizogenes contém genes que são capazes de se transferir para células vegetais. A expressão desses genes efetivamente transforma as células vegetais em fábricas produtoras de opina. Os opinos são usados pelas bactérias como fontes de nitrogênio e energia. As células infectadas formam galha em coroa ou tumores radiculares. Os plasmídeos Ti e Ri são, portanto, endossimbiontes das bactérias, que por sua vez são endossimbiontes (ou parasitas) da planta infectada.
Os plasmídeos Ti e Ri também podem ser transferidos entre bactérias usando um sistema (o tra, ou operon de transferência) que é diferente e independente do sistema usado para transferência entre reinos (o < i>vir, ou virulência, operon). Tais transferências criam cepas virulentas de cepas anteriormente avirulentas.
Aplicações de engenharia genética
A conjugação é um meio conveniente de transferir material genético para uma variedade de alvos. Em laboratórios, foram relatadas transferências bem-sucedidas de bactérias para leveduras, plantas, células de mamíferos, diatomáceas e mitocôndrias isoladas de mamíferos. A conjugação tem vantagens sobre outras formas de transferência genética, incluindo interrupção mínima do envelope celular do alvo e a capacidade de transferir quantidades relativamente grandes de material genético (consulte a discussão acima sobre transferência cromossômica de E. coli). Na engenharia de plantas, a conjugação do tipo Agrobacterium complementa outros veículos padrão, como o vírus do mosaico do tabaco (TMV). Embora o TMV seja capaz de infectar muitas famílias de plantas, estas são principalmente dicotiledôneas herbáceas. A conjugação do tipo Agrobacterium também é usada principalmente para dicotiledôneas, mas receptores de monocotiledôneas não são incomuns.
Contenido relacionado
Rim
Estresse abiótico
Morte